一种家蚕BmBDV的LAMP‑LFD快速试剂盒及检测方法与流程
本发明涉及一种家蚕BmBDV的LAMP-LFD快速试剂盒及检测方法,属于病毒疫病诊断技术领域。
背景技术:
家蚕二分浓核病毒(Bombyx mori Bidensovirus,BmBDV)属于细小病毒科浓核病毒亚科,该病毒具有高致死率,感染持续时间较长,引起慢性蚕病,是我国夏秋季节蚕茧等经济产品减产的重要原因之一。研究表明,BmBDV为无囊膜的球状病毒粒子,直径约20-24nm,包含2个线性单链DNA分子,大小分别约6.5kb(VD1)和6kb(VD2),其序列已测定并在GeneBank上登录(登录号DQ017268和DQ017269)。目前该病毒的检测方法主要为常规PCR检测法,但在实际检测工作中,现有的检测技术存在以下问题:一是灵敏度不够,无法检测到潜伏感毒样品;二是容易产生假阳性,对模板质量要求高;三是操作繁琐,对实验条件要求高,不利于养殖户和一线生产技术人员来操作。
LAMP是一种新型的核酸等温扩增检测技术,即依据环介导等温核酸扩增技术的原理,针对靶基因的特定区域设计4条特异性引物,反应时先由外部引物将内部引物扩增所需要的模板扩增出来,然后由内部引物对靶基因片段进行引导合成。由于内部引物所扩增出的片段含有与该引物5’端DNA片段的反相互补序列,因此这些反相互补序列之间形成茎-环结构,同时,另外一条内部引物与也可形成茎-环结构,片段的两端形成哑铃状结构,如此循环往复的过程最后形成花椰菜形状的茎-环结构,可在15min-60min之内实现109-1010倍的扩增。该技术简化了操作步骤,在等温条件下就可以高效、高特异地扩增靶序列。LAMP产物的检测一般采用琼脂糖凝胶电泳、浊度观察、荧光染料观察、侧向流层析试纸技术(LFD)等方法。
其中,LAMP-LFD法使得反应结果可以直接用肉眼观察,具有安全、快捷、高效的特点,适合应用推广。而且截止目前,该技术在家蚕BmBDV的检测中未见报道。
技术实现要素:
本发明的目的是针对现有技术中的缺陷,提供一种通过快速检测家蚕BmBDV的环介导恒温扩增方法检测家蚕家蚕二分浓核病毒的方法,并提供一种用于以上目的的LAMP-LFD检测试剂盒。所述试剂盒特异性强,而且操作简便快捷,克服现有检测方法不能在生产中直接应用的问题,适合家蚕BmBDV的筛查。
本发明所述的家蚕BmBDV病毒LAMP-LFD检测试剂盒包括:BmBDV病毒 LAMP预反应液:所述预反应液包括引物BmBDV-FIP和BmBDV-BIP、引物 BmBDV-F3和BmBDV-B3、引物BmBDV-LF和BmBDV-LB、 探针BmBDV-FITC-PROBE;
其中所述引物BmBDV-FIP如SEQ ID NO:3所示,引物BmBDV-BIP如SEQ ID NO:4所示,引物 BmBDV-F3如SEQ ID NO:1所示,引物BmBDV-B3如SEQ ID NO:2所示,引物BmBDV-LF如SEQ ID NO:5所示,引物 BmBDV-LB如SEQ ID NO:6所示, 探针BmBDV-FITC-PROBE如如SEQ ID NO:7所示。
所述LAMP预反应液中各引物和探针含量为:1.5~2.0mM 引物BmBDV-FIP和BmBDV-BIP,0.2~0.4mM引物 BmBDV-F3和BmBDV-B3,0.2~0.5mM 引物BmBDV-LF和BmBDV-LB,0.05~0.1μM 探针BmBDV-FITC-PROBE。
所述LAMP预反应液还包括:20~40mM Tris-HCl (pH8.0~9.0), 10~15mM 氯化钾, 15~20mM 硫酸铵, 8~10mM 硫酸镁, 0.1~0.2% Triton X-100,1.2~1.4mM dNTP, 6-8U Bst DNA 聚合酶大片段(New England Biolabs),0.6~0.8M 甜菜碱。
其中所述的引物序列具体为:
BmBDV-F3 (SEQ ID NO:1): 5’-TCTGACGTTGGTGGAAGT-3’ BmBDV-B3(SEQ ID NO:2): 5’-AACTTGCTTTCCACTCGA-3’ BmBDV-FIP(SEQ ID NO:3):
5’-biotin-TGAGGCGTCCATAGGACCTTTTTTGGAAGTGGAAAACGCAGT-3’ BmBDV-BIP(SEQ ID NO:4):
5’-GAGGATCTGGAGGTGGTGGTTTTTTTGGCTTGTAAATAGGTTGG-3’ BmBDV-LF(SEQ ID NO:5): 5’-ACCGCCCCCAGACACATT-3’ BmBDV-LB(SEQ ID NO:6): 5’-GGAGGTGCTTCAGCAGAGG-3’ 所属探针序列为:
BmBDV-FITC-PROBE(SEQ ID NO:7): 5’-FITC-TAGAGGAGGTGCTTCAGCAGAG-3’
本发明所述的家蚕BmBDV病毒LAMP-LFD检测试剂盒,所述试剂盒中还配有LFD试纸用的缓冲液、阳性对照样品、阴性对照样品以及LAMP核酸反应管中添加有稳定液,其中LFD试纸用的缓冲液为1×TAE缓冲液,阳性对照样品为BmBDV病毒基因组DNA,阴性对照样品为无核酸的去离子水,核酸反应稳定液为液体石蜡油。
本发明还提供一种家蚕BmBDV病毒的检测方法,所述检测方法采用上述BmBDV病毒LAMP-LFD检测试剂盒进行检测,按照下述步骤进行检测:
S1.家蚕样品中BmBDV基因组DNA的快速提取:
取20~30mg家蚕整蚕或蚕沙,或20µL家蚕血淋巴,加入80~100μL组织裂解液混合,37~55℃温育25~30min,95℃变性5min,取2~5μL作模板。组织裂解液包含50~100mM Tris-HCl, 1~4mM EDTA,pH7.0~8.0,100~200μg/mL蛋白酶K和RNase A,0.1~0.2M NaCl。
S2.家蚕BmBDV病毒LAMP扩增:
(1)根据待检样品数,配制所需的预反应液,在预反应液中加入2~5μL DNA模板,再加入适量的去离子水,使反应体系总体积为25μL。然后在61℃~65℃下反应30~60min。
(2)标记清楚后,将检测反应管置于61-65℃,反应30~60min,80℃灭活;其中最适反应温度为62℃,最适反应时间为30min。
S3.家蚕BmBDV病毒LFD试纸检测:
(1)取家蚕BmBDV病毒LAMP扩增产物6~10μL,置于LFD试纸加样孔;
(2)在LFD试纸加样孔一端,滴加50~100μL缓冲液,待缓冲液移动到试纸的另一端,表明反应基本结束,根据显色条带情况判断LAMP-LFD检测的结果。当仅出现质控带时表明反应结果为阴性,当质控带和检测带同时出现时,表明反应结果为阳性。
本发明所述的LFD检测试纸,是在改良胶体金技术的基础上,利用生物素(biotin)和FITC抗体等制备的侧向层析检测试纸。
与现有检测技术比较,本发明所提供的家蚕BmBDV病毒LAMP-LFD检测方法具有以下优点:
(1)本发明的快速诊断试剂盒检测灵敏度高,是常规PCR的103倍左右(图2,3);
(2)本发明的快速诊断试剂盒检测时间短,可以在45min内获得检测结果,比常规PCR节约3~4小时;
(3)本发明中的DNA提取方法简单快捷,不需要用到离心机,一步就可以进行后续LAMP反应,而且不用到氯仿、巯基乙醇等有害物质;
(4)本发明的快速诊断试剂盒对仪器设备要求低,不需要普通PCR所用的PCR仪、凝胶电泳和成像系统;
(5)本发明的检测试剂盒操作步骤简单,结果较染料法直观易判定(图1,2,4),处于生产一线的技术员和养殖户都可以按步骤指导进行操作;
(6)本发明的检测试剂盒对人和环境较安全,整个过程不使用有毒物质。
附图说明
图1为LAMP扩增产物进行凝胶电泳(A)和LFD试纸显色结果图(B);图中M:DL2000 DNA Marker (TaKaRa公司);左侧泳道1~9:模板分别为10-4,10-5,10-6,10-7,10-8,10-9倍稀释的基因组DNA;右侧1~6:为左侧实验结果的LFD试纸检测图。
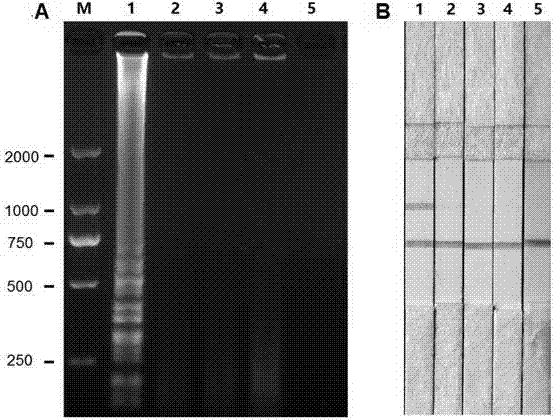
图2为检测BmBDV LAMP病毒特异性实验结果;图中A为LAMP扩增凝胶电泳结果;B为LAMP-LFD检测结果;图A中,M:DL2000 DNA Marker(TaKaRa公司)泳道1:家蚕二分浓核病毒(BmBDV);泳道2:家蚕浓核病毒(BmDNV);泳道3:家蚕核型多角体病毒(BmNPV);泳道4:家蚕微孢子虫(N. b.);泳道5:阴性对照。
图3为LAMP荧光显色法和普通PCR方法;图中M:DL2000 DNA Marker (TaKaRa公司);左侧泳道(图A)1~5:模板分别为10-5,10-6,10-7,10-8,10-9倍稀释的基因组DNA;中间(图B)为图A泳道对应的LAMP普通显色方法;右侧(图C)1~5:为同样模板的PCR检测图。
具体实施方式
以下结合附图实施例对本发明作进一步详细描述。
实施例1:
所需材料:
感染家蚕BmBDV病毒的样本来源于本实验室(江苏大学生命科学研究院);所用引物与探针由上海生工生物公司合成;Bst DNA 聚合酶大片段购自New England Biolabs公司;dNTP、购自promega公司;甜菜碱、硫酸镁等购自sigma公司。
S1. 家蚕BmBDV样品DNA的快速提取:
取20~30mg家蚕整蚕或蚕沙,或20µL家蚕血淋巴,加入100μL组织裂解液混合,37~55℃温育25~30min,95℃变性5min,取5μL作模板。
S2. 家蚕BmBDV病毒LAMP恒温扩增:
(1)根据待检样品数,配制相应数量的预反应液(1.6mM BmBDV-FIP和BmBDV-BIP,0.2mM BmBDV-F3,BmBDV-B3,BmBDV-LP和BmBDV-LB,0.05μM BmBDV-FITC-PROBE,20mM Tris-HCl, 10mM 氯化钾, 15 mM 硫酸铵, 8mM 硫酸镁, 0.1% Triton X-100,0.6M 甜菜碱,1.4mM dNTP, 8U Bst DNA 聚合酶大片段),每管检测预反应液体积为20μL;
(2)分别吸取5μL待检样品加入核酸检测反应管中,混合均匀;
(3)标记清楚后,将检测反应管置于62℃水浴锅中,反应30min;
S3. 家蚕BmBDV病毒LAMP扩增产物进行凝胶电泳:
(1)配置2%的琼脂糖凝胶,每个加样孔加入6μL的反应产物;
(2)电泳30分钟后凝胶成像,结果见图1的A图。
S4. LAMP扩增产物的LFD试纸检测:
(1)取BmBDV病毒LAMP扩增产物6μL,置于LFD试纸加样孔;
(2)在LFD试纸加样孔一端,滴加50μL缓冲液(上文提到的缓冲液为1×TAE缓冲液),待缓冲液移动基本结束,判断LAMP-LFD检测结果,见图1的B图。
图1 A侧图可见阶梯状的扩增条带,再利用LFD检测试纸条检验扩增产物,由图1 B图可见与电泳结果吻合,本发明的试剂盒和检测方法,可以灵敏有效的检测整蚕、蚕沙或家蚕血淋巴中的BmBDV病毒,并且,重复试验验证,检测结果稳定可靠。
实施例2:
所需材料:
感染家蚕BmBDV病毒,家蚕浓核病毒BmDNV,家蚕核型多角体病毒BmNPV,家蚕微孢子虫N. b.的样本均采集自江苏大学生命科学研究院;所用引物与探针由上海生工生物公司合成;Bst DNA 聚合酶大片段购自New England Biolabs公司;dNTP、购自promega公司;甜菜碱、硫酸镁等购自sigma公司。
家蚕二分浓核病毒(BmBDV)、家蚕浓核病毒(BmDNV)、家蚕核型多角体病毒(BmNPV)和家蚕微孢子虫(N. b.)来源于江苏大学生命科学研究院。
S1.样品DNA的快速提取:
分别取家蚕感染不同病原体的20~30mg家蚕整蚕或蚕沙,或20µL家蚕血淋巴,加入100μL组织裂解液混合,37~55℃温育25~30min,95℃变性5min,取5μL作模板。
S2. LAMP恒温扩增:
(1)根据待检样品数,配制相应数量的预反应液(1.6mM BmBDV-FIP和BmBDV-BIP,0.2mM BmBDV-F3,BmBDV-B3,BmBDV-LP和BmBDV-LB,0.05μM BmBDV-FITC-PROBE,20mM Tris-HCl, 10mM 氯化钾, 15 mM 硫酸铵, 8mM 硫酸镁, 0.1% Triton X-100,0.6M 甜菜碱,1.4mM dNTP, 8U Bst DNA 聚合酶大片段),每管检测预反应液体积为20μL;
(2)分别吸取5μL待检样品加入核酸检测反应管中,混合均匀;
(3)标记清楚后,将检测反应管置于62℃水浴锅中,反应30min;
S3. LAMP扩增产物进行凝胶电泳:
(1)配置2%的琼脂糖凝胶,每个加样孔加入6μL的反应产物;
(2)电泳30分钟后凝胶成像,结果见图2 A图。
S4. LAMP扩增产物的LFD试纸检测:
(1)取BmBDV病毒LAMP扩增产物6μL,置于LFD试纸加样孔;
(2)在LFD试纸加样孔一端,滴加50μL缓冲液(上文提到的缓冲液为1×TAE缓冲液),待缓冲液移动基本结束,判断LAMP-LFD检测结果,见图2B图。
图2为BmBDV LAMP特异性实验结果图;图中A为LAMP扩增凝胶电泳结果;B为LAMP-LFD检测结果;分别将家蚕二分浓核病毒(BmBDV)、家蚕浓核病毒(BmDNV)、家蚕核型多角体病毒(BmNPV)和家蚕微孢子虫(N. b.)作为反应模板,结果显示,本发明的方法检测结果与电泳结果吻合,具有非常好的特异性,对家蚕二分浓核病毒的检测精准,结果的观察更直观明了。
图3为LAMP荧光显色法和普通PCR方法比较的结果;M:DL2000 DNA Marker (TaKaRa公司);左侧泳道(A)1~5:模板分别为10-5,10-6,10-7,10-8,10-9倍稀释的基因组DNA;中间(B)泳道为A图对应的LAMP普通显色方法;右侧(C)1~5:为同样模板的PCR检测图。
从图3可以看出LAMP方法比普通PCR方法灵敏1000倍,LAMP-LFD比LAMP普通显色方法更加易于观察。
根据以上实验结果表明,BmBDV病毒LAMP-LFD检测试剂盒和检测方法可以快速、简便、灵敏的进行该病毒的现场检测。
SEQUENCE LISTING
<110> 江苏大学
<120> 一种家蚕BmBDV的LAMP-LFD快速试剂盒及检测方法
<130> 一种家蚕BmBDV的LAMP-LFD快速试剂盒及检测方法
<160> 7
<170> PatentIn version 3.3
<210> 1
<211> 18
<212> DNA
<213> 人工序列
<400> 1
tctgacgttg gtggaagt 18
<210> 2
<211> 18
<212> DNA
<213> 人工序列
<400> 2
aacttgcttt ccactcga 18
<210> 3
<211> 42
<212> DNA
<213> 人工序列
<400> 3
tgaggcgtcc ataggacctt ttttggaagt ggaaaacgca gt 42
<210> 4
<211> 44
<212> DNA
<213> 人工序列
<400> 4
gaggatctgg aggtggtggt ttttttggct tgtaaatagg ttgg 44
<210> 5
<211> 18
<212> DNA
<213> 人工序列
<400> 5
accgccccca gacacatt 18
<210> 6
<211> 19
<212> DNA
<213> 人工序列
<400> 6
ggaggtgctt cagcagagg 19
<210> 7
<211> 22
<212> DNA
<213> 人工序列
<400> 7
tagaggaggt gcttcagcag ag 22
- 还没有人留言评论。精彩留言会获得点赞!