一种新型有机铋配合物及其制备方法和催化应用与流程
本发明属于有机合成及催化领域,具体地说涉及一种新型有机铋配合物及其制备方法和催化应用。
背景技术:
金属有机化合物是指含有一个或多个金属-碳(m-c)键的化合物。因其在合成、催化、防污、药物、稳定剂等方面的广泛应用而受到人们的广泛关注。有机铋化合物是指含有铋-碳(bi-c)共价键的金属有机化合物。铋作为一种主族金属元素,在元素周期表中归属于15族,其化合物中通常使用3个6p电子成健,2个6s电子作为惰性电子对,因而三价铋化合物相对较为常见。然而,迄今为止,有机铋化合物作为催化剂在有机合成中的应用很少。原因可能是有机铋化合物的稳定性较差或者是路易斯酸性太弱,阻碍了他们的应用。为了克服克服这些缺点,我们需要开发对空气和水稳定的新型有机铋配合物。
氢胺化反应是指胺类化合物直接和炔烃发生加成反应得到亚胺及衍生物的一中有效的方法,符合原子经济,是目前合成亚胺及其衍生物最为有效的方法。氢胺化反应活化能高,因此需要借助过渡金属催化。最近的研究主要集中在锌、汞、铑、钯、锆等金属催化剂的制备,不幸的是,反应产率和催化效率都不令人满意。【参考文献:chemrev98(1998)675;angewcheminted43(2004)3368;organometallics15(1996)3770;jorgchem(2006)4555】。为了提高氢胺化反应的效率,我们需要开发新型的催化剂,而本发明提供的新型有机铋配合物金属催化剂就能很好的催化该反应。
采用直接催化合成有机铋配合物催化剂的方法目前还没有报道。我们采用廉价的芳基硼酸试剂,通过suzuki偶联得到新型的有机铋催化剂,并将其应用在氢胺化反应中,其产率和催化效率都有很大的提高。本发明报道一种新型有机铋配合物及其制备方法和催化应用。
技术实现要素:
本发明的目的在于提供一种新型有机铋配合物及其制备方法和催化应用。
为达到上述发明目的,本发明提出以下的技术方案:
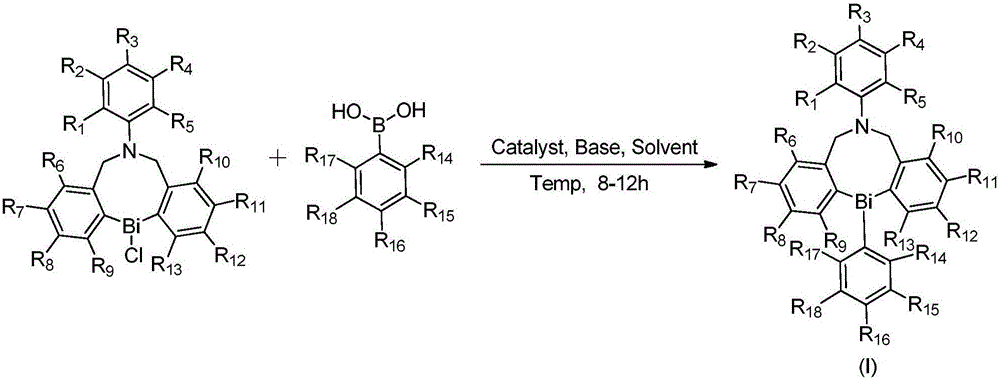
一种新型有机铋(iii)配合物的制备方法,其特征在于,以常用的有机溶剂作为反应溶剂,以含桥式氮原子配体的二苯基铋氯和芳基硼酸为原料,采用镍(ii)催化反应,反应完毕后过滤,重结晶得到新型有机铋(iii)配合物催化剂(i),产率为65%-95%。
一种亚胺及其衍生物的制备方法,其特征在于,以常用的有机溶剂作为反应溶剂,以芳基乙炔和苯胺类化合物为原料,采用新型有机铋(iii)配合物的催化剂(i)作为催化剂催化该反应,反应完毕后通过柱层析得到亚胺类化合物。
所述一种新型有机铋配合物具有以下结构式(i):
其中,r1、r2、r3、r4、r5基团为氢、甲基、甲氧基、乙基、叔丁基、氟、氯、溴、碘、乙氧基、异丙基、氰基、三氟甲基、正丁基、苯基中的一种或几种;r6、r7、r8、r9、r10、r11、r12、r13基团为氢、甲基、乙基、异丙基、氟、氯、溴、碘、叔丁基中的一种或几种;r14、r15、r16、r17、r18基团为氢、甲基、甲氧基、乙基、叔丁基、氟、氯、溴、碘、乙氧基、异丙基、氰基、甲酰基、乙酰基、三氟甲基、正丁基、苯基、乙烯基、乙炔基中的一种或几种。
所述一种新型有机铋配合物的制备方法,其特征在于,以常用的有机溶剂作为反应溶剂,以含桥式氮原子配体的二苯基铋氯和芳基硼酸为原料,采用镍(ii)催化反应,高产率、高选择性的得到新型有机铋配合物催化剂(i)。该催化剂在芳基炔烃和苯胺类化合物的氢胺化反应中有很好的选择性和催化效率。
所述一种新型有机铋配合物,其特征在于,r1、r2、r3、r4、r5基团为氢、甲基、甲氧基、乙基、叔丁基、氟、氯、溴、碘、乙氧基、异丙基、氰基、三氟甲基、正丁基、苯基中的一种或几种。
所述一种新型有机铋配合物,其特征在于,r6、r7、r8、r9、r10、r11、r12、r13基团为氢、甲基、乙基、异丙基、氟、氯、溴、碘、叔丁基中的一种或几种。
所述一种新型有机铋配合物,其特征在于,r14、r15、r16、r17、r18基团为氢、甲基、甲氧基、乙基、叔丁基、氟、氯、溴、碘、乙氧基、异丙基、氰基、甲酰基、乙酰基、三氟甲基、正丁基、苯基、乙烯基、乙炔基中的一种或几种。
所述一种新型有机铋配合物的制备方法,其特征在于,所述新型有机铋配合物制备所用溶剂选自四氢呋喃(thf)、甲苯(toluene)、丙酮(acetone)、乙腈(ch3cn)、n,n-二甲基甲酰胺(dmf)中的一种。
所述一种新型有机铋配合物的制备方法,其特征在于,所述新型有机铋配合物制备所用的促进剂为硝酸钾、醋酸钾、碳酸钾、碳酸钠、碳酸铯、碳酸氢钠、磷酸氢钾、磷酸二氢钾、叔丁醇钾、叔丁醇钠、乙酸钠中的一种。
所述一种新型有机铋配合物的制备方法,其特征在于,所述新型有机铋配合物制备所用的催化剂为醋酸镍、氯化镍、氟化镍、溴化镍、三氟甲磺酸镍、乙酰丙酮镍和二氯二(三苯基膦)镍中的一种。
所述一种新型有机铋配合物的制备方法,其特征在于,所述新型有机铋配合物制备的条件为:在氮气保护下反应8-12h。
所述一种新型有机铋配合物的制备方法,其特征在于,所述催化剂新型有机铋配合物制备中,重结晶所用溶剂为二氯甲烷、乙酸乙酯、正己烷、石油醚和乙醇中的一种或几种。
所述一种亚胺及其衍生物的制备方法,其特征在于,所述氢胺化反应溶剂选自四氢呋喃(thf)、甲苯(toluene)、丙酮(acetone)、乙腈(ch3cn)、氯仿、二氯甲烷中的一种。
所述一种亚胺及其衍生物的制备方法,其特征在于,所述氢胺化反应条件为:100℃下反应6-10h,其催化剂用量为2mol%-4mol%。
本发明所提供的一种新型有机铋配合物的制备方法为制备亚胺类化合物提供了一种新的途径,其优点在于新型有机铋配合物耐水抗氧,催化反应的原料来源广泛,目标产物的选择性和产率均较高,反应条件温和,反应操作简便,底物适用范围广泛。
【附图说明】
附图1所示是本发明提供的一种新型有机铋配合物的制备途径。
附图2所示是芳基炔烃和苯胺类化合物的氢胺化制备途径。
【具体实施方式】
本发明所提供的一种新型有机锑铋配合物的制备方法及催化合成亚胺类化合物的制备途径请参见附图1和2:
一种新型有机铋(iii)配合物催化剂的制备方法及催化应用
将含桥式氮原子配体的二苯基铋氯、芳基硼酸、镍催化剂和促进剂加入到反应器中,抽真空回填氮气3次,然后将溶剂加入反应器中,反应6-12h。反应完毕后减压除去溶剂,重结晶得到目标产物。为了检验新型有机铋(iii)配合物催化剂的催化活性,我们将其用于亚胺类化合物合成。
下面结合具体的制备实例对本发明做进一步说明:
实施例1
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为90%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r3、r4、r5为氢),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例1获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的油浴锅中反应10h。反应完毕后,经柱层析分离得到二苯基亚胺,产率为85%。
实施例2
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例2获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为90%。
实施例3
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为乙基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例3获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为90%。
实施例4
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入50ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为95%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例4获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为95%。
制备例5
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为叔丁基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在100℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例5获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为96%。
实施例6
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为正丁基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为85%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例6获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应9h。反应完毕后,经柱层析分离得到目标化合物,产率为88%。
实施例7
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为甲酰基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为79%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例7获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应9h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例8
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为乙酰基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为81%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例8获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为82%。
实施例9
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为氰基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为82%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲氧基),0.015mmol实施例9获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为82%。
实施例10
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为乙氧基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为82%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲氧基),0.015mmol实施例10获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例11
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为甲氧基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为82%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲氧基),0.015mmol实施例11获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为84%。
实施例12
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为氟),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为89%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲氧基),0.015mmol实施例12获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例13
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为氯),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为90%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲氧基),0.015mmol实施例13获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为88%。
实施例14
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为溴),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例14获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为91%。
实施例15
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为碘),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为94%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例15获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为93%。
实施例16
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为异丙基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为85%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例16获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例17
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为乙烯基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为85%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.015mmol实施例18获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例17
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r15、r17、r18基团为氢,r16为乙炔基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为86%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例18获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例18
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为95%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例18获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例19
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例19获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例20
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为乙酰基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为86%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例20获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为83%。
实施例21
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为异丙基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为86%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例21获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为84%。
实施例22
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为氟),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例22获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例23
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为叔丁基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例23获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为83%。
实施例24
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为叔丁基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例24获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例25
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r15、r16、r17、r18基团为氢,r14为甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为78%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例25获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例26
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r15、r16、r17、r18基团为氢,r14为氯),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为78%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例26获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为84%。
实施例27
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r15、r16、r17、r18基团为氢,r14为氟),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为75%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例27获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为89%。
实施例28
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢),9mmol芳基硼酸(r15、r16、r17、r18基团为氢,r14为乙基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应12h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为75%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为三氟甲基),0.015mmol实施例28获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例29
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为甲基),9mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.010mmol实施例29获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为83%。
实施例30
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为乙基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为88%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.010mmol实施例30获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为83%。
实施例31
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为叔丁基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为88%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.005mmol实施例31获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例32
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为氟),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为90%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.005mmol实施例32获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为88%。
实施例33
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为氯),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r9、r10为氢,r8为甲基),0.010mmol实施例33获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例34
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为氯),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.010mmol实施例34获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例35
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为溴),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为89%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例35获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为92%。
实施例36
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为碘),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应8h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例35获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例36
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为三氟甲基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为90%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r9、r10为氢),0.015mmol实施例36获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为88%。
实施例37
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为甲氧基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为84%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.015mmol实施例37获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为83%。
实施例38
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为乙氧基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为89%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.015mmol实施例38获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例39
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为甲基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为87%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.015mmol实施例39获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例40
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为甲基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.010mmol实施例40获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例41
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为乙基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.010mmol实施例41获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例42
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为叔丁基),8mmol芳基硼酸(r14、r15、r16、r17、r18基团为氢),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为88%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.010mmol实施例42获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为84%。
实施例43
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为叔丁基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.015mmol实施例43获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为86%。
实施例44
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为叔丁基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为91%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.010mmol实施例44获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例45
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为甲基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为89%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为三氟甲基),0.010mmol实施例45获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为84%。
实施例45
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r4为乙基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为89%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲氧基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.010mmol实施例46获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例46
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为乙基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为93%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.010mmol实施例46获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为85%。
实施例47
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为甲基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为94%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.010mmol实施例47获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为87%。
实施例48
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r4、r5、r6、r7、r8、r9、r10、r11、r12、r13基团为氢,r3为异丙基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为88%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.015mmol实施例48获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为89%。
实施例49
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r8、r9、r10、r11、r12、r13基团为氢,r7为异丙基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为86%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.015mmol实施例49获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为92%。
实施例50
在100ml反应管中加入6mmol含桥式氮原子配体的二苯基铋氯(r1、r2、r3、r4、r5、r6、r8、r9、r10、r11、r12、r13基团为氢,r7为甲基),8mmol芳基硼酸(r14、r16、r17、r18基团为氢,r15为三氟甲基),5mol%醋酸镍,2当量的碳酸钾,抽真空回填氮气三次,在氮气氛围下加入40ml甲苯,在120℃下反应10h。反应结束后减压除去甲苯,用乙酸乙酯和正己烷重结晶得到目标产物,产率为92%。
催化活性检验:
在10ml反应管中加入0.5mmol苯乙炔(r1、r2、r4、r5为氢,r3为甲基),0.5mmol苯胺(r6、r7、r8、r10为氢,r9为乙酰基),0.010mmol实施例50获得的新型有机铋配合物催化剂,然后加入2ml氯仿,将反应管放在100℃的加热器中反应10h。反应完毕后,经柱层析分离得到目标化合物,产率为88%。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制.应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围.因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!