靶向SIRT3激动剂及其在AML治疗药物中的应用的制作方法
本发明涉及靶向SIRT3激动剂及其在急性髓细胞白血病治疗药物中的应用,属于白血病治疗药物发现技术领域。
背景技术:
急性髓细胞性白血病(Acute myeloid leukemia,AML)是髓系造血干/祖细胞恶性疾病。以骨髓与外周血中原始和幼稚髓性细胞异常增生为主要特征,临床表现为贫血、出血、感染和发热、脏器浸润、代谢异常等。据统计AML约占成人白血病发病率的70%,且呈现逐年上升的趋势。目前临床上的主要治疗手段包括化疗,支持治疗和造血干细胞移植等。随着治疗方法的发展,特别是靶向疗法的开发,目前AML患者的完全缓解率和长期生存率都有了显著的提高。尽管如此,还有大约30%的患者的5年生存率仅为40%。随着精准医疗技术的发展,开发靶向性的小分子精准治疗药物是克服AML临床问题的关键。
近年来治疗AML的靶向小分子开发取得了丰硕的成果,主要集中在在FLT3,表观遗传(KMTs,HDAC,BRD4等),BCL-2及JNK/STAT等信号通路。如Sorafenib,Midostaurin,Quizartinib,Gilteritinib,Crenolanib,OTX015,Venetoclax等小分子靶向药物已经上市或处于临床研究阶段。SIRT3是一个线粒体内NAD+依赖的蛋白去乙酰化酶,能够通过调节自噬参与很多疾病进程,最新研究表明SIRT3调节的自噬在AML中扮演重要的角色。同时我们通过TCGA分析发现,SIRT3是AML的一个关键的预兆因子,与AML病人的生存密切相关。但是目前报道的SIRT3激动剂只有白藜芦醇及和厚朴酚,这两个小分子被证明均不是SIRT3的专一性激动剂,并且其活性较低。因此开发具有全新骨架的SIRT3小分子靶向激动剂成为治疗AML的一个新策略。
技术实现要素:
本发明解决的技术问题是提供一种作为SIRT3激动剂的新化合物。
本发明提供结构式如式Ⅰ所示的化合物或其药学上可接受的盐:
式Ⅰ
其中,R1为、或 或或 或或或或或或或 或; n为0或1。
本发明还提供上述化合物或其药学上可接受的盐在制备急性髓细胞白血病治疗药物中的用途。
进一步的,所述抗急性髓细胞白血病优选为SIRT3激动剂类药物,其用途为用于急性髓细胞白血病相关治疗。
本发明还提供一种药物组合物,它是包含有效剂量的上述化合物或其药学上可接受的盐的制剂。
本发明制备的化合物或其药学上可接受的盐,可以作为SIRT3激动剂,具有较明显的治疗急性髓细胞白血病效果。
附图说明
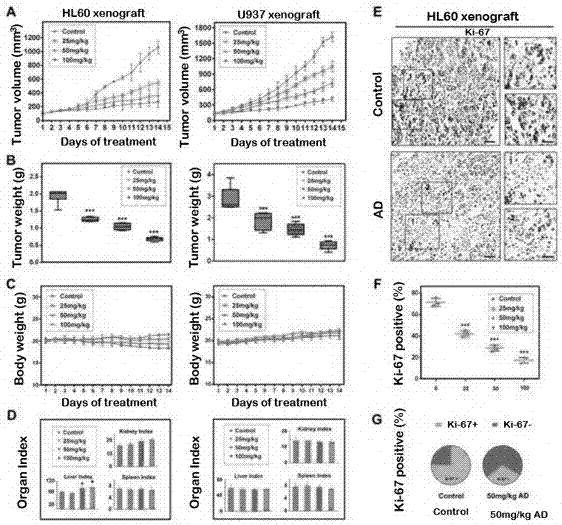
图1A为化合物13显著降低了HL60及U937移植瘤体积。
图1B为肿瘤体重变化图。
图1C为小鼠体重变化图。
图1D脏器变化图(肾,肝,脾)。
图1E为Ki67染色。
图1F、G为Ki67定量分析。
图2A为肿瘤组织中SIRT3 和 LC3-II免疫组化染色。
图2B、C为免疫组化定量分析统计图。
具体实施方式
本发明提供如式Ⅰ所示的化合物:
式Ⅰ
其中,R1为、或 或或 或或 或 或 或 或或 或; n为0或1。
作为优选方案,R1为,n=1。
下面是本发明的化合物的一些优选结构:
。
本发明还提供本发明所述的化合物的药学上可接受的盐。所述盐可以为硝酸盐、盐酸盐、硫酸盐或磷酸盐等。
本发明还提供上述化合物或其药学上可接受的盐在制备治疗急性髓系白血病药物中的用途。进一步的,所述抗急性髓系白血病药物优选为SIRT3激动剂类药物,用于急性髓系白血病的相关治疗。
本发明还提供一种药物组合物,它是包含有效剂量的上述化合物或其药学上可接受的盐的制剂。可以通过本领域已知的方法可将本发明化合物制成以下形式:片剂、胶囊剂、水性或油性溶液剂、混悬剂、乳剂、乳膏剂、软膏剂、凝胶剂、喷鼻剂、栓剂、用于吸入的细小分散的粉剂或气雾剂或喷雾剂、用于胃肠道外(包括静脉内、肌内或输注)的无菌水性或油性溶液或混悬剂或无菌乳剂。可采用无菌水或水-丙二醇溶液作为溶剂来制备液体制剂,还可将活性组分配制在聚乙二醇水溶液中。用于口服给予的水性溶液可通过将活性组分溶解在水中并按需要加入合适的着色剂、矫味剂、稳定剂和增稠剂来制备。口服使用的水性混悬剂可通过将细小分散的活性组分与粘性物质一道分散在水中,所述粘性物质如为天然合成胶、树脂、甲基纤维素、羧甲基纤维素和其他药剂领域已知的悬浮剂。
药物组合物可为单位剂量形式。在这些形式中,将所述组合物分成含适量活性组分的单位剂量。该单位剂量形式可为包装制剂,包装中包括分隔量的制剂,例如盒装片剂、胶囊剂和在管形瓶或安瓿中的粉剂。单位剂量形式还可为胶囊剂、扁囊剂或片剂或其可为适当数量的任何这些包装形式。
本发明的药物组合物,其活性成分可仅为本发明的化合物,也可与其他抗急性髓系白血病化合物组合作为活性成分。
在治疗过程中,可采用本发明的药物组合物与其他抗急性髓系白血病药进行联合治疗。
可通过同时、序贯或单独给予各种治疗成分可实现这种联合治疗。此类组合产品应用有效剂量范围内的本发明化合物和准许剂量范围内的其他药学活性剂。
下面结合实施例对本发明的具体实施方式做进一步的描述,并不因此将本发明限制在所述的实施例范围之中。
实施例1化合物1~14的合成。
化合物1~12采用如下反应式合成:
。
将原料(2-butylbenzofuran-3-yl)(4-hydroxy-3,5-diiodophenyl)methanone(10 mmol)溶于50 ml丁酮中,然后缓慢加入碳酸钾(20 mmol)加热回流0.5 h后,再缓慢滴加二溴乙烷或二溴丙烷(20 mmol)。回流反应8小时后,抽滤除去碳酸钾固体,用丁酮洗涤,收集滤液,旋干溶剂。随后用氯仿萃取(3 x 30 ml),合并有机相,无水硫酸镁干燥得到粗产物。粗产物用硅胶色谱柱纯化,石油醚:乙酸乙酯 (50:1)作为流动相得到中间体,为白色固体备用。
将上步中间体(5 mmol)溶于30 ml乙腈中,然后缓慢加入碳酸钾(10 mmol)及胺衍生物(10 mmol),催化量的碘化钾,加热回流24 h后,抽滤除去碳酸钾固体,用乙腈洗涤,收集滤液,旋干溶剂。随后用氯仿萃取(3 x 30 ml),合并有机相,无水硫酸镁干燥得到粗产物。粗产物用硅胶色谱柱纯化,氯仿:甲醇 (20:1)作为流动相得到产物,为淡黄色油状,两步收率 (50-70%)。
化合物 1 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.0 Hz), 7.43 (1H, dd, J = 7.9, 0.9 Hz), 7.32-7.27 (1H, m), 7.25-7.20 (1H, m), 4.17 (2H, t, J = 6.0 Hz), 2.94 (2H, t, J = 6.0 Hz), 2.84 (2H, t, J = 6.0 Hz), 2.43 (6H, s), 1.81-1.73 (2H, m), 1.40-1.31 (2H, m), 0.91 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.7, 166.1, 161.5, 153,7, 140.7, 140.7, 138.3, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.0, 58.8, 45.9, 45.9, 30.1, 28.2, 22.6, 13.7。
化合物 2 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.21 (2H, t, J = 6.0 Hz), 2.97 (2H, t, J = 6.0 Hz), 2.84 (2H, t, J = 7.9 Hz), 2.62 (4H, brs), 1.81-1.73 (2H, m), 1.68-1.63 (4H, m), 1.51-1.45 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.2, 161.5, 153,7, 140.7, 140.7, 138.3, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 70.7, 58.5, 58.5, 55.0, 55.0, 30.1, 28.2, 25.8, 25.8, 24.2, 22.5, 13.7。
化合物 3 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.42 (1H, d, J = 7.8 Hz), 7.32-7.27 (1H, m), 7.25-7.20 (1H, m), 4.15 (2H, t, J = 5.9 Hz), 3.12 (2H, t, J = 8.0 Hz), 2.91 (4H, q, J = 7.2 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.38-2.31 (2H, m), 1.81-1.74 (2H, m), 1.41-1.32 (2H, m), 1.28 (6H, t, J = 7.2 Hz), 0.92 (3H, t, J = 7.4 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.7, 166.2, 160.9, 153,7, 140.7, 140.7, 138.5, 126.4, 124.7, 123.9, 121.1, 115.8, 111.1, 90.9, 90.9, 71.3, 49.6, 46.8, 46.8, 30.1, 28.2, 26.2, 22.5, 21.0, 13.7, 10.2。
化合物 4 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.42 (1H, d, J = 7.8 Hz), 7.32-7.27 (1H, m), 7.25-7.20 (1H, m), 4.12 (2H, t, J = 6.0 Hz), 2.84 (2H, t, J = 7.9 Hz), 2.60 (2H, t, J = 7.0 Hz), 2.13-2.06 (6H, m), 1.81-1.69 (4H, m), 1.41-1.32 (2H, m), 0.93-0.88 (15H, m); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.7, 166.0, 161.7, 153,7, 140.7, 140.7, 138.2, 126.5, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 73.2, 64.0, 52.1, 30.1, 29.7, 28.2, 28.0, 26.7, 22.6, 21.0, 21.0, 13.7。
化合物 5 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.0 Hz), 7.41 (1H, d, J = 7.9 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.15 (2H, t, J = 6.0 Hz), 2.97 (2H, t, J = 7.9 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.80 (4H, brs), 2.34-2.27 (2H, m), 1.94-1.91 (4H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.2, 161.1, 153,7, 140.7, 140.7, 138.4, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.7, 58.8, 54.3, 54.3, 53.1, 30.0, 28.8, 28.2, 23.5, 23.5, 22.5, 13.7。
化合物 6 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.12 (2H, t, J = 6.0 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.78 (2H, t, J = 7.1 Hz), 2.61 (4H, brs), 2.27-2.20 (2H, m), 1.81-1.73 (2H, m), 1.68-1.63 (4H, m), 1.51-1.45 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz);13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.2, 161.5, 153,7, 140.7, 140.7, 138.3, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.9, 58.5, 58.5, 55.7, 55.4, 55.4, 30.1, 28.2, 27.0, 25.4, 24.2, 22.5, 13.7。
化合物 7 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.13 (2H, t, J = 6.0 Hz), 3.76 (4H, t, J = 4.6 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.69 (2H, t, J = 7.1 Hz), 2.58-2.52 (4H, m), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.2, 161.3, 153,7, 140.8, 140.8, 138.4, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.9, 67.0, 67.0, 55.4, 53.7, 53.7, 45.7, 30.1, 28.2, 27.0, 22.5, 13.7。
化合物 8 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.12 (2H, t, J = 6.0 Hz), 2.84 (2H, t, J = 7.9 Hz), 2.69 (2H, t, J = 7.1 Hz), 2.58-2.52 (4H, m), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.1, 161.4, 153.7, 140.7, 140.7, 138.3, 126.5, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 72.1, 55.2, 55.2, 54.9, 53.2, 53.2,46.1, 30.1, 28.2, 27.5, 22.5, 13.7。
化合物 9 1H-NMR (400 MHz, CDCl3), δ(ppm): 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.1 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.32-7.28 (1H, m), 7.26-7.22 (1H, m), 4.13 (2H, t, J = 6.0 Hz), 3.76 (4H, t, J = 4.6 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.69 (2H, t, J = 7.1 Hz), 2.58-2.52 (4H, m), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.5, 166.4, 159.9, 153.7, 140.7, 140.7, 138.9, 126.3, 124.7, 123.9, 120.9, 115.7, 111.2, 90.7, 90.7, 69.2, 54.9, 54.9, 52.2, 52.2, 48.4, 47.6, 30.0, 28.2, 24.6, 22.5, 13.7, 9.2。
化合物 10 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.14 (2H, s), 7.60 (1H, d, J = 8.1 Hz), 7.46 (1H, dd, J = 7.7 Hz), 7.35-7.18 (7H, m), 4.14 (2H, t, J = 6.5 Hz), 3.57 (2H, s), 2.85 (2H, t, J = 7.9 Hz), 2.72 (2H, t, J = 7.3 Hz), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.7, 166.3, 160.7, 153,7, 140.7, 140.7, 138.5, 132.1, 132.0, 129.2, 129.2, 128.8, 128.8, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.6, 52.8, 45.6, 30.1, 30.0, 28.2, 28.0, 22.5, 13.7。
化合物 11 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.14 (2H, s), 7.60 (1H, d, J = 8.1 Hz), 7.46 (1H, dd, J = 7.7 Hz), 7.35-7.18 (7H, m), 4.14 (2H, t, J = 6.5 Hz), 3.57 (2H, s), 2.85 (2H, t, J = 7.9 Hz), 2.72 (2H, t, J = 7.3 Hz), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.7, 166.3, 160.7, 153,7, 140.7, 140.7, 138.5, 132.1, 132.0, 129.2, 129.2, 128.8, 128.8, 126.4, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 71.6, 52.8, 45.6, 30.1, 30.0, 28.2, 28.0, 22.5, 13.7。
化合物 121H-NMR (400 MHz, CDCl3), δ(ppm): 8.20 (2H, s), 7.48 (1H, d, J = 8.0 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.38-7.30 (4H, m), 7.27-7.22 (3H, m), 4.15-4.06 (2H, m), 3.86 (1H, q, J = 6.5 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.16-2.09 (2H, m), 1.81-1.73 (2H, m), 1.42 (3H, d, J = 6.5 Hz), 1.41-1.32 (2H, m), 0.91 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.1, 161.5, 153.7, 140.7, 140.7, 139.0, 138.3, 129.1, 129.1, 128.3, 128.3, 127.0, 126.5, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 72.3, 62.3, 58.6, 54.2, 42.1, 30.1, 28.2, 28.0, 22.6, 13.7。
化合物 13 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.20 (2H, s), 7.48 (1H, d, J = 8.0 Hz), 7.41 (1H, d, J = 7.8 Hz), 7.38-7.30 (4H, m), 7.27-7.22 (3H, m), 4.15-4.06 (2H, m), 3.86 (1H, q, J = 6.5 Hz), 2.85 (2H, t, J = 7.9 Hz), 2.16-2.09 (2H, m), 1.81-1.73 (2H, m), 1.42 (3H, d, J = 6.5 Hz), 1.41-1.32 (2H, m), 0.91 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.1, 161.5, 153.7, 140.7, 140.7, 139.0, 138.3, 129.1, 129.1, 128.3, 128.3, 127.0, 126.5, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 72.3, 62.3, 58.6, 54.2, 42.1, 30.1, 28.2, 28.0, 22.6, 13.7。
化合物 14 1H-NMR (400 MHz, CDCl3), δ(ppm): 8.21 (2H, s), 7.48 (1H, d, J = 8.0 Hz), 7.43 (1H, dd, J = 7.9, 0.9 Hz), 7.36-7.24 (7H, m), 4.14 (2H, t,J = 6.5 Hz), 3.57 (2H, s), 2.85 (2H, t, J = 7.9 Hz), 2.72 (2H, t, J = 7.3 Hz), 2.26 (3H, s), 2.23-2.16 (2H, m), 1.81-1.73 (2H, m), 1.41-1.32 (2H, m), 0.92 (3H, t, J = 7.3 Hz); 13C-NMR (100 MHz, CDCl3), δ(ppm): 187.8, 166.1, 161.5, 153,7, 140.7, 140.7, 139.0, 138.3, 129.1, 129.1, 128.3, 128.3, 127.4, 126.5, 124.7, 123.9, 121.1, 115.9, 111.1, 90.9, 90.9, 72.3, 62.3, 54.2, 42.1, 30.1, 28.2, 28.0, 22.6, 13.7。
试验例1化合物1~14对SIRT3激动活性及抗肿瘤活性。
本实验的目的是检测本发明的化合物对体外SIRT3酶激活活性,及对细胞的自噬率活性。
ULK1酶活实验是利用ADP-Glo™ Kinase Assay + ULK1 Kinase Enzyme System (Promega, Madison, WI, USA)测得,通过GraphPad Prism5 software (San Diego, CA, USA)处理数据,结果见表1。细胞的自噬率活性是通过MDC荧光染色分析实验方法测定。
表1 化合物1~14激酶激动活性及自噬率活性
实验结果表明,本发明的化合物均对SIRT3具有激动活性及自噬活性,其中,化合物5、化合物11、化合物12、化合物13、化合物14的效果较好,最优的化合物13对SIRT3具有较强的激动活性及细胞毒活性。
试验例2化合物13的体内活性评价。
为了评价化合物13在体内抗肿瘤活性,两个血液瘤异种移植模型即HL60和U937细胞模型分别被使用。我们使用了三种不同剂量的化合物13体内研究:25毫克/千克,50毫克/千克和100毫克/公斤。在所有的模型中,化合物13表现出明显的肿瘤生长的抑制作用并呈剂量依赖性(图1A,B),在高剂量组小鼠体重稍稍减少,而在其他组中小鼠体重并明显变化(图1C)。一些脏器体重变化也被检测(图1D)。为了检查是否化合物调节的体内抑制肿瘤生长是与减少细胞增殖和增加自噬性细胞死亡相关。我们对肿瘤组织进行了Ki-67和LC3的免疫组化分析(图1E-G)。我们发现化合物13能够显著减少Ki-67阳性细胞数量并且增加自噬水平。为了进一步阐明化合物13在体内的作用机制我们进一步检测了SIRT3及LC3-II的表达情况,结果显示SIRT3和LC3-II的表达均显著增加(图2 A-C)。综上,这些结果表明化合物13在小鼠异种移植中具有良好的抗肿瘤活性。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种用于判断靶向单克隆抗体治疗肿瘤疗效的预测分子的制造方法与工艺
- 一种检测肺癌相关基因热点突变的试剂盒及其应用的制造方法与工艺
- 一种为肺癌提供离体个体化药物测试的方法及培养基与流程
- 一种谷胱甘肽/超声双重刺激响应纳米聚合物囊泡、其制备方法及应用与流程
- 一种多重刺激响应交联型聚合物纳米水凝胶、其制备方法及应用与流程
- 一种靶向CD47的免疫检查点抑制剂药物组合物及其制备方法与流程
- 具有淋巴靶向功能的生物自组装纳米晶注射剂及制备方法与流程
- 用于检测肝癌的基因标志物及其用途的制造方法与工艺
- 特异性shRNA筛选及其靶向Ang‑2基因抑制肺癌细胞的验证方法与流程
- 一种具有靶向功能仿病毒结构高分子囊泡及其制备与应用的制造方法与工艺
- 阻断UBE2M介导Neddylation修饰在肾细胞癌治疗中的应用的制造方法与工艺
- 无载体共组装肿瘤靶向抗癌纳米药物及其制备方法与应用与流程
- 一种用于判断靶向单克隆抗体治疗肿瘤疗效的预测分子的制造方法与工艺
- 一种靶向CD47的免疫检查点抑制剂药物组合物及其制备方法与流程
- 具有淋巴靶向功能的生物自组装纳米晶注射剂及制备方法与流程
- 用于检测肝癌的基因标志物及其用途的制造方法与工艺
- 特异性shRNA筛选及其靶向Ang‑2基因抑制肺癌细胞的验证方法与流程
- 一种多功能自动化生物细胞提取分离控制系统及采用该系统实现的细胞提取分离方法与流程
- 一种融合蛋白及光敏剂复合物及其制备方法和应用与流程
- 具有可视化和显示光斑边界功能的光动力治疗系统的制造方法与工艺