一种手性3-烯丙基取代苯酞类化合物的制备方法与流程
本发明涉及有机化合物和含有机有效成分的医药配制品技术领域,尤其涉及一种手性3-烯丙基取代苯酞类化合物的制备方法。
背景技术:
苯酞及其衍生物是指分子中含有苯并丁内酯结构单元的一类杂环化合物,它们广泛存在于天然产物和具有生理活性小分子中[(a)Xiong,M.-J.;Li,Z.-H.Curr.Org.Chem.2007,11,833-844.(b)Beck,J.J.;Chou,S.C.J.Nat.Prod.2007,70,891-900.(c)Mola,A.D.;Palombi,L.;Massa,A.Curr.Org.Chem.2012,16,2302-2320.]。除此之外,苯酞还是一类非常重要的天然产物以及有机合成中间体[(a)Mal,D.;Pahari,P.Chem.Rev.2007,107,1892-1918.(b)Donner,C.D.Tetrahedron.2013,69,3747-3773.]。特别是3-位取代苯酞类化合物,很多都表现出了良好的生理活性。中国发明专利(申请号:93117148.2申请日:1993-09-09)提供了一种芹菜甲素作为制备预防和治疗脑缺血引起的疾病的药物中的应用,其从芹菜籽油中提取得到的芹菜甲素(3-Butylphthalide),具有抗惊厥、促进大脑感觉缺失症(anesthesia)的愈合以及防治脑细胞缺血症等效果,目前己经被开发成为治疗脑卒中的特效药并且上市销售。化合物Fuscionarin或(-)-Hydrastine通过作用于人类CCR5受体,也就是重要的抗HIV靶点-阿片受体,阻断HIV病毒进入细胞的通道,从而表现出很好的抗HIV的效果[Yoganathan,K.;Rossant,C.;Ng,S.;Huang,Y.;Butler,M.S.;Buss,A.D.J.Nat.Prod.,2003,66,1116-1117.]。化合物(-)-Alcyopterosin E具有很好的细胞毒性[RajuKarmakar.;PallabPahari.;Dipakranjan Mal.Chem.Rev.2014,114,6213-6284.]。
鉴于手性3-取代苯酞类化合物良好的生理活性和广泛的医用价值,开发更多手性3-取代苯酞类化合物已引起了广泛的关注,中国发明专利(申请号:200910045731.7申请日:2009-02-03)公开了一种制备手性3-取代苯酞类化合物的方法,其利用手性双膦配体与镍的配合物催化的不对称串联反应实现,但制备条件繁琐复杂,不利于工业化生产。因此发展新型高效环保、工艺条件简便的制备方法具有极其重要的研究意义。
技术实现要素:
基于以上现有技术的不足,本发明所解决的技术问题在于提供一种工艺条件要求低、操作简便、高效快速、高产率(93%)的手性3-烯丙基取代苯酞类化合物的制备方法,该制备方法能快速高效合成具有一定对映体比例的手性3-烯丙基取代苯酞类化合物。
为了解决上述技术问题,本发明提供一种手性3-烯丙基取代苯酞类化合物的制备方法,以烯丙基硼酸频哪醇酯和邻甲酰基苯甲酸甲酯为原料,以手性磷酸为催化剂,以甲苯或甲苯与四氯化碳的混合溶液为溶剂,分子筛作为添加剂,-60℃或-40℃下反应48h,合成路线如下:
手性磷酸结构式为:
式中:Ar为2,4,6-三异丙基苯基。
作为上述技术方案的优选,本发明提供的一种手性3-烯丙基取代苯酞类化合物的制备方法进一步包括下列技术特征的部分或全部:
作为上述技术方案的改进,所述手性磷酸、烯丙基硼酸频哪醇酯、邻甲酰基苯甲酸甲酯的摩尔比为0.01:6:5。
作为上述技术方案的改进,所述溶剂中,四氯化碳和甲苯的摩尔比为0~2。
作为上述技术方案的改进,所述溶剂为甲苯时,反应温度为-40℃。
作为上述技术方案的改进,先将所述手性磷酸、邻甲酰基苯甲酸甲酯和溶剂混合均匀并冷却到所需温度,然后向混合体系中滴加所述烯丙基硼酸频哪醇酯。
与现有技术相比,本发明的技术方案具有如下有益效果:工艺条件简单,对工艺设备的要求低,成本低,制备过程操作简便,便于工业化生产;制备过程高效快速,产率高达93%,对映体比例高达79:21。
上述说明仅是本发明技术方案的概述,为了能够更清楚了解本发明的技术手段,还可依照说明书的内容予以实施,并且为了让本发明的上述和其他目的、特征和优点能够更明显易懂,以下结合优选实施例,详细说明如下。
附图说明
为了更清楚地说明本发明实施例的技术方案,下面将对实施例的附图作简单地介绍。
图1是本发明优选实施例1所制备产物的核磁氢谱图;
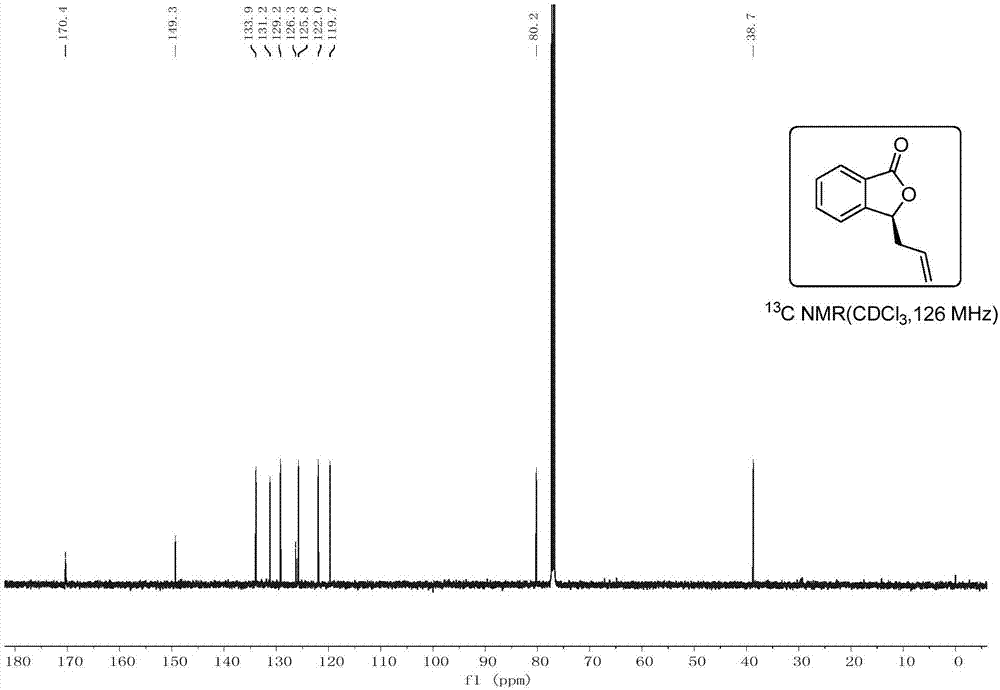
图2是本发明优选实施例1所制备产物的核磁碳谱图。
具体实施方式
下面详细说明本发明的具体实施方式,其作为本说明书的一部分,通过实施例来说明本发明的原理,本发明的其他方面、特征及其优点通过该详细说明将会变得一目了然。
实施例一
在反应瓶中加入手性磷酸(5mol%,3.8mg),分子筛(Molecular Sieve,MS)(50mg),邻甲酰基苯甲酸甲酯(0.1mmol,16mg),混合溶剂(甲苯/四氯化碳=1/1,0.2mL),混合均匀后,冷却至-60℃,滴加烯丙基硼酸频哪醇酯(0.12mmol,20mg),反应48h后,分离纯化得到产物手性3-烯丙基取代苯酞类化合物((R)-3-烯丙基苯并丁内酯),其结构为:
所采用的催化剂具有如下结构:
式中:Ar为2,4,6-三异丙基苯基。
所得产物为白色油状液体,产率为80%,对映体比例为79:21。其中,对映体比例通过手性高效液相色谱仪测定(测试条件:OJ-H手性柱,正己烷/异丙醇=99/1,流速=1.0mL/min,波长=254nm,tmajor=15.45min,tminor=18.35min)。
将所得产物进行核磁共振测试,所得图谱如图1(氢谱)和图2(碳谱)所示。从图1可以看出,1H-NMR(300MHz,CDCl3):δ=7.91(d,J=7.5Hz,1H),7.69(t,J=7.5Hz,1H),7.57-7.47(m,2H),5.85-5.71(m,1H),5.53(t,J=6.0Hz,1H),5.23-5.15(m,2H),2.81-2.62(m,2H),结果与产物结构一致。
从图2可以看出,13C-NMR(75MHz,CDCl3):δ=170.5(1C),149.4(1C),134.0(1C),131.3(1C),129.3(1C),126.3(1C),125.7(1C),122.1(1C),119.8(1C),80.3(1C),38.7(1C),结果与产物结构一致。
实施例二
在反应瓶中加入手性磷酸(5mol%,3.8mg),MS(50mg),邻甲酰基苯甲酸甲酯(0.1mmol,16mg),甲苯(0.2mL),冷却至-60℃,滴加烯丙基硼酸频哪醇酯(0.12mmol,20mg),反应48h后,分离纯化后得到目标产物。
所得产物为白色油状液体,产率为90%,对映体比例为74:26。其中,对映体比例通过手性高效液相色谱仪测定(测试条件:OJ-H手性柱,正己烷/异丙醇=99/1,流速=1.0mL/min,波长=254nm,tmajor=19.09min,tminor=22.08min)。
实施例三
在反应瓶中加入手性磷酸(5mol%,3.8mg),MS(50mg),邻甲酰基苯甲酸甲酯(0.1mmol,16mg),混合溶剂(甲苯/四氯化碳=2/1,0.2mL),冷却至-40℃,滴加烯丙基硼酸频哪醇酯(0.12mmol,20mg),反应48h后,分离纯化得到目标产物。
所得产物为白色油状液体,产率为93%,对映体比例为77:23。其中,对映体比例通过手性高效液相色谱仪测定(测试条件:OJ-H手性柱,正己烷/异丙醇=99/1,流速=1.0mL/min,波长=254nm,tmajor=19.28min,tminor=22.06min)。
本发明所述的手性3-烯丙基取代苯酞类化合物的制备方法简单,设计合理,工艺条件要求低,过程高效快速,产率高,适合大规模工业化生产。
以上所述是本发明的优选实施方式而已,当然不能以此来限定本发明之权利范围,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和变动,这些改进和变动也视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种可见光催化制备n-(2-甲酰基苯基)n-取代甲酰胺衍生物的方法
- 含有色酮结构的吡唑类n‐对硝基苯基马来酰亚胺衍生物及其制备方法与应用
- 含有色酮结构的吡唑类n-苯基马来酰亚胺衍生物及其制备方法与应用
- 一种3-(4-苯基-1h-咪唑-5-基)-1h-吲哚衍生物及其制备方法和应用
- 2-烷氧基-4-((1e,6e)-7-(4-氧代苯基)-3,5-二氧-1,6-庚二烯-1-基)苯酚金属盐衍生物 ...的制作方法
- N-取代苯基丙烯酰胺衍生物及其制备方法和用图
- (2e, 6e)-2-(3,5-二甲氧基苯基亚甲基)-6-(4-氯苯基亚甲基)环己酮及其衍生物的新应用
- 杀真菌的3-{苯基[(杂环基甲氧基)亚氨基]甲基}-杂环衍生物的制作方法
- 作为甲酰肽受体调节剂的苯基氨基甲酸酯衍生物的制作方法
- 杀真菌的3-{苯基[(杂环基甲氧基)亚氨基]甲基}-杂环衍生物的制作方法
- 用于苯乙烯多层结构的粘结层粘合剂的制作方法
- 生物基苯乙烯的用图
- 含六甲基苯环和卤代苯结构的黄原酸酯类化合物、其制备方法及用图
- 含有苯乙烯结构的自组装膜的下层膜形成用组合物的制作方法
- (e)-5-(羟基苯乙烯基)-1,3-二噻吩-2-磺酸酚酯及制备方法和应用
- (e)-3-羟基-5-(羟基苯乙烯基)噻吩-2-磺酸酚酯及制备方法和应用
- (e)-5-(羟基苯乙烯基)-1,3-二吡嗪-2-甲酸酚酯及制备方法和应用
- (e)-5-(羟基苯乙烯基)-1,3-二吡啶-2-甲酸酚酯及制备方法和应用
- (e)-5-(羟基苯乙烯基)-1,3-二呋喃甲酸酚酯及制备方法和应用
- 基于苯乙烯基的化合物、包含该基于苯乙烯基的化合物的着色材料、包含该着色材料的光 ...的制作方法