抗二肽基肽酶4的单克隆抗体及其制备方法和用途与流程
本发明涉及免疫学、药学及医学相关领域。本发明涉及抗二肽基肽酶4(dipeptidylpeptidase4,dpp-4)的单克隆抗体及其制备方法和用途,特别涉及用人二肽基肽酶4的b细胞表位作为半抗原,还特别涉及通过用一个小分子的分子内载体肽来偶联人二肽基肽酶4(dpp-4)的b细胞表位肽来制备多表位肽或抗原肽或肽免疫原并通过合成快速获得,肽免疫原免疫小鼠能产生强免疫应答,可用于制备免疫脾脏淋巴细胞,此免疫脾脏淋巴细胞可用于制备杂交瘤细胞制备单克隆抗体或通过已有技术提取其基因通过抗体库技术或基因工程来制备多种抗体。制备的单克隆抗体特异结合和抑制dpp-4活性,可开发dpp-4检测试剂及dpp-4抑制剂,所述单克隆抗体属于th2亚型抗体(th2亚型抗体在小鼠为igg1亚型抗体,在人为igg2a亚型抗体),此单克隆抗体能抑制dpp-4活性,特异的和dpp-4及含此b细胞表位的肽或蛋白结合,可以开发dpp-4检测试剂及dpp-4抑制剂,所述单克隆抗体为th2型抗体,能特异性识别结合及抑制dpp-4,升高glp-1和胰岛素,降低胰高血糖素,降体内血糖尿酸和肌酐及血脂四项,调节氧化应激,调节免疫平衡由th1趋向th2,降低th17,升高treg,减轻胰腺炎症,保护胰腺肾脏,可用于制备药物用于防治由于血糖和尿酸及肌酐和血脂异常、氧化应激紊乱引起的痛风、肾肝病、糖尿病及并发症、高血脂、as、心血管疾病及th1免疫调节偏高相关疾病,具有重要应用价值。
背景技术:
在1型糖尿病、类风湿性关节炎、多发性硬化及慢性甲状腺炎等疾病中,th1或th1分泌的细胞因子占优势,th1诱导发病,加重病情;向th2漂移则能减轻病症,甚至阻止发病,这与th1/th2的炎性及抗炎性反应有关。基于th1/th2漂移状态与各种疾病的关系,越来越多的研究正倾向于发现、开发能逆转或稳定th1/th2状态的药物和方法。抗原免疫生物,在小鼠体内th1会产生igg2a亚型抗体,th2型则会产生igg1亚型抗体,人类体内th1会产生igg1亚型抗体,th2型则会产生igg2a亚型抗体,th2亚型抗体可以增加th2类细胞因子的产生并控制th1偏高疾病,缓解疾病症状。
二肽基肽酶4又被称为t细胞表面抗原cd26,是一种细胞表面的丝氨酸蛋白酶。人们最早发现dpp4可作为一个治疗2型糖尿病的重要靶点。正是因为其对glp-1、gip等其他肠促胰岛素的降解。glp-1具有葡萄糖依赖性的促胰岛素分泌,抑制胰高血糖素分泌,促进β细胞再生和修复,和延缓餐后胃排空,增加饱足感等功能,gip同样具有促胰岛素分泌功能。然而glp-1、gip等在体内的半衰期只有1-2min,之后迅速被dpp4降解失活。dpp4抑制剂通过竞争性结合dpp4的活化部位,降低酶的催化活性,从而增加体内glp-1和gip的水平达到促进胰岛素分泌的作用,稳定控制血糖,改善β细胞功能,而且不会引起患者体重增加,并可避免低血糖风险。目前多种dpp4抑制剂如西格列汀、沙格列汀等化学合成药,已广泛应用于临床。
目前虽然也有报道dpp4抑制剂用于1型糖尿病(type1diabetesmellitus,t1dm)的治疗,但是由于其是化学药物,常常伴有长期服用副作用强,特别是患有分泌代谢疾病伴有高血压、高血脂和高血糖症的中老年人,长期控制不良导致肾脏受损。而t1dm是一种器官特异性的自身免疫性疾病。患者体内的胰岛素分泌细胞---胰岛β细胞被自身的免疫系统攻击,从而造成体内胰岛素的绝对缺乏,导致持续高血糖与长期代谢紊乱,使全身组织器官,特别是眼、肾、心血管及神经系统的损害及其功能障碍和衰竭。因此需要开发新的dpp4抑制剂,特别是抗体或免疫抑制剂来控制th1偏高疾病如1型糖尿病等,缓解疾病症状。基于dpp-4的b细胞表位并偶联本实验室制备的小分子肽载体获得抗原肽或肽免疫原来制备th2亚型单克隆抗体国内外没有报道。
小肽-载体蛋白偶联多用于制备抗多肽类抗体,单独的多肽通常太小不足以激起充分的免疫反应,因此通过用小分子b细胞表位或肽半抗原和载体蛋白偶联或融合后成为抗原肽免疫生物获得免疫脾脏淋巴细胞,用于制备杂交瘤细胞来制备单克隆抗体或通过提取免疫脾脏淋巴细胞基因用噬菌体抗体库或基因工程等来制备多种抗体。最普遍使用的载体是钥孔血蓝蛋白(klh,keyholelimpethemocyanin)比牛血清白蛋白(bsa)有更高的免疫原性,因而是最常被选用的载体蛋白。免疫系统是将此肽-蛋白作为一个整体来激起免疫反应的,因而产生的抗体中有针对多肽的,有针对链接剂的,也有针对载体蛋白的,因此后期产生过多种类抗体使筛选需要的抗体变得较为困难,此外,b表位等小分子肽和klh或blh偶联免疫后产生的抗体以th1抗体偏多,而th2抗体少于th1抗体,用于连接b细胞表位或肽半抗原形成的免疫原及其用来制备的抗体不太适合治疗th1偏高的疾病(如1型糖尿病及并发症和相关疾病,动脉粥样硬化,心血管病、老年痴呆、肾脏病,肾炎,类风湿性关节炎,反应性关节炎,多发性硬化,自身免疫性甲状腺炎,接触性皮炎,结节性红斑,习惯性流产等等)效果不佳。
本发明的单克隆抗体的制备是以dpp-4的b细胞表位为半抗原,与本实验室制备的分子内佐剂肽偶联,设计合成多表位肽作为抗原肽或肽免疫原,通过此类肽免疫原直接免疫生物制备获得免疫脾脏淋巴细胞,此分子内佐剂由hsp60的437~460位的一段24个氨基酸特异性多肽p277肽的主要th2表位p2肽段(448~460)和胰岛细胞特异抗原-胰岛素瘤相关蛋白(insulinomaassociatedprotein-2,ia-2)的近膜区jm2的626~630位的线形序列是一个b细胞表位(626feyqd630),命名其为ia2(5),通过连接肽组成,目前没有用p2和ia2(5)组成的载体肽来偶联小肽制备单克隆抗体抗体及其用途的报道。
本发明涉及免疫、药学及医学相关领域,涉及人二肽基肽酶4(dpp-4)的b细胞表位及含此类表位的肽免疫原以及偶联蛋白或表达的融合蛋白免疫原免疫动物后的血清含有高水平的能和特异性结合的th2抗体,能用于制备多抗、单克隆抗体和基因工程抗体等,还涉及基于人天然dpp-4的b细胞表位的改构肽及含有此类表位肽的肽免疫原以及偶联蛋白或表达的融合蛋白免疫原免疫动物后的血清含有高水平的能和二肽基肽酶4特异性结合的th2抗体,也能用于制备多抗、单克隆抗体和基因工程抗体等,还涉及含dpp4的b细胞表位和改构表位肽的免疫原及偶联蛋白、组合物或表达的融合蛋白用于制备防治糖尿病特别是1型糖尿病及其并发症等相关疾病的抗体特别是单克隆抗体和基因工程抗体,制备的抗体也能用于制备药物防治糖尿病及其并发症等相关疾病药物和开发检测含此类表位肽的抗原的用途。
技术实现要素:
发明目的:
有鉴于此,本发明的目的之一在于提供具有一种特异性结合二肽基肽酶4(dpp-4)的单克隆抗体mab及其制备方法和其在医药和免疫学上的用途。
本发明的目的之二提供了一种dpp-4鼠单克隆抗体mab的杂交瘤细胞株,分类命名为:杂交瘤细胞株cpultm-4e9;保藏于中国武汉市武昌区八一路299号武汉大学校内的中国典型培养物保藏中心,保藏日期为2017年10月24日,保藏编号为cctccno:c2017227。
本发明的目的之三还提供了一种抗dpp-4的单克隆抗体mab(命名为cpu-kd4),此单克隆抗体由上述杂交瘤细胞株产生。
基于上述获得的杂交瘤细胞株cpultm-4e9及分泌的单克隆抗体cpu-kd4可用测序技术获得重链可变区vh序列和轻链可变区vl序列,及其vh的3个cdr区的序列和vl的3个cdr区的序列,上述序列均包括氨基酸序列和核苷酸序列及其基于上述序列的应用。
获得的上述氨基酸序列和核苷酸序列也可以用于重组微生物和转基因动物或植物及其细胞,使它们作为生产工厂生产抗体或用于改造。
基于上述氨基酸序列或核苷酸序列及基于其获得的重组微生物和转基因动物或植物及其细胞,制备免疫原和制备免疫脾脏淋巴细胞来制备抗体,用于开发各种药学上可以接受的药物或组合物或偶联物或聚合物。
本发明提供了所述单克隆抗体cpu-kd4的制备方法按照如下步骤实现:
(1)免疫原和免疫淋巴细胞的制备:将ia2(5)肽段feyqd(氨基酸序列见seqidno.1)的c端和th2表位p2肽段(氨基酸序列见seqidno.2)的n端通过柔性肽或连接肽(由相同或不同氨基酸及不同数量的氨基酸组成)连接形成载体肽,命名为ia2(5)-p2-1(简写为ip)再和b细胞表位或合成肽半抗原(以b表示)的c端通过柔性肽或连接肽共价连接,形成多表位肽或叫抗原肽或叫肽免疫原b-ia2(5)-p2-1(简写为b-ip),本专利的b为二肽基肽酶4的b细胞表位o(氨基酸序列见seqidno.3),肽免疫原d41-ia2(5)-p2-1(氨基酸序列见seqidno.4)可以通过化学合成获得,此肽不需偶联bsa或klh,可直接作为免疫原免疫小鼠能产生强免疫应答,是此结构中的分子内载体肽显著增强连接的b细胞表位或合成肽半抗原的免疫原性,用此肽免疫原免疫生物体制备用于制备杂交瘤的免疫脾脏淋巴细胞,免疫脾脏淋巴细胞可用于制备杂交瘤细胞来制备单克隆抗体或通过提取免疫脾脏淋巴细胞基因通过抗体库或基因工程来制备多种抗体。抗原肽可用于筛选杂交瘤细胞克隆。在本专利中b细胞表位来自人dpp-4。获得的免疫脾脏淋巴细胞可以产生和dpp-4特异结合的抗体。进一步,以此人dpp-4的b细胞表位和klh偶联获得d41-klh,用同样方法来免疫来balb/c小鼠,d41-klh免疫后产生大于10000效价的免疫血清(含th1和th2型抗体,th1稍微多一点),而本发明的d41-ia2(5)-p2-1免疫后也能产生大于10000效价(th2抗体占绝对优势且高于d41-klh同样免疫产生的th2抗体),因此,同样免疫条件下,在制备th2抗体上采用b-ia2(5)-p2-1免疫balb/c小鼠制备免疫脾脏淋巴细胞来制备抗体。
(2)杂交瘤技术制备单克隆抗体cpu-kd4:进一步,将上述肽免疫原d41-ia2(5)-p2-1免疫balb/c小鼠获得的免疫脾脏淋巴细胞和sp2/0骨髓瘤细胞融合制备杂交瘤细胞,有限稀释法获得单克隆,抗原肽elisa法筛选阳性杂交瘤细胞,获得能分泌抗dpp-4特异性抗体的杂交瘤细胞株,命名为杂交瘤细胞株cpultm-4e9,elisa亚型鉴定为igg1(在小鼠为th2抗体),采用动物体内生产单抗的方法生产抗体,辛酸-硫酸铵沉淀法可以回收大部分的单抗,proteing柱层析进一步纯化获得单克隆抗体cpu-kd4。分别通过westernblot,亚型和效价测定实验,抑制dpp-4活性实验,治疗糖尿病小鼠实验来验证此方法制备的单克隆抗体的特异性和用途。
上述肽免疫原也可以用于重组微生物和转基因动物或植物及其细胞,使它们作为生产工厂,生产含上述肽免疫原的融合蛋白、偶联蛋白或偶联物、聚合物、组合物来免疫生物制备抗dpp-4的抗体和产生此抗体的免疫脾脏淋巴细胞。
进一步,还包含免疫学上可接受的载体和佐剂或者药学上可接受的辅料,包括但不限于:热休克蛋白hsp60/65、门冬酰胺酶、门冬酰胺酶-ttp、门冬酰胺酶-ttp-cetpc,fc,牛血清白蛋白(bsa),钥孔血蓝蛋白(klh),聚乙二醇,弗氏佐剂、铝佐剂、乳糖、蔗糖、葡萄糖、淀粉、纤维素类(如羧甲基纤维素、羟丙甲基纤维素等)、乙二醇、豆油、芝麻油等,来免疫生物制备抗dpp-4的抗体和产生此抗体的免疫脾脏淋巴细胞。
本发明的有益效果在于:
dpp-4的优势b细胞抗原表位成分单一,结构简单,摆脱天然dpp-4中的不良表位的影响,免疫反应针对性强,筛选杂交瘤简单。
本发明的抗原肽或肽免疫原中包含一种特异性分子内佐剂,该分子内佐剂由ia2(5)肽段feyqd的c端和th2表位p2肽段的n端通过柔性肽或连接肽连接形成载体肽,命名为ia-2(5)-p2-1(简写为ip),其再和b细胞表位或合成肽半抗原(以b表示)的c端通过柔性肽或连接肽共价连接,形成肽免疫原或抗原肽b-ia2(5)-p2-1(简写为b-ip),肽免疫原可以通过化学合成简单获得,在此结构中的分子内载体肽可以显著增强连接的b细胞表位或合成肽半抗原的免疫原性,易诱导产生th2类型的抗体,并且能成功制备单克隆抗体,杂交瘤细胞筛选简单,具有重要理论价值和广阔应用前景。
采用上述肽免疫原或抗原肽免疫生物体制备用于制备杂交瘤的免疫脾脏淋巴细胞,和以此人dpp-4的b细胞表位和klh偶联获得d41-klh,用同样方法来免疫来balb/c小鼠比较,d41-klh免疫后产生含th1和th2型抗体,而th1稍多一点,而本发明的d41-ia2(5)-p2-1免疫后也能产生大于10000效价而th2抗体占绝对优势且高于d41-klh产生的th2抗体,同样免疫条件下,在制备th2抗体上采用b-ia2(5)-p2-1类肽免疫原如41-ia2(5)-p2-1免疫balb/c小鼠获得的免疫脾脏淋巴细胞具有优势,此免疫脾脏淋巴细胞可用于制备杂交瘤细胞来制备单克隆抗体或通过提取免疫脾脏淋巴细胞基因来制备多种抗体。抗原肽可用于筛选杂交瘤细胞克隆。本专利制备获得的th2亚型单克隆抗体mab(命名为cpu-kd4)可以与含此b细胞表位或肽半抗原的目标抗原蛋白如dpp-4特异结合,可以开发特异检测试剂,可以抑制目标蛋白如dpp-4的酶活性,显著调节th1/th2平衡失调由th1偏向th2转移,能特异性识别结合抑制dpp-4,能显著升高glp-1,胰岛素,降低胰高血糖素,降体内血糖尿酸和肌酐及血脂四项,调节氧化应激,调节免疫平衡由th1趋向th2,降低th17,升高treg,增加尿酸和肌酐排泄,减轻胰腺炎症,保护胰腺肾脏,显著增强抗氧化能力,显著改善疾病的发病症状,可制备药学上可接受的药物用于防治高血脂、as、高尿酸症和糖尿病及并发症,防治th1/th2免疫平衡异常、th17异常、尿酸及肌酐异常、氧化应激紊乱引起的肾炎,痛风、肝病、高血脂、动脉粥样硬化、糖尿病及并发症、老年痴呆,眼病,心血管等th1偏高疾病。.根据本专利制备合成肽免疫原,再制备免疫脾脏淋巴细胞,再制备特异性单克隆抗体或特异抗体在治疗代谢性疾病中的开创性理论思路及实际应用具有重要意义。
保藏信息
用于保藏的dpp-4鼠单克隆抗体的杂交瘤细胞株的分类命名为:杂交瘤细胞株cpultm-4e9;
保藏单位名称:中国典型培养物保藏中心;
保藏单位简称:cctcc;
保藏单位地址:中国武汉市武汉大学;
保藏日期:2017年10月24日;
保藏编号:cctccno:c2017227。
附图说明
为了使本发明目的,技术方案和优点清楚,结合附图对本发明进行进一步详细描述,其中:
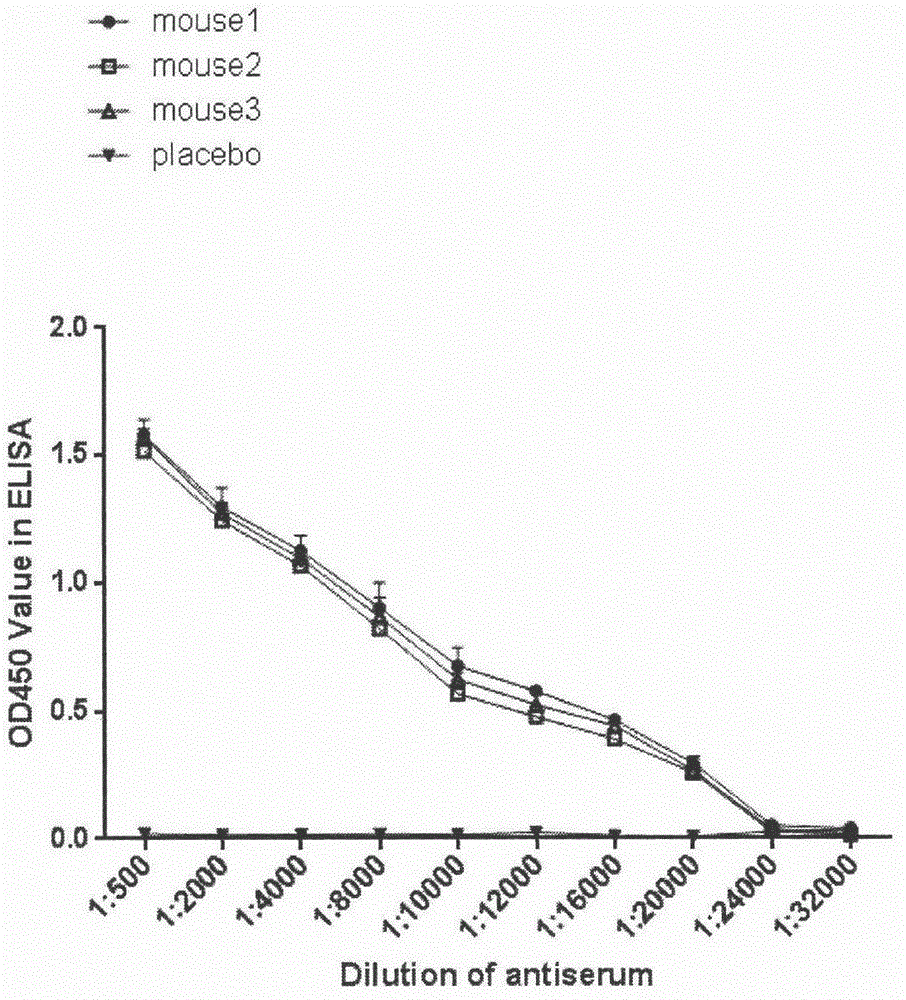
图1是本抗原肽或肽免疫原免疫小鼠后elisa测定鼠抗血清效价。
图2是本发明单克隆抗体mab(cpu-kd4)sds-page电泳图,其中m是蛋白分子量标准(kda),泳道1-6分别为制备及proteing柱纯化后抗体部分,免疫小鼠抗血清,原腹水,阳性杂交瘤细胞上清,辛酸-硫酸铵纯化后抗体,proteing纯化后抗体。
图3是本发明单克隆抗体亚型鉴定图。
图4为本发明单克隆抗体mab(cpu-kd4)与dpp-4特异结合的westernblot结果。
图5是本发明单克隆抗体抑制dpp-4活性的曲线。
图6为本发明单克隆抗体对stz诱导的糖尿病模型小鼠的降血糖效果
图7为本发明单克隆抗体对stz诱导的糖尿病模型小鼠的降尿酸、肌酐效果(图7a为血清尿酸变化,图7b为尿液尿酸变化,图7c为尿液肌酐变化)。
图8为本发明单克隆抗体对stz诱导的糖尿病模型小鼠的总抗氧化和降mda效果(图8a为总抗氧化效果,图8b为mda变化)。
图9为本发明单克隆抗体对stz诱导的糖尿病模型小鼠的治疗后脾脏细胞elisa检测细胞因子结果(图9a为il-10,图9b为ifn-γ),和流式检测th17和treg表达的结果(图9c为treg表达,图9d为th17表达)。
图10为本发明单克隆抗体对stz诱导的糖尿病模型小鼠的治疗后减轻胰腺炎症效果(图10为he染色检测胰腺的炎症病理分析图)。
具体实施方式
以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改或替换,均属于本发明的范围。
若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
实施例1:免疫用肽免疫原或抗原肽的制备:
将ia2(5)肽段feyqd(氨基酸序列见seqidno.1)的c端和th2表位p2肽段(氨基酸序列见seqidno.2)的n端通过柔性肽或连接肽连接形成载体肽,命名为ia2(5)-p2-1(简写为ip)再和人dpp-4的b细胞表位d41(以b表示,d41是dpp-4的一段多肽序列88vflenstfde97,共10个氨基酸残基,氨基酸序列见seqidno.3)的c端通过柔性肽或连接肽共价连接,形成肽免疫原b-ia2(5)-p2-1(本专利是d41-ia2(5)-p2-1,氨基酸序列见seqidno.4),肽免疫原或抗原肽均采用fmoc固相合成法合成,hplc检测纯度>90%。分析用b细胞表位d41采用fmoc固相合成法合成,hplc检测纯度>95%,b细胞表位d41再和传统载体蛋白klh或bsa偶联形成d41-bsa、d41-klh。
实施例2:动物免疫及杂交瘤细胞的制备
动物免疫和免疫脾脏淋巴细胞的制备:上述抗原肽以quickantibody-mouse5w佐剂乳化,与0.9%注射用生理盐水1∶1混匀,采用肌肉注射方法免疫6-8周龄balb/c小鼠,免疫剂量为100μg/只,间隔两周后用相同的免疫方法及剂量进行第二次免疫。免疫两次后眼眶取血以elisa法梯度稀释测定血清效价,选取抗体效价最高的小鼠的免疫脾脏淋巴细胞进行细胞融合。结论:上述抗原肽免疫小鼠后产生较高的效价(大于1∶10000),并可用以单克隆抗体的制备(图1)。
细胞融合:骨髓瘤细胞采用balb/c小鼠来源的sp2/0,融合时处于对数生长期;取上述免疫的小鼠脾脏,制成淋巴细胞单细胞悬液;免疫小鼠脾淋巴细胞与骨髓瘤细胞以1∶5-1∶10混合,滴加37℃的50%peg(ph8.0)1ml,加入不完全培养基及其余终止液,离心弃上清后加入hat培养基悬浮混匀,定容到50ml,分装到96孔细胞培养板中,置于37℃、5%co2恒温培养箱中进行培养。
筛选和克隆:融合7-10天内挑选细胞克隆,使用纯化的偶联bsa的dpp-4的b细胞表位肽和抗原肽进行elisa测试,标记细胞株号。对阳性孔细胞进行有限稀释,每次有限稀释后5-6天测定elisa值,挑取od450阳性值较高的单克隆孔进行有限稀释,直至elisa测定96孔板全板结果为阳性,挑取阳性值高的单克隆单株。
实施例3:单克隆抗体mab(命名为cpu-kd4)制备及纯化
小鼠单克隆抗体腹水的制备:采用动物体内生产单抗的方法。每只balb/c小鼠腹腔注射灭菌液体石蜡0.5ml,7天后,每只小鼠腹腔注射1×106个小鼠杂交瘤细胞。7天后观察小鼠腹水生产情况,如腹部明显膨大,即可抽取腹水。腹水中含有红细胞、细胞碎渣、纤维蛋白凝块以及脂质。先以低速离心去除沉淀细胞,再高速离心去除细胞残渣和小颗粒物质,用0.2μm微孔滤膜取出纤维蛋白凝块和脂质。
辛酸-硫酸铵沉淀法:初步纯化的腹水,以辛酸-硫酸铵沉淀法粗提免疫球蛋白,沉淀透析除去硫酸铵。
proteing柱层析纯化抗体:辛酸-硫酸铵沉淀法可以回收大部分的单抗,进一步用proteing结合抗体,测定各收集管中的蛋白含量,合并蛋白管;pbs透析,其后根据抗体的稳定性,加入防腐剂(0.020g/l叠氮钠),置4℃或冷冻保存。
实施例4:单克隆抗体mab(命名为cpu-kd4)的性质检测
实施例4-1:抗体纯度检测:利用sds-page方法鉴定纯化后单克隆抗体的纯度,如图2所示,单克隆抗体仅出现两条电泳条带,说明该单克隆抗体纯度高。结果表明,单克隆抗体分子量约160kda,由两条约55kda重链和两条约25kda的轻链组成。
实施例4-2:抗体亚类鉴定:采用间接elisa法,使用抗小鼠各种ig亚型的抗体鉴定上述杂交瘤细胞产生的抗体的ig亚型,结果显示igg1信号最强,本发明单克隆抗体亚型为igg1(图3)。
实施例4-3:抗体westernblot检测:将预染蛋白marker和纯化购买的dpp-4进行12%的sds-page分离。电泳结束后,取下电泳凝胶放入转移平衡缓冲液中平衡10-15min。切好的滤纸也放入转移缓冲液中浸润。将电泳凝胶叠放在铺好的三层滤纸上,将硝酸纤维素膜放在电泳凝胶上,将剩余的3张滤纸依次叠放在硝酸纤维素上,将转移盒装入盛有转移缓冲液的转移仪中,膜侧靠阳极,凝胶侧靠阴极,4℃层析柜中30v转移过夜。取出膜,将硝酸纤维素膜放入丽春红s染料中染色5min后于水中脱色,使完全脱色。将膜放入盛有5ml封闭液的小平皿中摇动1h。移去封闭液,加入5ml用封闭液稀释好的单克隆抗体1h,取出膜,放入较大平皿中,用200ml的ttbs洗4次,将膜移入小平皿中,加入5ml用封闭液稀释辣根过氧化物酶标记的二抗1h。放入较大平皿中,用200ml的ttbs洗4次,每次10-15min。取出膜放入现配的dab显色液中显色10-15min。取出晾干,拍照。
结论:本发明单克隆抗体仅特异性结合二肽基肽酶4(dpp-4)蛋白,而与其他蛋白无交叉反应(图4)。
实施例4-4:抗体体外dpp-4活性抑制率鉴定
dpp-4购于国外生物公司(进口分装)。抑制dpp4酶活性的抑制率检测实验原理为发色底物法。dpp4水解gly-pro-pna,生成pna(黄色),pna在405nm处有特征性吸收峰,通过酶标仪在405nm处测得吸光度值,来反应酶活性的高低(即各组血清中抗体对dpp4抑制程度的大小)。具体实验步骤为:1.将血清,缓冲液,酶于37摄氏度下分别孵育30分钟;2.按照酶,缓冲液,底物的顺序加入96孔板。总反应体系为100ul,分为空白对照组(0.26mmol/l底物5ul;tris-hcl缓冲液95ul),阴性对照组(0.5u/ldpp410ul;0.26mmol/l底物5ul;tris-hcl缓冲液85ul),阳性对照组(0.5u/ldpp410ul;0.26mmol/l底物5ul;5倍稀释的各组血清10ul;tris-hcl缓冲液75ul),阳性空白组(0.26mmol/l底物5ul;5倍稀释的各组血清10ul;tris-hcl缓冲液85ul)。3.37℃恒温培养箱反应60min,测定405nm处的吸光度。4.比较各组od405的值,或计算抑制率。
抗体对dpp-4抑制率的计算
抑制率的计算公式如下:抑制率(%)=(od阴性对照-od空白对照)-(od抑制剂-od抑制剂空白对照)/(od阴性对照-od空白对照)x100%。
如图5所示,抗体mab(cpu-kd4)具有显著体外抑制dpp-4酶活性作用,半数抑制率ic50为21.6μg/ml。
实施例5:抗dpp-4的鼠单克隆抗体cpu-kd4的抗体测序:
单克隆抗体cpu-kd4的vh和vl区的测序和cdr区的获得方法:
测序主要步骤如下:
(1)takararna抽提试剂盒提取杂交瘤细胞株cpultm-4e9的rna。
(2)由抽提出的rna,通过5’race反转录cdna,再进行轻链重链pcr扩增可变区基因(pcr仪型号:thermofisher2720),分别设计重链和轻链扩增引物,pcr结果显示kappa和igg引物扩增出目标条带,表明轻链为kappa链,重链为igg链。
(3)回收(j-e贝克曼离心机)相应pcr产物,分别与puc57/ecorv酶切载体平连后菌检获得重链及轻链可变区基因克隆并进行重链可变区vh和轻链可变区vl核苷酸序列测定。
使用seqman软件分析测定的序列,剔除非功能抗体基因,用imgt和snapgene分析蛋白序列获得单克隆抗体cpu-kd4的重链可变区vh和轻链可变区vl的序列。
(4)将seaman分析的单克隆抗体cpu-kd4的vh和vl区的序列再使用imgt在线分析即分别得到抗体vh和vl区中的cdr区序列。
实施例6:stz诱导的糖尿病模型建立及单克隆抗体cpu-kd4治疗模型效果测定:
实施例6-1:stz诱导的糖尿病模型的建立
4周龄雄性c57bl/6j小鼠(购自扬州大学比较医学中心,许可证号:scxr(苏)2012-0004。)用0.1mph4.4柠檬酸盐缓冲液配置stz浓度为7.5mg/ml,按50mg/kg剂量腹腔注射,每日1次,连续注射5次,于造模后第3、7、14天测定血糖值,以空腹血糖连续两次≥11.1mmol/l为成模标准。每周一次静脉给以上述制备的单克隆抗体药(25mg/kg)1h后,于小鼠眼眶后静脉丛采血,全血于2500r/min离心3min,离心后上层血清置于-70℃冰箱中保存备用。
实施例6-2:治疗糖尿病stz模型动物实验:
1分组实验:30只stz诱导糖尿病模型小鼠随机分成4组,每组10只,分别为:模型组(即溶剂组)给以pbs缓冲液,normal组为正常小鼠组,mab为抗体组每周给药1次,给药量为500μg/只/次,阳性药组西格列汀为每天口服给药1次。给药量为350μg/只/次。在模型成功(以血糖≥11.1mmol/l为准)后第2周第一次给药,之后每周给药1次,到13周。
2.血糖检测:糖尿病小鼠模型建立后,给药到第13周,采用断尾取血的方法用血糖仪定期测定小鼠的血糖。经stz造模的c57bl/6j雄性小鼠给予抗体后,小鼠的血糖变化情况如图6所示。实验结果表明,抗体cpu-kd4能显著降低糖尿病小鼠血糖,与溶剂组相比具有极显著差异(**p<0.01)。
3.糖耐量实验中胰岛素测定
在第9次免疫后,测定给药组和对照组小鼠的葡萄糖耐量情况。每组取6只小鼠,每只小鼠的血糖值在本组平均血糖值附近。小鼠禁食不禁水16h后,每只小鼠腹腔注射剂量为2g/kg的葡萄糖溶液。葡萄糖溶液的浓度为400mg/ml,体重20g的小鼠注射剂量为0.1ml。注射葡萄糖后0min,15min,30min,60min,120min,180min,240min,300min采用尾静脉取血的方式测定小鼠的血糖值。并在注射完葡萄糖后15min时取血,elisa测定血清胰岛素水平,具体的实验步骤按照试剂盒说明书进行,大致的操作流程如下:1、每孔加入50μl标准品,或者5倍稀释的血清。2、每孔加入100μl酶标二抗,保鲜膜缠绕后37℃孵育60min。3、washsolution满孔洗板4次。4、每孔加入50μl底物a和50μl底物b,轻轻混匀,37℃避光孵育15min。5、每孔加入50μl终止液(2mol/lh2so4)(颜色由蓝变黄)6、15min内在450nm波长处测定od值。7、通过标准曲线计算样品insulin水平。结果显示:500ug/只抗体给药组血清中胰岛素明显高于placebo组,结果具有显著性差异(**p<0.01),机体血糖调节能力显著改善好转。
3.尿酸检测:给药治疗后眼静脉从取血,室温静置待血液凝固后,4000r/min离心10min两次后分离血清,-70℃冻存。采用磷钨酸还原法测定血清中尿酸(sua)水平,按照南京建成相应试剂盒说明书进行测定。结果如图7a所示,抗体给药组具有显著的降尿酸效果,与溶剂组相比具有极显著差异(**p<0.01)。
4.尿液的尿酸肌酐检测:收集尿液,检测尿酸和肌酐含量结果如图7b和7c所示,抗体给药组具有显著的增加尿液尿酸(***p<0.001)和肌酐(**p<0.01)效果,与溶剂组相比具有极显著差异,说明抗体可增加尿酸肌酐排泄。
5.治疗后小鼠血清中总抗氧化能力(t-aoc)的测定
高尿酸小鼠模型建立后,每周最后一次给药后1h眼静脉从取血,室温静置待血液凝固后,4000r/min离心10min两次后分离血清,-70℃冻存,按照相应试剂盒说明书测定血清中总抗氧化能力(t-aoc)水平和mda水平。分别如图8a和8b所示,抗体给药组可以明显的减轻机体的氧化应激,与模型组相比具有极显著差异(**p<0.01)。
6.细胞因子检测
观测期结束后,取各组小鼠脾细胞进行培养,72h后离心细胞培养板,保留各组上清培养液。用elisa试剂盒分别检测ifn-γ和il-10等细胞因子水平。具体操作按试剂盒使用说明书进行。结果显示,与模型组相比,抗体给药组小鼠炎症因子ifn-γ(th1型细胞因子代表,图9b)水平明显下降,il-10(th2型细胞因子代表,图9a)明显升高,具有极显著差异(**p<0.01),而小鼠脾脏细胞中th1与th2分别通过分泌ifn-γ及il-10等细胞因子发挥各自免疫应答反应,说明抗体给药后,小鼠体内免疫调节类型由th1型转变为th2型。
7.为单克隆抗体免疫治疗模型小鼠后脾脏细胞th17、treg含量分析鉴定;
动物实验结束时,取实验组和对照组动物组织新鲜脾脏,常规处理制备脾脏细胞,按照流式分析常规方法进行标记,洗涤,检测treg(图9c)和th17(图9d)量。结果显示:单克隆抗体免疫治疗模型小鼠后treg细胞量显著增加,th17显著降低。
8.治疗后胰腺he染色及病理学观察
观察结束时,取各组小鼠胰腺,经10%福尔马林溶液固定24~72h,常规取材,脱水,石蜡包埋,制片(4μm厚切片),苏木精-伊红(he)染色。如图10所示,与模型组小鼠相比,抗体给药组小鼠的胰腺炎症程度显著减轻,说明该抗体对小鼠的胰腺具有较好的抗炎和保护作用。
实施例7.单克隆抗体cpu-kd4治疗1型糖尿病nod小鼠的效果:
实施例7-1.nod小鼠1型糖尿病模型。
雌性nod小鼠,鼠龄4~5周,体重18-20g,由北京华阜康生物科技有限公司提供scxk(京)2014-0004.
实施例7-2.动物免疫实验
1.模型建立:20只糖尿病模型小鼠随机分成2组,每组10只,分别为:placebo组(溶剂对照组,阴性对照组)、抗体给药组,每周一次静脉给上述制备的单克隆抗体药(25mg/kg)后,于小鼠眼眶后静脉丛采血,全血于2500r/min离心3min,离心后上层血清置于-70℃冰箱中保存备用,模型组(即溶剂组)给pbs缓冲液。
2.抗体组治疗糖尿病小鼠血糖和尿酸及肌酐和mda检测:在模型成功(以血糖≥13.19mmol/l为准)后每周给药1次,持续给药到34周。每次免疫前将糖尿病小鼠断尾取血,取血时用血糖监测仪检测小鼠血糖水平。结果如表1所示,结果表明,与溶剂组比较,抗体组显著降低糖尿病小鼠血糖和尿酸及肌酐和mda,具有统计学差异。可以开发用于治疗糖尿病及并发症。
表1单克隆抗体cpu-kd4治疗nod1型糖尿病nod小鼠的血糖、尿酸肌酐和mda检测
结论:本发明抗体是由小分子免疫调节肽或抗原肽或肽免疫原免疫小鼠后制备得到的针对dpp-4单个b细胞表位d41的单克隆抗体cpu-kd4,具有较高的纯度及特异性,并产生高效的抑制dpp-4的酶活性的作用,显著降低血糖同时对糖尿病模型小鼠具有显著降血清尿酸肌酐和血脂四项,增加尿酸肌酐排泄、缓解氧化应激、减轻胰腺炎症,保护胰腺肾脏、调节th1向th2免疫调节类型转变的效果,可用于糖尿病尤其是1型糖尿病效果显著基本能保持血糖正常值,降低死亡率,也对尿酸肌酐血脂异常、氧化应激紊乱引起的痛风、肝病、高血脂、动脉粥样硬化、糖尿病及并发症、老年痴呆,眼病,心血管疾病以及th1型免疫调节偏高相关疾病等上具有重要的应用价值;同时该抗体可结合dpp-4,可开发检测dpp-4的试剂。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管通过参照本发明的某些优选实施例已经对本发明进行了描述,但本领域的普通技术人员应当理解,可以在形式上和细节上对其作出各种各样的改变,而不偏离所附权利要求书所限定的本发明的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!