以CEA为靶点的嵌合抗原受体的制作方法
本发明涉及生物医学领域,具体而言,涉及一种以cea为靶点的嵌合抗原受体。
背景技术:
car-t(chimericantigenreceptort-cellimmunotherapy),即嵌合抗原受体t细胞免疫疗法。该疗法是一种出现了很多年但近几年才被改良使用到临床中的新型细胞疗法。在急性白血病和非霍奇金淋巴瘤的治疗上有着显著的疗效,被认为是最有前景的肿瘤治疗方式之一。正如所有的技术一样,car-t技术也经历一个漫长的演化过程,正是在这一系列的演化过程中,car-t技术逐渐走向成熟。
这种新的治疗策略的关键之处在于识别靶细胞的被称作嵌合抗原受体(car)的人工受体,而且在经过基因修饰后,病人t细胞能够表达这种car。在人体临床试验中,科学家们通过一种类似透析的过程提取出病人体内的一些t细胞,然后在实验室对它们进行基因修饰,将编码这种car的基因导入,这样这些t细胞就能够表达这种新的受体。这些经过基因修饰的t细胞在实验室进行增殖,随后将它们灌注回病人体内。这些t细胞利用它们表达的car受体结合到靶细胞表面上的分子,而这种结合触发一种内部信号产生,接着这种内部信号如此强效地激活这些t细胞以至于它们快速地摧毁靶细胞。
近年来,car-t免疫疗法除了被用来治疗急性白血病和非霍奇金淋巴瘤之外,经改进后,也被用来治疗实体瘤、自身免疫疾病、hiv感染和移植排斥等疾病,具有更广阔的应用空间。
癌胚抗原(carcinoembryonicantigen,cea)又称ceacam-5或cd66e,是一种重要的肿瘤相关抗原。在人体上皮细胞恶性肿瘤、90%的胃肠道肿瘤、胰腺癌、80%以上的非小细胞肺癌和50%左右的乳腺癌中,都有cea的高表达,即上述肿瘤呈cea阳性。但由于cea的抗原性很弱,不能有效地激活机体的特异性免疫反应,使得肿瘤细胞能够逃避免疫杀伤,导致这类肿瘤患者的死亡率较高。到目前为止,现有技术中在检测治疗cea靶点的car-t技术方面仍然很少,car在提升与cea靶点结合的灵敏度、特异性,以及更好地激活t细胞方面还有很大的技术空间。
有鉴于此,特提出本发明。
技术实现要素:
本发明涉及一种以cea为靶点的嵌合抗原受体,其由n端到c端顺次包括抗原结合区、il-10r1胞外域、il-15rβ链、共刺激结构域以及t细胞信号传导区功能结构域;
所述抗原结合区具有的重链互补决定区cdr-vh1、cdr-vh2、cdr-vh3的序列依次如seqidno:1~3所示,轻链互补决定区cdr-vl1、cdr-vl2、cdr-vl3的序列依次如seqidno:4~6所示。
与现有技术相比,本发明的有益效果为:
1、与传统肿瘤治疗方法相比,该方法副作用小。
2、il-15受体由α链、β链和γ链组成,其中β链和γ链与il-2共用;将il-10r1胞外域与il-15rβ链组成嵌合受体,car-t达到病灶后,会接触肿瘤微环境中的il-10,继而会使il-2/il-15促炎信号通路得以激活,提高car-t的杀伤效果和持久力。
3.抗原结合区具有很高的活性,且能够避免ca125配体对cea靶点结合的影响。
附图说明
为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
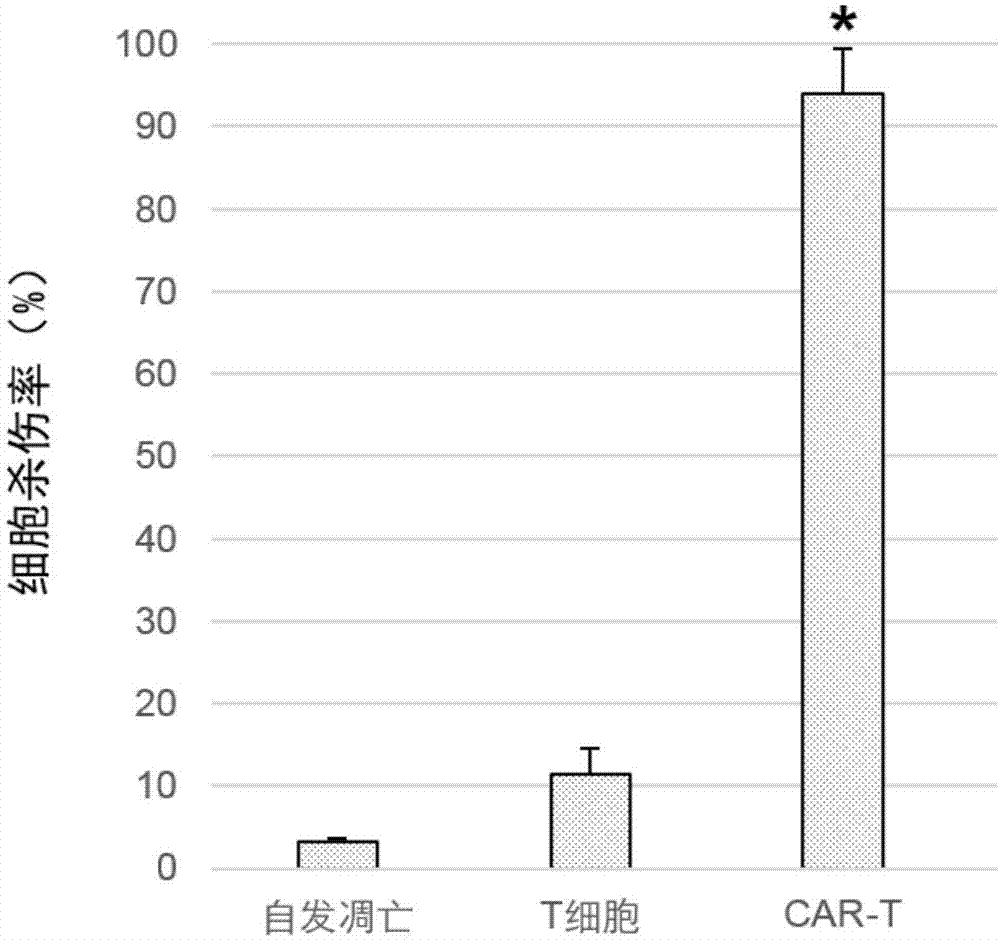
图1为本发明一个实施例中将cea-car片段和cea-car-control片段转染t细胞制备得到的car-t细胞进行体外杀伤对比;anova,*p<0.05,vst细胞组;
图2为本发明一个实施例中car-t细胞的体内验证;two-wayanova,*p<0.05,vspbs。
具体实施方式
本发明涉及一种以cea为靶点的嵌合抗原受体,其由n端到c端顺次包括抗原结合区、il-10r1胞外域、il-15rβ链、共刺激结构域以及t细胞信号传导区功能结构域;
所述抗原结合区具有的重链互补决定区cdr-vh1、cdr-vh2、cdr-vh3的序列依次如seqidno:1~3所示,轻链互补决定区cdr-vl1、cdr-vl2、cdr-vl3的序列依次如seqidno:4~6所示。
优选的,如上所述的嵌合抗原受体,所述il-10r1胞外域的序列如seqidno:7所示。
优选的,如上所述的嵌合抗原受体,所述il-15rβ链的序列如seqidno:8所示。
优选的,如上所述的嵌合抗原受体,所述共刺激结构域选自cd27,cd28,4-1bb,ox40,cd30,cd40,pd-1,lfa-1,cd2,cd7,light,nkg2c,b7-h3蛋白分子的共刺激信号传导区、与cd3ζ特异性结合的配体或其任意组合;
优选为cd28。
优选的,如上所述的嵌合抗原受体,所述抗原结合区选自人抗体、人源化抗体或嵌合抗体;或上述抗体类型的具有抗原结合活性的功能片段。
优选的,所述抗原结合区的重链骨架区序列依次如seqidno:9~12所示,轻链骨架区序列依次如seqidno:13~16所示;
优选的,所述抗原结合区选自scfv;
scfv由vi和vh连接得到,所用连接肽(linker)的序列为(ggggs)3。
优选的,如上所述的嵌合抗原受体,所述t细胞信号传导区功能结构域选自pkcθ、fcεriγ、zap70或cd3ζ或其任意组合;
优选的,所述t细胞信号传导区功能结构域选自cd3ζ。
根据本发明的一方面,本发明还涉及一种分离的核酸分子,所述核酸分子为dna或rna,其编码如上所述的嵌合抗原受体。
根据本发明的另一方面,本发明还涉及一种载体,其包含如上所述的核酸分子;
优选的,所述载体为逆转录载体,更优选为慢病毒。
根据本发明的另一方面,本发明还涉及一种宿主细胞,其被如上所述的载体转化;
优选的,所述宿主细胞为t细胞、nk细胞、cik细胞、dc-cik细胞。
根据本发明的另一方面,本发明还涉及一种制备car修饰的细胞的方法,所述方法包括:将如上所述的核酸分子、或如上所述的载体导入待修饰的细胞内,从而获得所述car修饰的细胞;
优选的,所述car修饰的细胞为t细胞、nk细胞、cik细胞、dc-cik细胞。
根据本发明的另一方面,本发明还涉及一种药物组合物,所述组合物含有药学上可接受的载体以及如上所述的载体、或如上所述的细胞。
根据本发明的另一方面,本发明还涉及如上所述的载体、或如上所述的细胞在制备用于治疗cea阳性实体瘤的治疗剂中的应用;
优选的,所述cea阳性实体瘤包括肺癌、结直肠癌、胃癌、乳腺癌、胰腺癌、直结肠癌、甲状腺癌、尿道癌、卵巢癌、胆管细胞癌、前列腺癌、支气管癌、唾液腺癌、小肠癌、大肠癌、胆管癌、胰管癌、尿道癌。
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
实施例1sc-fv的制备
1.动物免疫与单克隆抗体的制备
以人cea蛋白的胞外结构域部分多肽片段作为免疫原,与弗氏完全佐剂混合,免疫6周龄雌性balb/c小鼠(免疫原用量为100μg/小鼠),免疫方式为皮下多点免疫;两周之后,将免疫原与不完全弗氏佐剂混合,对所述小鼠进行加强免疫(免疫原用量为50μg/小鼠),免疫方式为皮下多点免疫;每隔两周以同样的方法进行加强免疫,共加强免疫3次。最后一次加强免疫后的第7天,摘除小鼠眼球,进行小鼠眼眶静脉丛采血并离心分离血清,elisa检测血清的抗体效价。若p/n≥2.1(p指免疫血清样品od450值减去空白对照od450值,n指阴性对照od450减去空白对照od450值),则判断为阳性。
从阳性血清中挑选抗体效价高的小鼠,在无菌状态下取小鼠的脾脏,制成脾细胞悬液,取对数生长期的骨髓瘤细胞sp2/0,与脾细胞融合,将融合后的细胞悬液分装至96孔细胞培养板,置于hat选择培养基中进行培养。用elisa方法进行多轮反复筛选,并进行单克隆化培养,最终经筛选获得阳性细胞株,将该抗体即为cg3,采用小鼠体内诱生法分别制备腹水型单克隆抗体,通过proteing亲和层析纯化所述抗体,备用。
2.单克隆抗体活性与亲和力分析
包被液稀释cea、ceacam-1、ceacam-3、ceacam-6、ceacam-8重组蛋白抗原到0.5ug/ml进行微孔板包被,每孔100ul,4℃过夜;次日,洗涤液清洗2次,拍干;加入封闭液(20%bsa+80%pbs),每孔120ul,37℃,1h,拍干;加入稀释后的cea单克隆抗体(cg3抗体),100ul/孔,37℃,30min(部分上清1h);洗涤液清洗5次,拍干;加入羊抗鼠igg-hrp,每孔100ul,37℃,30min;洗涤液清洗5次,拍干;加入显色液a液(50ul/孔),加入显色液b液(50ul/孔),10min;加入终止液,50ul/孔;酶标仪上450nm(参考630nm)处读od值。结果如下:
表1抗体活性分析数据
注:-代表活性低于1.0
从表1可知,本发明提供的cg3抗体具有较高的活性,且不与cea的同家族蛋白发生交叉反应。
亲和力分析
利用amc传感器,纯化出来的抗体用pbst稀释到10ug/ml,人cea重组蛋白用pbst进行梯度稀释:2000nmol、1000nmol、500nmol、250nmol、125nmol、62.5nmol、31.25nmol、15.625nmol、0nmol;运行流程:缓冲液1(pbst)中平衡60s,抗体溶液中固化抗体300s,缓冲液2(pbst)中孵育180s,抗原溶液中结合420s,缓冲液2中解离800s,用10mmph1.69gly溶液及缓冲液3进行传感器再生,输出数据。
表2亲和力分析数据
从表2可知,cg3抗体具有优异的抗体亲和力。
3.单克隆抗体的序列测定
将筛选得到的cg3抗体单克隆,进行抗体dna序列的测定。首先提取细胞mrna,使用rnapreppure试剂盒(tiangen,dp430)。步骤如下:悬浮细胞的收集1×107,300×g离心5min,将细胞收集到离心管中,仔细吸除所有培养基上清。立即进行裂解步骤。轻弹离心管底部,使细胞沉淀松散,加入适量裂解液rl600ul,旋涡震荡。将所有溶液转移至过滤柱cs上(过滤柱cs放在收集管中),12,000rpm(~13,400×g)离心2min,收集滤液。向滤液中加入1倍体积70%乙醇(通常为350μl或600μl),混匀,得到的溶液和沉淀一起转入吸附柱cr3中(吸附柱cr3放入收集管中),12,000rpm(~13,400×g)离心30~60sec,倒掉收集管中的废液,将吸附柱cr3放回收集管中。向吸附柱cr3中加入350μl去蛋白液rw1,12,000rpm(~13,400×g)离心30~60sec,倒掉收集管中的废液,将吸附柱cr3放回收集管中。向吸附柱cr3中央加入80μl的dnasei工作液,室温放置15min。向吸附柱cr3中加入350μl去蛋白液rw1,12,000rpm(~13,400×g)离心30~60sec,倒掉收集管中的废液,将吸附柱cr3放回收集管中。向吸附柱cr3中加入500μl漂洗液rw(使用前请先检查是否已加入乙醇),室温静置2min,12,000rpm(~13,400×g)离心30-60sec,倒掉收集管中的废液,将吸附柱cr3放回收集管中。12,000rpm(~13,400×g)离心2min,倒掉废液。将吸附柱cr3置于室温放置数分钟,以彻底晾干吸附材料中残余的漂洗液。将吸附柱cr3转入一个新的rnase-free离心管中,加入30~100μlrnase-freeddh2o室温放置2min,12,000rpm(~13,400×g)离心2min,得到rna溶液。
使用quantscriptrt试剂盒(tiangen,kr103)合成cdna第一链。步骤如下,将模板rna在冰上解冻;引物、10×rtmix(其中包含rnasin和dtt)、superpuredntp混合液、rnase-freeddh2o在室温(15~25℃)解冻,解冻后迅速置于冰上。使用前将每种溶液涡旋振荡混匀,简短离心以收集残留在管壁的液体。按照表1的逆转录体系配制混合液,彻底混匀,涡旋振荡时间不超过5min。简短离心,并置于冰上,最后将模板rna(50ng~2μg)加入到混合液中,彻底混匀,涡旋振荡时间不超过5sec,简短离心以收集管壁残留的液体。37℃孵育60min。将逆转录的产生的cdna第一链用于后续pcr反应(使用高突变引物进行扩增)。将pcr扩增得到的目的条带克隆到载体中。送至商业测序平台进行测序,获得其cdr区氨基酸序列。测得重链互补决定区cdr-vh1、cdr-vh2、cdr-vh3的序列依次如seqidno:1~3所示,轻链互补决定区cdr-vl1、cdr-vl2、cdr-vl3的序列依次如seqidno:4~6所示。
4.人源化cg3抗体单抗的制备
人源化的抗人cg3抗体单抗是根据leung等人(1995,moleculeimmunol32:1413-27)的方法获得的。在germline数据库中选取与鼠源抗体可变区序列匹配最好的人源化模板。将鼠源抗体cdr区移植到选择的人源化模板上,替换人模板的cdr区,得到移植的人源化抗体可变区。通过亲和力和稳定性筛选得到可用的人源化序列。抗原结合区的重链骨架区序列依次如seqidno:9~12所示,轻链骨架区序列依次如seqidno:13~16所示。
将重链可变区和轻链可变区以(ggggs)3linker进行连接,得到sc-fv序列。
实施例2嵌合抗原受体的构建
通过全基因合成信号肽、cea抗原结合结构域(实施例1制备得到的sc-fv),il-10r1胞外域、il-15rβ链、cd28共刺激结构域、cd3ζt细胞信号传导区:
cea-car:信号肽-ceascfv-il-10r1-il-15rβ-cd28-cd3ζ;
cd28的基因序列号为xm_006712862.1;cd3ζ的基因序列号为af228312.1;序列的选取参考sadelainm,naturebiotechnology,2013,31(1):71-5设计的嵌合抗原受体的结构。
实施例3cea-car-t慢病毒的构建
将cea-car片段克隆到慢病毒载体pcdnatm3.1(+)上,选用的插入酶切位点是nhei/bamhi。序列由申请人提供,组装程序有苏州吉玛基因有限公司完成。
实施例4car-t细胞的制备
t细胞为人源,采用将cd3阳性t细胞用lonzax-vivo15培养基(含il-2、il-7、il-15等细胞因子以及灭活ab血浆)进行培养。48小时后,细胞激活状态良好同时细胞数目基本维持不变,用含car的慢病毒(该病毒为pcdnatm3.1(+)-car重组载体的慢病毒,以一定的moi(2-4)对培养的细胞进行感染。12小时后,进行全量换液,以去除感染用的病毒,然后继续培养;根据细胞长势在后续的培养过程中进行细胞半换液,以补充细胞生长过程中所需的营养物质。细胞培养结束后,取样后分装至取样管中,标记后送至第三方进行质控检测。
将制得的car-t细胞中衣原体、支原体、内毒素以及微生物进行检测,制得的car-t细胞中衣原体、支原体、内毒素以及微生物进行检测结果均为阴性;将制得的car-t细胞进行car表达率的检测,结果表明表达率在57%以上。
实施例5car-t细胞的功能验证
1.4t1-luc小鼠原位乳腺癌瘤模型的构建
取雌性balb/c小鼠,选择处于对数生长期的4t1-luc乳腺癌细胞,以1×105个/0.2ml/只的数量接种于balb/c小鼠第四乳腺垫下,构建原位荷瘤小鼠模型,通过活检确定cea阳性的小鼠。分离原代肿瘤细胞进行验证。
细胞培养
a.乳腺癌细胞培养(1640+20%fbs)
计数并测定活率,离心后用生理盐水重悬,调整其活细胞浓度为3×108个/ml,总数达1.8×109个。
b.t细胞培养
计数并测定t细胞的活率,离心后用生理盐水重悬,调整其浓度为5×105个/ml,总数达到6×105个。
c.car-t细胞培养
测定car-t细胞的car含量百分比,计数并测定活率,离心后用生理盐水重悬,调整有效car-t细胞(活细胞且car表达为阳性,本实验例中所提到的car-t细胞,均指有效car-t细胞)的浓度并准备car-t细胞。
2.car-t细胞进行体外杀伤效果验证。
第一步:calcein-am标记靶细胞
1)将calcein-am用dmso稀释成1mg/ml;
2)将靶细胞用全培养基重悬成1×106/ml的密度;
3)加入15μm的calcein-am,37℃、5%co2培养30min,每10min轻轻混匀;
4)1500rpm离心,去上清,用全培养基重悬,重复两遍;
第二步:杀伤
1)将标记好的靶细胞按照5000-50000个/ml的密度重悬,取100μl加入到96孔板中;
2)按照适当的et比加入100μl效应细胞,每组3个平行;同时,有单独的a组6个平行,只有靶细胞(spontaneousrelease);有单独的b组6个平行,只有靶细胞+2%tritonx-100(maximumrelease);
第三步:
1)37℃、5%co2培养4小时后,离心,取75μl上清,转移到一个新的培养板上;
2)样品利用pectramaxgeminidual-scanningmicroplatespectrofluorimeter检测(excitationfilter:485±9nm;band-passfilter:530±9nm),数据以afu的形式显示;
3)计算细胞裂解的百分比:[(testrelease-spontaneousrelease)/(maximumrelease–spontaneousrelease)]*100。
实验结果如图1所示。
从图1可以看出,car-t细胞对cea阳性的乳腺癌细胞具有很强的杀伤能力。
3.car-t细胞的体内验证
1.细胞接种
用生理盐水重悬乳腺癌细胞,调整其活细胞浓度为3×108个/ml,在冰上将其与matrigel按照2:1的体积比充分混匀。通过皮下注射的方式进行接种(接种于裸鼠中)。
2.小鼠肿瘤模型给药。记录肿瘤接种当天为d0,在d7的时候给予pbs或car-t。通过超声辅助微创注射的方式进行将cat细胞及对照液直接注入肿瘤组织内,所有小鼠均单次给药,具体给药如表1所示。
表1给药具体信息
二、药效评价:
1、小鼠观察
从购入小鼠起,至给药后4周连续每天观察小鼠的生存状况,严格监控动物的体格特征,记录可能发生的不良情况如体重减少10%以上、脱毛、腹泻、结膜炎以及瘫痪等情况。经观察得知,两组间无明显差异。
2、体重测定
分组时测定小鼠体重后随机分组;接种前和给药前分别测定小鼠体重;给药后每周2次测定小鼠体重。体重能反映出小鼠健康状况以及肿瘤增殖情况。用电子天平测量小鼠体重,小数点后保留一位有效数字。经测定得知,两组之间无明显差异。
3、肿瘤体积的测量
接种后每周2次测定小鼠的肿瘤长径和短径,由此计算肿瘤体积。肿瘤体积能反映出小鼠体内肿瘤的增殖情况。用游标卡尺测量肿瘤长径和短径,肿瘤体积(mm3)=肿瘤长径(mm)×肿瘤短径2(mm2)×0.5。比较两组之间的差异。具体结果如图2所示。
从图可知,在d7时,空白组(n=10)和实验组(n=12)的肿瘤体积分别为428mm3以及397mm3,说明肿瘤模型造模成功。实验组随car-t注入,肿瘤体积不断缩小,在d28时,实验组的肿瘤体积降到了33mm3,而空白组的肿瘤体积则达到了2439mm3。
4、小鼠生存期的测定
每天观察小鼠的生存状况,当小鼠肿瘤体积达到3000mm3即记为死亡,记录接种后4周内每只小鼠死亡的时间及组别并统计,4周后肿瘤体积未达到3000mm3则记为存活小鼠。统计每组小鼠的平均生存时间。生存期反映了小鼠体内肿瘤的增殖情况。用游标卡尺测量肿瘤长径和短径,肿瘤体积(mm3)=肿瘤长径(mm)×肿瘤短径2(mm2)×0.5。经测定得知,相对于溶剂对照组,car-t细胞治疗组能显著延长生存期。
上述结果可以看出,本发明提供的car-t细胞可以显著抑制模型动物中的肿瘤生长,具备抗肿瘤的功能。
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,但本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
sequencelisting
<110>杭州普略生物科技有限公司
<120>以cea为靶点的嵌合抗原受体
<160>17
<170>patentinversion3.3
<210>1
<211>9
<212>prt
<213>人工序列
<400>1
ilemethisglnasptrpleuasngly
15
<210>2
<211>8
<212>prt
<213>人工序列
<400>2
glyasnserphethrcysserval
15
<210>3
<211>10
<212>prt
<213>人工序列
<400>3
glulysargleugluglnvalalathrile
1510
<210>4
<211>7
<212>prt
<213>人工序列
<400>4
thrthrproproservaltyr
15
<210>5
<211>11
<212>prt
<213>人工序列
<400>5
valalathrilesersertrpglysertyrgly
1510
<210>6
<211>9
<212>prt
<213>人工序列
<400>6
phemetasptyrmetglyglnglyser
15
<210>7
<211>332
<212>prt
<213>homosapiens
<400>7
metglygluasnserglyalaleuseralaglnalaalavalglypro
151015
glyglyargalaargprogluvalargsermetvalaspvalleuala
202530
asphisalaglygluleuvalargthraspserproasnpheleucys
354045
servalleuproserhistrpargcysasnlysthrleuprovalala
505560
phelysvalvalalaleuglyaspvalproaspglythrvalvalthr
65707580
valmetalaglyasnaspgluasntyrseralagluleuargasnala
859095
seralavalmetlysasnglnvalalaargpheasnaspleuargphe
100105110
valglyargserglyargglylysserphethrleuthrilethrval
115120125
phethrasnprothrglnvalalathrtyrhisargalailelysval
130135140
thrvalaspglyproarggluproargarghisargglnlysleuglu
145150155160
aspglnthrlyspropheproaspargpheglyaspleugluargleu
165170175
argmetargvalthrproserthrproserproargglyserleuser
180185190
thrthrserhispheserserglnproglnthrproileglnglythr
195200205
sergluleuasnpropheseraspproargglnpheaspargserphe
210215220
prothrleuprothrleuthrgluserargpheproaspproargmet
225230235240
histyrproglyalametseralaalapheprotyrseralathrpro
245250255
serglythrserileserserleuservalalaglymetproalathr
260265270
serargphehishisthrtyrleuproproprotyrproglyalapro
275280285
glnasnglnserglypropheglnalaasnproserprotyrhisleu
290295300
tyrtyrglythrserserglysertyrglnphesermetvalalagly
305310315320
serserserglyglyaspargserprothrargmet
325330
<210>8
<211>351
<212>prt
<213>homosapiens
<400>8
argglntyrphethrvalthrasnvalileilephephealapheval
151015
leuleuleuserglyalaleualatyrcysleualaleuglnleutyr
202530
valargargarglyslysleuproservalleuleuphelyslyspro
354045
serpropheilepheileserglnargproserprogluthrglnasp
505560
thrilehisproleuaspgluglualapheleulysvalserproglu
65707580
leulysasnleuaspleuhisglyserthraspserglypheglyser
859095
thrlysproserleuglnthrglugluproglnpheleuleuproasp
100105110
prohisproglnalaaspargthrleuglyasnglygluproproval
115120125
leuglyaspsercysserserglyserserasnserthraspsergly
130135140
ilecysleuglngluproserleuserproserthrglyprothrtrp
145150155160
gluglnglnvalglyserasnserargglyglnaspaspserglyile
165170175
aspleuvalglnasnsergluglyargalaglyaspthrglnglygly
180185190
seralaleuglyhishisserproprogluprogluvalproglyglu
195200205
gluaspproalaalavalalapheglnglytyrleuargglnthrarg
210215220
cysalagluglulysalathrlysthrglycysleugluglugluser
225230235240
proleuthraspglyleuglyprolyspheglyargcysleuvalasp
245250255
glualaglyleuhisproproalaleualalysglytyrleulysgln
260265270
aspproleuglumetthrleualaserserglyalaprothrglygln
275280285
trpasnglnprothrgluglutrpserleuleualaleusersercys
290295300
seraspleuglyileserasptrpserphealahisaspleualapro
305310315320
leuglycysvalalaalaproglyglyleuleuglyserpheasnser
325330335
aspleuvalthrleuproleuileserserleuglnserserglu
340345350
<210>9
<211>23
<212>prt
<213>homosapiens
<400>9
lysilemetvalthrthrglnseraspasntrpproileserglygly
151015
glnlysvalaspmetalacys
20
<210>10
<211>17
<212>prt
<213>homosapiens
<400>10
trptyrglnglnleuleuileargphealaserglnserileserleu
151015
val
<210>11
<211>28
<212>prt
<213>homosapiens
<400>11
argpheileglyserglyargalaasnglnserileserasnasnile
151015
serservalglnalagluaspleualaasptyrphe
2025
<210>12
<211>8
<212>prt
<213>homosapiens
<400>12
alaglythrlysleugluleulys
15
<210>13
<211>23
<212>prt
<213>homosapiens
<400>13
gluvalasnleuvalgluserglyglyleuglnseraspleutyrarg
151015
leusercysalaalasergly
20
<210>14
<211>18
<212>prt
<213>homosapiens
<400>14
metsertrpvalcysmetilethrasnphelysglyleuglutrpval
151015
serser
<210>15
<211>33
<212>prt
<213>homosapiens
<400>15
tyrproaspsermetlysglythrleuserleuserproglygluarg
151015
tyrleuglnmetglnglnlysproalagluaspthralavaltyrtyr
202530
cys
<210>16
<211>12
<212>prt
<213>homosapiens
<400>16
trpglytyrphecysglnglnserthrvalserala
1510
<210>17
<211>19
<212>prt
<213>homosapiens
<400>17
metglucyssercysvalmetleuphepheleuservalthrthrgly
151015
valhisser
- 还没有人留言评论。精彩留言会获得点赞!