一种受核盘菌诱导的油菜启动子pBnGH、鉴定方法和应用与流程
本发明属于植物基因工程技术领域,具体涉及一种受核盘菌诱导的油菜启动子pbngh、鉴定方法和应用。该启动子可用于通过植物基因工程技术改善植物的菌核病抗性。
背景技术:
启动子是rna聚合酶特异识别、结合和启动基因转录的一段dna序列,其作为基因转录的“开关”,调控着基因的转录时间和表达程度。启动子按其功能及作用方式可分为组成型启动子、组织特异型启动子和诱导型启动子。植物基因工程将外源基因导入到受体植物细胞,并整合到受体染色体,使其受体植物获得相应的遗传表型。传统的基因工程大多用组成型表达启动子,如(camv)35s、ubiquitin启动子等。但是这一类启动子最大的缺点是:它使外源基因在植物整个生命周期、所有组织都持续强烈表达,对植物造成能量的过度消耗或产生毒害作用。因此诱导型启动子或者组织特异型启动子的利用在植物基因工程中越来越受到重视。特别是利用逆境诱导型启动子来控制抗逆基因的表达,在没有逆境胁迫下,它控制的编码基因本底表达或不表达,一旦出现逆境胁迫,编码基因迅速大量表达,从而使植物表现出抗逆表型,在作物抗逆育种中具有重要作用。目前已经有一些逆境诱导型启动子被鉴定和利用,如rd29a启动子(yamaguchi-shinozakiandshinozaki,characterizationoftheexpressionofadesiccation-responsiverd29geneofarabidopsisthalianaandanalysisofitspromoterintransgenicplants,mgg,1993,236(2-3):331-340;kasuga等,improvingplantdrought,salt,andfreezingtolerancebygenetransferofasinglestress-inducibletranscriptionfactor.naturebiotechnol,1999,17(3):287;kasuga等,acombinationofthearabidopsisdreb1ageneandstress-induciblerd29apromoterimproveddrought-andlow-temperaturestresstoleranceintobaccobygenetransfer.plantcellphysiol,2004,45(3):346-350)、bs3启动子(lahaye等,pathogen-induciblepromotersandtheiruseinenhancingthediseaseresistanceofplants,u.s.patent,2015,no.9,133,467)、oshox24启动子(nakashima等,comparativefunctionalanalysisofsixdrought-responsivepromotersintransgenicrice.planta,2014,239(1):47-60)和abrc1启动子(lee等,expressionofarabidopsiscbf1regulatedbyanaba/stressinduciblepromoterintransgenictomatoconfersstresstolerancewithoutaffectingyield.plant,cellenviron,2003,26(7):1181-1190)。
菌核病是由核盘菌引起的真菌性病害,每年导致油菜产量损失10%—20%,是制约我国油菜生产最主要的病害。培育抗(耐)病油菜品种是防治油菜菌核病最为经济有效的途径。然而,现有的油菜品种及其近缘种中缺乏有效抗源,导致油菜抗菌核病育种进展缓慢。因此在鉴定抗病相关基因后,通过植物基因工程技术手段在作物中使抗病基因在核盘菌诱导型启动子调控下特异高表达,以提高作物对菌核病的抗性,减少产量损失,是作物抗菌核病育种的一个重要手段。但是植物中核盘菌诱导型启动子的研究还未见报道。因此分离和鉴定核盘菌诱导型启动子对作物抗菌核病育种具有非常重要的意义。
技术实现要素:
为了克服上述缺陷,本发明在甘蓝型油菜中通过转录组分析,发现一个被核盘菌强烈诱导表达的基因bngh(bnac01g21880d),进一步通过定量pcr(qpcr)分析发现该基因在正常生长的油菜各器官(除根)中在表达量极低,并且在一些非生物胁迫下(如冷、盐、peg等)和茉莉酸甲脂、水杨酸、乙烯利等激素处理下未显著诱导表达,只在高温处理后显著诱导表达。因此本发明认为bngh为核盘菌诱导表达基因。随后鉴定并克隆了该基因的启动子,定义为核盘菌诱导启动子pbngh。进一步将该启动子驱动gus报告基因(pbngh::gus)转入拟南芥中,发现gus能够被核盘菌、茉莉酸甲脂诱导表达,但在拟南芥正常生长组织如叶片、茎秆、花、角果、种子中表达量极低,并且在水杨酸、乙烯利等激素处理下均无明显诱导表达。
为了实现上述发明目的,本发明所采用的技术方案为:一种受核盘菌诱导的油菜启动子pbngh,pbngh的序列如seqidno.1所示。
本发明还提供包含前述的受核盘菌诱导的油菜启动子pbngh的表达载体,并命名为pbngh83。
本发明还提供受核盘菌诱导的油菜启动子pbngh的克隆方法。该启动子克隆自甘蓝型油菜抗菌核病品系j964。
本发明的另一个目的是提供油菜启动子pbngh或前述的表达载体在提高植物的菌核病抗性中的应用。具体方法为:将包含受核盘菌诱导的油菜启动子pbngh的表达载体转化目标植物。
受核盘菌诱导的油菜启动子pbngh的鉴定方法,通过定量pcr分析油菜启动子pbngh基因在正常生长的油菜各器官中的表达量,在非生物胁迫下、激素处理下观察是否显著诱导表达;
克隆油菜启动子pbngh基因,将该启动子驱动gus报告基因转入拟南芥中;通过定量pcr分析油菜启动子pbngh基因在正常生长的拟南芥各器官中的表达量,在非生物胁迫下、激素处理下观察是否显著诱导表达。
综上所述,本发明的申请人在国际上首次提供了一个菌核病病原菌核盘菌诱导的植物启动子pbngh。可以利用本发明启动子构建成抗菌核病相关基因的植物表达载体,通过遗传转化提高植物的菌核病抗性。
附图说明
序列表seqidno.1是本发明从甘蓝型油菜中分离克隆的核盘菌诱导的启动子pbngh的核苷酸序列;
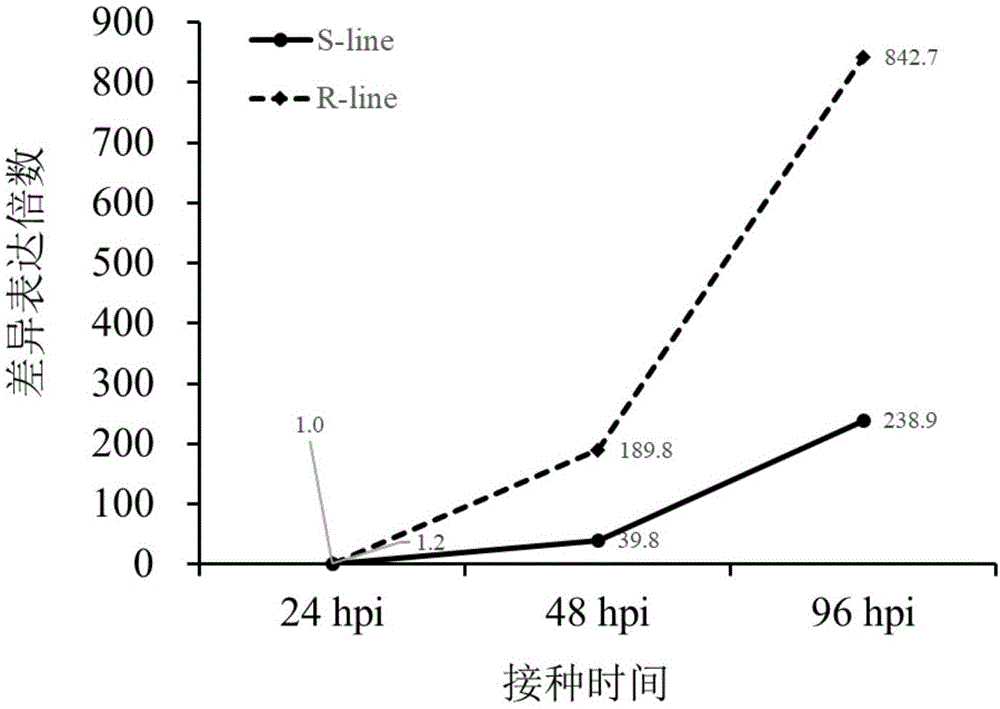
图1.甘蓝型油菜抗病材料(r-line)和感病材料(s-line)在接种核盘菌后24h、48h以及96h相对于未接种对照(mock)bngh基因的表达量差异倍数;hpi(hourpostinoculation);
图2.甘蓝型油菜各组织中bngh基因的相对表达量;相对表达量根据转录组数据计算,bngh(fpkm)/bnubq10(fpkm);
图3.qrt-pcr分析甘蓝型油菜bngh基因在非生物胁迫和激素处理下的表达变化;差异表达倍数为处理后bngh的相对表达量除以其在相应对照条件下的相对表达量。数据表示为平均数±标准差(3次生物学重复),内参基因为bnubq10(bnaa10g06670d);
图4.pbngh启动子与gus融合基因在拟南芥不同器官或者组织的表达。图a-f:gus染色结果,标尺代表2mm;图g:gus基因相对表达量检测,数据表示为平均数±标准差(3次生物学重复),内参基因为atef-1a;
图5.拟南芥中pbngh启动子与gus融合基因在不同激素处理(a、b)或者核盘菌接种处理(c、d)后的表达分析;图a:水(h2o)、乙烯(et)、水杨酸(sa)、茉莉酸甲酯(meja)处理6h和12h后的gus染色结果;图c:核盘菌(ss)及其对照(无菌菌丝块,mock)处理12h和24h后的gus染色结果;标尺代表5mm;图b和d:gus基因相对表达量检测,数据表示为平均数±标准差(3次生物学重复),内参基因为atef-1a;
图6.pbngh83载体的质粒图谱。
具体实施方式
以下实施例中进一步定义本发明,根据以上的描述和这些实施例,本领域技术人员可以确定本发明的基本特征,并且在不偏离本发明精神和范围的情况下,可以对本发明做出各种修改和改变,以使其使用各种用途和条件。除特殊注明外,本发明所采用的均为该领域现有技术。
实施例1:甘蓝型油菜抗病材料和感病材料中bngh基因的表达变化
本实验用的两个材料分别为j964(抗病材料,r-line)和j902(感病材料,s-line),都为冬性甘蓝型油菜纯系材料,由实验室多年的菌核病抗性材料筛选中得到。
病原菌来自华中农业大学微生物国家重点实验室李国庆老师提供的核盘菌ss-1。该菌株暗光下保存于的4℃冰箱中,使用前接种在马铃薯培养基(pda,25%马铃薯提取液、2.5%葡萄糖、1.5%琼脂,ph调至5.86)上,23℃,暗光下活化两次后用于接种。
在油菜终花期采用成株期活体茎秆接种方法进行接种,具体方法如下:用7mm打孔器打取新生边缘菌丝用于接种,用保鲜膜将菌丝块固定。每个植株在主茎离地30-60cm处的三个不同的节间分别接种,同时用不含菌丝的pda块用同样的方法接种作为对照处理。接种后24、48和96h分别用刀片取接种点长宽各为10mm,深1mm的茎秆组织。每个取样时间点r-和s-line的接种与对照都分别取5株的茎秆组织(共15个接种点)混合作为一个样品,并且设置3个生物学重复。取样后立即放入液氮中,后保存于-80℃冰箱。
采用植物总rna提取试剂盒(全式金,中国)进行rna的抽提,实验程序参照该试剂盒的说明书。用rnase-freednasei(thermoscientific,美国)去除基因组dna的污染。将每个生物学重复中的三个时间点的对照混合为一个混合对照样品抽提rna,所以每个材料的每个生物学重复共4个rna样品(3个接种样品(24、48、96h)和1个混合对照)。每个样品取1.5μg总rna,稀释至50μg,利用
转录组数据的分析参考发明人已经发表论文(wu等,comparativetranscriptomicanalysisuncoversthecomplexgeneticnetworkforresistancetosclerotiniasclerotioruminbrassicanapus,scirep,2016,6:19007)。根据转录组数据分析甘蓝型油菜抗病材料(r-line)和感病材料(s-line)在接种核盘菌后24h、48h以及96h相对于未接种对照(mock)bngh基因的表达量差异倍数。
实施例2:启动子pbngh的克隆
根据甘蓝型油菜‘darmor-bzh’参考基因组序列调取bngh基因(bnac01g21880d)起始密码子上游2000bp左右序列设计引物扩增启动子序列,引物序列为(bnghpro-f:5’-ccaaaggaagacaaggagca-3’(seqidno.2);bnghpro-r:5’-agcaagaagaagatacagtggga-3’(seqidno.3))。
利用ctab法提取甘蓝型油菜抗菌核病品系j964基因组dna作为模板,进行pcr反应,反应程序如下:预变性95℃5min,变性95℃30s,退火57℃30s,延伸72℃2min,反应33个循环后充分延伸72℃7min。结束后用康为公司的dna回收试剂盒纯化回收dna,并将纯化的dna片段连接到peasy-bluntsimple载体中(全式金,中国),25℃孵育1小时,转化e.colitranst1感受态细胞,挑选阳性克隆提质粒,由擎科公司完成测序,保存质粒命名为bnghpro-1。测序结果显示获得一个长度为1820bp的dna片段,如seqidno.1所示的核苷酸序列,与参考基因组序列完全一致,为预期的启动子pbngh序列。
seqidno.1
实施例3:甘蓝型油菜各组织中bngh基因的相对表达量
试验材料j9712种植于江苏扬州大学实验田中。分别对其子叶、苗期(1月大)叶、苗期(1月大)根、茎、薹茎叶、顶端分生组织(sam)、花蕾、未授粉子房、14d种子、14d角果皮、24d种子、24d角果皮、34d种子、34d角果皮,50d种子和50d角果皮进行取材,所有组织样本都从多个植株上获取并混合作为一个样品,并设置三个生物学重复,取样后立即放入液氮中,后保存于-80℃冰箱。
采用植物总rna提取试剂盒(全式金,中国)进行rna的抽提,实验程序参照该试剂盒的说明书。用rnase-freednasei(thermoscientific,美国)去除基因组dna的污染。采用实施例1一样的方法进行rna-seq文库的构建、测序和分析,结果相对表达量表示如图2。bngh基因在油菜苗期根中表达量最高(内参基因bnubq10表达量的0.1),另外在不同时期的角果皮中也有微弱表达,总的来说该基因在油菜各个组织中表达量都非常低。
实施例4甘蓝型油菜bngh基因在非生物胁迫和激素处理下的表达变化
取温室生长约30d的j9712作为实验材料进行非生物胁迫和激素处理,激素处理包括水杨酸(sa)、脱落酸(aba)、茉莉酸甲酯(meja),乙烯利(eth),非生物胁迫处理则包括peg(聚乙二醇)、冷(4℃)、热(42℃)及过氧化氢(h2o2)进行处理;非生物胁迫和激素处理均设置平行对照处理。
激素处理具体步骤:各激素配制采取现配现用的原则,其中meja处理浓度为200μm,sa处理浓度为1mm,aba处理浓度为100μm,eth处理浓度为1mm。采取活体叶面喷施,叶片开始滴水为度的方式进行,将处理后的油菜用保险膜整株覆盖进行保湿,分别在处理后3和6h取样。同时以喷蒸馏水的样品作为对照。取大小一致的5个叶片作为一个样本,并设置3个生物学重复。取下的叶片立即放入液氮中,后保存于-80℃冰箱。
非生物胁迫处理具体步骤:用15%的peg进行模拟干旱处理,处理后5d进行取样,同时以水培5d的植株作为对照;用200mm的nacl进行盐胁迫处理,处理后6h进行取样,同时以水培的植株作为对照;用4℃进行冷胁迫处理,处理后6h进行取样,同时用22℃正常生长的植株作为对照;用42℃进行热胁迫处理,处理后1h进行取样,同时22℃正常生长的植株作为对照;h2o2处理方式和激素处理一致,处理浓度为100μm,处理后3和6h进行取样。取大小一致的5个叶片作为一个样本,并设置3个生物学重复。取下的叶片立即放入液氮中,后保存于-80℃冰箱。
采用植物总rna提取试剂盒(全式金,中国)进行rna的抽提,实验程序参照该试剂盒的说明书。用反转录试剂盒(诺维赞,中国)对rna进行反转录,用于qrt-pcr的模板。采取定量的方式对bngh的表达量进行检测,每个样本设置三个技术重复,定量所用的sybrgreenmix及耗材均来自于abi,美国。bngh的qrt-pcr的引物序列为:bngh-f:5’-gaaacgctgcgacttttgataa-3’(seqidno.4)bngh-r:5’-catcgaacatggcgaacaaata-3’(seqidno.5),内参基因为bnubc10,引物序列为:bnubc10-f:5’-tccatccgacagcccttactct-3’(seqidno.6)bnubc10-r:5’-acactttggtcctaaaagccacc-3’(seqidno.7)。反应体系及反应程序如表1和表2。
表1qrt-pcr反应体系
表2qrt-pcr反应程序
根据内参基因计算bngh在处理前后的相对表达量,最终用差异表达倍数表示处理前后的表达差异,差异表达倍数为处理后bngh的相对表达量除以其在相应对照条件下的相对表达量,如图3。数据表示为平均数±标准差(3次生物学重复)。所用方法均为现有技术。结果表明bngh基因在热胁迫下会显著诱导表达,但相比于核盘菌侵染后的表达变化小的多,在其他非生物胁迫及激素处理下均不显著差异表达。
实施例5构建pbngh启动子序列与gus基因融合的重组载体并转化拟南芥(columbia)
以质粒bnghpro-1dna为模板,通过pcr在pbngh启动子序列两端添加限制性内切酶的bamhi识别位点。反应结束后用1%琼脂糖凝胶电泳检测,回收纯化目的片段,将纯化后的目的片段及植物表达载体pbi101同时用bamhi进行酶切并连接。将上述获得的启动子段连接在gus基因的上游获得重组载体,命名为pbngh::gus,用电激法将重组载体转化农杆菌gv3101。
通过农杆菌介导转化拟南芥columbia生态型,将收到的t0代种子灭菌后铺在在含有50mg/l卡那霉素筛选培养上,将筛选出来的苗子移栽到土中继续培养,通过pcr的方式鉴定阳性,并收获转基因种子。所述转化方法采用现有技术。
实施例6pbngh::gus转基因拟南芥各组织中gus表达水平检测
取在温室生长20d的整株幼苗,真叶(45d苗)、根(45d苗)、茎秆、花蕾及角果的样本,并设置三个生物学重复。一部分样品用于gus染色分析,另一部分样品用于定量分析。
gus染色实验方法:(1)配制合适体积的gus染色液(1×pbs,ph,7.4;10mmedta;0.5mmk3[fe(cn)6];0.5mmk4[fe(cn)6];0.1%tritonx-100(v/v);0.5mg/mlx-gluc),将待染色样品置于染色液中,真空处理30min。(2)37℃水浴6h至过夜。(3)用70%乙醇为样本脱色,每小时换一次脱色液,直至70%乙醇颜色为无色透明。gus基因的表达量检测采用qrt-pcr方法,rna的提取、反转录以及qrt-pcr的试验方法与实施例4中一致。gus基因qrt-pcr所用的引物序列为:gus-f:5’-agtgaagggcgaacagttcctgat-3’(seqidno.8);gus-r:5’-ttcagcgtaagggtaatgcgaggt-3’(seqidno.9)。内参基因为atef-1a,(引物序列为atef-1a-f:5’-tgagcacgctcttcttgctttca-3’(seqidno.10);atef-1a-r:5’-ggtggtggcatccatcttgttaca-3’(seqidno.11)。
经上述不同组织及核盘菌接种后不同时间的转基因植株的gus分析结果如图4所示。gus染色结果表明gus在拟南芥20d苗期,45d真叶,茎秆及角果中的表达都相对较低,其中在45d根的表达相对较高(图4a-f),与实施例3中油菜各组织中bngh表达的结果大体一致。qrt-pcr的结果与gus染色结果一致(图4g)。
实施例7pbngh::gus转基因拟南芥在激素处理及核盘菌接种后gus表达水平检测
取在温室生长的30d的真叶,采用活体喷施的方式对转基因植株进行激素处理。激素处理包括meja(茉莉酸甲酯),sa(水杨酸)和eth(乙烯利),其中meja处理浓度为100μm,sa处理浓度为100μm,eth处理浓度为7mm,取样时间点为处理后6和12h,处理方法和实施例4中一致。设置三个生物学重复。一部分样品用于gus染色分析,另一部分样品用于定量分析。
取在温室生长的30d的真叶,采用离体接种核盘菌的方式在偏离主叶脉中上方的地方接种。在接种后12和24h取样同时以不含菌丝的pda块作为对照组,并设置三个生物学重复。一部分样品用于gus染色分析,另一部分样品用于定量分析。gus染色试验方法,rna的提取及qrt-pcr的试验方法与实施例6中的一致。
经上述不同激素处理及核盘菌接种后不同时间的转基因植株的gus分析结果如图5所示。qrt-pcr和gus染色结果都表明gus在sa和et处理后不表达,此外在meja处理6h也不表达,但在meja处理12h有微弱的表达(图5a,b)。qrt-pcr和gus染色结果都表明gus在接种核盘菌之后显著诱导表达,并且随着接种的时间的增加,其诱导表达愈烈(图5c,d)。
实施例8pbngh83载体的构建
以质粒bnghpro-1dna为模板,通过pcr在pbngh启动子序列两端分别添加限制性内切酶的pmei和spei识别位点。在植物表达载体pmdc83的基础上,通过酶切连接的方式将原有的2×camv35s启动子替换为本发明的pbngh启动子。载体的构建方法同实施例5。pbngh83载体的质粒图谱如图6所示。
经上述这些实验结果说明启动子pbngh是受到核盘菌诱导表达的,是一个病原相关的启动子,并且该启动子在正常生长条件以及在激素及大多数非生物胁迫处理后也不能诱导其表达,为提高植物的抗病性提供一定的利用资源。
本发明在从甘蓝型油菜中分离克隆并鉴定了一个菌核病病原菌核盘菌诱导启动子pbngh。该启动子的核苷酸序列为序列表中seqidno.1所示的核苷酸序列。实验证明,该启动子调控的基因能对核盘菌侵染产生特异性的应答反应,但在油菜和拟南芥的叶片、茎秆、花蕾、角果、种子中表达量极低,仅在根中有一定的表达。此外该启动子不被激素处理和大多数非生物胁迫诱导,仅对高温产生一定的应答反应。本发明还提供了含有pbngh的表达载体,并命名为pbngh83。利用pbngh启动子调控抗性基因的表达,仅仅在核盘菌侵袭时才剧烈诱导抗性基因的表达,增强油菜对核盘菌的抵抗能力。
以上显示和描述了本发明的基本原理、主要特征以及本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
序列表
<110>扬州大学
<120>一种受核盘菌诱导的油菜启动子pbngh、鉴定方法和应用
<130>xhx2018122103
<141>2018-12-21
<160>11
<170>siposequencelisting1.0
<210>1
<211>1784
<212>dna
<213>brassicanapusl.
<400>1
ccaaaggaagacaaggagcaatcgatactcctctacgcttgtcgtaactgtgatcaccag60
gtacatacattgctttctttgatcaaattagggttccatgtgctttgtaaacgaagctgt120
gtgttttatgtgctatgaaacaaaactagggtttcgtgtttctaatgtgcttttgagaca180
gagctatggcttacacggttaagaatcgaagcttagaacttgaaattaaaccgagaaaag240
gagaaaattaacgagttttagatccacaatccagctctcgttgtccttgtttttagatca300
atgcttatatcagttaagagttgctgttaagtgtcaaacgcttggaactatatgacgtga360
ttgattttctatgttaacgtgatccatccatccagcagccttgaacctttcgtgttacac420
gttatcgagttcttgaattttcagggtcttttatgatcattttagtttttacctagtcta480
attatgaatttgctgatttctgaggggccgttcagaaaactcgttcttgtctatgaatac540
gtggaaactgaaaattgtcatctttagccgccggctgctgtgtgatatcataaaaagttg600
atgagtataatcttctcgatagaactattaatgataaagcctacgttaccgtattgaatt660
atgtatgttgaaattgtcaacaaatttatttttattgaagtttatgtttcaaacgaatca720
ttgtatataatacacgattatggatggttaggtatagaaactggagtctctacaagatga780
ttgaaagtttcgcgtgggctgctgtttgctttcaaattataatatccacagttgaagtga840
tgacattatctcaactcaacttgacaaagcatattccttcttcctaaatatgtaatcaaa900
taagaaaattaacaattgcttagaaaaaatcaaattggaccaccacaaaggtcaagtaat960
cagtaataacctcatgagtggaattatactagaaccattgacattgaataagagcttatc1020
ttaatttcacaagttacaagttgttgcaacttgcacgtaagagacaaaacttcaaatgtc1080
tatatttgttgttggtgaagttgtttatatctaatagatatctgagagatcacatgtaca1140
aattctattggaaaggattcactctacaaataaaagtttaacttgtatagagtttagttc1200
taccgaatgtacaaacccaaaatctcttactaaaaagaaaaagttaaatagtcattcaaa1260
atctcttacgtgcttaatcgaatttgtttctcgtcattcgtttaatattagtactaaata1320
tttgattaaatacacctggagtcaaataaaatcaaattttgtataggtaaagacagaaaa1380
aatacattaggattgatttaacagtgttggaaaacataagcaatctcctatctactttct1440
cgatttggaaagggacatttctctacccatttttcgacatgatcttctcattgttacata1500
cattcatcttgtatttacactcgagccgaccttacatactcaattacttgacccgactaa1560
tgactttaaatttcatttaataaacagtaatttttttattctcactcaactctacataat1620
acacaatttatacgaacatatccatattcttaattataaaataaataaataaactcaagt1680
atacgcaccatattttgcatataaaaaagcttaagcataaacccaattagacaatgagtt1740
atcgataacccacagtatcaatagacttacacatcaatttcgat1784
<210>2
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>2
ccaaaggaagacaaggagca20
<210>3
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>3
agcaagaagaagatacagtggga23
<210>4
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>4
gaaacgctgcgacttttgataa22
<210>5
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>5
catcgaacatggcgaacaaata22
<210>6
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>6
tccatccgacagcccttactct22
<210>7
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>7
acactttggtcctaaaagccacc23
<210>8
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>8
agtgaagggcgaacagttcctgat24
<210>9
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>9
ttcagcgtaagggtaatgcgaggt24
<210>10
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>10
tgagcacgctcttcttgctttca23
<210>11
<211>24
<212>dna
<213>人工序列(artificialsequence)
<400>11
ggtggtggcatccatcttgttaca24
- 还没有人留言评论。精彩留言会获得点赞!