一种含磷氮配体烷基铝化合物的制备方法与应用与流程
本发明涉及一类有机铝化合物的制备方法与应用,特别涉及2-二苯基磷苯甲醛-苯胺烷基铝化合物的制备方法及其在内酯和交酯开环聚合方面的应用。
背景技术:
可降解聚酯高分子材料在环境友好、生物相容等方面相较于传统高分子材料具有明显的优势,是新一代的、有广阔发展前景的材料,并符合生态和可持续发展的要求。这其中,脂肪族聚酯是一类非常重要的可降解高分子材料,近年来得到了快速的发展。
生物可降解聚酯如pcl、pla等具有良好的生物相容性、生物降解性,在自然环境条件下可完全生物降解,对环境不产生任何污染,因而被广泛的用于医药领域,如可以用作药物载体,通过控制降解速率来调节药物释放速率,还可用作手术缝合线,可在生物体内自然降解,对生物体无毒无害,无需拆线。此外,生物可降解聚酯也正在向工业、农业领域发展,用以代替以石油为原材料的塑料等难降解材料,是优异的环境友好材料。
目前广泛研究和应用的脂肪族聚酯包括聚乳酸(pla)、聚己内酯(pcl)、聚乙醇酸(pga)、聚羟基丁酸酯(phb)及其它们的共聚物,主要通过催化单体开环聚合的方法制备,普遍采用的催化剂有异丙醇锌、辛酸亚锡等。其中最为广泛使用的是辛酸亚锡,它具有较快的反应速率,可以得到产率高、分子量高的聚酯材料,但是其也存在着反应活性不是很高,需要较长的反应时间和较高的反应温度的缺点。近年来,有机金属铝化合物由于其出色的催化内酯开环聚合方面的特性,作为开环聚合催化剂受到人们的极大关注,用于制备分子量可控、分子量分布窄、嵌段或者立构规整的生物降解脂肪族聚酯高分子材料。这些有机金属铝催化剂中比较具有代表性的催化剂模型包括萨伦(salen)铝催化剂(j.am.chem.soc.,2002,124,1316;proc.natl.acad.sci.u.s.a.2006,103,15343),水杨醛亚胺铝催化剂(macromolecules,2005,38,5363;daltontrans.2012,41,11587;organometallics2009,28,2179),桥联双酚-铝催化剂(macromolecules2001,34,6196),四苯基卟啉铝催化剂(j.am.chem.soc.2004,126,11030),双金属铝催化剂(organometallics2014,33,6474;chem.commun.2008,4717)。
申请人前期报道了一系列铝金属催化剂,用于脂肪族聚酯合成,如chinesej.polym.sci.2018,36,149;j.polym.sci.,parta:polym.chem.2018,56,611;newj.chem.2017,41,2358;organometallics2017,36,1736;并申请了相关发明专利zl201610369322.2,zl201610370061.6,zl201610383016.4。上述报道或专利所涉及催化剂均为含氮和氧的铝金属催化剂,而本发明报道了一种含磷和氮的铝金属催化剂,特别涉及2-二苯基磷苯甲醛-苯胺烷基铝化合物的制备方法及其在开环聚合中的应用。铝催化剂具有制备简单、成本低、活性高、可控性好的特点,所制备脂肪族聚酯具有微观结构可控、可降解、生物相容性好的特点。
技术实现要素:
本发明的目的是提供一种2-二苯基磷苯甲醛-苯胺烷基铝化合物的制备方法及其在开环聚合中的应用。
本发明提供一种式(i)所示2-二苯基磷苯甲醛-苯胺烷基铝化合物:
其中,r选自甲基,乙基,异丙基;r1选自氢,甲基,异丙基,二苯甲基;r2选自氢,异丙基。
优选的,本发明铝金属配合物选自如下任意一种配合物:
al1:l1alme2l1=2-ph2p-c6h4-ch2-nh-c6h5;
al2:l2alme2l2=2-ph2p-c6h4-ch2-nh-2,6-me-c6h3;
al3:l3alme2l3=2-ph2p-c6h4-ch2-nh-2,6-ipr-c6h3;
al4:l1alme2l4=2-ph2p-c6h4-ch2-nh-2,6-ph2ch-4-ipr-c6h2;
本发明提供了上述2-二苯基磷苯甲醛-苯胺烷基铝化合物的制备方法,其包括以下步骤:
(1)在氮气氛围下,2-二苯基磷苯甲醛与取代苯胺按0.8~1.2:0.8~1.5摩尔比例混合后,加入催化剂量的对甲基苯磺酸5~20mg,在甲醇和二氯甲烷混合溶剂中(甲醇和二氯甲烷体积比为1:1~5)搅拌反应6~48小时;将混合溶剂减压除去,所得产物加入甲醇,超声,产物过滤抽干,所得亚胺加入2~5摩尔当量的四氢铝锂,反应两天,即可得到2-二苯基磷苯甲醛-苯胺配体。
(2)将2-二苯基磷苯甲醛-苯胺配体溶于30~100ml无水溶剂中,加入1.0~1.5摩尔当量烷基铝,氮气保护下搅拌反应12~24小时,反应温度20~100℃;减压除去溶剂,用不良溶剂洗涤三次,得到相应的烷基铝化合物。
上述制备方法中,所述无水溶剂选自苯、甲苯、二甲苯、四氢呋喃,优选甲苯;不良溶剂选自正己烷、正戊烷、正庚烷、环己烷,优选正己烷。
本发明还提供了上述式(i)所示2-二苯基磷苯甲醛-苯胺烷基铝化合物在催化内酯和交酯开环聚合反应中的应用。
上述应用中,所述内酯和交酯包括己内酯、丙交酯、乙交酯、丁内酯、戊内酯、庚内酯、辛内酯,优选己内酯。
上述应用中,所述二苯基磷苯甲醛-苯胺烷基铝化合物与所述交酯和内酯的摩尔比为1:10~10000,优选1:100。
上述应用中,所述聚合反应的溶剂可为苯、甲苯、正己烷、四氢呋喃和二氯甲烷,优选甲苯。
上述应用中,所述聚合反应的温度为0℃~110℃。
上述应用中,所述聚合反应的时间为0.1~12h。
上述应用中,所述聚合反应可以加入醇作为助催化剂,所述醇为甲醇、乙醇、异丙醇、正丁醇、乙二醇、丙三醇、苄醇;所述醇与所述2-二苯基磷苯甲醛-苯胺烷基铝化合物的摩尔比为0~30:1,优选1:1。
本发明提供的2-二苯基磷苯甲醛-苯胺烷基铝化合物的制备方便,成不低廉,性质稳定,同时具有较高的催化活性,特别适合催化己内酯开环聚合。通过对聚合反应条件的控制,可以调控聚合物的分子量大小,从几千到几十万。
附图说明
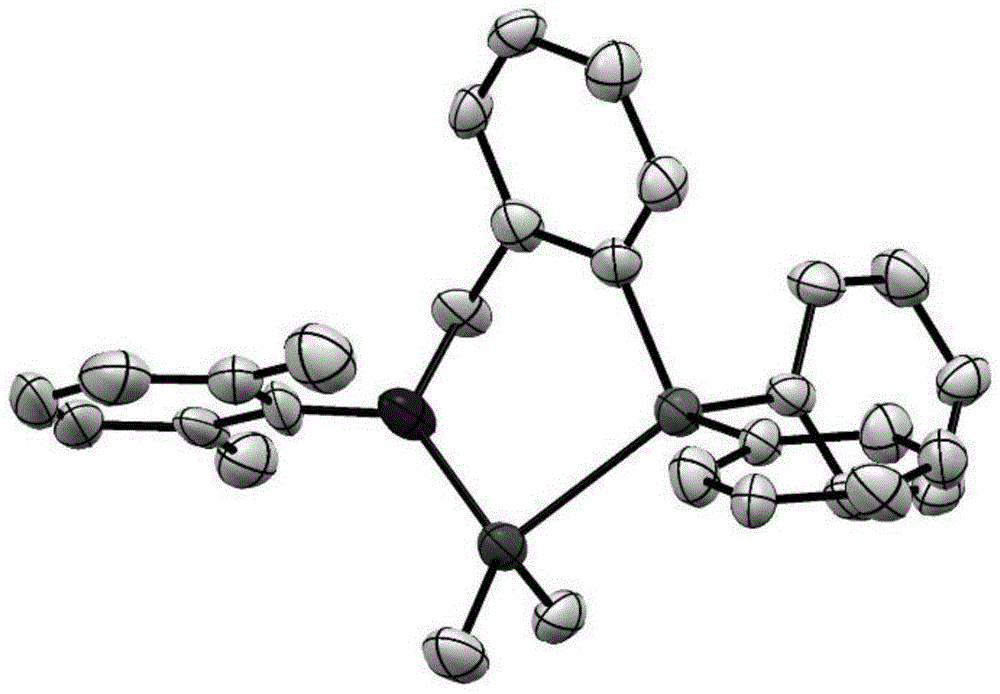
图1为化合物al2的晶体结构图。
图2为化合物al3的晶体结构图。
图3为化合物al4的晶体结构图。
图4为实施例6所得聚合物的gpc图。
图5为实施例7所得聚合物的gpc图。
图6为实施例8所得聚合物的gpc图。
图7为实施例9所得聚合物的gpc图。
图8为实施例9所得聚合物的malditof图。
具体实施方式
通过实施例进一步说明本发明,但本发明并不限于此。本发明的实施例可以使本专业的技术人员更全面的理解本发明。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
本发明中l1(2-ph2p-c6h4-ch2-nh-c6h5)、l2(2-ph2p-c6h4-ch2-nh-2,6-me-c6h3)和l3(2-ph2p-c6h4-ch2-nh-2,6-ipr-c6h3)分别根据文献newjournalofchemisty,2003,27,414和chemistry-aeuropeanjournal,2007,13,834中报道的方法合成。
实施例1、配体l4(2-ph2p-c6h4-ch2-nh-2,6-ph2ch-4-ipr-c6h2)的制备
将2,6-二(二苯基甲基)-4-异丙基-苯胺(2,6-ph2ch-4-ipr-c6h2-nh2,4.67g,10.0mmol),2-二苯基磷苯甲醛(2.90g,10.0mmol),对甲苯磺酸10mg混合在100ml甲苯中,氮气氛围下回流12小时,用甲醇洗,取所得产物亚胺(2-ph2p-c6h4-ch=n-2,6-ph2ch-4-ipr-c6h2,2.22g,3mmol)与lialh4(0.57g,15mmol)溶于60ml无水四氢呋喃中,氮气氛围中室温反应2天,先后用0.57ml水,0.57ml15%的氢氧化钠水溶液淬灭,处理得到白色固体l4化合物1.93g,2.6mmol,产率87%。1hnmr(cdcl3):δ7.34–7.11(m,25h),7.04(d,j=7.0hz,8h),6.83(dd,j=7.4and4.5hz,1h),6.64(s,2h),6.17(s,2h),4.09–4.01(br,2h),3.28–3.20(br,1h),2.61(hept,j=6.7hz,1h),0.97(d,j=6.9hz,6h).13cnmr(cdcl3):144.62,144.36,143.43,143.09,138.80,136.78(d,jpc=10.2hz),135.50(d,jpc=13.7hz),133.99,133.80,129.81,129.53(d,jpc=5.7hz),129.38,128.76,128.66(d,jpc=6.9hz),128.26,127.73,127.39,126.20,53.79,53.57,51.29,33.55,24.02.31pnmr(cdcl3):-16.28.anal.calcdforc54h48np:c,87.42;h,6.52;n,1.89.found:c,87.23;h,6.36;n,1.57.
实施例2、化合物al1(l1alme2)的制备
在氮气氛围下,将配体l1(2-ph2p-c6h4-ch2-nh-2,6-ph2ch-4-ipr-c6h2,0.367g,1mmol)溶于20ml甲苯中,缓慢加入1.1摩尔当量alme3(1.2mmol,0.6ml,2m甲苯溶液),80℃搅拌16小时。将甲苯溶剂减压除去,加入正己烷(3×10ml)洗涤,得到白色固体al1化合物0.354g,0.82mmol,82%。1hnmr(cdcl3):δ7.66(t,j=6.3hz,1h),7.47(t,j=7.5hz,1h),7.45–7.41(m,2h),7.39–7.32(m,4h),7.30–7.20(m,5h),7.10(t,j=8.3hz,1h),7.02(dd,j=8.5and7.3hz,2h),6.79(d,j=8.1hz,2h),6.49(t,j=7.2hz,1h),4.52(s,2h),-0.50(d,jph=4.3hz,6h).13cnmr(cdcl3):154.29,149.89(d,jpc=14.1hz),135.81,133.60(d,jpc=12.9hz),131.30,130.74,130.38(d,jpc=9.5hz),129.13,129.03,128.85,128.51,128.19,127.51(d,jpc=5.6hz),127.11,126.80,115.05,52.05,-7.92(d,jpc=21.1hz).31pnmr(cdcl3):-26.27.anal.calcdforc27h27alnp:c,76.58;h,6.43;n,3.31.found:c,76.50;h,6.22;n,3.18.
实施例3、化合物al2(l2alme2)的制备
实验步骤同实施例2,配合物al2(l2alme2)收率:0.361g,0.80mmol,80%。1hnmr(cdcl3):δ7.56–7.49(m,2h),7.49–7.43(m,4h),7.43–7.36(m,4h),7.31(t,j=7.4hz,1h),7.22(t,j=7.4hz,1h),7.09–7.01(m,2h),6.99(d,j=7.4hz,2h),6.84(t,j=7.4hz,1h),4.15(s,2h),1.98(s,6h),-0.67(d,jph=3.7hz,6h).13cnmr(cdcl3):152.46,150.98(d,jpc=13.4hz),137.80,134.92,134.03(d,jpc=12.7hz),130.95,130.80,129.15(d,jpc=9.1hz),128.89,128.82,128.59,128.08,127.40,127.11,127.01(d,jpc=5.7hz),122.61,57.49,19.59,-9.18(d,jpc=21.3hz).31pnmr(cdcl3):-25.01.anal.calcdforc29h31alnp:c,77.14;h,6.92;n,3.10.found:c,77.05;h,6.71;n,2.99.
实施例4、化合物al3(l3alme2)的制备
实验步骤同实施例2,配合物al3(l3alme2)收率:0.385g,0.76mmol,76%。1hnmr(cdcl3):δ7.53–7.49(m,2h),7.48–7.44(m,4h),7.39(t,j=8.4hz,4h),7.30(t,j=7.4hz,1h),7.22(t,j=7.4hz,1h),7.13(d,j=6.7hz,1h),7.10(d,j=6.5hz,1h),7.06–7.01(m,3h),4.22(s,2h,ch2-n),3.33(hept,j=6.9hz,2h,chmeme),1.07(d,j=6.9hz,6h,chmeme),0.80(d,j=6.9hz,6h,chmeme),-0.72(d,jph=3.9hz,6h,al-me).13cnmr(cdcl3):150.70,150.56,149.53(d,jpc=4.1hz),148.22(d,jpc=1.2hz),135.26,133.68(d,jpc=12.8hz),130.76,130.57,129.44(d,jpc=9.5hz),129.10,128.98(d,jpc=9.0hz),128.80,127.11,127.01(d,jpc=5.6hz),126.83,123.51,123.22,59.71(d,jpc=3.7hz),28.06,25.09,24.36,-9.88(d,jpc=21.5hz).31pnmr(cdcl3):-25.94.anal.calcdforc33h39alnp:c,78.08;h,7.74;n,2.76.found:c,77.98;h,7.49;n,2.65.
实施例5、化合物al4(l4alme2)的制备
实验步骤同实施例2,化合物al4(l4alme2)收率:0.686g,0.86mmol,86%。1hnmr(cdcl3):δ7.45–7.37(m,2h),7.36–7.29(m,8h),7.20–7.00(m,14h),6.94–6.87(m,1h),6.85(d,j=7.2hz,4h),6.81–6.76(m,4h),6.70(s,2h),6.20–6.21(m,1h),6.09(s,2h),3.84(s,2h),2.62(hept,j=6.9hz,1h),0.99(d,j=6.9hz,6h),-0.76(d,jph=4.2hz,6h).13cnmr(cdcl3):151.12,150.97,150.73(d,jpc=4.5hz),146.60,145.64,144.51,142.44,142.26,135.35,133.72(d,jpc=12.6hz),130.74,130.55,129.78(d,jpc=13.2hz),129.59,129.23,129.06,128.93(d,jpc=9.2hz),128.63,128.57,128.50,128.25,128.13,127.67(d,jpc=8.0hz),126.40,126.34,126.08,125.34(d,jpc=6.4hz),124.93,124.64,59.61,51.15,33.29,23.88,-8.71(d,jpc=21.9hz).31pnmr(cdcl3):-26.81.anal.calcdforc56h53alnp:c,84.29;h,6.69;n,1.76.found:c,84.02;h,6.51.49;n,1.88.
实施例6、化合物al1和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al1(8.5mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在25℃反应20min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:93%。该聚己内酯的数均分子量mn:1.24×104g/mol,分子量分布pdi=1.14。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例7、化合物al2和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al2(9.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在25℃反应20min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:79%。该聚己内酯的数均分子量mn:1.14×104g/mol,分子量分布pdi=1.20。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例8、化合物al3和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al3(10.2mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在25℃反应20min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:75%。该聚己内酯的数均分子量mn:1.01×104g/mol,分子量分布pdi=1.19。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例9、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al4(16.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在25℃反应20min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:95%。该聚己内酯的数均分子量mn:1.33×104g/mol,分子量分布pdi=1.14。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例10、化合物al1和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al1(8.5mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应10min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:>99%。该聚己内酯的数均分子量mn:1.31×104g/mol,分子量分布pdi=1.33。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例11、化合物al2和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al2(9.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应10min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:56%。该聚己内酯的数均分子量mn:8.3×103g/mol,分子量分布pdi=1.41。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例12、化合物al3和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al3(10.2mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应10min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:63%。该聚己内酯的数均分子量mn:8.7×103g/mol,分子量分布pdi=1.41。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例13、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,20μmol配合物al4(16.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应10min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:>99%。该聚己内酯的数均分子量mn:1.44×104g/mol,分子量分布pdi=1.21。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例14、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,10μmol配合物al4(8.0mg),1.1μl苄醇(10μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应15min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:96%。该聚己内酯的数均分子量mn:2.61×104g/mol,分子量分布pdi=1.41。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例15、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,4μmol配合物al4(3.2mg),0.4μl苄醇(4μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应30min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:>99%。该聚己内酯的数均分子量mn:5.12×104g/mol,分子量分布pdi=1.32。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例16、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,2μmol配合物al4(1.6mg),0.2μl苄醇(2μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应60min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:>99%。该聚己内酯的数均分子量mn:7.32×104g/mol,分子量分布pdi=1.29。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例17、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.456gε-己内酯,加入1mltol,2μmol配合物al4(1.6mg),0.2μl苄醇(2μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在110℃反应15min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:91%。该聚己内酯的数均分子量mn:1.19×105g/mol,分子量分布pdi=1.53。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例18、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,10μmol配合物al4(8.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应15min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:93%。该聚己内酯的数均分子量mn:1.29×104g/mol,分子量分布pdi=1.18。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例19、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,4μmol配合物al4(3.2mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应30min,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:97%。该聚己内酯的数均分子量mn:1.38×104g/mol,分子量分布pdi=1.13。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例20、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,2μmol配合物al4(1.6mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应2h,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:90%。该聚己内酯的数均分子量mn:1.18×104g/mol,分子量分布pdi=1.13。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例21、化合物al4和苄醇催化ε-己内酯的聚合
schlenk瓶中,无水无氧条件下,加入0.228gε-己内酯,加入1mltol,1μmol配合物al4(0.8mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应3h,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:90%。该聚己内酯的数均分子量mn:1.15×104g/mol,分子量分布pdi=1.10。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
实施例22、化合物al4和苄醇催化l-丙交酯的聚合
schlenk瓶中,无水无氧条件下,加入0.288gl-丙交酯,加入1mltol,20μmol配合物al4(16.0mg),2.1μl苄醇(20μmol)溶于1mltol,用注射器加入到schlenk瓶中引发聚合。控制反应温度在70℃反应4.5h,加入1ml5%乙酸甲醇溶液,倒入甲醇中使聚合物沉淀析出,过滤后真空干燥24小时得聚己内酯。转化率:91%。该聚己内酯的数均分子量mn:1.17×104g/mol,分子量分布pdi=1.16。数均分子量的测定方法为凝胶渗透色谱法,agilent1260infinity,thf为溶剂,流速1mlmin-1,测试温度40℃。
- 还没有人留言评论。精彩留言会获得点赞!
- 配体化合物、用于烯烃低聚反应的催化剂体系及使用该催化剂体系的烯烃低聚方法
- 配体化合物、茂金属化合物和使用其制备基于烯烃的聚合物的方法
- 一种配体化合物、制备方法及其应用
- 配体化合物、用于烯烃低聚反应的催化剂体系以及使用其的用于烯烃低聚反应的方法
- 配体化合物、用于烯烃低聚反应的催化剂体系以及使用其的用于烯烃低聚反应的方法
- 配体化合物、用于烯烃低聚反应的催化剂体系以及使用其的用于烯烃低聚反应的方法
- 配体化合物、有机铬化合物、用于乙烯低聚反应的催化剂体系以及使用其的乙烯低聚方法
- 一种含有双螺旋结构大环芳炔化合物及其合成方法
- 芳基连接的双酚盐的合成及其用于具有活化剂-载体的烯烃聚合催化剂系统的制作方法
- 一种氨基葡萄糖衍生配体化合物及制备方法、三羰基锝-99m标记的配合物、制备方法及用图