用于药物负载缓释的多级孔金属有机骨架材料的制备方法与流程
本发明属于药物负载和缓释载体制备领域,具体涉及一种用于药物负载和缓释的金属有机骨架材料(简称hp-cu-btc)的制备方法。
背景技术:
通常,由于药物在体内存在许多固有化的缺点,例如生理状况不稳定、溶解度低、毒副作用大等,导致许多临床药物的治疗效果大大降低,还对人体健康造成负面影响。近年来,为了满足高效利用药物的需求,药物缓释在药物研究领域备受关注,并已成为重要研究方向之一,其在减少服药次数、降低药物毒副作用及提高生物利用度等方面都具有重要意义。
药物载体材料是构成药物缓释系统的关键部分。现有的载体材料主要分为无机材料和有机材料。无机材料主要包括沸石、介孔二氧化硅等材料,但大多药物只能通过简单物理吸附连接在材料表面,所以载药率较低。有机材料主要包括脂质体、胶束等聚合物,但物化学稳定性较弱,因此在释放药物时存在“爆释”现象,无法达到提高药效的目的。
金属有机骨架材料(metalorganicframeworks,mofs)是一类由金属离子与有机配体配位桥接形成的多孔材料。mofs作为药物载体材料具有以下优点:(1)具有可调的孔道结构,通过对孔径尺寸的调节提高药物负载的选择性;(2)具有较高的比表面积,可提升药物负载率;(3)具有良好的生物相容性、生物降解性;(4)具有表面可修饰性,可通过化学修饰,调节药物负载以及释放性能。
目前为止,多级孔mofs主要通过模板辅助等方法直接合成得到的。例如,郑丽明等(功能材料,2015,11(46),11112-11117)采用三嵌段共聚物p123作为软模板剂,1,3,5-三甲苯、正癸烷作为扩孔剂,在水热条件下成功合成了hp-cu-btc。中国发明专利cn104667876b公开的技术方案采用nacl纳米粒子作为硬模板剂,通过调节nacl纳米粒子的用量,获得不同孔洞性质的多级孔mof材料。但是,对于大多数多级孔mofs而言,去除客体分子或后处理也会导致其骨架网络的相互交错或破坏,使mofs稳定性下降。除此之外,模板剂大都具有一定的生物毒性,在制备过程中难以去除,不适合应用于生物材料的制备。
技术实现要素:
有鉴于此,本发明的目的在于克服现有技术缺陷,提供一种用于药物负载和缓释的金属有机骨架材料(简称hp-cu-btc)的制备方法,其制备的hp-cu-btc药物载体具有比表面积高、孔径可调、结构相对稳定、生物相容性良好,载药量高,能够实现药物缓释的特点。
为了达成上述目的,本发明的技术方案是:
用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)制备离子液体微乳液:依次称取乳化剂和离子液体置于反应瓶中,混合搅拌10~20min,再加入醇类溶剂,搅拌20~30min,得到离子液体微乳液;
(2)制备金属有机骨架材料:将一定量的金属盐和有机配体依次倒入上述离子液体微乳液中,搅拌后转移至高压反应釜,通入co2,反应1~5h,反应结束后,进行清洗,而后进行干燥,干燥后得到金属有机材料hp-cu-btc。
进一步地,步骤(1)中,所述乳化剂为脂肪醇聚氧乙烯醚-5、脂肪醇聚氧乙烯醚-7、脂肪醇聚氧乙烯醚-9、聚乙二醇辛基苯基醚、壬基酚聚氧乙烯醚-10、山梨醇脂肪酸酯中的其中一种或多种混合。
进一步地,步骤(1)中,所述离子液体为1-乙基-3-甲基咪唑四氟硼酸盐、1-丁基-3-甲基咪唑四氟硼酸盐、1-丁基-3-甲基咪唑六氟硼酸盐、1-丁基-3-甲基咪唑六氟磷酸盐和1-丁基-3-甲基咪唑四氟磷酸盐中的其中一种或多种混合。
进一步地,步骤(1)中,所述醇类溶剂为甲醇、乙醇、乙二醇、丙醇、丙二醇和丙三醇中的其中一种或多种混合。
进一步地,步骤(1)中,所述离子液体和醇类溶剂的体积比为1:0.2~5。
进一步地,步骤(2)中,所述金属盐为无水硫酸铜、五水合硫酸铜、无水醋酸铜、一水合醋酸铜、无水硝酸铜和六水合硝酸铜中的其中一种或多种混合。
进一步地,步骤(2)中,所述金属盐与有机配体的摩尔比例为1:0.5~2。
进一步地,步骤(2)中,所述co2的压力为1~5mpa。
进一步地,步骤(2)中,所述有机配体为均苯三甲酸。
采用上述技术方案后,本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,具有以下有益效果:本发明利用高压co2可以改变溶剂的物理化学性质,促进金属有机材料的成核结晶过程,结合离子液体微乳液体系,能够在较短的时间内合成具有多级孔结构的hp-cu-btc,并且保证合成过程中的环保绿色,无其它添加剂。同时,该方法制备得到的hp-cu-btc具有高比表面积、孔径可调、结构稳定、生物相容性好等性质,不仅能够提高药物负载量与药物选择性,还实现药物的长效缓慢释放。
附图说明
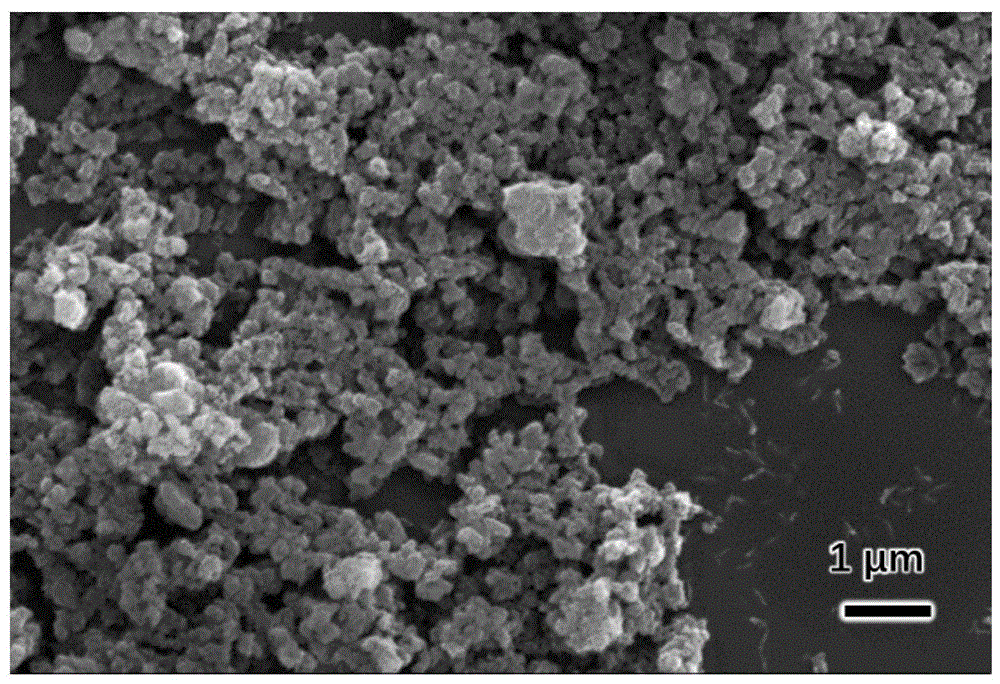
图1为本发明中实施例1制备的hp-cu-btc的扫描电镜图。
图2为本发明中实施例2制备的hp-cu-btc的n2物理吸附等温线图(内插图为孔径分布图)。
图3为本发明中实施例3制备的hp-cu-btc对盐酸阿霉素(dox)药物释放的曲线图。
具体实施方式
为了进一步解释本发明的技术方案,下面通过具体实施例来对本发明进行详细阐述。
实施例1
一、制备金属有机骨架材料(简称hp-cu-btc)
本发明用于药物负载缓释的金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取0.5mltx-100、3ml1-丁基-3-甲基咪唑六氟硼酸盐至反应瓶中,混合搅拌10min,再加入9ml丙二醇,搅拌30min,得到离子液体微乳液。
(2)将188mg金属盐无水硝酸铜[cu(no3)2]、104mg有机配体均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,然后转移至高压反应釜,通入压力3mpa的co2,反应3h,反应结束后,采用乙醇清洗3遍,而后置于60℃烘箱干燥,干燥后得到hp-cu-btc。
本发明的金属有机材料(hp-cu-btc)的sem图如图1所示,图中标尺为1μm,图1显示hp-cu-btc具有良好的粒度分散性,有利于药物的负载和释放。
需要说明的是,步骤(1)中,tx-100作为乳化剂使用,本发明的乳化剂为脂肪醇聚氧乙烯醚-5、脂肪醇聚氧乙烯醚-7、脂肪醇聚氧乙烯醚-9、聚乙二醇辛基苯基醚(tx-100)、壬基酚聚氧乙烯醚-10(tx-10)和山梨醇脂肪酸酯中的其中一种或多种混合。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即载药hp-cu-btc(hp-cu-btc-dox)室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为45%,载药率为31%,而传统cu-btc的包封率为23%,载药率为19%,验证了本发明hp-cu-btc具有较高的载药性能。
进一步地,在负载试验后,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs(磷酸缓冲盐溶液)进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=5时,其最终药物释放率为48%。
实施例2
一、制备hp-cu-btc
本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取1mltx-100、4ml1-丁基-3-甲基咪唑四氟磷酸盐至反应瓶中,混合搅拌10min,再加入8ml乙醇,搅拌30min。
(2)将250mg无水硫酸铜[cu(so4)2]、208mg均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,转移至高压反应釜中,通入5mpaco2,反应2h。反应结束后,采用乙醇清洗3遍,置于60℃烘箱干燥,干燥后得到hp-cu-btc。
hp-cu-btc的n2物理吸附等温曲线图及孔径分布图,如图2所示,其bet比表面积为380m2/g,而没有通入co2制备的传统cu-btc的bet比表面积仅为200m2/g,说明本发明hp-cu-btc具有较高的比表面积。吸附等温曲线有明显的回滞环,而且孔径大多分布在3nm以上,说明其具有多级孔结构。相比之下,许多传统方法制备的cu-btc材料的孔径均小于2nm,不具备多级孔结构。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即hp-cu-btc-dox室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为35%,载药率为26%。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=5时,其最终药物释放率为45%。
实施例3
一、制备hp-cu-btc
本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取1.2mltx-100、2ml1-丁基-3-甲基咪唑六氟磷酸盐至反应瓶中,混合搅拌20min,再加入8ml乙二醇,搅拌30min。
(2)将90mg无水醋酸铜[cu(oac)2]、52mg均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,转移至高压反应釜,通入5mpaco2,反应3h。反应结束后,采用乙醇清洗3遍,置于60℃烘箱干燥,干燥后得到hp-cu-btc。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即hp-cu-btc-dox室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为40%,载药率为29%。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。当pbs的ph=5时,药物释放曲线图(如图3所示)表明其药物释放较为缓慢,且48h后的最终药物释放率为52%,与传统cu-btc的药物释放率(15%)相比,本发明hp-cu-btc具有长效、有效的药物释放性能。
实施例4
一、制备hp-cu-btc
本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取2mltx-100、5ml1-丁基-3-甲基咪唑四氟硼酸盐至反应瓶中,混合搅拌15min,再加入5ml甲醇,搅拌30min。
(2)将150mg一水合醋酸铜[cu(oac)2·h2o]、104mg均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,转移至高压反应釜,通入3mpaco2,反应3h。反应结束后,采用乙醇清洗3遍,置于60℃烘箱干燥,干燥后得到hp-cu-btc。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即hp-cu-btc-dox室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为36%,载药率为26%。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=5时,其最终药物释放率为50%。
实施例5
一、制备hp-cu-btc
本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取1.5mltx-100、6ml1-丁基-3-甲基咪唑六氟硼酸盐至反应瓶中,混合搅拌20min,再加入4ml丙三醇,搅拌30min。
(2)将205mg六水合硝酸铜[cu(no3)2·6h2o]、104mg均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,转移至高压反应釜,通入5mpaco2,反应4h。反应结束后,采用乙醇清洗3遍,置于60℃烘箱干燥,干燥后得到hp-cu-btc。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即hp-cu-btc-dox室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为38%,载药率为27%。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=5时,其最终药物释放率为49%。
实施例6
一、制备hp-cu-btc
本发明用于药物负载缓释的多级孔金属有机骨架材料的制备方法,包括以下步骤:
(1)依次取2mltx-100、8ml1-乙基-3-甲基咪唑四氟硼酸盐至反应瓶中,混合搅拌20min,再加入2ml丙三醇,搅拌30min。
(2)将205mg六水合硝酸铜[cu(no3)2·6h2o]、156mg均苯三甲酸依次倒入离子液体微乳液中,搅拌1~2min,转移至高压反应釜,通入3mpaco2,反应5h。反应结束后,采用乙醇清洗3遍,置于60℃烘箱干燥,干燥后得到hp-cu-btc。
二、hp-cu-btc的负载和缓释试验
进一步地,称取20mghp-cu-btc加入2mg/ml盐酸阿霉素(dox·hcl)甲醇溶液中,避光搅拌12h,反应结束后离心,取上清液稀释后进行紫外测试(dox特征峰为495nm)。将离心得到沉淀物即hp-cu-btc-dox室温真空干燥24h,避光贮藏。结果表明该hp-cu-btc的包封率为44%,载药率为31%。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=7.4)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液进行紫外测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=7.4时,药物几乎无释放。
进一步地,称取5mghp-cu-btc-dox加入12mlpbs(ph=5)中,避光搅拌(37℃,150r/min)。在1h,3h,5h,8h,12h,24h,48h时分别离心取8ml上清液采用紫外进行药物浓度测试,再补充8ml新鲜pbs进入原溶液继续避光搅拌。研究表明,当pbs的ph=5时,其最终药物释放率为48%。
本发明公开了用于药物负载缓释的多级孔金属有机骨架材料的制备方法(简称hp-cu-btc)的制备方法,将hp-cu-btc的合成原料,依次溶解在含有连续相及分散相的离子液体微乳液中,随后通入co2高压气体,室温反应得到应用于药物递送的hp-cu-btc。该制备方法操作简单、工艺绿色环保、重复性好、耗时短,制备得到的hp-cu-btc,具有多级孔结构、比表面积大、载药量高、药物释放率高的特点,不仅能够提高药物负载量与药物选择性,实现药物的长效缓慢释放。
上述实施例和附图并非限定本发明的产品的制备方法,任何所属技术领域的普通技术人员对其所做的适当变化或修饰,皆应视为不脱离本发明的专利范畴。
- 还没有人留言评论。精彩留言会获得点赞!