一种阳离子型多孔材料的制备方法及其应用与流程
本发明属于金属-有机框架领域,具体涉及一种阳离子型多孔材料的制备方法及其应用。
技术背景
工业生产(金属电镀业,皮革制造与业和水泥生产业)过程中通常会产生的cr(vi)含氧阴离子(包括cro42-,cr2o72-和hcro4-)已被美国环境保护局归类为a类人类致癌物。因此,对废水中cr(vi)含氧阴离子的去除受到人们的重视。目前,去除cr(vi)含氧阴离子的方法有氧化还原法、沉淀法、生物处理和膜过滤等,其中吸附法操作简便,副产物少,可行性高,效率高,是去除水中含氧阴离子的最佳选择之一。
结构中具有阳离子纳米空腔和可交换阴离子的阳离子型多孔材料备受关注,因为这类材料可作阴离子吸附剂,通过阴离子交换吸附去除阴离子污染物。然而,与中性和阴离子型多孔材料相比,阳离子多孔材料数量较少。目前,主要的阳离子多孔材料为阴离子交换树脂、层状氢氧化物(ldh)、阳离子型金属-有机框架(mof)和阳离子聚合物网络(cpns)等。这些阳离子型材料在含氧阴离子吸附方面还存在诸如吸附容量低、吸附速率慢、重复使用率低、水中稳定性差等不足,因此,发展新型的阳离子型多孔材料非常有必要。
配位笼是一类具有特殊几何形状和内腔的离散的配位分子,目前在药物输送、分子识别和均相催化等研究领域都有潜在的应用。一些配位笼具有大的空腔和高的正电荷,可以吸附容纳阴离子,但是,由于它们的可溶性,往往用于溶液中的分子识别与催化等,很少作为固态吸附剂应用于液相吸附中。而且目前也没有针对重金属铬的具有高效吸附作用的基于配位笼的阳离子型多孔材料。
技术实现要素:
本发明的目的在于克服现有技术中配位笼溶解性的问题,难以作为固态吸附剂应用于液相吸附中,以及没有针对重金属铬的具有高效吸附作用的基于配位笼的阳离子型多孔材料的问题,提供了一种阳离子型多孔材料的制备方法及其应用。
本发明通过的目的通过以下技术方案予以实现:
一种阳离子型多孔材料的制备方法,包括以下步骤:
s1.制备amoc-1
s11.将3,5-二(4-吡啶基)-苯甲醛和硝酸钯按照摩尔比为2:(1~3)溶于溶剂中,排除溶液中的气体以后将溶液在60~80℃条件下反应5~10h;
s12.在步骤s11反应结束后,在溶液中加入体积为溶液体积3~5倍的二氧六环,完全沉淀以后过滤洗涤,保留沉淀物;
s2.制备cl-amoc-1
s21.将步骤s1得到的amoc-1和bapb按照质量比为(2~3):1混合,然后进行研磨25~40min;
s22.将步骤s21研磨之后的混合物用有机溶剂进行洗涤,然后干燥即得。
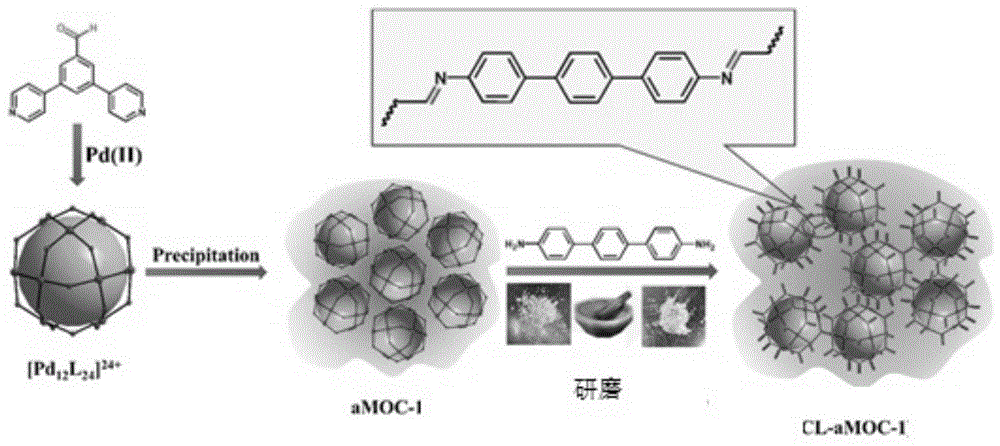
本发明的方法,通过将配位笼进一步通过共价键链接起来,形成扩展的基于配位笼的框架材料,可以降低材料在水中的溶解性以及提高稳定性,使其适合于液相吸附应用中。如图1所示,本发明构建阳离子型多孔材料的路线,首先选用同时包含配位点和共价反应位点的有机配体与pd(ii)离子组装成具有共价反应位点的配位笼,即通过3,5-二(4-吡啶基)-苯甲醛和硝酸钯反应形成分子笼pd12l24(l为3,5-二(4-吡啶基)-苯甲醛),然后再通过1,4-二(4-氨基苯基)苯(bapb)与上述分子笼上的醛基反应形成共价键,将多个分子笼连接形成具有三维框架的多孔材料。
优选地,所述步骤s11中,3,5-二(4-吡啶基)-苯甲醛和硝酸钯的摩尔比为2:1。
优选地,所述步骤s11中,反应时间为8h。
优选地,所述步骤s12中,用丙酮对沉淀进行洗涤,然后再在60~80℃干燥5~7h。
优选地,所述步骤s21中,amoc-1和bapb的质量比为2.5:1。
优选地,所述步骤s22中,洗涤具体步骤为:先用60~75℃的二甲基亚砜进行洗涤3~6次,然后再用丙酮洗涤2~5次。
上述阳离子型多孔材料的制备方法所制备得到的阳离子型多孔材料。
上述阳离子型多孔材料在吸附cro42-和cr2o72-上的应用。
优选地,在ph为2~8的环境中对cro42-和cr2o72-的吸附。
与现有技术相比,本发明具有以下技术效果:
本发明提供的一种阳离子型多孔材料的制备方法,反应条件温和,在常温研磨的反应条件下,将含醛基的阳离子配位笼(amoc-1)与1,4-二(4-氨基苯基)苯(bapb)通过醛胺缩合反应连接成一种无定型的阳离子型多孔框架材料cl-amoc-1。cl-amoc-1可快速高效地吸附水中cro42-和cr2o72-,饱和吸附容量分别为245.1mg/g和311.5mg/g。吸附的cr(vi)含氧阴离子可以快速地洗脱,该材料的循环使用性能良好。此外,cl-amoc-1可用去除电镀废液中的cr(vi)。
附图说明
图1本发明合成原理流程示意图;
图2实施例获得的cl-amoc-1的pxrd图(a),amoc-1、cl-amoc-1和bapb的红外光谱(b),amoc-1和cl-amoc-1的拉曼光谱(c);
图3实施例获得的cl-amoc-1的热重曲线(a),cl-amoc-1在77k下的n2吸附等温线(插图为相应的孔径分布)(b);
图4实施例获得的cl-amoc-1的扫描电镜图;
图5cl-amoc-1与cr2o72-(a)和cro42-(b)离子作用的随时间变化的紫外光谱;
图6cl-amoc-1对三种含氧阴离子的吸附数据与拟一级动力学模型(a)和拟二级动力学模型(b)拟合;
图7cl-amoc-1对两种含氧阴离子的吸附等温线(t=48h,t=30℃)(a);含氧阴离子吸附数据分别与langmuir(b)、freundlich(c)和temkin(d)吸附方程的拟合;
图8cr2o7@cl-amoc-1在nano3溶液中解吸20min的紫外光谱(a);cl-amoc-1对cr2o72-的可循环吸附性能(b);
图9ph对cl-amoc-1吸附cr(vi)的影响(a);竞争阴离子对cl-amoc-1吸附含氧阴离子去除率的影响(b);
图10在不同时间cl-amoc-1吸附含cr(vi)电镀废水的紫外光谱(a);在不同时间点cl-amoc-1吸附cr(vi)时,电镀废水中cr的浓度的变化(b);吸附电镀废液cr(vi)后的解吸实验(插图为相应的溶液或固体的颜色变化)(c)。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面结合具体实施例和对比例将对本发明的技术方案进行详细的描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本发明所保护的范围。
除特殊说明,本实施例、对比例以及实验例中所用的设备均为常规实验设备,所用的材料、试剂无特殊说明均为市售得到,无特殊说明的实验方法也为常规实验方法。
实施例
s1.制备amoc-1
向15ml的反应瓶中加入3,5-二(4-吡啶基)-苯甲醛(52mg,0.20mmol)、二水合硝酸钯(26.6mg,0.10mmol)和6ml二甲基亚砜。向反应瓶中鼓入氩气30秒,充分进行气体置换。放入70℃恒温烘箱中,加热8小时,得溶液为澄清的橙黄色溶液。向该溶液中缓慢加入24ml二氧六环,得到白色絮状物,离心分离,收集白色固体,用丙酮洗涤三次,浸泡3天,70℃下真空干燥6小时,即可得产物;
s2.制备cl-amoc-1
将75mgamoc-1和27mgbapb置于研钵中,用小药勺混匀,然后研磨30分钟。肉眼可观察到混合物的颜色从浅灰色变为黄色。用70℃的二甲基亚砜洗涤所得的固体4次(每次用15ml),接着用丙酮洗涤3次(每次15ml),目的是洗去未反应的amoc-1和bapb。最后,将黄色的固体真空100℃干燥12h得到cl-amoc-1,产率为86%。
实验例
(1)实验仪器:
日本理学rigakux射线粉末衍射仪(室温,40kv,40ma)、德国铂金·埃尔默spectrumtwo傅里叶变换红外光谱仪(数据收集范围为4000至400cm-1)、renishawinvia共聚焦显微拉曼光谱仪(数据收集范围为2000至200cm-1,激光波长为785nm)、德国耐驰tg209f3热重分析仪(氮气氛围,升温速率10℃min-1,30-800℃)、美国麦克asap2460气体吸附仪(77k,通过氮气的吸附-脱附评价孔结构)、英国马尔文zetasizernanozs90纳米粒径电位分析仪(25℃,悬浊液样品浓度为0.5mg/ml)、美国phenomprox台式扫描电子显微镜-能量光谱仪、美国赛默飞世尔k-alpha+x-射线光电子能谱仪、日本岛津uv-2700紫外可见分光光度计(带积分球)、美国赛默飞世尔icap-7400电感耦合等离子发射光谱仪。
(2)实验试剂:
配体3,5-二-4-吡啶基苯甲醛购买于广州研创生物技术发展有限公司;pd(no3)2·2h2o购买于北京华威锐科化工有限公司;k2cro4、k2cr2o7和1,4-二(4-氨基苯基)苯(bapb)购买于上海阿拉丁生化科技股份有限公司;溶剂试剂由天津大茂化学试剂厂购买。
(3)对实施例获得的阳离子多孔材料(cl-amoc-1)通过pxrd、红外光谱以及拉曼光谱进行表征,表征结果如图2所示。
合成后的cl-amoc-1的pxrd图谱仅有一个宽峰,表明cl-amoc-1是无定形粉末(图2a)。从红外光谱分析可以看出,cl-amoc-1的大多数峰与amoc-1的峰相似,这意味着笼状结构在cl-amoc-1中保留了下来。与反应原料bapb和amoc-1的红外光谱相比,cl-amoc-1的氨基(3200-3600cm-1)和醛基(1699cm-1)的峰强度明显降低(图2b),表明氨基和醛基发生了反应。此外,在1491cm-1出现了一个新峰,这可能归属于bapb中苯基的伸缩振动。在拉曼光谱中(图2c),1705cm-1处属于醛的峰在cl-amoc-1中消失了,这进一步证实了c=o发生了反应;同时,1608cm-1处的峰增强且变宽,这可能是由联苯结合到cl-amoc-1后c=c键的伸缩振动增强引起;在1174和1199cm-1处观察到了一些新峰,这可能是由bapb的c-n键振动引起。
(4)对实施例获得的阳离子多孔材料(cl-amoc-1)进行热重分析、对n2的吸附-解吸以及sem表征,结果如图3所示。
如图3a所示,cl-amoc-1在120℃之前仅有轻微的重量损失;在160℃时观察到约9.5%的重量损失,这可能是一些只反应了一个氨基的bapb分子的释放失重。框架在约270℃有一个平台,在此温度前框架温度,温度高于270℃时整个框架开始分解。cl-amoc-1对n2的吸附-解吸等温线(图3b)属于具有h3滞后环的iv型等温线,表明了介孔结构的存在。cl-amoc-1的比表面积为11.13m2/g。比表面这么小可能是因为空腔被大量的no3-阴离子占据,这在阳离子骨架中是一种常见的现象。另外,bjh孔径分布表明cl-amoc-1中存在两种类型的孔(图3b插图):一种大约2nm,可能是由moc的孔腔引起;另一种是大约10nm,可能是由moc之间通过bapb连接引起。从sem图可观察到,cl-amoc-1呈现不规则的颗粒状,粒径范围约为500至2000nm(图4)。
(5)吸附动力学实验:将10mgcl-amoc-1固体添加到30ml10-4m的含氧阴离子水溶液中,持续搅拌悬浮液,在给定的时间点取约2.5ml上清液测定含氧阴离子的浓度。cr(vi)含氧阴离子的浓度通过uv-vis测定。
选择两种含氧阴离子cro42-和cr2o72-来研究cl-amoc-1的吸附性能。如图5所示,加入cl-amoc-1后,cro42-、cr2o72-的浓度迅速降低。仅3min后,cro42-和cr2o72-的去除率分别约为99.7%和88.0%,它们几乎在5min内达到吸附平衡,相应的去除率分别99.7%和97.85%。
用拟一级动力学和拟二级动力学方程来分析随时间变化的吸附容量数据,结果表明,拟二级动力学的拟合效果明显比拟一级动力学好。如图6和表1所示,cro42-、cr2o72-的拟二级动力学方程拟合的r2值分别为0.9996、0.9949(图6b),而拟一级动力学方程拟合的r2值仅有0.5269-0.7303(图6a)。结果表明,cl-amoc-1对含氧阴离子吸附速率决定步骤可能是一个化学过程。
表1cl-amoc-1吸附含氧阴离子的平衡容量、速率常数及其相关系数r2
(6)将5mgcl-amoc-1加入浓度范围为10~400ppm系列含氧阴离子水溶液(25ml)中,静置24h,然后测定各含氧阴离子的平衡浓度。实验平行3次,取平均值用于吸附容量的计算和相关数据的拟合。
测定了含氧代阴离子的吸附等温线,进一步探究cl-amoc-1的吸附容量。如图7a所示,cl-amoc-1对cro42-和cr2o72-的最大吸附容量分别为224mg/g和323mg/g。用三种不同的吸附等温方程,即langmuir模型、freundlich模型和temkin模型,来拟合不同含氧阴离子的吸附等温线数据。拟合结果见图7b-7d和表2。cr2o72-的相关数据最符合langmuir模型,r2为0.9633,这表明cl-amoc-1对cr2o72-的吸附可能是典型的单分子层吸附。而cro42-除了langmuir方程拟合程度较好外,freundlich方程拟合程度也较适当,这表明这两个阴离子的吸附不仅单分子层吸附,而且吸附可能受到了cl-amoc-1表面活性位点分布不均匀影响。
表2cl-amoc-1对不同含氧阴离子的吸附参数
(7)为了测试cl-amoc-1的循环使用性质,将进行过吸附实验的吸附剂通过离心回收,然后加入到一定体积1mnano3溶液洗脱,1h后可达到脱附平衡。通过uv-vis光谱法测定含氧阴离子的浓度。
吸附剂的回收在实际的工业上应用中有着至关重要的作用。因此,选择了在50ppmcr2o72-溶液中饱和吸附后的cr2o7@cl-amoc-1进行的解吸实验。当将cr2o7@cl-amoc-1浸入1mnano3水溶液中时,仅1min后就大约解吸了70%的所吸附的离子,且20min内达到解吸平衡(图8a)。解吸样品洗涤干燥活化后再次用于cr2o72-的吸附,结果如图8b所示。5个循环后,相对吸附容量仍有原来的85%,这表明cl-amoc-1具有良好的可回收性。
(8)选择性吸附实验:将5mgcl-amoc-1加到25ml含氧阴离子和干扰离子(cl-,no3-,clo4-,so42-)等摩尔比(1:1,1mm)的混合溶液中,静置24h后测定分析对象的平衡浓度。
实际的工业废水的ph通常是偏酸或偏碱的,因此探究ph值对cl-amoc-1吸附cr(vi)的影响是很有必要的。从图9a可以看出,该吸附剂在ph为2~8的范围内对cr(vi)的去除率超过80%。当ph值大于9时,去除率开始下降。表明cl-amoc-1在弱碱、中性和酸性环境的吸附作用更好。
通过添加相同摩尔当量的竞争离子(cl-,no3-,clo4-,so42-),探索了竞争离子对含氧阴离子去除的影响。如图9b所示,在大多数情况下,目标含氧阴离子的相对去除率仍超过85%。
(9)在电镀废液中cr(vi)的吸附测试
含cr(vi)的电镀废水是电镀行业常见的污染源,只有对其进行去污处理才能排放到自然水体中。含cr(vi)的电镀废水通常是酸性的,并且含有硫酸根离子,从上述吸附研究结果来看,cl-amoc-1可适用于去除电镀废水中cr(vi)含氧阴离子。为了证实这一点,将20mgcl-amoc-1添加到30ml电镀废水(适当稀释使其可用于仪器检测)中,并通过uv-vis和icp检测cr(vi)的浓度随时间的变化。从紫外吸收光谱的结果可以看出,cr(vi)的浓度仅在1min内就大大降低,并且在3min内基本达到吸附平衡(图10a)。icp测试表明,cr(vi)的浓度从吸附前的22.4ppm降低到吸附后的0.47ppm(图10b),此浓度已达到污染物排放标准。此外,溶液的颜色从浅黄色变为无色,粉末的颜色变深,这也证实了cr(vi)含氧阴离子的吸附。cr(vi)解吸实验发现吸附在cl-amoc-1上的含氧阴离子可以解吸(溶液由无色变为浅黄色),表明该材料可以重复使用(图10c)。
最后应当说明的是,以上实施例仅用以说明本发明的技术方案,而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细地说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!