一种轴手性聚集诱导发光化合物及其制备方法与应用与流程
本发明涉及荧光材料领域,特别是涉及一种具有聚集诱导发光特性的轴手性化合物及其制备方法与应用。
背景技术:
在固态或聚集状态使用的新型有机发光半导体功能材料,与传统无机半导体材料相比,具有高灵敏性、好的器件柔性、低成本、小装置尺寸、大面积制备以及便于集成等优势,在有机光电子研究领域受到越来越多的关注(Chem.Phys.Lett.,1974,29,277,Chem.Rev.2007,107,1011)。除了有机光电子器件,有机发光材料在信息存储(J.Mater.Chem.C,2013,1,3376;Chem.Soc.Rev.,2013,42,857;Adv.Mater.,2013,25,378;Chem.Soc.Rev.,2013,42,8895.)和生物科学(Chem.Rev.,2013,113,192;Chem.Sci.,2012,3,984.)等方面也表现出广泛的应用。
在现代技术应用中,荧光材料往往需要制成固体或薄膜形式,荧光分子间呈现聚集状态。传统的荧光化合物在聚集状态下荧光减弱甚至不发光,即聚集导致了荧光猝灭(aggregation-caused quenching,ACQ)。这一现象使有机荧光材料的发展受到了限制,因此急需开发在聚集状态下保持强发光的材料和系统。在2001年,唐本忠等发现苯基噻咯类化合物(Chem.Commun.2001,1740.)具有聚集诱导发光特性(aggregation-induced emission,AIE)。具有聚集诱导发光性质的化合物从根本上克服了聚集导致荧光猝灭的难题,引起了广泛的研究兴趣,至今已开发出覆盖可见波长范围的AIE体系,并将具有这种特性的荧光分子应用于生物/化学传感器(J.Mater.Chem.2010,20,1858.)及光电材料(Acc.Chem.Res.2012,45,544.)等领域。
近年来,可用于手性识别的新型传感器研究受到广泛的关注。手性识别是当前生物分析和现代药物研发等领域中的关键课题,对药物研发以及疾病诊断等领域具有重要的意义。聚集诱导发光材料主要基于非手性化合物,而具有手性特征的聚集诱导发光材料的开发和研究相对滞后,限制了其在手性识别领域中的应用。此外,现有技术中的方法是通过金属催化偶联生成多芳基取代乙烯或者环戊二烯结构,并扩大分子的π共轭结构来增大分子发射波长。这种方法不足之处在于合成路线步骤长、合成工作量大,得到的化合物分子间相互作用的增强易导致诱导发光淬灭、易受光氧化影响以及产物溶解度降低等问题。
技术实现要素:
针对现有技术的以上缺陷和不足,本发明提供了一种轴手性荧光染料化合物及其制备方法与应用,目的在于合成出具有聚集诱导发光性质的轴手性荧光染料。
本发明提供的轴手性荧光染料化合物,其消旋体结构通式为:其中,R为乙氧基和甲基中的至少一种;其S型手性对映异构体的结构式为:其中,R独立地选自:乙氧基、甲基中的一种;其R型手性对映异构体的结构式为其中,R独立地选自:乙氧基、甲基中的一种。
本发明提供的制备上述轴手性荧光染料化合物的方法,包括如下步骤,其中,所述R为乙氧基:
在哌啶存在的条件下,将2,2’—二羟基—[1,1’—联萘]—3,3’—二醛和丙二酸二乙酯于有机溶剂中回流反应,得到所述轴手性化合物。
该方法的步骤中,所述有机溶剂为下述两种溶剂中的至少一种:甲醇或者乙醇;所述2,2’—二羟基—[1,1’—联萘]—3,3’—二醛独立地选自:2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体、S型对映异构体、R型对映异构体中的一种;所述哌啶与所述2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的摩尔比为1:1-1:10,优选1:1;所述丙二酸二乙酯与2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的摩尔比为1:1-3:1,优选2:1;回流反应中,时间为6-48小时,优选6-24小时,温度为50-80℃,优选60-80℃。
此外,本发明提供的制备上述轴手性荧光染料化合物的方法,包括如下步骤,其中,所述R为甲基:
在哌啶存在的条件下,将2,2’—二羟基—[1,1’—联萘]—3,3’—二醛和乙酰乙酸乙酯于有机溶剂中回流反应,得到所述轴手性化合物。
该方法的步骤中,所述有机溶剂为下述两种溶剂中的至少一种:甲醇或者乙醇;所述2,2’—二羟基—[1,1’—联萘]—3,3’—二醛独立地选自:2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体、S型对映异构体、R型对映异构体中的一种;所述哌啶与所述2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的摩尔比为1:1-1:10,优选1:1;所述乙酰乙酸乙酯与2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的摩尔比为1:1-3:1,优选2:1;回流反应中,时间为6-48小时,优选6-24小时,温度为50-80℃,优选60-80℃。
另外,本发明提供的上述轴手性荧光染料化合物在制备手性有机发光材料、轴手性荧光探针及其在荧光识别中的应用,也属于本发明的保护范围。
本发明提供的轴手性荧光染料化合物,由于其骨架为由香豆素组成的共轭体系,因而具有香豆素类荧光染料的特点,具有较长的发射波长、大斯托克斯位移,在固体状态时呈现黄色荧光。在四氢呋喃\水的混合溶液中,此类化合物的荧光强度随水比例的增加逐渐增强,含水比例为80%时达到最大,这说明其具有聚集诱导发光增强效应。本发明提供的上述轴手性荧光染料化合物的方法,合成简单,产物产率高,经仪器检测所得化合物的结构正确,稳定性好,在有机发光材料和荧光测试领域具有很好的应用前景。
【附图说明】
图1为实施例1制备所得轴手性荧光染料化合物的核磁氢谱。
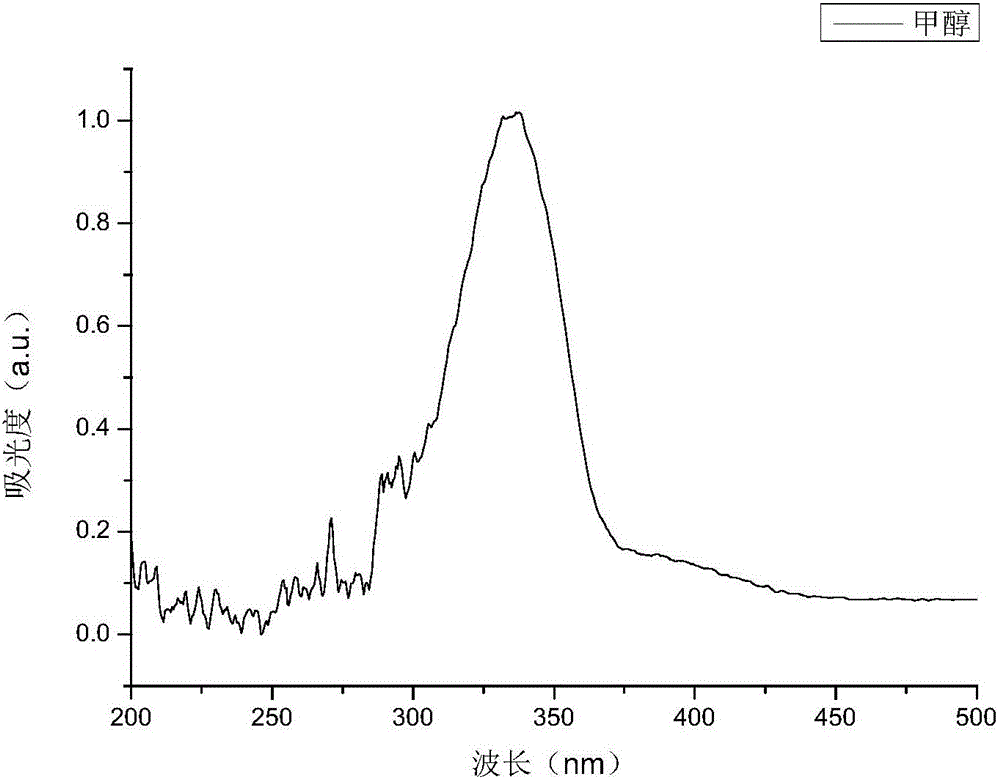
图2为实施例1制备所得轴手性荧光染料化合物的激发光谱。
图3为实施例1制备所得轴手性荧光染料化合物在甲醇溶液中的发射光谱。
图4为实施例1制备所得轴手性荧光染料化合物在四氢呋喃和水的混合溶液中的发射光谱。
【具体实施方式】
下面结合具体实施例对本发明作进一步说明,但本发明并不限于以下实施例。
实施例1、
反应式如下:
在100mL圆底烧瓶中依次加入1.0g(2.9mmol)2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体、50mL乙醇、0.94g(6.0mmol)丙二酸二乙酯和0.25g(2.9mmol)哌啶,加热回流24h,冷却至室温,有固体析出,过滤,干燥,得到黄色粉末状产物1.1g,产率70%。
将上述实施例中2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体换为S型2,2’—二羟基—[1,1’—联萘]—3,3’—二醛,其他步骤与上述实施例完全相同,得到S型产物。
将上述实施例中2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体换为R型2,2’—二羟基—[1,1’—联萘]—3,3’—二醛,其他步骤与上述实施例完全相同,得到R型产物。
该化合物的结构检测结果如下:
S型产物的比旋光度:[α]D25=+140(c=0.05,CH2Cl2);R型产物的比旋光度:[α]D25=-166(c=0.05,CH2Cl2);
1H NMR(500MHz,CDCl3)δ8.71(s,2H),8.37(s,2H),8.07(d,J=8.2Hz,2H),7.52(t,J=7.5Hz,2H),7.40(t,J=7.6Hz,2H),7.14(d,J=8.5Hz,2H),4.40(q,J=7.1Hz,4H),1.40(t,J=7.1Hz,6H)。
HRMS(ESI)m/z=535.1377(calcd for C32H22O8+H+=535.1387)。
图1为该实施例制备所得轴手性荧光化合物的核磁氢谱,由上述检测结果可知,该化合物结构正确。
实施例2、
反应式如下:
在100mL圆底烧瓶中依次加入1.0g(2.9mmol)2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体、50mL乙醇、0.78g(6.0mmol)乙酰乙酸乙酯和0.25g(2.9mmol)哌啶,加热回流24h,冷却至室温,有固体析出,过滤,干燥,得到黄色粉末状产物1.0g,产率73%。
将上述实施例中2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体换为S型2,2’—二羟基—[1,1’—联萘]—3,3’—二醛,其他步骤与上述实施例完全相同,得到S型产物。
将上述实施例中2,2’—二羟基—[1,1’—联萘]—3,3’—二醛的外消旋体换为R型2,2’—二羟基—[1,1’—联萘]—3,3’—二醛,其他步骤与上述实施例完全相同,得到R型产物。
该化合物的结构检测结果如下:
S型产物的比旋光度:[α]D25=+234(c=0.05,CH2Cl2);R型产物的比旋光度:[α]D25=-258(c=0.05,CH2Cl2);
1H NMR(500MHz,(CD3)2SO)δ8.92(s,2H),8.91(s,2H),8.27(d,J=8.3Hz,2H),7.64(t,J=7.5Hz,2H),7.53(t,J=7.6Hz,2H),7.16(d,J=8.6Hz,2H),2.55(s,6H)。
HRMS(ESI)m/z=475.1169(calcd for C30H18O6+H+=475.1176)。
由上述检测结果可知,该化合物结构正确。
紫外和荧光光谱的测定(以实施例1所得产物为例),配制10-3mol/L待测物的N,N-二甲基甲酰胺溶液为母液。以甲醇为溶剂,将母液分别稀释至10-5mol/L和10-6mol/L;以四氢呋喃和四氢呋喃\水的混合溶液为溶剂,将母液稀释至10-6mol/L。选取10-5mol/L待测物的甲醇溶液测定其紫外-可见吸收光谱,得到紫外-可见吸收曲线,其最大吸收峰在330nm处。以330nm为激发波长,选取10-6mol/L待测物的甲醇溶液测定其荧光光谱,得到荧光发射曲线,其最大发射波长在505nm处。以330nm为激发波长,选取10-6mol/L待测物的四氢呋喃和四氢呋喃\水的混合溶液测定其荧光光谱,得到荧光发射曲线。与四氢呋喃溶液相比,在四氢呋喃\水的混合溶液中,待测物的最大发射波长发生明显红移,而且在505nm处其荧光强度随水比例的增加逐渐增强,含水比例为80%时荧光强度达到最大。其中,图2为实施例1制备所得化合物的激发光谱;图3为实施例1制备所得化合物在甲醇溶液中的发射光谱;图4为实施例1制备所得化合物在四氢呋喃和水的混合溶液中的发射光谱。
- 还没有人留言评论。精彩留言会获得点赞!