一种测定生物样品中糖复合物含量的新方法与流程
本发明涉及糖复合物(多糖、糖蛋白、糖脂)在生物样品中简单、灵敏、准确、无放射性污染、适用范围广泛的检测和示踪方法。属于药物分析技术领域。
背景技术:
糖复合物是生物体内除蛋白质和核酸以外的又一类重要的生物大分子,具有多种多样的生物学功能,它几乎没有小分子化合物具有的异化生物代谢毒性,使用比较安全,和其他药物的相互作用比较少。由于其上述特点和对许多目前缺少治疗药物的疾病具有良好的前景,已成为生命科学研究和新药开发中极受重视的一类化合物。但是,由于其结构十分复杂,分离纯化困难,缺少简单、灵敏的检测方法,其生物利用度和药代动力学的研究十分困难,严重制约了其研究和开发。
生物利用度和药代动力学是借助动力学原理对药物的吸收、分布、代谢和排除(ADME)过程进行研究。它是集中药理学、药物化学、分析化学、数学等学科于一体的边缘学科。它承担着阐明药物作用机制和科学内涵;设计及优选给药方案;促进新药开发剂型优选和质量控制;在药物的研发、应用中具有重要的作用和位置。
糖复合物的生物利用度和药代动力学的研究相对困难,主要原因是缺少理想的在生物样品中的检测方法。目前糖复合物生物样品中的检测方法主要有:色谱法、放射性同位素标记法、荧光测定法和生物测定法。由于糖类结构及其在体内代谢的特点,其样品和代谢产物是一组结构和分子量近似的化合物。色谱法、生物法、荧光标记法对糖类化合物的药代动力学研究,或因为检测方法灵敏度不高、干扰强或因生物样品处理困难、对测定结果影响严重等原因,使其应用受到严重限制。同位素标记法应用的较多,该方法的灵敏度高、适用范围广,应用较多。但是该方法对实验条件要求苛刻和成本高、易造成放射性污染。寻找和建立简单、方便的示踪和测定方法,是在糖复合物药代动力学,包括生物利用度研究中的关键技术,也是糖复合物研究中亟待解决的关键科学问题之一。
糖蛋白因其含有胺基或酪氨酸可同碘发生取代反应,对于不含有胺基的糖复合物,可通过制备它的荧光素衍生物后,再进行碘代反应,生成稳定的、对糖类结构影响较小的碘代化合物。在同位素标记法进行糖的药代动力学研究中,以碘的放射性同位素对糖复合物进行标记是经典和适用的方法。
电感耦合等离子体质谱(Inductively coupled plasma mass spectrometry,ICP-MS),是近年发展起来的新的分析测试技术。它不仅可以取代传统的无机分析技术如电感耦合等离子体光谱技术、石墨炉原子吸收等,进行定性、定量分析及同位素比值的准确测量等,还可检测上述方法难以检测的元素,如卤族元素;同时它还可以与其他技术如HPLC、HPCE、GC联用进行元素的形态、分布特性等的分析,具有灵敏度高、结果稳定的特点。将碘代多糖与ICP-MS检测技术相结合,集成创新,有望建立一种新的简单、方便、可靠、适用范围广的糖复合物示踪和测定方法。
本发明完成前未发现有关碘代糖复合物与ICP-MS相结合测定生物样品中糖复合物含量的报道,本发明具有广泛的应用前景。
技术实现要素:
本发明的目的之一是制备碘代糖复合物.根据糖复合物化学性质的不同,进行不同的取代反应.
一、对于含有络氨酸糖复合物,直接通过化学反应,以共价键与碘连接,生成碘代糖复合物。该反应可通过氯胺T催化,直接进行碘的取代反应,生成碘代多糖.
二、对多糖、糖脂类不含有可同碘直接发生取代反应的成分,首先制备其与荧光素的衍生物,再将碘与荧光素反应,制备碘-荧光素-多糖复合物。
本发明的目的之二是以电感耦合等离子体质谱(Inductively coupled plasma mass spectrometry,ICP-MS)测定碘代糖复合物的含量。
ICP-MS是近年发展起来的新的分析测试技术。它不仅可以取代传统的无机分析技术如电感耦合等离子体光谱技术、石墨炉原子吸收等,进行定性、定量分析及同位素比值的准确测量等,还可检测上述方法难以检测的元素,如卤族元素;同时它还可以与其他技术如HPLC、HPCE、GC联用进行元素的形态、分布特性等的分析,具有灵敏度高、结果稳定的特点。
本发明是根据测定的碘含量,计算各样品中糖复合物的含量。将碘代多糖与ICP-MS检测技术相结合,建立新的生物样品中测定多糖含量的方法,为集成创新,该方法是简单、方便、可靠、适用范围广的糖复合物的示踪和测定方法,具有实质的突出特点和显著的技术进步。
具体操作为:
1、一种测定生物样品中多糖含量的新方法,所述的方法为:
(1)糖蛋白中含有游离胺基,在催化剂的催化下,游离胺基中的氢可被碘取代,生成碘代多糖,具体操作方法为:取糖蛋白样品0.2g,以水5ml溶解,以氯胺T为催化剂,加入浓度为0.5mol/L的碘化钾碘1ml,进行碘代反应,反应产物经凝胶柱层析纯化,收集糖蛋白类化合物部分,冷冻干燥得到碘代糖蛋白;
(2)对于不含有游离氨基的多糖、糖脂,可首先制备它们与荧光素的衍生物,再与碘进行取代反应,具体操作方法为:取样品1g,溶解二甲基亚砜在10ml中,加吡啶10滴,加入荧光素0.1g,再加入二月桂酸二丁基锡20mg,95℃混合加热2小时,加入无水乙醇50mL,放置,倾去上清,以乙醇反复清洗,洗去多余的染料,离心,得荧光素-多糖复合物,该复合物按照步骤(1)中所述进行碘代反应,制得碘代多糖或碘代糖脂;
(3)由步骤(1)或者(2)所制备的糖复合物的碘代产物,进行动物或细胞实验,收集需测定的样品,经消化后,以ICP-MS测定样品中碘的含量,根据样品中碘的标记量,换算成各样品中糖复合物的含量。
下面以银耳糖蛋白为例对本发明测定方法的具体内容进行详细说明。由于无市售样品可用,我们需自制银耳糖蛋白,作为研究的样品。
糖复合物包含糖蛋白、多糖和糖脂。糖蛋白均含有一定量的络氨酸,可同碘直接发生取代反应;多糖和糖脂由于不含有可同碘直接发生反应的基团,需制成可同碘发生取代反应的衍生物后,与碘反应生成碘代衍生物。生成的碘代糖复合物,测定碘含量后,进行动物或细胞实验,制备需要的生物样品;经消解后,以ICP-MS测定其中碘的含量,根据样品中碘含量,计算样品中糖复合物的含量。
一.碘代糖蛋白-的制备
1.银耳糖蛋白的制备 我们以前的研究表明,采用适当的方法,可由银耳制备银耳糖蛋白,解决无合适商品试剂的问题。因此糖蛋白以银耳多糖复合物为代表.制备方法为:取银耳孢糖一公斤,加入5倍量纯水,加温至70℃,搅拌2小时,离心(3000rpm,10min.),收集上清液,减压蒸发至700ml,搅拌下加无水乙醇4000ml,静置过夜后离心,收集沉淀部分,冷冻干燥。粗制银耳糖蛋白经Sephadex G-100中压凝胶柱层析,收集分子量1万的部分,浓缩,冻干,得到银耳糖蛋白。
2.银耳糖蛋白样品的分析 干燥后的样品中总糖、糖醛酸、蛋白质分别以苯酚-硫酸法、间羟二酚法、Lowery法测定,甘露糖、葡萄糖醛酸和牛血清白蛋白为标准品,结果表明其中总糖的含量为80.2%,糖醛酸含量为6.5%,蛋白质含量为7.8%;分子量分布以HPGPC法测定,以系列右旋糖酐为分子量对照品,OHPAK-SB804HQ色谱柱,RID-10A检测器,流动相为0.7%的硫酸钠溶液,结果通过GPC软件计算,银耳多糖复合物的峰位分子量为10.23KDa;组成糖分析采用PMP衍生化法,根据各标准单糖和样品衍生物的保留时间和峰面积,确定样品中组成糖的种类和比例,结果表明,该多糖复合物中糖的部分由木糖、甘露糖、葡萄糖醛酸以及葡萄糖组成;蛋白部分由精氨酸、络氨酸、丙氨酸、色氨酸、苯丙氨酸等9种氨基酸组成。分析结果表明,制得的银耳糖蛋白符合要求。
3.银耳糖蛋白样品的碘代 样品500mg以5ml纯水溶解,加入NaI溶液(0.5mol/L)3ml,充分混匀,加入氯胺T溶液(0.1g/ml)3ml,充分混匀后震荡反应1min,加入偏重亚硫酸钠3ml(0.1g/ml),混匀后加入碘化钾5ml(0.1g/ml),充分混匀,离心(5000r/min,10min)后取上清,冷冻干燥,得碘代银耳糖蛋白。
4.碘代银耳糖蛋白的纯化 碘代银耳糖蛋白的分离纯化在中压凝胶色谱仪上进行。碘代银耳糖蛋白200mg,以纯水溶解后上样到Sephadex G-50凝胶色谱柱(40cm x5cm),以水洗脱,收集洗脱液(10ml/管),根据该色谱柱的内外水体积确定开始和结束收集时间。以苯酚-硫酸法测定各管中的糖含量,以糖含量为纵坐标,管数为横坐标作图,根据洗脱图(见图1),收集10-25管,浓缩、冷冻干燥,得到纯化碘代银耳糖蛋白。
5.碘代银耳糖蛋白的分析
通过碘取代反应制得的碘代银耳糖蛋白进行了光谱分析。紫外光谱表明,碘代前后其最大吸收均在234nm,未发生改变。红外光谱表明,碘代前后发生了明显改变,碘代后最大吸收为:3363、3267、1631、1527、1396、1303、1087、902、810、624、536cm-1,而碘代前,银耳糖蛋白的最大吸收为:3309、2931、1462、1381、1319、1261、1084、1022、729、624cm-1,产生了明显的卤代烷烃峰(536cm-1),表明碘通过化学键连接到糖中。碘代银耳糖蛋白通过ICP-MS测定其碘代率为0.55%,进一步表明,碘代反应成功。
6.碘代糖蛋白稳定性研究
碘标记后的糖复合物在进行动物、细胞实验时是否稳定,以下述实验进行了研究:
取碘代银耳糖蛋白10mg,溶解在10ml细胞培养液()中,置于37C0恒温振荡,分别在1,2,3小时吸取2ml,通过Sephadex G-50进行凝胶柱层析(30cm X 1cm),水洗脱液以自动收集器收集(1ml/管),以ICP-MS隔管测定其中的碘含量,结果表明,碘代银耳糖蛋白和经培养1,2,3小时的碘代银耳糖蛋白的层析曲线基本相同,在小分子量的流分(Ve)附近未检测到游离的碘,表明碘代银耳糖蛋白中的碘未发生裂解,碘代产物稳定。
二.样品的处理将碘代糖复合物样品或冻干后的生物样品粉碎,在顶空进样瓶(10ML)内准确称取适量,加入4ml超纯水润湿后依次加入3ml TMAH和0.1ml H2O2,混匀,旋紧顶盖,80℃下超声破碎30min,定容至25ml。以0.45um滤膜过滤,滤液进行ICP-MS测定。
三.样品的测定测定在电感耦合等离子体-质谱(ICP-MS)(Agilent JL-713-IP001-YQ030)上进行.
ICP-MS设定的条件如下表:
表1 ICP-MS仪器的参考工作条件
四.测定结果
1方法检出限和线性范围
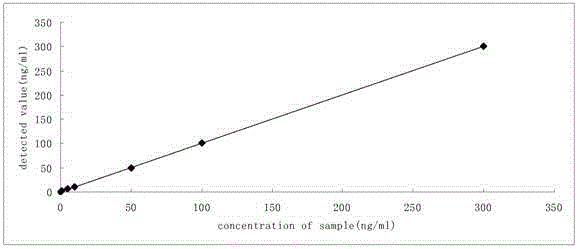
1%TMAH溶液作为溶剂,配制1mg/ml的NaI标准溶液,分别稀释至5ng/ml、10ng/ml、50ng/ml、100ng/ml、300ng/ml碘标准工作溶液。测得工作曲线(见图2)的标准方程为y=0.0075×+0.0232,R=0.9996,线性范围较宽。
2方法精密度
准确称取0.05g碘代银耳糖蛋白,样品处理过程同前,重复测定10次,进行精密度实验,实验结果见下表(表2),从结果中可知,样品测定的相对标准偏差(RSD)值为3.89%。
表2碘代银耳糖蛋白精密度测定结果(n=10)
3方法重现性
准确称取0.05g碘代银耳糖蛋白,共6份,每份处理过程同,进行方法重现性实验,实验结果见表3,从结果中可知,样品测定的相对标准偏差为4.5%。
表3碘代银耳糖蛋白重现性测定结果
4方法稳定性
50mg碘代银耳糖蛋白样品,消解后每隔两小时测定一次,结果如表4。表明在8小时内样品稳定。
表4碘代银耳糖蛋白重现性测定结果
5.加标回收率
本方法以碘代银耳糖蛋白为试样进行回收率实验,准确称取碘代银耳糖蛋白,以纯水溶解,制成50mg/3.5ml溶液共6份,每份添加1mg/ml碘化钠标准溶液0.5ml,处理过程同7,将滤液稀1000倍.实验结果见表5,根据实验结果计算,加标回收率在92%-101%之间,RSD值为5.16%。
表5碘代银耳糖蛋白加标回收率测定结果
五.银耳糖蛋白在生物样品中的含量及分布
5.1生物样品的制备方法
SD大鼠在适应环境3天后进行实验。采血前禁食12h,自由饮水。本试验以碘代银耳糖蛋白为样品,分为实验组和空白对照组,每组3只大鼠,实验组给予给碘代银耳糖蛋白,空白组给予生理盐水,给药剂量为0.2g/只,给药容量为12m L/只,灌胃给药,取血方式为眼球取血和腹主动脉取血;1h取血点为大鼠左眼,2h取血点为大鼠右眼,3h取血点为大鼠腹主动脉,每只大鼠共3次取血,将血液0.5ml除最后稀释10倍外,其他处理过程同前.取给药3h后大鼠心、肝、脾、肺、肾分别真空冷冻干燥,称重,研磨均匀,称取样品100mg,除最后滤液不必稀释外,其他处理过程同前。
5.2实验结果
5.2.1不同时间点大鼠血液中银耳糖蛋白含量测定结果
一般情况下,大鼠的血容量占体重的7.4%,大鼠平均体重190g,故大鼠体内全血量以12.6ml计算出一只大鼠全血中银耳糖蛋白含量。由结果可见(表6),随着给药后时间的增加,吸收入血量也在增加,3小时后,将近5%的银耳糖蛋白存在血液中。
表6不同时间点大鼠全血中银耳多糖含量
5.2.2碘代银耳糖蛋白给药3小时后,在大鼠主要脏器中含量结果见表7;
表7大鼠内脏中含有碘代银耳糖蛋白的量
由测定结果可见,该方法灵敏度高,结果稳定。
本发明将碘代多糖与ICP-MS检测技术相结合,建立新的生物样品中测定多糖含量的方法,为集成创新,具有实质的突出特点和显著的技术进步。
附图说明
下面结合附图和实施方案对本发明进一步说明。
图1是碘代银耳糖蛋白的分离纯化洗脱图;
图2是方法检出限和线性范围曲线图。
下面结合实施例对本发明作进一步详细说明。但下述的实施例仅仅是本发明的简易例子,并不代表或限制本发明的权利保护范围,本发明的保护范围以权利要求书为准。
具体实施方式
为更好地说明本发明,便于理解本发明的技术方案,本发明的典型但非限制性的实施例如下。
实施例1银耳糖蛋白的测定
其方法与结果与前述发明内容中相同,在此不再赘述。
实施例2碘代多糖、糖脂的测定
天然产物中许多糖的复合物不含有络氨酸,不能与碘直接发生取代反应。需要将它们首先与可同碘发生取代发生的基团连接,再进行碘的取代反应。
一、荧光素(FITC)标记多糖
荧光素可在碱性条件下与多糖中的发生取代反应,生成荧光素-多糖复合物。该复合物在生理条件下稳定,是荧光标记多糖常用的方法。
1、多糖样品
我们选择杏鲍菇多糖(PEPI)作为样品。PEPI为实验室自制的均
一多糖,不含有蛋白。
2、荧光素标记PEPI
样品(1g)溶解在10ml二甲基亚砜中,加10滴吡啶,加入FITC0.1g,再加入二月桂酸二丁基锡20mg,95℃混合加热2h。加入无水乙醇50ML.放置,倾去上清,以乙醇反复清洗,洗去多余的染料,离心,得FITC-PEPI复合物。
3、碘代荧光素-PEPI和样品的纯化
荧光素-PEPI的碘取代反应方法同糖蛋白的碘代方法,在此不再赘述。
碘代多糖的纯化方法同碘代银耳糖蛋白的纯化方法。测定方法同银耳糖蛋白,在此不再赘述。
样品的处理及样品的测定均同银耳多糖蛋白的方法,在此不再赘述。
二、杏鲍菇多糖在生物样品中的含量及分布
1、生物样品的制备方法
实验分组和给药剂量均同银耳糖蛋白。
2、实验结果
2.1不同时间点大鼠血液中杏鲍菇多糖含量测定结果
一般情况下,大鼠的血容量占体重的7.4%,大鼠平均体重190g,故大鼠体内全血量以12.6ml计算出一只大鼠全血中银耳糖蛋白含量。由结果可见(表8),1h时,杏鲍菇多糖在血液中的浓度达到高峰,随着给药后时间的增加,吸收入血量减少。
表8不同时间点大鼠全血中杏鲍菇多糖含量
2.2杏鲍菇多糖给药3小时后,在大鼠主要脏器中含量结果见表9。
表9大鼠内脏中含有碘代杏鲍菇多糖的量
- 还没有人留言评论。精彩留言会获得点赞!