纳米金包银比色探针的制备方法及其检测铅离子的方法与流程
本发明涉及铅离子检测的技术领域,具体涉及纳米金包银比色探针的制备方法及其检测铅离子的方法。
背景技术:
铅是典型的慢性或积累性毒物。铅可对许多人体器官带来不良影响,特别是对人的肺、肾脏、生殖系统、心血管系统有较大的损害;影响表现为肾损伤、智力下降、不育、流产以及高血压,还会引起铅脑病、多发性神经炎、腹绞痛、溶血性贫血等。幼儿和儿童体内铅含量过高,会直接影响发育,而且这种影响是全身性的,具有不可逆性。目前我国儿童血铅水平整体已有所下降,但部分地区儿童血铅水平仍然较高,这与其居住环境和食物铅超标等因素密切相关。
目前,铅离子的检测方法包括双硫腙比色法、火焰原子吸收光谱法等。然而,这些技术一般都需要复杂的预处理,分析非常耗时,需要昂贵的仪器,选择性较低,限制了它们的实际应用。检测铅离子的贵金属纳米传感器已经有大量的报道,大体上主要分为两类。一类方法是基于纳米颗粒的团聚反应进行的。第二类方法是基于金纳米颗粒的刻蚀反应进行的。这些方法最早是在2009年(Anal. Chem. 2009, 81, 9433–9439)报道的,其原理在于,在2-巯基乙醇和硫代硫酸钠存在下,铅在金纳米颗粒表面形成铅金合金,铅离子间接催化了巯基乙醇刻蚀金的反应,从而实现对铅离子的高灵敏度、高选择性检测。此体系使用的金纳米颗粒溶液是红色的,所以,如果被测定溶液是红色的,会对检测结果造成影响。因此,需要开发其他颜色的纳米溶液用于克服类似问题。而单纯的银纳米颗粒又不能基于此类反应检测铅离子。
技术实现要素:
本发明所要解决的技术问题是,克服现有技术的不足,提供一种操作较简单,成本较低,选择性好,灵敏度高的纳米金包银比色探针的制备方法及其检测铅离子的方法。
本发明解决其技术问题采用的技术方案是,
本发明之纳米金包银比色探针的制备方法,包括以下步骤:
将氯金酸溶液和硝酸银溶液加入烧瓶中,加热沸腾后,加入柠檬酸钠溶液,混合溶液沸腾回流10~30 min后,停止加热,并搅拌至室温,即得到橙黄色的纳米金包银比色探针溶液。
进一步地,所加入的氯金酸溶液中的氯金酸、硝酸银溶液中的硝酸银与柠檬酸钠溶液中的柠檬酸钠的摩尔比为1:2.85~3.15:11.4~11.8。
进一步地,所述氯金酸溶液的摩尔浓度为0.05~0.25 mmol/L。所述硝酸银溶液的摩尔浓度为0.15~0.75 mmol/L。所述柠檬酸钠溶液的摩尔浓度为0.03~0.18 mol/L。
本发明之纳米金包银比色探针检测铅离子的方法,包括以下步骤:
准备离心管(一般为8个),分别将100~500 µL 摩尔浓度为50~100 mmol/L的Gly-NaoH缓冲溶液(优选pH为9.6~10.3)、300~800µL本发明所制得的纳米金包银比色探针溶液加入离心管中,混合均匀,加入20~100 µL摩尔浓度为50~250 mmol/L的硫代硫酸钠溶液,并分别加入100~500 µL不同浓度的铅离子(可为0 nmol/L、5 nmol/L、50 nmol/L、500 nmol/L、5 µmol/L、50 µmol/L、500 µmol/L、5 mmol/L)溶液,混合均匀,反应10~30 min后,再加入20~40 µL摩尔浓度为50~250 mmol/L的2-巯基乙醇(2-ME)溶液,震荡,然后在室温下静置1~2 h。观察反应溶液颜色变化或者检测溶液的UV-Vis光谱变化,定性或定量分析铅离子的存在或含量。
在上述技术方案中,若反应溶液颜色由橙黄色变浅,则待测样品溶液中含有铅离子,且溶液中铅离子的浓度大于或等于5 nmol/L,若需要定量分析,检测混合溶液中UV-Vis光谱变化,确定溶液中铅离子的浓度;若反应溶液颜色没有变化,说明待测样品溶液没有铅离子,或者溶液中铅离子的浓度小于5 nmol/L,若需要定量分析,检测混合溶液中UV-Vis光谱变化,确定溶液中铅离子的浓度或有无铅离子。
在上述技术方案中,所述定量分析中,建立标准曲线进行定量检测,包括以下步骤:
(1)配制不同浓度的铅离子超纯水溶液,其中,铅离子的浓度分别为:0 nmol/L、5 nmol/L、50 nmol/L、500 nmol/L、5 µmol/L、50 µmol/L、500 µmol/L、5 mmol/L;
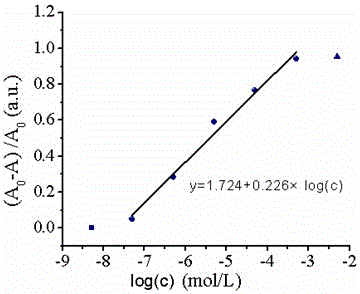
(2)准备8个干净的离心管,分别将100 µL摩尔浓度为50 mmol/L的Gly-NaoH缓冲溶液(pH=10)、760 µL制得的纳米金包银比色探针溶液加入离心管中,混合均匀,加入20 µL摩尔浓度为50 mmol/L的硫代硫酸钠溶液,并分别加入步骤(1)所制得的100 µL不同浓度的铅离子(0-5 mmol/L,8个梯度)溶液,混合均匀,反应15 min后,再加入20 µL摩尔浓度为50 mmol/L的2-巯基乙醇(2-ME)溶液,震荡,然后在室温下静置1.5小时。测定混合溶液的UV-Vis光谱变化,以y=(A0− A)/A0的值为纵坐标,Α0:空白组(铅离子浓度为0 nmol/L的溶液)的最大吸收峰的吸光度,A:加铅离子混合溶液(铅离子浓度>0 nmol/L的溶液)的最大吸收峰的吸光度;以铅离子浓度值为横坐标绘制标准曲线,得出二者之间在50nmol/L-500 µmol/L区间呈线性关系,其方程式为 y=1.724+0.226×log(c), c为摩尔浓度,摩尔浓度单位为mol/L,相关系数R为 0.983,可用于铅离子的定量检测,其最低检测下限由3σ计算为0.1nmol/L.
在上述技术方案中,所述纳米金包银比色探针检测铅离子溶液的检测范围为:5 nmol/L~5 mmol/L, 其线性范围为50nmol/L-500 µmol/L。
本发明用柠檬酸钠溶液还原氯金酸和硝酸银的混合溶液,得到金包银纳米颗粒溶液;铅离子在2-巯基乙醇和硫代硫酸钠(Na2S2O3)辅助下对金包银纳米探针具有刻蚀反应,铅离子浓度越大,其刻蚀效果越明显,溶液的颜色越淡,利用紫外-可见分光光度计对溶液吸光度的测定,可以实现对铅离子的检测。
本发明的设计原理和理论基础:
(1)本发明制备的直径在纳米级的纳米金包银粒子,其基本单元都是微小尺寸的粒子,故具有很多宏观粒子所不具备的物理特性,如光学效应、小尺寸效应、表面效应、宏观量子隧道效应、介电限域效应、久保效应以及一些其他的特殊效应。
(2)金包银纳米粒子会和溶液中的 S2O32-反应, 复合物Au(S2O3)23-会在金包银纳米颗粒表面快速形成,当溶液中加入Pb2+离子和2-巯基乙醇时,金包银纳米粒子表面的金迅速溶解形成Au+-2-ME络合物,由于金比银的氧化能力强,Au+-2-ME又迅速和纳米粒子上的银反应形成Ag+-2-ME,金包银纳米粒子的粒径逐渐变小,并伴随着紫外图谱的改变。纳米颗粒的吸收光的能力与其直径有关,一般说来,同等浓度下,直径越大的纳米颗粒,其吸收光强度越大,直径越小的纳米颗粒,其吸收光强度较小。因此,利用纳米颗粒吸收光强度与直径的关系,获取在不同铅离子浓度下2-ME/S2O32—Au@AgNPs吸收光强度信息,进而实现对铅离子的检测。附图3很好的解释了上述所说的传感机制,有效的证明金包银纳米颗粒能够作为比色传感器。
(3)选择性测试:
准备9个干净的离心管,分别将100 µL摩尔浓度为 50 mmol/L的Gly-NaOH缓冲溶液(pH=10)、760 µL本发明制得的纳米金包银比色探针溶液加入离心管中,混合均匀,加入20 µL摩尔浓度为 50 mmol/L的硫代硫酸钠溶液,并分别加入100 µL 100 nmol/L 的硝酸铅,5 μmol/L的氯化镉、氯化铬、氯化铁、氯化钾、硝酸锰、氯化钠、硝酸镍、硝酸锌溶液,混合均匀,反应15 min后,再加入20 µL 50 mmol/L的2-ME溶液,震荡,然后在室温下静置1.5小时。然后,分别转移到石英比色皿中,在紫外-可见分光光度计中检测并记录其紫外-可见吸收光谱,计算给出(A0-A)/A0, 参见附图4。
如图4所示,可以发现,在Pb2+存在的情况下,其最大吸收值是其他离子的1000倍左右,而5 µmol/L的Cd2+,Cr3+,Fe3+,K+,Mn2+,Na+,Ni2+,Zn2+均不能对Pb2+检测产生明显干扰。因此,我们可以得出结论,该反应体系不仅具有十分低的检测下限,还具有良好的选择性。
本发明金包银纳米颗粒的吸收和散射截面积要比金纳米颗粒强,而且金包银纳米颗粒具有和金一样的化学稳定性,非常适合用作探针去检测被测物,能够降低检测下限。
本发明的有益效果在于:
(1)本发明制备的纳米金包银比色探针具有灵敏度高、响应迅速、选择性好等优点,金包银探针溶液呈黄色,在被测样品溶液呈红色时,比金纳米颗粒有更强的抗干扰能力,比色法检测铅离子的检出最低浓度由3σ计算得出为0.1 nmol/L,比已经报道文献中检测下限都要低。
(2)本发明中制备探针所使用的试剂均无毒害作用,探针的合成方法简单且制备过程中也不产生污染环境的物质。
(3)本发明的检测方法操作简单、快速,不需要借助复杂昂贵的大型仪器,成本低廉,可实现裸眼检测,适用于大规模的现场快速检测。
附图说明
图1为不同浓度铅离子溶液加入纳米金包银比色探针溶液中的UV-Vis变化光谱图;
图2为不同浓度铅离子溶液加入纳米金包银比色探针溶液中,(A0− A)/A0同铅离子浓度之间关系的标准曲线图及线性拟合公式;
图3纳米金包银探针对Pb2+离子检测作用的传感机制;
图4为不同金属离子加入纳米金包银比色探针溶液中,混合溶液的(A0− A)/A0变化图。
具体实施方式
为了更好的解释本发明,以下结合具体实施例进一步阐明本发明的主要内容,但本发明的内容不仅仅局限于以下实施例。
实施例1
本实施例之纳米金包银比色探针的制备方法,包括以下步骤:
将100ml 氯金酸(摩尔浓度为0.0607mmol/L)溶液和100ml硝酸银(摩尔浓度为0.1821mmol/L)溶液加入到烧瓶中,加热至沸腾后,加入2 mL 0.035 mol/L的柠檬酸钠溶液,混合溶液继续沸腾回流20 min后,停止加热,并搅拌至室温,即得到橙黄色的纳米金包银比色探针溶液。
通过 TEM(透视电子显微镜)进行表征,所得纳米金包银比色探针溶液中的纳米金包银比色探针为球形颗粒,其直径约为28.6 nm,其溶液的紫外可见光谱最大吸收峰波长为433 nm。
本实施例之纳米金包银比色探针检测铅离子的方法,包括以下步骤:
准备8个干净的离心管,分别将100 µL摩尔浓度为50 mmol/L 的Gly-NaoH缓冲溶液(pH=10)、760 µL制得的纳米金包银比色探针溶液加入离心管中,混合均匀,加入20 µL 50 mmol/L的硫代硫酸钠溶液,并分别加入100 µL不同浓度的铅离子(0 nmol/L、5 nmol/L、50 nmol/L、500 nmol/L、5 µmol/L、50 µmol/L、500 µmol/L、5 mmol/L,8个梯度)溶液,混合均匀,反应15 min后,再加入20 µL 50 mmol/L的2-巯基乙醇溶液,震荡,然后在室温下静置1.5小时。观察溶液颜色的变化,若反应颜色由橙黄色变浅,则待测样品溶液中含有铅离子,且溶液中铅离子的浓度大于或等于5 nmol/L,若需要定量分析,检测混合溶液中UV-Vis光谱变化,确定溶液中铅离子的浓度;若所述反应颜色没有变化,说明待测样品溶液没有铅离子,或者溶液中铅离子的浓度小于5 nmol/L,若需要定量分析,检测混合溶液中UV-Vis光谱变化,确定溶液中铅离子的浓度或有无铅离子。
所述定量分析中,建立标准曲线进行定量检测,包括以下步骤:
(1)配制不同浓度的铅离子超纯水溶液,其中,铅离子的浓度分别为:0 nmol/L、5 nmol/L、50 nmol/L、500 nmol/L、5 µmol/L、50 µmol/L、500 µmol/L、5 mmol/L;
(2)准备8个干净的离心管,分别将100 µL摩尔浓度为50 mmol/L的Gly-NaoH缓冲溶液(pH=10)、760 µL制得的纳米金包银比色探针溶液加入离心管中,混合均匀,加入20 µL摩尔浓度为50 mmol/L的硫代硫酸钠溶液,并分别加入步骤(1)所制得的100 µL不同浓度的铅离子(0-5 mmol/L,8个梯度)溶液,混合均匀,反应15 min后,再加入20 µL摩尔浓度为50 mmol/L的2-巯基乙醇溶液,震荡,然后在室温下静置1.5小时。测定混合溶液的UV-Vis光谱变化,以y=(A0− A)/A0的值为纵坐标,Α0:空白组(铅离子浓度为0 nmol/L的溶液)的最大吸收峰的吸光度,A:加铅离子混合溶液(铅离子浓度>0 nmol/L的溶液)的最大吸收峰的吸光度;以铅离子浓度值为横坐标绘制标准曲线,得出二者之间在50nmol/L-500 µmol/L区间呈线性关系,其方程式为 y=1.724+0.226×log(c), c为摩尔浓度,摩尔浓度单位为mol/L,相关系数R为 0.983,可用于铅离子的定量检测。
- 还没有人留言评论。精彩留言会获得点赞!