一种兰索拉唑左旋异构体的测定方法与流程
本发明涉及一种药物及其制剂的质量检测方法,特别是涉及右兰索拉唑原料和其制剂中左旋异构体检测方法,属于对药品进行质量控制的技术领域。
背景技术:
右兰索拉唑缓释胶囊是新型治疗胃食管反流病的药物。右兰索拉唑是兰索拉唑的右旋异构体,左旋异构体在右兰索拉唑原料中变成了异构体杂质,应严格控制左旋异构的限量。因此,建立右兰索拉唑原料及其制剂中左旋异构的分析方法具有重要意义。
专利ZL01819816.3,“(R)或(S)-兰索拉唑的结晶方法”,右兰索拉唑异构体的分析方法,色谱条件如下:
色谱柱:CHIRALCEL OD(4.6×250mm);流动相:己烷-乙醇(90:10);流速:1.0ml/ml;检测波长:285nm。
文献“奥美拉唑、兰索拉唑对映体及相关物质在不同手性柱的分离比较”(分析化学研究简报,第30卷,第12期,1494页)报道了兰索拉唑对映体在多种手性色谱柱上的分离情况,色谱柱填料包括:AD、OD、CHI-TBB、AGP。
左旋异构体和右旋异构体能充分的分离,但左旋异构体与一个或多个右兰索拉唑的特异性杂质分离度差,建立的分析方法专属性不够强,无法通过严格方法学验证。因此,已有的兰索拉唑左旋异构体测定方法无法满足药品质量标准和质量控制的要求。
技术实现要素:
本发明的目的在于:提供一种右兰索拉唑原料和其制剂中左旋异构体的检测方法,该方法可满足药品质量研究方法学验证的要求,可用于药品的质量控制。
为实现上述目的,本发明采取了以下技术方案:
一种右兰索拉唑原料和其制剂中左旋异构体的检测方法,采用手性色谱柱,正相液相色谱法测定。
采用表面共价键合有直链淀粉-三(3,5-二甲基苯基氨基甲酸酯)的硅胶为液相色谱柱填料,流动相为甲基叔丁基醚-乙酸乙酯-甲醇-二乙胺混合溶剂系统,检测波长为280-290nm,流速为0.8-1.2ml/min。以主成分自身对照法计算右兰索拉唑中左旋异构体的量。
本发明方法所述的流动相甲基叔丁基醚-乙酸乙酯-甲醇-二乙胺比例优选65:35:5:0.1。本发明方法所述的波长优选285nm。本发明方法所述的手性色谱柱优选:IA,5微米填料,250×4.6mm。
本发明方法检测灵敏度高,精密度好,特别针对右兰索拉唑制剂中的特定杂质的专属性强,是严格控制右兰索拉唑原料和制剂的有效方法。
附图说明
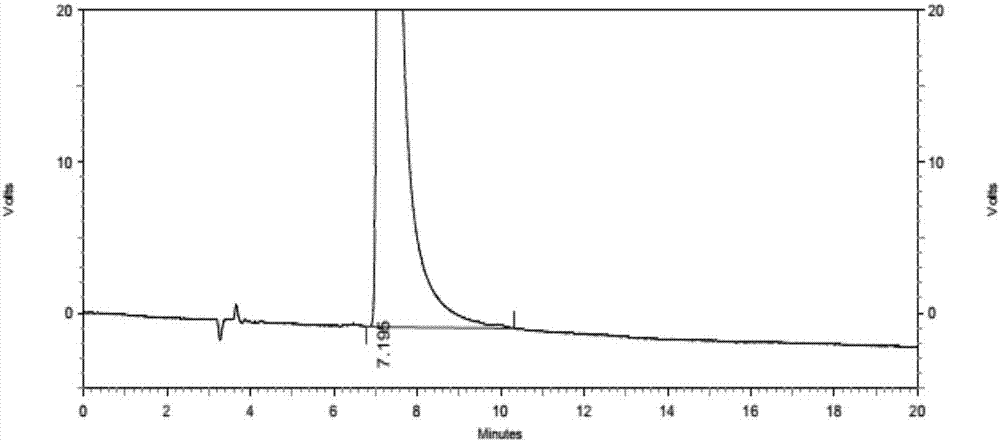
图1系统适用性HPLC图谱
图2光降解HPLC图谱
图3碱降解HPLC图谱
图4热降解HPLC图谱
图5酸降解HPLC图谱
图6未降解HPLC图谱
实施方式
下面通过实施例对本发明进行更详细的说明,但本发明并不限于这些例子。
实施例1系统适用性试验
色谱柱:IA,5微米填料,250×4.6mm。
流动相:甲基叔丁基醚-乙酸乙酯-甲醇-二乙胺(65:35:5:0.1)。
检测波长:285nm,柱温:25℃,流速:1.0ml/min,进样体积:10μl。
供试品溶液:取右兰索拉唑原料5mg,置10ml量瓶中,加流动相溶解,得供试品溶液。
系统适用性溶液:取右兰索拉唑原料5mg,加适量流动相溶解,加兰索拉唑砜化物储备液,兰索拉唑硫化物储备液,左兰索拉唑储备液适量,定容,制备每毫升含右兰索拉唑500μg,左兰索拉唑2.5μg,兰索拉唑砜化物2.5μg和兰索拉唑硫化物2.5μg的溶液。
测定结果显示,左旋异构体与右兰索拉唑、兰索拉唑砜化物和兰索拉唑硫化物分离度良好。
实施例2强制降解试验
采用实施例1中色谱条件,进行了酸破坏、碱破坏、氧化破坏、高温破坏及光照破坏试验,验证分析方法的专属性。
1.酸破坏:取右兰索拉唑制剂细粉适量,置离心管中,加0.1mol/L盐酸乙醇溶液适量,放置约30分钟,加流动相超声溶解、离心,取上清液作为酸破坏溶液。
2.碱破坏:取右兰索拉唑制剂细粉适量,置离心管中,加0.1mol/L氢氧化钠乙醇溶液适量,放置约30分钟,加流动相超声溶解、离心,取上清液作为碱破坏溶液。
3.高温破坏:取右兰索拉唑制剂细粉适量,置离心管中,加流动相适量,超声、离心后取上清液,置60℃烘箱中,加热约0.2小时,取出放至室温,作为高温破坏溶液。
4.光照破坏:取右兰索拉唑制剂细粉适量,置离心管中,加流动相适量,超声、离心后取上清液,置4000Lx强光下照射4小时,作为光照破坏溶液。
测定结果显示,右兰索拉唑制剂经酸破坏、碱破坏、热破坏试验后,杂质增加;酸降解产物的保留时间在3.98min,碱降解和热降解产物的保留时间在4.26min。各降解产物与主峰和左旋异构体分离良好。
- 还没有人留言评论。精彩留言会获得点赞!