声学亲和分离的制作方法
本公开涉及生物材料的分离。
发明背景
已经在多种背景中应用生物材料的分离。例如,在许多分析过程中使用将蛋白质与其它生物材料分开的分离技术。
发明概述
本公开描述了通过流体室中分布的功能化材料实现的用于分离生物材料的方法、系统和装置的技术,所述功能化材料结合特定的靶材料,如重组蛋白质和单克隆抗体。通过声学驻波的波节和波腹捕获功能化材料,诸如用亲和蛋白包被的微载体。在此方法中,在不接触的情况下捕获功能化材料(例如使用机械通道、导管、镊子等)。
在一方面,进行样品的层析分析的一些方法包括:在声学驻波场内位置处的填充有液体的室中保留功能化材料,所述位置分布在所述室内部,在那里声压幅度在与关闭声学换能器(acoustictransducer)时相比升高,或者与在关闭所述声学换能器时基本上相同;使含有样品的流体流入所述填充有液体的室中,在那里已经通过声学声透射(insonification)保留功能化材料,使得与所述功能化材料具有互补特征的样品的部分与所述功能化材料结合,而样品的其它部分通过所述室;并且随后加工室内部的流体以使与其中保留的功能化材料结合的样品的部分从室洗脱。实施方案可以包括一个或多个以下特征。
方法可以包括使样品的部分从室中洗脱并且进入分析箱(analysisbin)。
加工室内部的流体可以包括:使流体通过大小排阻柱,其中第一流体动力学半径的蛋白质样品在具有第二流体动力学半径的样品前洗脱,此时所述第一流体动力学半径大于所述第二流体动力学半径。
加工室内部的流体可以包括:提高流体的离子强度以使与功能化材料结合的样品的部分洗脱。
加工室内部的流体可以包括:调节流体的ph水平以使与功能化材料结合的样品的部分洗脱。
加工室内部的流体可以包括:降低流体的离子强度以使与所述功能化材料结合的样品的部分重折叠成天然形成,使得样品的部分和所述功能化材料之间的疏水性相互作用降低。
方法可以包括测定洗脱到分析箱的样品的部分的定量水平以形成层析读出。方法可以包括测定所述定量水平包括测定质量或体积。测定所述定量水平可以包括测量分析箱中样品的部分的光吸收指数。
在一些实施方案中,样品的部分与功能化材料上的结合位点形成抗原-抗体相互作用。在样品的部分的配体与功能化材料上的基质缀合时,样品的部分与功能化材料结合。功能化材料包括功能化微珠。功能化微珠包含对相应抗体具有亲和力的特定抗原配体。
在一些实施方案中,使含有蛋白质样品的流体流入填充有液体的室中包括:循环含有蛋白质样品的流体,使得样品超过一次流过所述室内部分布的位置,在那里声压幅度与关闭声学换能器时相比升高,或者与在关闭所述声学换能器时基本上相同。
在一些实施方案中,样品是蛋白质样品。样品包括靶化合物,诸如重组蛋白质和单克隆抗体、病毒和活细胞(例如t细胞)。
用于层析分析的一些装置包括:流动室,所述流动室具有彼此相对的第一壁和第二壁,并且配置为接受含有功能化材料的流体;第一壁上安装的声学换能器和第二壁上安装的反射器,使得在开启所述声学换能器时,在所述室内部创建多维度声场,所述室包含声压幅度从关闭所述声学换能器时升高的第一空间位置和声压幅度与关闭所述声学换能器时基本上相同的第二空间位置,其中在多维度声场的第一或第二位置处捕获功能性材料;和入口,所述入口与流动室偶联并且配置为使蛋白质样品流过捕获功能化材料的流动室,使得与功能化材料具有互补特征的蛋白质样品的部分与功能化材料结合,而蛋白质样品的其它部分和其它材料诸如细胞碎片通过流动室。实施方案可以包括一个或多个以下特征。
装置可以包括分析箱,其配置为接受与功能化材料结合的蛋白质样品的部分并且随后从功能化材料洗脱,使得获得蛋白质样品的部分的层析测量。
装置还可以包含:大小排阻柱,其与流动室偶联并且配置为使与功能化材料结合的蛋白质样品的部分从功能化材料洗脱。
装置还可以包含疏水性相互作用层析柱,其与流动室偶联并且配置为使与功能化材料结合的蛋白质样品的部分从功能化材料洗脱。
装置还可以包含:离子交换层析柱,其与流动室偶联并且配置为使与功能化材料结合的蛋白质样品的部分从功能化材料洗脱。
装置还可以包含:质谱仪以测量分析箱中蛋白质样品的部分的量。
装置还可以包含光学分光计以测量分析箱中蛋白质样品的部分的量。
也可以通过缓冲液或其它过程洗脱从表面洗脱重组蛋白或单克隆抗体后循环功能化微载体。这允许更大的表面积和功能化微载体与来自生物反应器的表达蛋白质的亲和相互作用,增加声学流化床层析过程的效率。
装置提供排列中的功能化颗粒,所述排列提供比填充柱更多的颗粒间空间。较低的密度降低了非靶生物材料堵塞官能化颗粒之间流动路径的可能性。含有靶生物材料的再循环介质实际上通过使游离的靶生物材料多次通过官能化颗粒来增加装置的捕捉表面积。非靶生物材料如细胞的接触减少可以帮助保持用于生产例如蛋白质的细胞的存活力。本文描述的技术可以用于高密度细胞培养、新的研究应用、大的生产培养体积(例如超过1000升)、有效的监测和培养控制、细胞培养应用中的成本和污染降低。
在本说明书中描述的主题的一个或多个实施方案的细节在附图和下面的描述中阐述。主题的其他特征、方面和优点将从描述、附图和权利要求书中变得显而易见。
附图简述
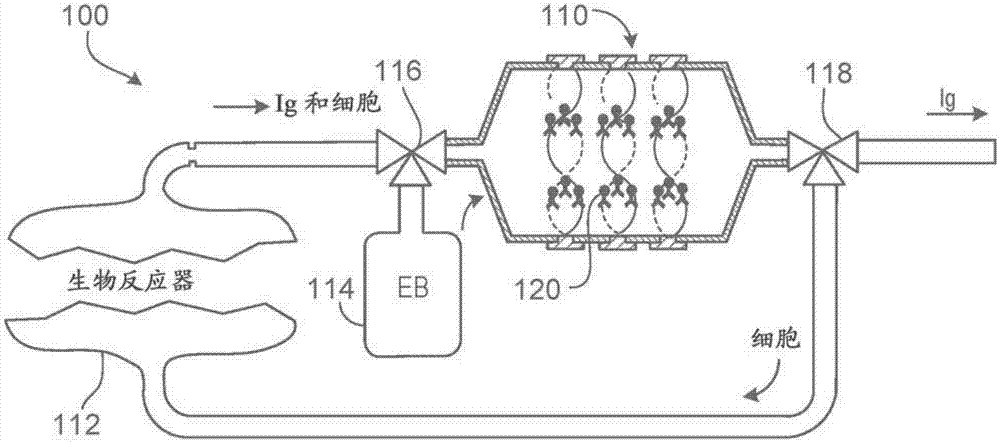
图1a是使用声学亲和滤器中保持的功能化材料以捕捉生物反应器中产生的生物材料的系统的示意图。
图1b是显示图1a的亲和层析系统的部分的示意图,所述亲和层析系统使用分布在流体室中的功能化材料床,使得功能化材料床结合特定蛋白质。
图1c-1e显示了运行过程中图1a的系统。
图2是从流体中提取蛋白质样品作为层析输入并且进入分析箱中的过程的流程图。
图3的照片显示了微珠的示例性床,所述微珠分布在流体室中并且捕获在流体室中创建的多维度声波的波节和波腹处。
图4是功能化材料直接在生物反应器内的细胞培养悬浮液中温育的过程的流程图。
图5是将浆料装载在层析柱中并以类似于常规层析程序的方式处理的过程的流程图。
图6是可以在专用循环中与层析柱类似使用内部具有微珠的声学亲和滤器的过程的流程图。
图7显示了使用大小排阻层析从流体中提取和分析蛋白质。
图8显示了使用离子交换层析从流体中提取和分析蛋白质。
图9是用于产生单克隆抗体和重组蛋白质的系统的示意图。
图10a和10b是用于产生单克隆抗体和重组蛋白的系统的示意图。
各个附图中类似的参考编号和名称指示类似的元件。
发明详述
本公开描述了用于在具有捕获功能化材料的波节和波腹的声学驻波分布中保留功能化材料的方法、系统和装置。功能化材料包括对选定的生物材料,诸如例如生物分子(即,蛋白质、脂质、碳水化合物和核酸)、病毒、病毒样颗粒、囊泡和外来体具有特定亲和力的结合剂。
(例如,选定的蛋白质、生物分子、大分子和超分子结构)。声学驻波场分布可以在流体室内部位置处在无接触或物理支持的情况下保留功能化材料(例如层析珠)。
功能材料保留在流体室中的非侵入性方式创建原位基质结构。通过使细胞样品流过该基质结构,与保留的功能化材料具有互补特征的生物材料可以与功能化材料结合,而其他材料通过流体室。随后,可以对含有具有附着的生物材料的功能化材料的流体进行进一步处理以提取生物材料。
在一些系统中,具有互补特征的蛋白质可以结合功能化材料,而其他蛋白质和/或细胞组分通过。该过程允许选择性捕获和分离特定的配体、蛋白质、抗体、游离dna、病毒或细胞,或任何与互补决定簇缀合的物体,而允许流体流中的其他颗粒流过具有捕获的功能化材料(如颗粒和珠)的声学驻波。
图1a显示了系统100,其使用功能化材料作为声学亲和滤器110的部分来捕捉生物反应器112中产生的材料。系统100包括声学亲和滤器110、生物反应器112和洗脱缓冲液储器114。操作生物反应器112以使细胞111(其例如可以是生物反应器112中含有的中国仓鼠卵巢(cho)细胞(见图1b-1e))产生材料113,所述材料例如可以是单克隆抗体或重组蛋白(见图1b-1e)。系统100通过使含有细胞111和材料113的流体通过声学亲和滤器110来提取材料113。声学亲和滤器110保留材料113,同时细胞111和碎片/非靶组分115(见图1b-1e)通过。三通阀116提供生物反应器112的出口、洗脱缓冲液储器114的出口和声学亲和滤器110的入口之间的可控连接。另一个三通阀118提供生物反应器112的入口、声学亲和滤器110的出口和系统100的出口之间的可控连接。声学亲和滤器110可以预载有对产生的材料具有亲和力的层析树脂的微珠120,或者微珠120可以在温育期间存在于生物反应器112中(见图1c-1e)。
图1b是更详细显示声学亲和滤器110的结构和功能的示意图。声学亲和滤器110包括声学换能器122和反射器124。声学换能器122和反射器124安装在声学亲和滤器110的中心部分126的相对壁上。图1b显示了循环中系统110的操作,其中微珠120被预加载在声学亲和滤器110中而不是最初存在于生物反应器112中。
图1c-1e显示了循环操作的系统100,其中微珠120在温育期间存在于生物反应器112中并且在捕捉模式下用附着的靶化合物捕捉(见图1c)。洗脱后(见图1d),将功能化材料返回到生物反应器(见图1e)。
声学换能器122包括诸如压电材料的振动材料。当操作时,声学换能器122可以创建平面波分布、多维度声场分布、或平面波和多维度声场分布的组合。在声学换能器122和反射器124之间产生的声波分布可以产生具有声学辐射力的空间模式的驻波分布。在图1b中,声学亲和滤器110的中央部分126中的声波分布由曲线117表示。
声学换能器122可以由电压信号,例如频率为100khz至10mhz的脉冲电压信号驱动,使得振动材料以较高阶振动模式振动以产生声波,其由反射器124反射以创建驻波(来自平面波、多维度波、或平面波和多维度波的组合)。多维度声波可以由振动材料的较高阶模式摄动产生。在某些情况下,声波是由振动材料的较高阶模式摄动产生的多分量波(multiplecomponentwave)。在一些情况下,声波是由振动材料的较高阶模式摄动产生的多分量波和由振动材料的活塞运动产生的平面波的组合。较高阶振动模式可以是在通式(m,n)中,其中m和n是整数并且m或n中的至少一个大于1。在该实例中,声学换能器122以比(2,2)更高阶的振动波节振动,这产生更多的波节和波腹,导致声学亲和滤器110中的三维驻波。
声学换能器122可以可变地配置为产生较高阶的振动模式。在一些实施方案中,振动材料配置为具有直接暴露于流体层的外表面,例如流过流动室的流体中的微载体和培养细胞的混合物。在一些实施方案中,声学换能器包括覆盖振动材料的外表面的磨损表面材料(wearsurfacematerial),磨损表面材料具有半波长或更小的厚度和/或是氨基甲酸乙酯(urethane)、环氧树脂(epoxy)或硅酮涂层材料、聚合物或类似的薄涂层材料。在一些实施方案中,声学换能器包括具有顶端、底端和内部体积的壳体。振动材料可以位于壳体的底端并位于内部容积内并且具有面向壳体的顶端的内表面。在一些实例中,将声学材料的内表面直接暴露于顶端壳体。在一些实例中,声学换能器包括与声学材料的内表面接触的背衬层(backinglayer),背衬层由基本透声的材料制成。一个或多个配置也可以组合在声学换能器122中以用于生成多维度声驻波。
声辐射力可以具有相同数量级的轴向力分量和侧向力分量。空间模式可以表现为密度的周期性变化。更具体地,可以在流体介质中创建压力波节平面和压力波腹平面,其分别对应于峰声辐射力平面和底声辐射力平面。在图1b中,声辐射力平面的峰和底对应于捕获珠120的位置。波节和波腹的此种空间模式可以与流体介质中的滤器非常类似地发挥功能,以捕获特定尺寸或尺寸范围的颗粒,而不能捕获不同尺寸或尺寸范围的颗粒。在一些配置中,例如,可以通过调节声透射频率、换能器的功率、或流体速度配置空间模式,以允许一些材料自由流过,而捕获一些特定功能化材料,诸如具有特定抗原构造的微载体。换言之,可以针对具有功能化表面的微载体专门调谐声驻波。
一些系统由其他功能化材料或微载体(例如,顺磁珠或水凝胶颗粒)实施。微载体可以设计成具有允许锚定依赖性细胞系的附着和生长的表面化学。微载体可以由许多不同的材料制成,所述材料包括deae(n,n-二乙基氨基乙基)-葡聚糖、玻璃、聚苯乙烯塑料、丙烯酰胺、胶原和藻酸盐。微载体材料以及不同的表面化学可以影响细胞行为,包括形态和增殖。微载体的表面化学可以包括胞外基质蛋白、重组蛋白、肽和带正电荷或带负电荷的分子。微载体描述具有介于01.和1000微米之间的特征尺寸(例如平均直径、主轴长度、长度、或宽度)的材料。
在一些实施方案中,通过用分布在整个基质中的带正电的deae基团替换交联葡聚糖基质形成微载体。此类型的微载体可以用于建立的细胞系以及用于从原代细胞和正常的二倍体细胞株的培养物生产病毒或细胞产物。
在一些实施方案中,通过将变性胶原的薄层化学偶联至交联葡聚糖基质形成微载体。由于胶原表面层可以被多种蛋白水解酶消化,它提供了从微载体收获细胞,同时保持最大细胞存活力和膜完整性的机会。
在一些配置中,微载体的功能化表面可以包含特异性抗体配体。此特异性抗体配体可以对特定抗原(如cd34或ck8)具有亲和力,所述特定抗原允许结合特定类型的细胞(对于这些抗原分别为干细胞或ctc)。利用捕获的具有亲和力修饰表面的微载体作为声学流化床滤器,其中将特定的蛋白质、抗体或细胞吸引到官能化微载体的表面,并与微载体一起保持在声驻波中。
亲和中心的实例包括酶、抗体、适体、寡核苷酸、链霉亲合素等。可以使用“经典”rna或dna单体,或核酸模拟物(例如pna,lna等)或这两者的混合物合成寡核苷酸。对附着于微载体的亲和中心特异性的感兴趣的物体与声驻波中捕获的微载体的亲和中心结合。感兴趣的物体可以包括生物分子、病毒、和活细胞。为了结合亲和中心,它们可以携带互补决定簇,如针对链霉亲合素的生物素、针对抗体的抗原、互补寡核苷酸等。通过此种方法,可以从二级流体系统中选择性除去细胞和颗粒流体系统,诸如血液中感兴趣的生物分子、病毒、或活细胞。感兴趣的细胞包括例如中国仓鼠卵巢(cho)细胞和浆细胞。感兴趣的材料的实例包括例如免疫球蛋白、单克隆抗体和重组蛋白、与互补决定簇缀合的生物物体,如标记的蛋白质,病毒和具有互补表位的生物分子等。
图2显示了使用功能化材料(例如,微珠120)从载体流体提取靶化合物(例如,材料或单克隆抗体113)的过程200。在声学驻波场内的峰和谷位置处在填充有液体的室(例如,声学亲和滤器)中保留功能化材料(步骤210)。含有靶化合物的流体流入通过声学声透射保留功能化材料的填充有液体的室中,使得通过保留的功能化材料从流体中过滤靶化合物(步骤212)。在室内部处理流体以使靶化合物的捕获部分洗脱(步骤214)并收集洗脱的靶化合物(步骤216)。
例如,使用图1a-1e中显示的系统100,可以使用过程200来捕捉靶化合物。在系统100的操作之前,声学亲和滤器110预加载有层析树脂的微珠120,所述层析树脂对产生的材料具有亲和力。由图1b-1d中的波浪线标示的声驻波场117内的峰和谷位置处在填充有液体的声学亲和滤器110中保留微珠120。
关闭三通阀116和三通阀118,同时操作生物反应器以使生物反应器112中含有的细胞111产生材料113。当期望的蛋白质生产、细胞的存活力和辅助细胞碎片达到规定条件时,切换到过滤/捕捉将连续发生以用于灌注和补料分批生物反应器。在当今的生物反应器过程中,较高的细胞浓度和较长的发酵时间导致较高的药物滴度和较高的生产产率。这些生物反应器条件降低细胞存活力,增加细胞碎片,并提高细胞培养液中有机成分的浓度。这些组分的无定形、胶体性质倾向于使分离过程复杂化。澄清技术的选择也将考虑与下游过程(如层析和超滤)整合的任何要求。过滤步骤如深度过滤可以用来减轻下游滤器和过程的负荷。
在达到期望水平的材料113后,操作三通阀116以提供生物反应器112的出口与声学亲和滤器110的入口之间的流体连接。例如,当靶化合物达到5克/l浓度的浓度时将系统100切换(自动或手动)为捕捉模式。当靶化合物达到0.5-20克/l(例如,超过1克/l、超过2.5克/l、超过5克/l、超过7.5克/l、超过10克/l、超过15克/l、小于17.5克/l、小于15克/l、小于10克/l、小于5克/l、或小于2.5克/l)的浓度时,一些系统配置为切换到捕捉模式。
操作三通阀118以在声学亲和滤器110的出口与生物反应器112的入口之间提供流体连接。通过管道泵(未显示)将培养物悬浮液循环通过所得的流体回路。一些系统使用其他泵或流体转移机构来使流体流动。
随着培养悬浮液流体流过声学亲和滤器110,细胞111与培养悬浮液流体一起在流体回路周围继续并返回到生物反应器。将声学亲和滤器110调谐以提供具有100-500微米(例如,200-400微米、大于200微米、大于250微米、大于300微米、大于350微米、大于200微米、大于200微米、大于200微米、小于500微米、小于450微米、小于400微米、小于350微米、小于300微米)的特征尺寸(例如、宽度、长度或直径)和25-150微米(例如,50和100微米之间、大于25微米、大于50微米、大于75微米、大于100微米、小于150微米、小于125微米、小于100微米、小于75)的波节间间隔(例如,从一个波节的边缘到相邻波节的边缘)。具有这些特性的声学亲和滤器可以促进细胞111和其他非靶材料的容易通过。
例如,将声学亲和滤器110调谐并且预加载以将微珠120维持于小于50%(例如,小于40%、小于30%、小于20%、小于15%、小于10%)的体积比率,所述体积比率是由微珠120占据的体积除以含有微珠120的过滤区域126的部分的总体积的体积比率。此体积比率反映微珠的低密度排列,并有利于细胞111、细胞碎片和非特异性蛋白质的容易通过,并且低于典型填充柱中的体积比率。较低的体积比和增加的间距降低非靶生物材料堵塞官能化颗粒之间流动路径的可能性。含有靶生物材料的再循环介质实际上通过使游离靶生物材料多次通过功能化颗粒来增加装置的捕捉表面积。非靶生物材料的接触减少可以帮助保存非靶生物材料,诸如用于生产蛋白质的细胞。本文描述的技术可用于高密度细胞培养、新的研究应用、大的生产培养体积(例如超过1000升)、有效的监测和培养控制、细胞培养应用中成本和污染降低。
材料113比细胞111小得多。一些材料113与微珠120接触并被微珠120保持。然而,一些材料113与培养悬浮液流体一起围绕流体回路继续并返回到生物反应器112。系统100通过使悬浮液流体和含有的材料113多次(例如,4、6、8、10次或更多次)通过声学亲和滤器来补偿相对于填充柱减小的每体积微珠120的表面积的此种效应。在此捕捉过程中,操作生物反应器112以继续产生更多材料113。在一些系统中,将功能化材料悬浮在反应器中,在培养物中培养以收集靶化合物,然后将培养物悬浮液泵送过声学亲和滤器,其收集功能化材料和相关靶化合物。
操作三通阀116以关闭来自生物反应器112的出口管道并打开洗脱缓冲液储器114与声学亲和滤器110之间的流体连接以将系统从捕捉模式切换至洗脱模式。操作三通阀118以关闭进入生物反应器112的入口管道并打开声学亲和滤器110与系统100的收集出口之间的流体连接。洗脱缓冲液从微珠120释放材料113并通过系统100的收集出口将材料113携带出系统100。可以将微珠120恢复并保持在声学亲和滤器中以用于系统100的下一个操作循环。在将功能化材料悬浮在反应器中的系统中,可以将微珠120释放并返回到生物反应器112中(见例如图1c-1e)。
图3是构建用于揭示在亲和声学亲和滤器中捕捉和悬浮层析珠的实验设置的部分的平面图。用彼此相邻的两个换能器310和它们间的互补钢反射器312来构建1”x1”x1”系统300。此系统也具有钢底侧,并且使顶部对空气保持开放。用干净的去离子水将系统填充到其容纳容量。观察到以2.3mhz驱动并且调整为提供具有约77微米间隔的约337微米宽的波节的示例性1英寸x1英寸声学亲和滤器以有效维持聚苯乙烯微珠,用于使通过的靶化合物亲和捕捉。
从来自gelifescience的hitrap蛋白ahp1ml柱中提取具有直径34微米的蛋白a偶联的sepharose层析微珠。蛋白a结合单克隆和多克隆抗体。因此,如果将这些微珠置于含有此类抗体的溶液中,则它们将紧密结合抗体,将它们从溶液中分离出来。将这些微珠320添加到系统中的水。
微载体或微珠可以具有正或负的声学对比因数。例如,具有反射入射声波驻波的反射核心的微载体具有正对比因数。此类微载体可以通过声辐射力驱动到压力平面内的压力波节热点。具有吸收核心的微载体可以比反弹这些波接受更多的入射声学驻波。此类微载体可以具有负对比因数,并且可以由声辐射力驱动到压力波腹平面。另一方面,细胞不被声透射过程捕获,并可以与流体介质一起流动。
然后,以2.23mhz固定频率在45v恒定电压给换能器供能。如预测的,微珠320沿着捕捉线自身排列,所述捕捉线紧密反映使用有限元分析预测的预期模式。
图4显示了方法500,其中将功能化材料直接在生物反应器112内的细胞培养悬浮液中温育。微珠120(或其他功能化材料)在生物反应器112内温育期间结合靶蛋白。将来自生物反应器112的细胞培养物悬浮液泵送过声学亲和滤器110。当细胞和其他材料通过声学亲和滤器110时,在声学亲和滤器中保留微珠120和附着的靶蛋白。
取决于用户的目标,可以将细胞弃去或返回到生物反应器(510)中。关于珠,存在有多种选择。例如,在一种方法中,关闭声学亲和滤器110的换能器,从而释放含有微珠120和附着的靶蛋白质(512)的浆体。回收浆体,并在声学亲和滤器外部进一步处理。在另一种方法中,内部具有微珠120的声学亲和滤器110可以在专用循环(514)中与层析柱类似使用。
图5显示了方法500的一个实施方案,其中将浆体加载在层析柱中并以类似于常规层析程序的方式处理。它通常包括包装浆体、清洗珠、洗脱蛋白质、并重建珠。清洗通常用缓冲溶剂进行,所述缓冲溶剂除去非特异性结合的物质,而蛋白质仍然特异性结合珠。洗脱从珠中除去蛋白质。取决于亲和力或结合中心,可以通过改变ph和/或离子强度,通过失活亲和中心(例如形成复合物的蛋白质的变性),通过过量的竞争配体等来进行洗脱。此过程基本上使亲和中心失活。或者,可以将回收的浆体置于滤器的顶部,并用与层析柱方法相似的溶剂进行清洗。
蛋白质回收后,可以将珠弃去或返回到反应器中。为了重复使用它们,必须重建珠(必须重新活化亲和中心)(516)。为了重建它们,用合适的溶剂(例如用于离子交换珠的具有低离子强度的缓冲液)清洗珠。
可以以分批或连续模式从声学亲和滤器110中回收珠。在分批模式下,将细胞悬浮液的流动中断并且将装载有蛋白质的珠粒通过底部端口收集或通过渗透物端口洗出。在连续模式下,调节声捕获方式,使得保留的珠不随着渗透物流动而逃出声学亲和滤器,而是浓缩,沉淀并通过底部(浓缩物端口)收集。
浆体可以按顺序或交错模式收集。在前者中,将细胞悬浮液流动中断,持续浆体回收的时间。因此,可以用单一单元进行此过程。在后者中,将细胞悬浮液流动重定向到另一个单元,而第一个单元处于浆料回收模式下。
图6显示了过程500的实施方案,其中内部具有微珠的声学亲和滤器110可以在专用循环(514)中与层析柱类似地使用。在此实施方案中,原位处理珠,而不从声学亲和性滤器110除去。以与上述相同的方式,用清洗、洗脱和重建溶剂(分别为518、520和522)处理保留的珠。在此操作过程中,将细胞悬浮液流动中断或重定向到另一个声学单元以继续珠回收过程。
图7显示了使用大小排阻层析来后处理功能化材料和附着的靶化合物的浆体,其中不同的靶化合物具有不同的大小。此种方法可以用于从对于亲和分离感兴趣的几个区域从功能化材料中分离捕获的感兴趣的生物分子、病毒或活细胞。例如,功能化材料可以包括结合不同靶化合物或非选择性结合多种化合物的部分。当溶剂从功能化材料中释放结合的化合物时,较大的蛋白质首先洗脱,因为它们不能进入吸附剂/分析物复合物的孔并且具有更直接的通过柱的路径。较小的蛋白质可以进入孔隙,具有更复杂的路径,因此花费更长的时间穿过基质并从柱中洗脱。
图8显示了使用离子交换来后处理功能化材料和附着的靶化合物的浆体。在此方法中,从功能化材料释放靶化合物,例如通过增加缓冲液的离子强度或通过调节缓冲液的ph值。在高离子强度下,将蛋白质部分去溶剂化,使它们采取替代构象,其中通常掩埋的疏水性残基更加暴露。这些残基然后可以与缀合到基质的疏水官能团形成疏水相互作用。降低离子强度导致蛋白质重折叠成其天然构象,掩埋其疏水性残基。这减少蛋白质和固定相之间的疏水相互作用,促进蛋白质洗脱。
图9显示了掺入生物反应器-声学亲和滤器循环回路的用于产生治疗性蛋白质的系统900,如图1中所示的系统100。系统900包括第一种子生物反应器910、第二种子生物反应器912和生产生物反应器914,其利用表达治疗性蛋白质如单克隆抗体和重组蛋白质的细胞群体。声学亲和滤器916捕捉单克隆抗体和重组蛋白,并且使用几个滤器和柱进行后处理。
第一种子生物反应器910(又名n-2生物反应器)是300升生物反应器,其接收来自用于初始细胞生产的袋式反应器918和来自培养基制备系统920的输入。第二种子生物反应器912(又名n-1生物反应器)是2,000升生物反应器,其接收来自第一种子生物反应器910和培养基制备系统922的输入。生产生物反应器914(又名n生物反应器)是15,000升,其接收来自第二种子生物反应器912和培养基制备系统924的输入。其他系统可以包括与系统900中包含的那些生物反应器不同的生物反应器数目和/或具有不同尺寸的生物反应器。
流动回路中包含生产生物反应器914和声学亲和滤器916,该流动回路还包括图1中所示并且在相关文本中描述的其他部件。如上所述操作环路,以在声学亲和滤器916内部的活化材料上产生并捕获靶化合物。声学亲和滤器916提供从生物反应器的细胞澄清和收获,并产生相对纯的产物,其虽然大部分是纯的,但仍然需要除去小部分工艺和产品相关的杂质。
系统900包括配置为除去大于0.2微米的任何剩余颗粒的抛光滤器(polishingfilter)926、离子交换层析柱928、疏水性相互作用柱930、和最终抛光滤器932。一些系统包括不同的后捕获处理部件。
离子交换层析柱928使用掺入阳离子和阴离子交换层析除去非靶蛋白。如以上参照图7所讨论,将特定蛋白质(靶标或非靶标蛋白质)附着于柱介质。
疏水性相互作用柱930使用疏水性的性质将蛋白质彼此分开。在此柱中,将疏水基团(如苯基、辛基或丁基)附着到固定柱。通过柱的蛋白质能够与柱子上的疏水基团相互作用并与其结合,所述蛋白质在其表面上具有疏水性氨基酸侧链。在此层析过程中,通常使用与离子交换层析中使用的条件相反的条件来设计分离。在此分离中,首先将具有高离子强度的缓冲液(通常是硫酸铵)施加到柱。缓冲液中的盐减少样品溶质的溶剂化,因此随着溶剂化减少,暴露的疏水区域被介质吸附),混合模式层析或羟基磷灰石层析-hap。hap的机理是复杂的,并且涉及带负电荷的蛋白质羧基和树脂上带正电荷的钙离子,以及带正电的蛋白质氨基和树脂上带负电荷的磷酸根离子之间的非特异性相互作用。通过调节缓冲液的ph值,可以将碱性或酸性蛋白质选择性吸附到柱上;可以通过改变也可以选择的缓冲液盐浓度来实现洗脱。这些步骤提供病毒、宿主细胞蛋白质和dna材料的额外分离,以及除去聚集体、不需要的产物变体种类和其他次要污染物。
最终的抛光滤器932使用超滤膜提供渗滤以从包含蛋白质、肽、核酸和其他生物分子的溶液中完全除去、替换或降低盐或溶剂的浓度。方法选择性地利用可渗透(多孔)膜滤器,以将溶液和悬浮液的组分根据其分子大小分离成最终制剂缓冲液。
另外,一些系统包括蛋白a层析后保持的低ph和病毒过滤步骤以实现足够的病毒清除。
已经描述了本发明的多个实施方案。然而,应该理解,可以在不脱离本发明的精神和范围的情况下进行各种修改。
例如,图10a和10b显示了用于产生靶化合物,诸如例如单克隆抗体和重组蛋白的系统600的操作。系统1000类似于图1a中所示的系统100,但不包括从声学亲和滤器110的出口回到生物反应器112的再循环回路。图10a显示了处于捕捉模式的系统1000,其中靶化合物113、浆细胞111和碎片从生物反应器112流到声学亲和滤器110。在声学亲和滤器110中,官能化颗粒(例如微珠120)捕捉靶化合物113,而浆细胞111和碎片115流过。图10b显示了处于洗脱模式的系统1000,其中操作三通阀116以关闭来自生物反应器112的出口管道并打开洗脱缓冲液储器114和声学亲和滤器110之间的流体连接。从功能化材料释放靶化合物,并在系统1000的出口收集。
gork’ov模型是针对驻波中的单一颗粒,并且限于相对于流体和颗粒中的声场的波长较小的颗粒尺寸。它也没有考虑流体和颗粒的粘度对辐射力的影响。因此,该模型不能用于本文讨论的宏观规模(macro-scale)超声波分离器,因为颗粒簇可以增长得相当大。因此,使用了不受粒径限制的声辐射力的更复杂且完整的模型。所实施的模型基于yuriiilinskii和evgeniazabolotskaya的理论工作,如aipconferenceproceedings,第1474-1卷,第255-258页(2012)中所述。这些模型还包括流体和颗粒粘度的影响,并因此是声辐射力的更准确计算。
当声学驻波在液体中传播时,快速振荡可以对悬浮在液体中或液体之间界面上的颗粒产生非振荡力。此力称为声辐射力。力源自传播波的非线性。由于非线性,波在其传播时失真,并且时间平均值为非零。通过串行扩展(根据微扰理论),第一个非零项将是二阶项,其解释了声辐射力。对流体悬浮液中的颗粒或细胞的声辐射力是颗粒或细胞任一侧上的辐射压力差的函数。除与周围介质相比以不同速度振动,从而将波辐射的非刚性颗粒的效应以外,辐射力的物理描述是入射波和散射波的叠加。下面的等式呈现对平面驻波中的流体悬浮液中的颗粒或细胞上的声辐射力的分析表达式。
其中βm是流体介质的压缩率,ρ是密度,
其中ρp是颗粒密度,ρm是流体介质密度,βp是颗粒的压缩率,并且βm是流体介质的压缩率。
对于多维度驻波,声辐射力是三维力场,并且计算力的一种方法是gor’kov方法,其中主要的声辐射力fr定义为场电位u的函数,
并且f1和f2是如下限定的单极和偶极分布:
其中
其中p是声压,u是流体颗粒速度,λ是细胞密度ρp与流体密度ρf的比率,σ是细胞声速度cp与流体声速度cf的比率,vo是细胞的体积,并且<>指示波时段内取平均值的时间。
gork’ov模型是针对驻波中的单一颗粒,并且限于相对于流体和颗粒中的声场的波长较小的颗粒尺寸。它也没有考虑流体和颗粒的粘度对辐射力的影响。因此,该模型不能用于本文讨论的宏观规模超声波分离器,因为颗粒簇可以增长得相当大。因此,使用了不受粒径限制的声辐射力的更复杂且完整的模型。所实施的模型基于yuriiilinskii和evgeniazabolotskaya的理论工作,如aipconferenceproceedings,第1474-1卷,第255-258页(2012)中所述。这些模型还包括流体和颗粒粘度的影响,并因此是声辐射力的更准确计算。
因此,其他实施方案在所附权利要求书的范围内。
- 还没有人留言评论。精彩留言会获得点赞!