用于肿瘤标志物检测的核酸适配子传感器及其制备方法与流程
本发明涉及半导体材料与器件以及生物化学领域,特别是利用gan基高电子迁移率晶体管(hemt)研制的检测肿瘤标志物的核酸适配子传感器及其制备方法。
背景技术:
众所周知,癌症威胁着全球人类的健康,由癌症引发的死亡人数也呈逐年增长的趋势。癌症作为世界上第二大致死因素,在2015年已经累计造成880万起死亡病例,约占全球死亡总数的六分之一。其中,肺癌、胃癌、肝癌、结直肠癌、食管癌、女性乳腺癌、甲状腺癌、宫颈癌、脑瘤和胰腺癌是我国主要的恶性肿瘤,约占全部新发病例的75%。肺癌、肝癌、胃癌、食管癌、结直肠癌、胰腺癌、乳腺癌、脑瘤、白血病和淋巴瘤是主要的肿瘤死因,约占全部肿瘤死亡病例的80%。中国医学科学院肿瘤医院院长赫捷表示,大多数恶性肿瘤有10年至15年的潜伏时间来纠正,然而超六成患者发现时已到中晚期。实际上,目前我国肿瘤发病率在世界范围内处于较低水平,但治愈率也较低,其中一个原因就是发现晚。因此,实现恶性肿瘤的早期诊断,具有极其深远的意义。
肿瘤标志物是肿瘤细胞通过基因表达而合成、分泌,或是机体对肿瘤反应而异常产生或表达水平异常的一类物质,它在患者体内含量远高于健康成人体内含量,在肿瘤早期发现、诊断及预后中均起到重要作用。肿瘤标志物检测是临床上发现肿瘤的重要手段,目前临床常用的肿瘤标志物及其主诊的肿瘤类型主要有:癌胚抗原(cea),癌抗原19-9(ca19-9),甲胎蛋白(afp),醛缩酶,癌胚铁蛋白,铁蛋白(sf)可作为肝癌的有效诊断标志物;前列腺特异抗原(psa)在前列腺癌中阳性率高达30%~86%,其升高水平与肿瘤密切相关;癌胚抗原(cea)等其他相应肿瘤标志物在乳腺癌,结肠直肠癌,胆囊癌,食管癌,卵巢癌,胃癌等的早期诊断,预后判断和治疗中发挥着重要作用。
核酸适配子(aptamer)是一小段经过体外筛选selex技术(systematicevolutionofligandsbyexponentialenrichment,即指数式富集法配体演化技术)而得到的寡核苷酸链,它是从人工合成的dna或rna随机库中筛选出来的,能与对应的配体靶分子进行高亲和力和强特异性的结合,是目前应用最广泛的dna探针。相对于传统的蛋白质抗体,核酸适配子具有很多优点,如亲和力高,特异性强,制备简单,易于进行化学修饰与分离,靶分子分布范围广,与目标靶分子的结合条件可控,稳定性好等。核酸适配子与靶分子结合原理完全不同于传统的抗原与抗体结合的机理,一般情况下,无需知道结合内部结构及原理,只要通过selex技术筛选出特定的具有很高的结合力的核酸序列即可,已经被应用于生物化学,医学检验,药物合成筛选,环境监测等领域,有着广泛的发展空间和良好的应用前景。
近年来,以氮化镓(gan)为典型代表的第三代宽禁带半导体材料和器件的研发、突破和逐步走向成熟,与传统的si和gaas半导体相比,gan具有禁带宽度大、击穿电场高、电子迁移率高、抗辐射能力强、对生物分子无毒性和良好的化学稳定性等优异特性;而且gan可以与algan和alingan等合金材料构成异质结,其异质结界面上大的能带带阶不连续及压电极化和自发极化可产生高浓度的二维电子气(2deg),电子浓度比algaas/gaas异质结提高了一个数量级。因此,基于gan材料的hemt器件在生化检测领域具有十分重要的应用价值。algan/gan异质结构中,即使algan势垒层非故意掺杂,在异质结界面处也能获得高浓度的二维电子气(1013cm-2量级),这主要是由以下两个方面造成:一是由于gan/algan异质结存在非常强的自发极化和压电极化作用;二是由于gan和algan材料存在大的导带带阶不连续,使得形成的二维电子气被有效的限制在禁带宽度较窄的gan一侧。二维电子气密度和gan基外延材料的表面状态息息相关,材料表面状态的微小变化便可以引起二维电子气浓度的改变。由于algan/gan异质结构材料的这一特性,使得其在传感器领域日渐显露出独特的优势。
现有的gan基hemt生物传感器在检测癌症抗原方面都采用的是传统的抗原与抗体结合机理,检测极限浓度比较高,例如b.s.kang等人针对乳腺癌抗原和前列腺癌抗原的检测极限浓度分别为0.25μg/ml,10pg/ml,李加东等人的无栅型algan/ganhemt生物传感器检测前列腺癌的极限浓度为0.1pg/ml。由于核酸适配子相对于抗体对抗原的亲和力更强,更易捕获溶液中微量的抗原分子,因此gan基核酸适配子生物传感器可以检测到更低浓度的抗原溶液,灵敏度更高,检测极限浓度可以达到pg/ml以下甚至fg/ml量级。
技术实现要素:
本发明的目的在于,提高肿瘤标志物检测的灵敏度,使检测极限浓度达到pg/ml以下甚至fg/ml量级。
为实现上述目的,本发明提供如下技术方案:
本发明提供一种用于肿瘤标志物检测的gan基hemt核酸适配子传感器,包括:
gan基hemt,其包括栅极区域、源极区域和漏极区域,栅极区域位于源极区域和漏极区域之间;
源极电极和漏极电极,分别与所述gan基hemt上的源极区域和漏极区域形成欧姆接触;
栅极电极,与所述gan基hemt上的栅极区域形成肖特基接触;
氮化硅薄膜保护层,其位于所述源极电极、漏极电极和所述栅极电极的周边及上侧,仅露出与各电极接触的区域;
核酸适配子单链,形成于所述栅极电极上,其能对肿瘤标志物进行高灵敏性及特异性识别。
其中,肿瘤标志物本身所带的电荷会影响到所述栅极电极表面电荷的分布,进而影响到所述gan基hemt沟道中的二维电子气浓度,从而使源漏电流发生变化。
优选的,在上述的gan基hemt核酸适配子传感器中,所述源极电极和漏极电极之间的距离为5μm-30μm。
优选的,在上述的gan基hemt核酸适配子传感器中,所述栅极电极由以下材料之一构成:ni/au薄膜、au薄膜或au纳米颗粒。
优选的,在上述的gan基hemt核酸适配子传感器中,所述栅极电极的厚度为5nm-50nm,栅极区域面积为200μm2-1200μm2。
优选的,在上述的gan基hemt核酸适配子传感器中,所述栅极电极均制备独立的电极引线,所述电极引线通过施加电压来测试器件的栅控能力并以此来衡量传感器件的灵敏性,提高肿瘤标志物检测的灵敏性也避免了试剂的浪费。
优选的,在上述的gan基hemt核酸适配子传感器中,所述核酸适配子单链分子通过共价键合法或非共价结合法在栅极电极上固定,能对肿瘤标志物进行高灵敏性及特异性识别,所述核酸适配子通过末端修饰的巯基官能团在栅极电极表面形成au-s键,从而实现在传感器栅极电极上的固定。
相应地,本发明还公开了一种检测肿瘤标志物的gan基hemt核酸适配子传感器的制备方法,包括:
步骤1:制备gan基hemt;
步骤2:在所述gan基hemt上制作源极电极和漏极电极;
步骤3:在所述gan基hemt的栅极区域制作栅极电极;
步骤4:利用磁控溅射工艺在所述gan基hemt上溅射ti/al/ti/au作为各电极的金属引线pad;
步骤5:利用pecvd(plasmaenhancedchemicalvapordeposition,等离子体增强化学气相沉积法)工艺沉积氮化硅薄膜用作保护层,并通过icp刻蚀仅露出与各电极接触的区域窗口;
步骤6:在栅极电极上固定经巯基修饰后的生物敏感膜。
其中,步骤6中的该生物敏感膜能特异性识别肿瘤标志物,受到肿瘤标志物本身电荷的影响,使得所述栅极表面电荷分布发生变化,进而影响所述gan基hemt沟道中二维电子气浓度,使得源漏电流发生变化。
优选的,在上述检测肿瘤标志物的gan基hemt核酸适配子传感器的制备方法中,所述步骤1中的gan基hemt,其结构包括:
蓝宝石衬底或硅衬底或碳化硅衬底;
高阻半绝缘gan缓冲层,形成于所述衬底上,其生长厚度为2μm-3.5μm;
高迁移率gan沟道层,形成于所述高阻半绝缘gan缓冲层上,其生长厚度为50nm-100nm;
薄层aln插入层,形成于所述高迁移率gan沟道层上,其生长厚度为1nm-5nm;
n型掺杂或非故意掺杂algan势垒层,形成于所述薄层aln插入层上,其生长厚度为20nm-30nm。
gan盖帽层,形成于所述n型掺杂或非故意掺杂algan势垒层上,其生长厚度为1nm–10nm。
本发明的有益成果在于:本发明结合gan基hemt高的电子迁移率及二维电子气浓度等优点,以及对肿瘤标志物抗原具有高亲和力的核酸适配子在传感器栅区表面形成的生物敏感膜,可以将以癌胚抗原(cea)为例的肿瘤标志物的检测极限提升到一个新的高度,预计可以达到pg/ml以下甚至fg/ml量级,大大提高了传感器检测灵敏度,实现恶性肿瘤的早期诊断,造福广大癌症患者。本发明可对肿瘤标志物实现快速,实时检测,特异性强,灵敏度高,有助于恶性肿瘤的预防医治,实现医疗装置的便携化、智能化。
附图说明
为进一步说明本发明的具体技术内容,以下结合附图详细说明如下,其中:
图1是本发明中用于检测肿瘤标志物的gan基hemt核酸适配子传感器的结构示意图;
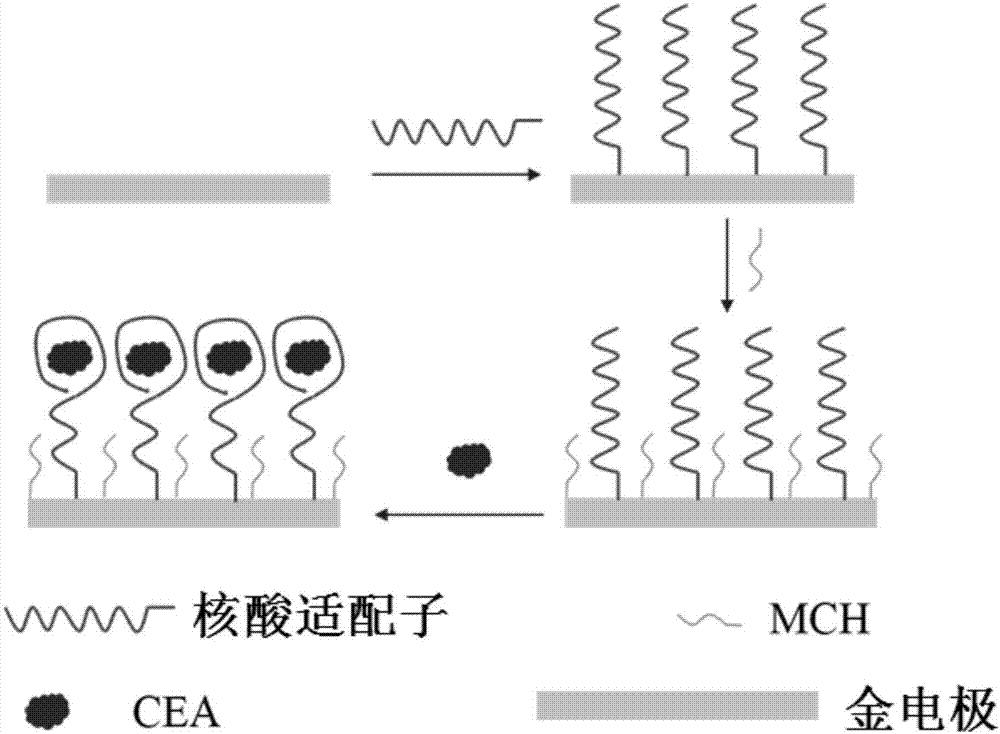
图2是本发明中栅区表面核酸适配子固定及捕获癌胚抗原(cea)的过程示意图。
图3是本发明的一个实施例的cea核酸适配子传感器检测不同浓度的cea溶液时ids随时间变化示意图。
图4是本发明的一个实施例的cea核酸适配子传感器的i-v测试结果图。
【附图标记说明】
1gan基hemt
2源极电极和漏极电极
3栅极电极
4电极引线pad
5氮化硅薄膜保护层
6核酸适配子单链
10衬底
11高阻半绝缘gan缓冲层
12高迁移率gan沟道层
13薄层aln插入层
14n型掺杂或非故意掺杂algan势垒层
15gan盖帽层
具体实施方式
为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明作进一步的详细说明。
图1是本发明中用于检测肿瘤标志物的gan基hemt核酸适配子传感器的一个实施例的结构示意图。如图1所示,该实施例的传感器包括gan基hemt1,该gan基hemt1上端面分布有栅极区域、源极区域和漏极区域,栅极区域位于源极区域和漏极区域之间,源极电极和漏极电极2,分别与所述gan基hemt上的源极区域和漏极区域形成欧姆接触,栅极电极3,与所述gan基hemt上的栅极区域形成肖特基接触,氮化硅薄膜保护层5,其位于所述源、漏电极和所述栅极电极的周边及上侧,仅露出与各电极接触的区域,在所述栅极电极上固定有核酸适配子单链6,用于检测肿瘤标志物。
该实施例中,gan基hemt包括衬底10,以及依次形成于衬底10上的高阻半绝缘gan缓冲层11,高迁移率gan沟道层12,薄层aln插入层13,n型掺杂或非故意掺杂algan势垒层14,gan盖帽层15。
该实施例中,gan基hemt上的源、漏电极是用磁控溅射法生长的厚度约220nm的钛铝钛金合金,并在880℃氮气氛围中30s快速退火形成欧姆接触。氮化硅,二氧化硅或光刻胶用作器件保护层,防止水溶液等影响到器件检测性能。电极引线pad4分别连接于源、漏电极,用于与外电路相连接,便于检测电流信号变化。
所述栅极电极用来固定生物敏感膜,其材质为ni/au薄膜、au薄膜和au纳米颗粒之一,厚度为5nm-50nm,栅极区域面积为200μm2-1200μm2。
所述核酸适配子的分子通过共价键合法或非共价结合法在栅极电极上固定,能对肿瘤标志物进行高灵敏性及特异性识别,所述核酸适配子通过末端修饰的巯基官能团在栅极电极表面形成au-s键,从而实现在传感器栅极电极上的固定。
上述用于检测肿瘤标志物的gan基hemt核酸适配子传感器的制备方法包括:
步骤1:制备gan基hemt。
在该实施例中,采用金属有机物汽相外延方法(mocvd)在蓝宝石衬底上依次生长高阻半绝缘gan缓冲层,高迁移率gan沟道层,薄层aln插入层,n型掺杂或非故意掺杂algan势垒层,gan盖帽层。
步骤2:在所述gan基hemt上制作源、漏电极。
在该实施例中,光刻曝光出欧姆接触区域,利用磁控溅射工艺,在欧姆接触区域溅射ti/al/ti/au,丙酮剥离后在氮气环境下退火30秒,退火温度为880℃,形成源极和漏极。接着,利用光刻胶保护器件有源区,用icp干法刻蚀的方法刻蚀掉除有源区以外的区域,直至刻蚀到缓冲层,得到器件所在的有源区台面。
步骤3:在所述gan基hemt的栅极区域制作栅金属电极。
在该实施例中,利用磁控溅射工艺在栅极区域溅射au薄膜,薄膜厚度为5nm-50nm。
步骤4:利用磁控溅射工艺在所述gan基hemt上溅射ti/al/ti/au作为源漏电极、栅极电极的金属引线pad。
步骤5:利用pecvd工艺沉积氮化硅薄膜用作保护层,并通过icp刻蚀仅露出与各电极接触的区域窗口。
步骤6:在栅极电极上固定经巯基修饰后的核酸适配子。
在该实施例中,首先要合成核酸适配子,即一段特定序列的核苷酸碱基序列(5’-hs-(ch2)6-ataccagcttattcaatt-3’),其可以对癌胚抗原(cea)进行特异性识别,在其末端修饰有巯基官能团。取适量核酸适配子,溶解于te缓冲溶液(10mmoll-1tris-hcl,1mmoll-1edta,0.1moll-1nacl,ph=7.40)中,使得最终浓度为50μm,将配置好的核酸适配子溶液储存于-20℃环境中。金电极表面经piranha溶液(30%h2o2/70%浓h2so4)清洗处理后,将其浸没在50μl核酸适配子溶液中,在常温下过夜反应(12小时),形成用于检测cea的生物敏感膜,然后用上述te缓冲溶液冲洗,将电极表面未结合的物质洗脱,接着将金电极浸泡在1mm巯基乙醇溶液中1h,以封闭可能残余的活性位点,避免非特异性吸附,得到gan基hemt核酸适配子传感器。
图2是本发明中栅区表面核酸适配子固定及捕获癌胚抗原(cea)的过程示意图。如图2所示,金电极表面在固定核酸适配子之后,进一步用巯基乙醇(mch)来封闭活性位点,以及最后核酸适配子捕获癌胚抗原(cea)的过程。
图3是本发明的一个实施例的cea核酸适配子传感器检测不同浓度的cea溶液的ids随时间变化示意图。如图3所示,在0.5v恒定偏压下,当向传感区域分别滴加0.5pg/ml和5pg/ml的抗原溶液时,漏电流并没有发生明显的改变,当滴加50pg/ml的抗原溶液时,电流有了很明显的上升,增长值约为11.5μa。此测试结果图证明了gan基hemt传感器与核酸适配子结合是可以对一些肿瘤标志物进行检测的,且检测极限浓度已达pg/ml量级。
图4是本发明的一个实施例的cea核酸适配子传感器的i-v测试结果图。如图4所示,在0-7v源漏电压范围内,分别测试了gan基hemt传感器在栅极固定核酸适配子前后,以及检测不同浓度的cea溶液时漏电流的变化情况。固定核酸适配子之后,传感器的漏电流有了很明显的上升,向传感区域分别滴加浓度范围为50pg/ml-5ng/ml的cea溶液,饱和电流随着浓度的增加而单调上升。在漏电压2.5v处,栅区固定核酸适配子之后,漏电流上升了500μa,当滴加50pg/ml的cea溶液时,电流上升了300μa,当滴加浓度为50ng/ml的抗原溶液时,饱和电流不再有明显改变。图4中,自下至上依次为栅区未固定核酸适配子(hemt)、固定cea核酸适配子(modifiedceaaptamer)、滴加50pg/ml的cea溶液、滴加500pg/ml的cea溶液、滴加5ng/ml的cea溶液和滴加50ng/ml的cea溶液各情形下的器件的i-v曲线。
经过实践验证,本发明的技术方案可适用于癌胚抗原(cea),癌抗原19-9(ca19-9),癌抗原125(ca125),甲胎蛋白(afp),醛缩酶,癌胚铁蛋白,铁蛋白(sf),前列腺特异抗原(psa),神经元特异性烯醇化酶(nse),鳞状上皮细胞癌抗原(scc)等肿瘤标志物生物传感器的研制。
以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 普适型用于同时检测多种肿瘤标志物的微流控芯片装置的制造方法
- 男性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 女性适用的典型肿瘤标志物联合检测用微流控芯片装置的制造方法
- 一种检测口腔癌的标志物及其试剂盒的制造方法与工艺
- microRNA 标志物组及其在制备检测胃癌淋巴结转移试剂盒中的应用的制造方法与工艺
- 基于弹性蛋白酶荧光底物检测乳腺癌肿瘤标志物CA153的酶联免疫试剂盒制备方法与制造工艺
- 检测和评价力量训练效果的miRNA标志物或其组合及其应用的制造方法与工艺
- 一种最优超平面的构建方法、动态优化系统和构建装置与制造工艺
- 癌症标志物及癌症的判定方法与制造工艺
- 检测尿液中单羟酚类代谢物的试剂盒及其制备方法与制造工艺