锂离子电池用硫化物系固体电解质和固体电解质化合物的制作方法
本发明涉及锂离子电池的固体电解质以及可以适合用作该固体电解质的锂离子电池用硫化物系固体电解质化合物。
背景技术:
锂离子电池是具有下述结构的二次电池:在充电时,锂以离子的形式从正极溶出并移动包藏至负极,在放电时,锂离子相反地从负极回到正极。锂离子电池具有能量密度大、寿命长等特征,因此被广泛地用作摄像机等家电产品、笔记本型计算机、移动电话机等便携式电子设备、动力工具等电动工具等的电源,最近还被应用至搭载于电动汽车(ev)或混合动力汽车(hev)等中的大型电池。
这种锂离子电池由正极、负极以及夹持于该两电极的离子传导层构成,该离子传导层一般使用在由聚乙烯、聚丙烯等多孔质膜构成的隔板中充满非水系的电解液而成的构成。然而,作为电解质,由于如此使用了以可燃性有机溶剂作为溶剂的有机电解液,因而不仅需要用于防止挥发或泄露的结构和材料方面的改善,还需要安装抑制短路时的温度升高的安全装置、及用于防止短路的结构和材料方面的改善。
对此,使用固体电解质、并将电池全固态化而成的全固态型锂电池由于不使用可燃性有机溶剂,因而能够实现安全装置的简化,而且可以使制造成本和生产率优异,此外还具有在电池内串联层积而实现高电压化的特征。另外,这种固体电解质中,li离子以外并不移动,因而可期待不发生因阴离子的移动引起的副反应等安全性和耐久性的提高。
对于这种电池中使用的固体电解质,要求离子电导率尽可能高、而且在化学和电化学方面稳定,例如已知卤化锂、氮化锂、锂氧酸盐或它们的衍生物等作为其候补材料。
关于这种固体电解质,例如专利文献1中公开了一种硫化物系的固体电解质,其是使通式li2s-x(其中,x表示sis2、ges2、b2s3中的至少一种硫化物)表示的锂离子传导性硫化物玻璃中存在由磷酸锂(li3po4)构成的高温锂离子传导性化合物而得到的。
另外,在专利文献2中,作为为结晶质且显示出室温下的离子电导率为6.49×10-5scm-1这样非常高的离子电导率的材料,公开了下述硫化物系的固体电解质,其特征在于,其含有通式li2s-ges2-x(其中,x表示ga2s3、zns中的至少一种)表示的作为复合化合物的锂离子传导性物质。
在专利文献3中,作为锂离子传导性和分解电压高的硫化物陶瓷,公开了下述锂离子传导性硫化物陶瓷,其特征在于,其以li2s和p2s5作为主要成分,以摩尔%表示计具有li2s=82.5~92.5、p2s5=7.5~17.5的组成,其中优选以摩尔比计具有li2s/p2s5=7的组成(组成式:li7ps6)。
在专利文献4中,公开了下述锂离子传导性材料,其由化学式:li+(12-n-x)bn+x2-(6-x)y-x(bn+为选自p、as、ge、ga、sb、si、sn、al、in、ti、v、nb和ta中的至少一种,x2-为选自s、se和te中的至少一种,y-为选自f、cl、br、i、cn、ocn、scn和n3中的至少一种,0≤x≤2)表示,并具有硫银锗矿型晶体结构。
在专利文献5中,作为除锂离子的高流动性外还能够进行单层的调合的固体化合物,公开了下述锂硫银锗矿,其为由通式(i)li+(12-n-x)bn+x2-6-xy-x表示的锂硫银锗矿,该式中,bn+选自由p、as、ge、ga、sb、si、sn、al、in、ti、v、nb和ta组成的组,x2-选自由s、se和te组成的组,y-选自由cl、br、i、f、cn、ocn、scn、n3组成的组,0≤x≤2。
在专利文献6中,作为与现有的固体电解质相比能够显著提高电导率的新的硫化物系固体电解质,公开了下述硫化物系固体电解质,其含有具有li7ps6的结构骨架、且p的一部分被si置换而成的组成式:li7+xp1-ysiys6(其中,x为-0.6~0.6,y为0.1~0.6)。
现有技术文献
专利文献
专利文献1:日本专利第3184517号公报
专利文献2:日本专利第3744665号公报
专利文献3:日本特开2001-250580号公报
专利文献4:日本特开2011-96630号公报
专利文献5:日本特表2010-540396号公报
专利文献6:日本特开2013-137889号公报
技术实现要素:
发明要解决的课题
作为锂离子电池中使用的固体电解质材料化合物,从离子电导率优异等方面出发,本发明人着眼于下述化合物,其具有立方晶系硫银锗矿型晶体结构并由li7-xps6-xclx表示。
但是,该化合物与水分或氧的反应性极高,因而若与大气接触,则存在与大气中的水分反应而产生硫化氢的问题。而且,即便在与干燥空气接触的情况下,也存在有时与空气中的氧反应而使电导率降低的问题。
于是,本发明涉及一种具有立方晶系硫银锗矿型晶体结构的锂离子电池用硫化物系固体电解质化合物,提出一种新的锂离子电池用硫化物系固体电解质化合物,该化合物能够抑制与大气接触时的硫化氢的产生量,即使在放置于干燥空气中的情况下也可以维持高电导率。
用于解决课题的方案
本发明提出一种锂离子电池用硫化物系固体电解质化合物,其特征在于,该锂离子电池用硫化物系固体电解质化合物含有立方晶系硫银锗矿型晶体结构的结晶相并由组成式(1):li7-x+yps6-xclx+y表示,上述组成式(1)中的x和y满足0.05≤y≤0.9和-3.0x+1.8≤y≤-3.0x+5.7。
发明的效果
与由li7-xps6-xclx的化学计量组成所表示的硫化物系固体电解质化合物相比,本发明提出的硫化物系固体电解质化合物的耐氧化性优异,放置于干燥空气中后也可以维持高电导率。而且,耐水性优异,即使与大气接触,也能够有效地抑制因与大气中的水分反应所产生的硫化氢产生量,在这方面也优异。例如,即使电池被破坏、硫化物系固体电解质化合物与大气接触,也能够有效地抑制硫化氢的产生,因而能够提供安全的全固态电池。
由此,本发明提出的硫化物系固体电解质化合物可以特别适合用作锂离子电池的固体电解质。
附图说明
图1是示出实施例1、8和16中得到的样品的xrd图谱的图。
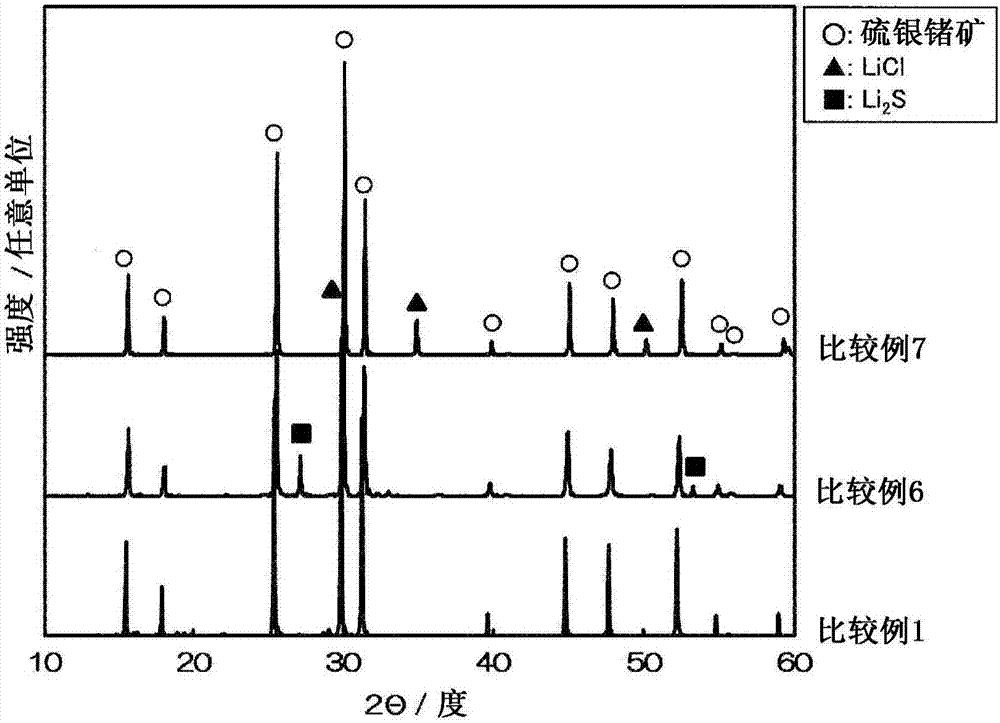
图2是示出比较例1、6和7中得到的样品的xrd图谱的图。
图3是示出实施例和比较例的组成范围的图。
图4是在横轴为licl添加量(y)、纵轴为干燥空气暴露后电导率的坐标中,对实施例和比较例的值作图而成的图。
图5是在横轴为licl添加量(y)、纵轴为h2s产生量的坐标中,对实施例和比较例的值作图而成的图。
具体实施方式
下面,对本发明的实施方式详细地进行说明。但是,本发明的范围不限定于以下说明的实施方式。
本实施方式的硫化物系固体电解质(称为“本固体电解质”)为下述锂离子电池用硫化物系固体电解质,其含有立方晶系硫银锗矿型晶体结构的结晶相,含有组成式(1):li7-x+yps6-xclx+y所表示的硫化物系固体电解质化合物(称为“化合物a”)。
本固体电解质可以由立方晶系硫银锗矿型晶体结构的单一结晶相构成,也可以由含有立方晶系硫银锗矿型晶体结构的结晶相和以licl表示的结晶相的混合相构成。
需要说明的是,作为含有立方晶系硫银锗矿型晶体结构的结晶相和以licl表示的结晶相的混合相,除了立方晶系硫银锗矿型晶体结构的结晶相与以licl表示的结晶相的混合相以外,还包括含有这以外的结晶相的情况。
如图3所示,从维持干燥空气放置后的电导率以及抑制硫化氢产生的方面考虑,上述组成式(1)中的x和y优选满足下述(i)和(ii)的条件。
(i)··0.05≤y≤0.9
(ii)··-3.0x+1.8≤y≤-3.0x+5.7
其中,关于条件(i),特别优选为0.05≤y≤0.6,其中更优选为0.05≤y≤0.4。
另外,关于条件(ii),特别优选为-3.0x+2.7≤y≤-3.0x+5.7,其中更优选为-3.0x+3.3≤y≤-3.0x+5.7。
此外,在本固体电解质含有立方晶系硫银锗矿型晶体结构的结晶相和以licl表示的结晶相的情况下,除了上述(i)和(ii)以外,优选进一步满足下述(iii)和(iv)的条件。
(iii)··0.05≤y≤0.4
(iv)··-3.0x+3.9≤y≤-3.0x+5.7
其中,关于条件(iii),特别优选为0.05≤y≤0.2,其中更优选为0.1≤y≤0.2。
另外,关于条件(iv),特别优选为-3.0x+4.2≤y≤-3.0x+5.7,其中更优选为-3.0x+4.2≤y≤-3.0x+5.1。
另外,在本固体电解质含有立方晶系硫银锗矿型晶体结构的结晶相和以licl表示的结晶相的情况下,在该化合物a的x射线衍射图谱(射线源:cu)中,相对于在2θ=25.3~25.9°附近、更详细而言在2θ=25.4~25.8°附近所检测出的立方晶系硫银锗矿型结晶相的(220)面的峰强度ia(220),在2θ=34.8~35.0°附近、更详细而言在2θ=34.8~34.9°附近所检测出的licl结晶相的(200)面的峰强度il(200)的比例[il(200)/ia(220)]优选为0.30以下。
此时,[il(200)/ia(220)]为0.30以下是指能够较高地维持干燥空气放置后的电导率,并且能够抑制硫化氢的产生,该情况下,若适量含有licl则进一步优选。
从该方面考虑,[il(200)/ia(220)]优选为0.30以下,其中进一步优选为0.20以下,其中更进一步优选为0.01以上或0.10以下,其中特别优选为0.05以上。
本固体电解质只要含有化合物a即可,但也可以包含其它材料、成分。作为其它材料,可以举出其它固体电解质材料、或li2s、li3ps4、li4p2s6、lipscl、licl等。但并不限于这些。
但是,本固体电解质优选化合物a为主材料,优选化合物a占本固体电解质整体的50质量%以上、尤其是80质量%以上、尤其是90质量%以上(包括100质量%),其中特别优选仅由化合物a构成。
另外,除了上述其它材料以外,本固体电解质也可以包含对本发明效果的不良影响少的程度、即小于5质量%、尤其是小于3质量%的程度的不可避免的杂质。
(耐湿性)
关于本固体电解质,可以将干燥空气暴露后的电导率提高为1×10-3s·cm-1以上、进一步能够提高为2×10-3s·cm-1以上。
需要说明的是,本说明书中的“干燥空气”是指:用空气干燥机等除去至水分浓度为100ppm以下(以露点计约为-42℃以下)后的空气。
(硫化氢产生量)
本固体电解质可以将放置于大气中时的硫化氢(h2s)产生量抑制为小于10cm3·g-1、尤其是小于1.0cm3·g-1。
(离子传导性)
已知硫化物系固体电解质原本的离子传导性优异,与氧化物相比,在常温下容易形成与活性物质的界面,能够降低界面电阻。其中,本固体电解质由于硫缺陷少、结晶性高,因而电子传导性低、锂离子传导性特别优异。
(制造方法)
接着,对化合物a或本固体电解质的制造方法的一例进行说明。但是,此处说明的制造方法仅为一例,并不限定于该方法。
化合物a或本固体电解质例如可以通过将硫化锂(li2s)粉末、五硫化二磷(p2s5)粉末与氯化锂(licl)粉末混合并进行烧制而获得。
关于硫化锂(li2s)粉末、五硫化二磷(p2s5)粉末与氯化锂(licl)粉末的比例,优选将38.8份~72.0份(摩尔%)的硫化锂(li2s)粉末、10.2份~12.4份(摩尔%)的五硫化二磷(p2s5)粉末和15.6份~51.0份(摩尔%)的氯化锂(licl)粉末进行混合。
另外,作为原料的混合方法,例如优选用球磨机、珠磨机、均化器等进行粉碎混合。
此时,粉碎混合中,若通过机械合金化法等非常强力的机械粉碎混合使原料粉末的结晶性降低或非晶化,或者使原料混合粉末均质化,则阳离子与硫的结合断开,在烧制时生成硫缺陷,表现出电子传导性。因此,能够维持原料粉末的结晶性的程度的粉碎混合是理想的。
如上所述进行混合后,根据需要使其干燥,接下来在非活性气氛或硫化氢气体(h2s)流通下进行烧制,根据需要进行破碎或粉碎,根据需要进行分级,由此可以得到。
需要说明的是,对于硫化物材料,若温度升高,则容易产生硫缺陷,因此以往用石英管等封入而进行烧制。但是,这样的话,在工业上难以制造。另外,由于所封入的石英管被密闭,因而在石英管内所含有的气体因加热而膨胀,石英管内的压力升高,有可能破裂。因此,封入时需要尽可能为真空状态。但是,在真空状态中,硫化物材料内容易产生硫缺陷。
对此,化合物a从200℃左右起进行结晶化,因而即使在比较低的温度下烧制,也能够合成。因此,通过在非活性气氛或者硫化氢气体(h2s)流通下于350℃以上进行烧制,能够制作基本上不存在硫缺陷的、作为目标化学组成的硫化物的化合物a。
其中,烧制时使用硫化氢气体的情况下,由于烧制时硫化氢分解而生成的硫气体,能够提高烧制试样附近的硫分压,因而在高烧制温度下也难以生成硫缺陷,能够降低电子传导性。由此,在含有硫化氢气体的气氛下进行烧制时,烧制温度优选设定为350℃~550℃,其中特别优选设定为450℃以上或500℃以下。
如此在硫化氢气体(h2s)流通下进行烧制时,通过以350℃~550℃进行烧制,可以使硫化物中的硫不发生缺陷而进行烧制。
另一方面,在非活性气氛下进行烧制的情况下,与硫化氢气体的情况不同,烧制时无法提高烧制试样附近的硫分压,因此在高的烧制温度的情况下容易生成硫缺陷,电子传导性升高。因此,在非活性气氛下进行烧制的情况下,烧制温度优选为350℃~500℃,其中特别优选为350℃以上或450℃以下、尤其是400℃以上或450℃以下。
需要说明的是,通常为了使原料粉末完全反应、使未反应相消失,优选流通硫化氢气体并在450℃以上进行烧制,但使用粒径小、反应性高的原料粉末的情况下,低温下也可促进反应,因而也可以在非活性气氛下进行烧制。
另外,上述的原料在大气中极不稳定,与水分反应而分解,产生硫化氢气体或发生氧化,因而优选通过置换为非活性气体气氛的手套箱等将原料设置于炉内而进行烧制。
通过如此制造,可以抑制硫缺陷的生成,可以降低电子传导性。因此,若使用化合物a作为固体电解质来制作全固态锂离子电池,可以使作为电池特性的充放电特性及循环特性良好。
<本固体电解质的用途>
本固体电解质可以用作全固态锂离子电池的固体电解质层、或混合于正极·负极合剂中的固体电解质等。
例如通过形成正极、负极和在正极和负极之间由上述固体电解质构成的层,可以构成全固态锂离子电池。
此时,本固体电解质的耐水性和耐氧化性优异,即便在干燥空气中处理,特性劣化也少,因而即便在例如干燥室等中也能够进行全固态锂离子电池的组装作业。
此处,由固体电解质构成的层可以利用下述方法形成涂膜,之后经过加热干燥将溶剂而制作,所述方法为:例如将包含固体电解质和粘结剂及溶剂的浆料滴加至基体上,用刮刀等刮擦的方法;在浆料接触后用气刀切去的方法;丝网印刷法;等等。或者,也可以对于固体电解质的粉体,通过压制等制作压粉体后,适当加工而制作。
作为正极材料,可以适当使用用作锂离子电池的正极活性物质的正极材料。作为正极活性物质,例如作为物质,可以举出例如尖晶石型锂过渡金属氧化物、具有层状结构的锂过渡金属氧化物、或橄榄石、或者这些中的两种以上的混合物。
关于负极材料,也可以适当使用用作锂离子电池的负极活性物质的负极材料。
例如,本固体电解质的电化学性质稳定,因而能够使用以与锂金属匹敌的低电位(约0.1vvsli+/li)进行充放电的人造石墨、天然石墨、难石墨化性碳(硬碳)等碳系材料作为锂离子电池的负极活性物质。因此,在使用本固体电解质作为锂离子电池的电解质的同时,使用碳系材料作为负极活性物质,由此能够大幅提高全固态锂离子电池的能量密度。由此,例如能够构成具有本固体电解质、和人造石墨、天然石墨、难石墨化性碳(硬碳)等含有碳的负极活性物质的锂离子电池。
另外,也可以使用作为高容量负极材料有前途的硅活性物质来作为锂离子电池的负极活性物质。在使用一般的电解液的锂离子电池中,通过反复进行充放电,确认到劣化从硅活性物质的颗粒表面进行的倾向。在该劣化部分,吸入了电解液成分的氧的硅的氧化进行,因而尝试了用氟置换电解液中包含的碳酸盐的一部分,或者出于为了避免与电解液的接触而在活性物质表面形成覆膜的目的,尝试了添加几%的碳酸亚乙烯酯(vc)等。通过使用本固体电解质作为锂离子电池的电解质,并且使用硅活性物质作为负极活性物质,具有下述优点:不仅不包含作为氧源的电解液,而且固体电解质自身的耐氧反应性、耐水分反应性提高,因而固体电解质带入电池内的作为杂质的氧量也少。因此,能够进一步提高保存特性等耐久性。由此,可以构成例如具有本固体电解质和硅系负极活性物质的锂离子电池。
<使用本固体电解质的锂离子电池的使用方法>
关于使用本固体电解质的锂离子电池、例如具备本固体电解质、包含硅的负极活性物质(也称为“硅负极活性物质”)和包含锂复合氧化物的正极活性物质的锂离子电池的使用方法,在充放电循环中,优选将初次充电的终止电压设定为高于第2次以后的充电的终止电压。
在上述的锂离子电池中,作为负极活性物质,只要包含50质量%以上、优选为70质量%以上、特别优选为90质量%以上的硅,则也可以包含其它材料、例如石墨或锡等。这些其它材料也可以以与硅的合金的方式含有。
已知硅负极活性物质的容量大于石墨负极活性物质。例如,即便利用硅负极活性物质的40%左右的容量,与石墨负极活性物质相比也能够实现足够高的容量。另外,在使用硅负极活性物质所具有的100%的容量来对电池进行充放电的设计中,电池的寿命无法长时间持续。因此,在使用硅负极活性物质的锂离子电池中,通常为以相较于硅负极活性物质所具有的容量相当低的容量对电池进行充放电的设计。但是,这样的话,存在无法发挥硅负极活性物质本来所具有的性能的问题。
为了解决该课题,如上所述,通过将初次循环的充电的终止电压设定为高于第2次以后的循环的充电的终止电压而进行充电,提高硅负极活性物质的活性度,从而能够以均等的负荷率使硅负极活性物质发挥功能,其结果,能够提高电池的寿命特性(循环特性)。
在上述使用方法中,初次充电的终止电压优选设定为比第2次以后的充电的终止电压高0.1v以上来进行充电,其中更优选设定为高0.3v以上、尤其是高0.5v以上来进行充电。初次与第2次以后的充电终止电压之差的上限值不是临界性的,典型地为2v左右。
需要说明的是,上述锂离子电池的使用方法能够应用于具备硅负极活性物质的锂离子电池。特别是,通过应用于包含具有立方晶系硫银锗矿型晶体结构的结晶相的化合物的硫化物系固体电解质,能够与本固体电解质的情况同样地提高循环特性。与此相对,在使用电解液系的电解质的锂离子电池的情况下,若初次循环时施加高电压,则电解液有可能发生分解,因而难以应用。
其中,在具备本固体电解质以外的硫化物系固体电解质的锂离子电池的情况下,由于附随于硅负极活性物质的氧的影响,在高温状态下进行充放电时的寿命特性有可能降低。与此相对,本固体电解质与其它硫化物系固体电解质相比,能够抑制与氧的反应的特性优异,因而若将上述使用方法应用于使用本固体电解质的锂离子电池,则可以得到即便在高温状态下进行充放电也能够维持寿命特性(循环特性)的特别优异的效果。
<术语的说明>
本发明中,“固体电解质”是指固体状态的离子、例如li+能够移动这样的全部物质。
另外,本发明中记为“x~y”(x、y为任意的数字)的情况下,只要没有特别声明,则包括“x以上y以下”的含义、以及“优选大于x”或“优选小于y”的含义。
另外,记为“x以上”(x为任意的数字)或“y以下”(y为任意的数字)的情况下,包括“优选大于x”或“优选小于y”的含义。
另外,本发明中“锂离子电池”广泛地包括通过锂离子在正极与负极之间移动而进行充放电的二次电池。
实施例
下面,基于实施例来说明本发明。但是,本发明不限定于这些实施例来解释。
(实施例·比较例)
按照形成表1所示的原料组成(摩尔%)的方式,使用硫化锂(li2s)粉末、五硫化二磷(p2s5)粉末和氯化锂(licl)粉末,分别进行称量使总量达到5g,用球磨机粉碎混合15小时,制备混合粉末。将该混合粉末填充至碳制容器中,将该混合粉末一边在管状电炉中以1.0l/分钟流通硫化氢气体(h2s、纯度100%),一边以200℃/小时的升降温速度将其在500℃烧制4小时。之后,用研钵将试样破碎,用网孔为53μm的筛进行整粒,得到粉末状的样品。
此时,上述称量、混合、在电炉中的安放、从电炉中的取出、破碎和整粒操作均在用充分干燥后的ar气体(露点-60℃以上)置换的手套箱内实施。
<组成的测定>
对于实施例和比较例中得到的样品,利用icp发射光谱法测定组成,将组成式示于表中。
<x射线衍射>
利用x射线衍射法(xrd、cu射线源)对实施例和比较例中得到的粉末状的样品进行分析,确定了生成相。
另外,根据此时得到的x射线衍射图谱,计算出在2θ=34.8~35.0°附近检测出的(200)面的峰强度il(200)相对于在2θ=25.3~25.9°附近检测出的(220)面的峰强度ia(220)的比例[il(200)/ia(220)]。
<硫化氢(h2s)的产生量的测定>
对于实施例和比较例中得到的样品,在用充分干燥后的ar气体(露点-60℃以下)置换的手套箱内分别称量50mg,放入通过层积而密闭的袋中。其后,将容量1755cm3的丙烯酸制的盒放入在大气气氛中以室温(25℃)和湿度30%所保持的恒温恒湿槽中,保持至丙烯酸制的盒的内部与恒温恒湿槽内的环境相同为止,之后将放入有样品的密闭袋在恒温恒湿槽中开封,将样品迅速地配置于丙烯酸制的盒中。对于将样品配置于丙烯酸制的盒中后立即经过300秒为止所产生的硫化氢,利用硫化氢传感器(理研计器制造gx-2009)测定了硫化氢浓度。由经过300秒后的硫化氢浓度计算出硫化氢的容积,求出硫化氢产生量。
<初始电导率的测定>
对于实施例和比较例中得到的样品,在用充分干燥后的ar气体(露点-60℃以下)置换的手套箱内以200mpa的压力进行单轴加压成型,制作直径10mm、厚度2mm~5mm的颗粒,进而在颗粒上下两表面涂布作为电极的碳糊料,之后在180℃进行30分钟热处理,制作了离子电导率测定用样品。离子电导率测定在室温(25℃)下使用交流阻抗法进行。
<干燥空气曝露后的电导率的测定>
将实施例和比较例中得到的样品放入用平均露点为-45℃的干燥空气进行了置换的手套箱内,放置6小时。之后,将样品再次放入用充分干燥后的ar气体(露点-60℃以下)置换的手套箱内,与初始电导率的测定同样地测定了干燥空气曝露后的离子电导率。
表1中的“x”、“y”分别表示组成式:li7-x+yps6-xclx+y的x、y,“初始”表示初始电导率,“干燥空气曝露6小时”表示干燥空气曝露6小时后的电导率。
另外,在表1的生成相的项目中,“a”表示立方晶系硫银锗矿型晶体结构的li7-x+yps6-xclx+y相构成的单相,“a+licl”表示该li7-x+yps6-xclx+y相与licl相的混合相,“a+li2s”表示该li7-x+yps6-xclx+y相与li2s相的混合相。
[表1]
[表1]
由上述表1的结果和目前为止进行的试验结果可知:若为含有立方晶系硫银锗矿型晶体结构的结晶相且由组成式(1):li7-x+yps6-xclx+y所表示的硫化物系固体电解质化合物,且该固体电解质化合物中上述组成式(1)中的x和y满足0.05≤y≤0.9和-3.0x+1.8≤y≤-3.0x+5.7,则在上述试验中能够将硫化氢(h2s)的产生量抑制为小于10cm3·g-1,而且在上述试验中能够将干燥空气暴露后的电导率提高为1.0×10-3s·cm-1以上。
由图4可知,大致x为0.8以上的情况下,licl添加量(y)为0.2左右时,显示出高电导率,进而若licl添加量(y)增大,则电导率缓慢地降低。关于这点,认为:通过添加licl而使licl在化合物a的颗粒的表面析出,从而抑制硫化物固体电解质颗粒与干燥空气的接触,因此即便暴露于干燥空气后也能够维持高电导率。其中,若licl的添加量增多,则干燥空气中所含有的略微的水分与licl的反应被促进,与水分进行了反应的licl与化合物a发生反应,因而在干燥空气暴露后无法维持高电导率。
由图5可知,若licl添加量(y)增大,则h2s产生量降低。认为这是因为,通过添加licl,licl在化合物a的颗粒的表面析出,由此抑制化合物a的颗粒与干燥空气的接触,因而变得难以与干燥空气中所含有的略微的水分进行反应。
<使用本固体电解质化合物的锂离子电池的制作和使用方法>
(电池的制作)
将纯硅粉末(d50:2.5μm、氧浓度0.7wt%)47.5质量份和实施例1中得到的样品(本固体电解质粉末)的粒度调整品(d50:3.1μm)47.5质量份、作为导电助剂的乙炔黑(电气化学工业制造)5质量份进行混合,成型为厚度100μm的圆板状,制作出负极颗粒。
另外,将实施例1中得到的样品(本固体电解质粉末)的粒度调整品(d50:3.1μm)成型为厚度100μm的圆板状,制作出固体电解质颗粒。
另外,将锂复合氧化物(lini0.5co0.2mn0.33o2)粉末(d50:2.5μm)60质量份、实施例1中得到的样品(本固体电解质粉末)的粒度调整品(d50:3.1μm)38质量份和乙炔黑2质量份进行混合,成型为厚度100μm的圆板状,制作出正极颗粒。
用负极电极堵塞上下开口的聚丙烯制的圆筒(开口直径10.5mm、高度18mm)的下侧开口部,在该负极电极上依次放置上述负极颗粒、上述固体电解质颗粒和上述正极颗粒,用正极电极堵塞上侧开口部,制作出模具电池。
(充放电条件)
使用如上所述制作的模具电池,如下实施充放电试验(参照试验·实施例试验),对高温循环特性进行了评价。
在参照试验中,将电池放入环境试验机内,该环境试验机按照对电池进行充放电的环境温度为25℃的方式进行了设定,进行准备以能够充放电,静置而使电池温度达到环境温度后,第1次循环以0.1c恒流恒电位充电至4.2v后,以0.1c恒流放电至2.5v,第2次循环使充放电范围为4.2v~2.5v而进行充放电。接着,变更设定条件以使环境温度为60℃,静置而使电池温度达到环境温度后,第3次循环以后使充放电范围为4.2v~2.5v,充电以0.1c恒流恒电位、放电以0.1c恒流进行1个循环充放电,之后以0.2c进行20次充放电循环。
与此相对,在实施例试验中,将电池放入环境试验机内,该环境试验机按照对电池进行充放电的环境温度为25℃的方式进行了设定,进行准备以能够充放电,静置而使电池温度达到环境温度后,第1次循环以0.1c恒流恒电位充电至4.5v后,以0.1c恒流放电至2.5v,第2次循环使充放电范围为4.2v~2.5v而进行充放电。接着,变更设定条件以使环境温度为60℃,静置而使电池温度达到环境温度后,第3次循环以后使充放电范围为4.2v~2.5v,充电以0.1c恒流恒电位、放电以0.1c恒流进行1个循环充放电,之后以0.2c进行20次充放电循环。
需要说明的是,在上述的比较例试验和实施例试验中,使3ma为1c,基于该1c的电流值计算出各自的c倍率的电流值,用于容量维持率的评价。
(结果)
其结果,在参照试验中,第20次循环的容量维持率为62.9%;与此相对,实施例试验中容量维持率为95%。另外,在该实施例试验中未确认到通常在包含电解液的电池中确认到的被认为是来自电解液分解反应的气体产生。
由这样的试验结果和迄今为止本发明人所进行的试验结果可知,关于至少具备本固体电解质和硅负极活性物质的锂离子电池的使用方法,通过在充放电循环中将初次充电的终止电压设定为高于第2次以后的充电的终止电压而进行充放电,从而可以提高硅负极活性物质的活性度,能够以高负荷率使硅负极活性物质发挥功能,能够提高电池的寿命特性(循环特性),并且本固体电解质能够抑制附随于硅负极活性物质的氧的影响,因而能够提高上述高温环境(40℃以上)下的充放电中的寿命特性(循环特性)。
并且还可知,此时,更优选初次充电的终止电压设定为高于第2次以后的充电的终止电压而进行充电。
- 还没有人留言评论。精彩留言会获得点赞!