微尺度和中尺度冷凝器装置的制作方法
背景技术:
本发明涉及微尺度和/或中尺度冷凝器装置,更具体地涉及用于微流分离和/或纯化中尺度和/或纳米尺度粒子的微尺度和/或中尺度冷凝器阵列。
纯化粒子(例如胶体)的能力对于纳米材料的实际应用和分析是重要的。在生物学和医学中这是最重要的,其中范围从蛋白质、囊泡和细胞器的生物胶体构成所有生物的分子结构单元。纯化典型地做出一个空间要求:所希望的胶体可以转移到一个特定空间,由此将它们从其他污染物和不希望的物种中去除。许多纳米技术和生物技术已经涉及纯化技术,包括凝胶电泳、层析、离心、亲和结合和分子筛分。在所有这些技术中,消耗能量以将胶体物质从混合物物理转移到未污染的溶剂中,从而实现纯化。
尽管已确立的纯化技术成功,芯片实验室和/或微流体技术的新兴领域对这些经典方法提出了挑战。快速和精确地在芯片上纯化少量样品(特别是对于稀有样品或远程位置)的需要已经抵消了胶体纯化技术(如离心和/或亲和方法)的许多先前优点,这可能需要大的机器或易碎的化学物来操作。已经证明基于周期性纳米结构或“超材料”的新技术对于芯片上纯化系统是有效的,一个实例是微米级和纳米级的确定性侧向移位(“纳米dld”),其使用不对称的中等尺度柱体阵列将胶体混合物的射流侧向移位成大小分类的流。这种方法的变体,称为纳米级冷凝器阵列(“nca”),使用流体流动本身的操纵产生了胶体混合物在流动流中的侧向分裂,从而产生了移位粒子的几乎与尺寸无关的方法。
尽管芯片上超材料方法如纳米dld和nca具有优势,但仍存在吞吐量的问题。诸如nanodld和nca的技术具有极低的流速(例如,<1纳升/每小时(nl/hr))由于对流体流动的纳米尺度尺寸限制效应,并且芯片上电泳方法不产生明显的质量流,使得从芯片上技术制备样品是非常不切实际的。这在芯片实验室(lab-on-a-chip)技术中留下了未满足的空间,其中芯片可以处理样品但是不能使得产品足够用于进一步分析(例如,芯片上或芯片外)。
技术实现要素:
下面给出概述以提供对本发明的一个或多个实施例的基本理解。本概述不旨在标识关键或重要元素,或描绘本发明的范围或权利要求的任何范围。其唯一目的是以简化形式呈现概念,作为稍后呈现的更详细描述的序言。在本文所述的本发明的实施例中,描述了关于用于中尺度和/或纳米尺度粒子的微流体分离和/或纯化的微尺度和/或中尺度冷凝器阵列的设备和/或方法。
根据本发明的实施例,提供了一种装置。该装置包括电容阵列,该电容阵列包括多个柱体,柱体排列成多个列。大于或等于约0.5微米的柱体间隙位于所述柱体的第一列中的所述柱体的第一柱体与所述第一列中的所述柱体的第二柱体之间。第一柱体与第二柱体相邻。另外,柱体可以界定晶格,所述晶格使流过冷凝器阵列的流体侧向移位。
根据本发明的另一个实施例,提供了一种方法。该方法包括在包括冷凝器阵列的微通道处接收流体。所述方法还包括由阵列在侧向于所述微通道的侧壁的方向上从所述流体中移位粒子。此外,该方法包括以大于约1.0纳升/小时的速率从微通道输出粒子。另外,所述阵列可包括多个柱体,所述多个柱体界定晶格,所述晶格在流体流动穿过所述阵列时侧向地移位流体。
根据本发明的另一个实施例,提供了另一种方法。该方法包括在包括冷凝器阵列的微通道处接收样品流体和溶剂流体。所述方法还包括由所述阵列从侧向于所述微通道的侧壁的方向上的从样品流体中移位样品,其中所述样品可以被移位到所述溶剂流体中。此外,该方法包括以大于约1.0纳升/小时(nanolitersperhour)的速率从微通道输出样品。另外,所述阵列可以包括多个柱体,所述多个柱体可以限定晶格,所述晶格可以在所述样本流体流过所述冷凝器阵列时侧向地移动所述样本。
因此,本文所述的本发明的各种实施方式涉及微尺度和/或中尺度冷凝器阵列设计,其可:在宽尺寸带上操纵纳米尺度和/或中尺度粒子(例如,胶体);并且包括微尺度和/或中尺度流体通道(例如,包括孔和/或间隙),其允许比常规纳米尺度超材料更高的吞吐率。在此描述的微米级和/或中等级冷凝器阵列提供了粒子(例如,胶体纯化)同时维持低流体阻力,由此使芯片能够输出可感知的流体流(例如,100-1000+微升/小时(μl/hr))以用于低至中等体积制备应用的能力。
附图说明
图1是体现本发明的电容器阵列的图;
图2是体现本发明的冷凝器阵列的柱体形状图;
图3a是体现本发明用于将一个或多个粒子朝向收集壁移位的冷凝器阵列的图;
图3b是体现本发明用于将一个或多个粒子朝向子通道移位的冷凝器阵列的图;
图4是体现本发明的包括具有变化的柱体间隙的多个级的冷凝器阵列的图;
图5a是体现本发明的包括具有变化的移位方向的多个状态的冷凝器阵列的图;
图5b是体现本发明的包括多个具有变化的移位方向的多个状态的冷凝器阵列的图;
图6示出了根据本文所述的一个或多个实施例的可包括柱体间隙梯度的示例非限制性冷凝器阵列的图。
图7是体现本发明的冷凝器阵列的图,该冷凝器阵列用于将一个或多个粒子朝向收集壁移位以促进微流体纯化;
图8是实施本发明的冷凝器阵列的图,该冷凝器阵列用于将一个或多个粒子朝向收集通道移位以促进微流体纯化;
图9是体现本发明的用于促进经由一个或多个冷凝器阵列的微流体分离的方法的流程图;以及,
图10是体现本发明的一种用于促进经由一个或多个冷凝器阵列的微流体纯化的方法的流程图。
具体实施方式
以下详细说明仅是说明性的并且不旨在限制本发明和/或本发明的应用或用途。此外,没有意图被在前面的背景技术或概述部分中或在具体实施方式部分中呈现的任何表达或暗示的信息所约束。
现在参考附图来描述本发明的一个或多个实施例,其中,贯穿全文,相同的附图标记用于指代相同的元件。在以下描述中,出于解释的目的,阐述了许多具体细节以便提供对本发明的更全面的理解。然而,显然,在各种情况下,可以在没有这些具体细节的情况下实践本发明的实施例。
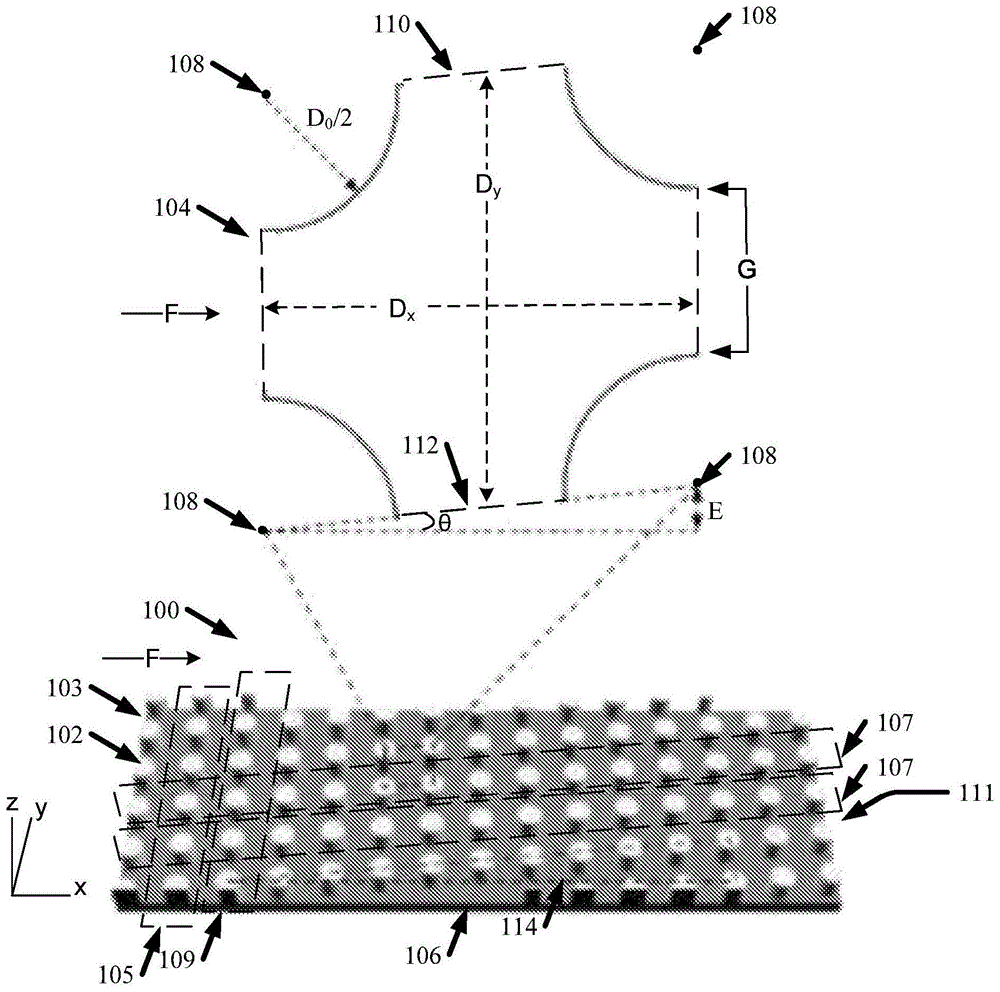
图1是体现本发明的冷凝器阵列100的图。阵列100位于微通道103内并且包括多个柱体102。阵列100基于由柱体102限定的一个或多个晶格结构104促进的流体动力混乱的原理来操作。阵列100可以是微尺度冷凝器阵列和/或中尺度冷凝器阵列。例如,阵列100可在微尺度和/或中尺度上具有一个或多个几何形状。如在此使用的,术语“微尺度”是指具有一个或多个特征尺寸大于或等于1微米并且小于或等于999微米的装置、设备、和/或特征。如在此使用的,术语“中等尺度”是指具有一个或多个特征尺寸大于或等于0.1毫米并且小于或等于100毫米的装置、设备、和/或特征。
流体沿图中箭头“f”所示的方向流过微通道103,从而流过阵列100。当流体流f被引导通过阵列100时,柱体102使流体本身偏转,导致流体流的次要侧向分量,其在微通道103的长度上不平均。流体的净侧向移位使流体的粒子侧向移动;并且由此在阵列100内实现空间移位或“冷凝”。阵列100将粒子浓缩成浓缩流。此外,浓缩的流可以包含特定尺寸的粒子或不同尺寸的粒子。
将流体的粒子(例如,胶体)凝结成浓缩流可用于浓缩样品和/或制备用于基于用于纯化的尺寸/化学进一步分离成流的样品。由于阵列100自身操纵流体流动,流体内的粒子无论尺寸如何都经历相同的侧向移位。阵列100实现的冷凝(例如,侧向流体移位)取决于晶格结构104和/或柱体102的几何形状。现有技术已经仅在纳米级(例如,对于所有尺寸小于500纳米(nm))上指定了几何形状。冷凝器阵列100可包括操纵纳米尺寸粒子的微米级结构。
如图1所示,柱体102被布置在列(例如,沿着“y”轴横穿微通道103的列105)和行(例如,沿着“x”轴横穿微通道103的行107)中。另外,包括柱体102的相邻列105、109可以被布置为彼此偏移(例如,沿着y轴),从而相对于微通道103的壁106成角度地定位行。图1示出了由四个柱体(例如,柱体102可以是四个柱体之一的示例)限定的晶格结构104的展开图。
晶格结构104由柱体中的四个柱体限定(例如,其中一个或多个柱体可以如在柱体102处所示)。晶格结构104可以位于整个阵列100或阵列100的一部分处。此外,四个柱体102可以彼此相邻。例如,列105的两个相邻的柱体102和行107的两个相邻的柱体102可限定一个晶格结构104,其中列105和行107可彼此相邻。图1以虚线示出了限定晶格结构104的四个示范性柱体102的示例。此外,如图1所示,虚线描绘由四个柱体102限定的晶格结构104的展开图。本领域普通技术人员将认识到,阵列100可以包括在微通道100内除了图1所示的扩展晶格结构104的位置之外的一个或多个位置中的一个或多个晶格结构104。
如图1所示,“e”表示顺序列的柱体102的中心108之间的侧向移位。柱体102的连续列之间的侧向移位(例如,由e表示)由公式1表征:dy/n。阵列100的侧向移位(例如,由e表示)可大于或等于0.01和/或小于或等于0.3。
如图所示1,“dy”表示沿着阵列100的y轴跨越晶格结构104的第一距离。dy从晶格结构104的第一边界110延伸到晶格结构104的第二边界112。进一步,第一边界110可由柱体102的第一行107的第一中心线限定,并且第二边界112由柱体102的第二行107的第二中心线限定;其中,第一行107和第二行107可以彼此相邻。dy可以大于或等于1μm和/或小于或等于100μm。
如图1所示,“n”表示用于克服侧向移位并且将两个列对准放置的顺序列的数目。例如,对于图1所示的阵列101,n等于10,如虚线三角形114所示,其例示了侧向移位。
此外,如图1所示,“dx”表示沿着阵列100的x轴跨越晶格结构104的第二距离。dx可以从晶格结构104的第三边界116延伸到晶格结构104的第四边界118。进一步,第三边界116可由柱体102的第一列105的第三中心线限定,并且第四边界118可由柱体102的第二列105的第四中心线限定;其中,第一列105和第二列105可以彼此相邻。另外,沿着与沿着其测量dx的第二方向(例如,沿着阵列100的x轴)正交的第一方向(例如,沿着阵列100的y轴)测量dy。dx可以大于或等于1μm并且小于或等于100μm。
此外,如图1所示,“d0”表示限定主题晶格结构104的柱体102的直径。d0可以大于或等于0.5μm和/或小于或等于99.5μm。此外,柱体102可以具有大于或等于1μm和/或小于或等于100μm的高度。如图1所示,“g”表示同一列105的相邻柱体102之间的柱体间隙。阵列100可具有大于或等于0.5微米(μm)和/或小于或等于100μm的g。此外,如图1所示,“θ”表示微通道103的壁106各自的角度。θ可大于0度且小于90度。
晶格结构104的晶格比由公式2表征:dx/dy。晶格比可以大于0.1和/或小于或等于1.0以促进阵列100的操作。另外,阵列100的几何比由公式3表征:d0/dy。几何比可大于0.1且小于或等于1.0以促进阵列100的操作。此外,阵列100可包括大于或等于100列的柱体102以促进操作。例如,阵列100可具有大于或等于0.1毫米(mm)且小于或等于10mm的总长度(例如,沿着x轴)。包含本文所述的几何形状中的一者或一者以上的阵列100可促进微尺度和/或中尺度阵列100结构和/或促进高吞吐率。
图2是柱体(例如,柱体102)的形状的示图。图2示出了示例柱体102的横截面。虽然图2描绘了六个示范性形状,柱体102的架构不限于此。本领域的普通技术人员将认识到,柱体(例如,柱体102)可以形成为图2中描绘的柱体的替代形状,基于本文中所描述的信息,可以促进其他几何尺寸(例如,关于阵列100和/或晶格结构104)。图2示出了圆形形状202、三角形形状204、正方形形状206、u形形状208、环形形状210、五边形形状212(例如,不规则五边形)。
图3a和3b是微通道300、302的图。在附图3a和3b中,阵列100横穿整个微通道300、302;然而,阵列100可以横越微通道300、302的一部分。一个或多个微通道300、302可以具有微通道103的结构和/或功能。
侧向移位(例如,由图1中的e表示)。1)定义柱体102的行沿着微通道300、302的轴向长度(例如,沿着x轴)的角度(例如,由θ表示)。进而,该角度(例如,由θ表示)限定了冷凝器阵列100的侧向移位方向(例如,由箭头“ld”表示)。侧向移位方向(例如,由箭头ld表示)表示粒子移位的方向。流体可以通过阵列100在稳定状态下流动(例如,在由箭头f指示的流体方向上),受到诸如电渗流、压力驱动流、毛细管流、其组合等的外部驱动力的影响。
在图3a中示出的微通道300可以是壁聚焦微通道,其中,粒子在朝向收集壁304的侧向移位方向(例如,由箭头ld表示)上移位。此外,粒子沿着收集壁304收集,从而形成浓缩的粒子流。经由微通道300的入口侧306向阵列100提供流体。流体流动(例如,在由箭头f指示的方向上)通过阵列100至微通道300的出口侧308,其中,流体和粒子离开阵列100和微通道300。当流体流动通过阵列100时,流体内的粒子朝向收集壁304移位(例如,在由箭头ld指示的方向上)。当粒子沿着收集壁304收集时,粒子形成通过微通道300的出口侧308的一部分离开阵列100的浓缩流。在图3a中,粒子通过阵列100的流动由区域310例示。因此,微通道300(例如,壁聚焦微通道)包括单个侧向移位方向(例如,由箭头ld表示),其推动粒子抵靠收集壁304,实现入口流冷凝成浓缩流。
在图3b中示出的微通道302是通道聚焦微通道,其中流体在多个侧向方向(例如,由箭头ld指示)上朝向收集通道312(例如,子通道)移位。此外,粒子沿着收集通道312收集,形成浓缩的粒子流。经由微通道302的入口侧306向阵列100提供流体。流体流动(例如,在由箭头f指示的方向上)通过阵列100至微通道302的出口侧308,其中,流体和粒子离开阵列100和微通道302。当流体流动通过阵列100时,粒子在朝向收集通道312的第一侧向移位方向上移位,并且其他粒子在朝向收集通道312的第二侧向移位方向上移位。换言之,阵列100的晶格结构104可以被配置为在第一侧向移位方向上移位粒子,而阵列100的其他晶格结构104可以被配置为在第二侧向移位方向上移位粒子。
当粒子沿着收集通道312收集时,粒子形成离开微通道302的出口侧308的一部分的浓缩流。在图3b中,粒子通过阵列100的流动由区域314例示。因此,微通道302(例如,通道聚焦微通道)包括具有两个相对侧流的镜面,其将粒子推入阵列100内的单个流中,称为收集通道312。
通过缩放柱体102的两个部分(例如,冷凝器阵列100的两个部分),收集通道312可以位于沿着微通道的侧向宽度(例如,沿着y轴)的任何坐标处。而图3b示出了沿着阵列100的中间定位的收集通道312,收集通道312可以进一步定位在图3b所示的位置的左侧或右侧。此外,侧向方向(例如,由箭头ld指示)可以向外反射以抵靠微通道302的两个壁移位粒子。
阵列100可包括均匀的几何形状或变化的几何形状。例如,图4是包括变化几何形状的微通道400的图。微通道400包括具有多个级(stage)的阵列100或具有相应几何结构的多个相邻阵列100,该多个级具有相应几何结构。为了简单起见,微通道400在本文中被描述为包括具有多个级的阵列100,每个级可以具有不同的几何形状。微通道400可以具有微通道103、300、302的结构和/或功能。
流体从入口侧306到出口侧308(例如,在由箭头f指示的方向上)流过微通道400。当流体流过微通道400时,流体由阵列100操纵。阵列100包括多个级,诸如第一级402、第二级404、第三级406和第四级408。而图4示出了四个级,还设想了另外的或更少的级。阵列100可包括任何数量的所需级,使得流体动力阻力不妨碍所需通过量。阵列100的每一级可由不同的几何结构表征,其包括但不限于:不同的柱体102宽度(例如,由d0表示)、不同的柱体102高度、不同的柱体102形状、不同的柱体102间隙(例如,由g表示)、不同的侧向移位(例如,由e表示)、不同的柱体102行角(例如,由θ表示)、不同的第一距离(例如,由dy表示)、不同的第二距离(例如,由dx表示)、不同的晶格比、不同的几何结构比、其组合和/或类似物。图4示出了柱体102间隙(例如,由g表示)可以随着微通道400的阵列100的每个顺序级而变窄。
当流体流过阵列100时,它被每个级不同地操纵。阵列100的每一级可具有不同的柱体间隙大小(例如,由g表示),从而对于四种不同的胶体种类a至d引起不同的偏转角。胶体种类的大小可以变化并且可以表征为a>b>c>d。第一级402使最大的胶体种类a抵靠收集壁304移位,在这里它被侧通道或出口隔离。每个另外的级具有改进的几何比(例如,通过d0/dy表征),这增加了次最大胶体的偏转角,允许所有胶体种类的系统冷凝和分离。换言之:第二级404使第二大胶体物质b抵靠收集壁304移位,在这里它可以被另一侧通道或出口隔离。第三级406使第三最大胶体物质c抵靠收集壁304移位,在这里它可以被另一侧通道或出口隔离。第四级408使第四大胶体物质d抵靠收集壁304移位,在这里它可以被另一侧通道或出口隔离。如图4所示,第三区域410描绘了最大胶体种类a的流路,第四区域412描绘了第二最大胶体种类b的流路,第五区域414描绘了第三最大胶体种类c的流路,并且第六区域416描绘了第四最大胶体种类d的流路。这允许基于尺寸从单个流体流中纯化出多种胶体种类。
图5a和5b是包括阵列100的微通道500、502的图,这些阵列促进粒子在多个侧向移位方向上的移位。微通道500和微通道502的阵列100包括多个级,其呈现多个侧向移位方向。
关于图5,流体可以从入口侧306通过微通道500流动(例如,在由箭头f指示的流体方向上)到出口侧308。当流体流过微通道500时,阵列100以变化的侧向移位方向(例如,如箭头ld所示)移位流体内的相应粒子物质。例如,阵列100的第五级504使流体沿第一侧向移位方向(例如,如图5a的箭头ld所示,向右侧)移位。由此,第一胶体种类(例如,a)沿着收集壁304移位并且形成通过出口侧308离开阵列100的浓缩流(例如,如箭头a所描绘的)。而且,阵列100的第六级506在第二侧向移位方向(例如,如图5a的箭头ld所示,向左侧)上移位流体。由此,第二胶体种类(例如,b)沿着第二收集壁508移位并且形成通过出口侧308离开阵列100的另一浓缩流(例如,如箭头b所描绘的)。第七区域510描绘了第一胶体种类(例如,a)通过阵列100的流动路径。第八区域512描绘了第二胶体种类(例如,b)通过阵列100的流动路径。
关于图5b,流体可以从入口侧306通过微通道502流动(例如,在由箭头f指示的流体方向上)到出口侧308。当流体流动通过微通道502时,阵列100在不同的侧向移位方向(例如,如箭头ld所示)上移位流体内的相应粒子物质。例如,阵列100的第七级514沿第一侧向移位方向(例如,如图5b的箭头ld所示,向图中的右侧)移位流体。由此,第一胶体种类(例如,a)沿着收集壁304移位并且形成通过侧出口(例如,如箭头a所描绘的)离开阵列100的浓缩流。同样,阵列100的第八级516在第二侧向移位方向(例如,图5a中如箭头ld所示向图中左侧)上移位流体。由此,第二胶体种类(例如,b)可以沿着第二收集壁508移位并且形成通过出口侧308(例如,如箭头b所描绘的)离开阵列100的另一浓缩流。此外,冷凝器阵列100的第九级518再次使流体沿第一侧向移位方向移位。由此,第三胶体种类(例如,c)沿着收集壁304移位并且形成另一浓缩流,该另一浓缩流通过出口侧308离开阵列100(例如,如箭头c所描绘的)。第九区域520描绘了第一胶体种类(例如,a)通过阵列100的流动路径。第十区域522描绘了第二胶体种类(例如,b)通过阵列100的流动路径。第十一区域524描绘了第二胶体种类(例如,c)通过阵列100的流动路径。
因此,图5a和5b示出了阵列100,其中每个连续级的侧向方向可以变化以按尺寸操纵粒子群体。在图5a所示的两级实施例中,操纵了两种胶体射流,使得较大种类(例如,a)在通道(例如,收集壁304)的一侧冷凝并分离,并且第二种类(例如,b)在相对侧(例如,第二收集壁508)偏转并冷凝。该空间分离允许两个粒子射流随后在阵列100的出口(例如,出口侧308)处分离,以实现高分辨率分离。图5b中示出了三级设计,对3种粒子(例如胶体)射流实现相同的分离。本领域的普通技术人员将理解,任何数目的级(各自具有变化的几何形状和长度)可以顺序地运行以实现粒子的不同偏转和分离。其中阵列100促进多个侧向移位方向的本发明的实施方式具有基于尺寸分离和/或纯化各种粒子(例如,胶体)的优点。
图6是包括多级冷凝器阵列100的微通道600的示图。如图6所示,包括微通道600的阵列100的各种阴影表示相应的阵列100的几何形状。图6描绘了阵列100的四个示范性级的展开图,其具有相应的几何形状(例如,变化的柱体102间隙g)。图.6展示分级阵列100,其中不同几何形状之间的转变是每一柱体102行107之间的逐渐改变。与分级设计中的突然转变相反,包括所示的粒子偏转梯度变化的阵列100可用于粒子混合物,其中尺寸差是连续分布(分散),因此需要连续分馏以达到效果分离。
图7是微通道700的图,其包括壁聚焦阵列100并且促进样品流体的纯化。
微通道700包括与样品入口702和溶剂入口704流体连通的阵列100。样品流体流过样品入口702(例如,在由箭头“sa”指示的方向上)并且进入阵列100中。溶剂流体流过溶剂入口704(例如,在由箭头“s”指示的方向上)并且进入阵列100中。样品和溶剂流体流动通过阵列100(例如,在由箭头f指示的方向上)并且经由污染物出口706和样品出口708离开。当流体流过阵列100时,流体在侧向移位方向(例如,在由箭头ld指示的大体方向上)上移位。此外,样品流体内的样品朝向收集壁304移位。而且,溶剂流体朝向收集壁304移动。样品和溶剂流体沿着收集壁304收集并且形成浓缩的流,该流经由样品出口708离开阵列100。样品流体内的污染物保持没有收集壁304并且经由污染物出口706离开阵列100。第十二区域710描绘了溶剂流体通过阵列100的流动路径。第十三区域712描绘了样品通过阵列100的流动路径。此外,第十四区域714描绘了污染物通过阵列100的流动路径。
微通道700纯化具有高带通的胶体样品,如细胞外囊泡。在这种情况下,纯化将感兴趣的胶体种类与存在于原始注射的样品流中的在一定尺寸范围之外的其他胶体、更大和更小的粒子(包括盐、小分子、污染物等)分离。该纯化通过同时注入与样品流同轴的纯溶剂流进行。该纯溶剂流,其组成由用户根据应用要求选择,产生了一个清洁的溶液空间,粒子可以被偏转到该空间中,从而实现纯化。
图8是微通道800的图,其包括通道聚焦阵列100以促进样品流体的纯化。
微通道800包括与样品入口702和溶剂入口704流体连通的阵列100。样品流体流过样品入口702(例如,在由箭头sa指示的方向上)并且进入阵列100中。同样,溶剂流体流过溶剂入口704(例如,在由箭头s指示的方向上)并且进入阵列100中。样品和溶剂流体流动通过冷凝器阵列100(例如,在由箭头f指示的方向上)并且经由污染物出口706和样品出口708离开。当流体流动通过阵列100时,流体朝向多个侧向移位方向(例如,在由箭头ld指示的方向上)移位。此外,样品流体内的一个或多个样品朝向收集通道312移位。而且,溶剂流体朝向收集通道312移位。该样品和溶剂流体可以沿着收集通道312收集并且形成浓缩的流,该浓缩的流经由样品出口708离开阵列100。相比之下,样品流体内的污染物保持没有收集通道312并且经由污染物出口706离开阵列100。第十五区域802描绘了溶剂流体通过阵列100的流动路径。第十六区域804描绘了样品通过阵列100的流动路径。而且,第十七区域806描绘了污染物通过阵列100的流动路径。
本发明的各种实施例可用于设计促进样品纯化的微通道。而图7和8示出了单个溶剂入口704,还设想了包括与阵列100流体连通的多个溶剂入口704的微通道。另外,微通道700和800可以被修改成包括多级安排(例如,根据图4-6中所示的本发明的实施例)纯化和/或收集多个粒度范围。例如,在此描述的阵列100(例如,图7和/或8的阵列100)。可包括多壁聚焦(例如,双壁聚焦)配置和/或多通道聚焦(例如,双通道聚焦)配置。
图9是使用冷凝器阵列100从流体中分离一个或多个粒子的方法900的流程图。
在902处,方法900包括在包括一个或多个阵列100的微通道103、300、302、400、500、502、600、700、800处接收流体。流体经由入口(例如,入口侧306)在微通道103、300、302、400、500、502、600、700、800处被接收。流体以稳定的速率(例如,经由压力系统)被供应到微通道103、300、302、400、500、502、600、700、800。
在904,方法900包括通过阵列100在侧向(例如,侧向移位方向)于微通道103、300、302、400、500、502、600、700、800的侧壁的方向上移位粒子。此外,在906,方法900包括以大于约1.0nl/hr的速率从微通道103、300、302、400、500、502、600、700、800输出(例如,经由诸如侧出口308的出口)粒子。可以在906处以大于或等于1.0纳升/小时并且小于或等于60毫升/小时(ml/hr)的速率输出该一个或多个粒子。
图10是用于使用冷凝器阵列100纯化样品流体的方法1000的流程图。
在1002处,方法1000包括在包括一个或多个阵列100的微通道103、300、302、400、500、502、600、700、800处接收样品流体和溶剂流体。在微通道103、300、302、400、500、502、600、700、800处经由入口(例如,入口侧306、样品入口702和/或溶剂入口704)接收样品和溶剂流体。以稳定的速率(例如,经由压力系统)将样品和溶剂流体供应至微通道103、300、302、400、500、502、600、700、800。
在1004,方法1000包括通过阵列100在侧向于微通道103、300、302、400、500、502、600、700、800的侧壁的方向(例如,侧向移位方向)上从样品流体移位样品。此外,样品由阵列100移入溶剂流体中。此外,在906,方法900包括以大于约1.0纳升/小时(nl/hr)的速率从微通道103、300、302、400、500、502、600、700、800输出(例如,经由诸如侧出口308的出口、污染物出口706和/或样品出口708)粒子。粒子可以以大于或等于1.0纳升/小时(nl/hr)且小于或等于60毫升/小时(ml/hr)的速率在906输出。
术语“或”旨在表示包含性的“或”而不是排他性的“或”。也就是说,除非另外指明或从上下文中清楚可见,“x采用a或b”旨在意指任何自然的包含性排列。即,如果x采用a;x采用b;或者x采用a和b两者,则在任何前述情况下都满足“x采用a或b”。此外,在本说明书和附图中使用的冠词“一个/一种(a)”和“一个/一种(an)”总体上应被解释为意指“一个或多个”,除非另外指明或从上下文中清楚看出是针对单数形式。如在此所使用的,术语“示例”和/或“示范性”用于意指充当示例、实例或说明。为了避免疑问,本文公开的主题不受这样的示例的限制。此外,在此描述为“实例”和/或“示范性”的任何方面或设计不一定被解释为比其他方面或设计优选或有利,也不旨在排除本领域普通技术人员已知的等效示范性结构和技术。
上述内容仅包括系统和方法的示例。当然,出于描述本发明的目的,不可能描述部件的每个可想到的组合和方法,但是本领域普通技术人员可以认识到本发明的许多进一步的组合和置换是可能的。此外,就在详细说明、权利要求、附件和附图中使用术语“包括”、“具有”、“拥有”等而言,此类术语旨在以与术语“包含”类似的方式是包括性的,因为“包含”在权利要求中用作过渡词时被解释。已经出于说明的目的呈现了本发明的不同实施例的描述,但并不旨在是穷尽性的或局限于本发明。在不脱离本发明的范围的情况下,许多修改和变化对本领域的普通技术人员而言将是显而易见的。选择在此使用的术语以最佳地解释本发明的原理、实际应用或在市场上找到的技术上的技术改进,或使得本领域普通技术人员能够理解本发明。
- 还没有人留言评论。精彩留言会获得点赞!