使用MDM2抑制剂和DNA甲基转移酶抑制剂的组合治疗方法与流程
本发明涉及治疗癌症的药物和方法,包括组合具有鼠双微体2(mdm2)抑制活性的化合物和dna甲基转移酶抑制剂。
背景技术:
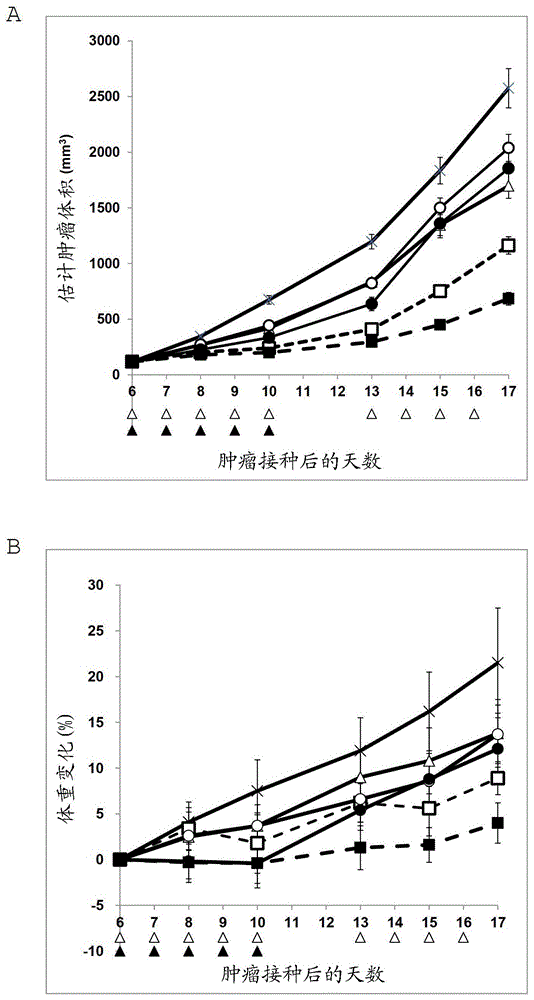
:已知p53是抑制细胞癌变的重要因子。p53是一种转录因子,其响应各种应激诱导参与细胞周期和细胞凋亡的基因的表达。p53被认为通过其转录调节功能抑制细胞的癌变。事实上,在约一半的人类癌症病例中观察到p53基因的缺失或突变。同时,已知鼠双微体2(mdm2)(一类e3泛素连接酶)的过表达是一种癌变因素。mdm2是一种蛋白质,其表达由p53诱导。mdm2通过以下方式来负调节p53:与p53的转录活性结构域结合从而降低p53的转录活性,将p53从细胞核中输出,并通过作为针对p53的泛素连接酶进一步介导p53的降解。因此,认为在mdm2过表达的细胞中促进p53的功能失活和p53的降解,导致癌变(非专利文献1)。关注mdm2的这种功能,已经尝试了许多使用抑制mdm2对p53功能的抑制的物质作为候选抗肿瘤剂的方法。已经报道了靶向mdm2-p53结合位点的mdm2抑制剂的实例,其包括螺羟吲哚衍生物(专利文献1至15和非专利文献1至3),吲哚衍生物(专利文献16),吡咯烷-2-甲酰胺衍生物(专利文献17),吡咯烷酮衍生物(专利文献18),异吲哚啉酮衍生物(专利文献19和非专利文献4)和二螺吡咯烷化合物(专利文献20)。近年来,表观基因组异常作为一种新的癌变机制受到关注。已经发现,除了dna序列异常之外,诸如dna高甲基化或组蛋白高度修饰(hypermodification)的表观基因组异常与肿瘤抑制基因的失活或致癌基因的异常活化密切相关。正在开发关注表观基因组异常的药物产品(表观基因组药物)(非专利文献5至7)。dna甲基转移酶是一种催化dna甲基化的酶。已经报道了各种肿瘤中dna甲基转移酶的异常活化,并且dna甲基转移酶是表观基因组药物的最知名的靶标之一。从很久以前就已知核苷类似物如阿扎胞苷和地西他滨作为合成核酸抑制剂。然而,后来发现这些药物通过抑制dna甲基转移酶将高度甲基化状态恢复到其正常状态。因此,阿扎胞苷在2004年和地西他滨在2006年被美国fda批准为表观基因组药物。还已经越来越多地研究了诸如阿扎胞苷和地西他滨的dna甲基转移酶抑制剂与其他抗癌剂的组合使用(非专利文献5)。引用列表专利文献专利文献1:wo2006/091646专利文献2:wo2006/136606专利文献3:wo2007/104664专利文献4:wo2007/104714专利文献5:wo2008/034736专利文献6:wo2008/036168专利文献7:wo2008/055812专利文献8:wo2008/141917专利文献9:wo2008/141975专利文献10:wo2009/077357专利文献11:wo2009/080488专利文献12:wo2010/084097专利文献13:wo2010/091979专利文献14:wo2010/094622专利文献15:wo2010/121995专利文献16:wo2008/119741专利文献17:wo2010/031713专利文献18:wo2010/028862专利文献19:wo2006/024837专利文献20:wo2012/121361专利文献21:wo2008/039218专利文献22:wo2013/059738非专利文献非专利文献1:j.am.chem.soc.,2005,127,10130-10131非专利文献2:j.med.chem.,2006,49,3432-3435非专利文献3:j.med.chem.,2009,52,7970-7973非专利文献4:j.med.chem.,2006,49,6209-6221非专利文献5:trendspharmacol.sci.,2010,31,536-546非专利文献6:drugdiscov.today,2011,16,418-425非专利文献7:cell.signal.,2011,23,1082-1093。发明概述技术问题本发明提供治疗癌症的药物和方法,其包括组合具有mdm2抑制活性的化合物和dna甲基转移酶抑制剂。本发明提供了用于治疗癌症的具有极高抗肿瘤效果的优异药物和方法。问题的解决方案作为广泛研究的结果,本发明人发现组合使用作为具有mdm2抑制活性的化合物的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐与作为dna甲基转移酶抑制剂的阿扎胞苷或地西他滨特别产生优异的抗肿瘤效果,并完成了本发明。具体而言,本发明涉及以下[1]至[22]:[1]一种用于癌症治疗的药物,其包含组合施用的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂。[2]根据[1]的药物,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和所述dna甲基转移酶抑制剂分别作为活性成分包含在不同的制剂中,并在相同时间或不同时间施用。[3]根据[1]的药物,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和所述dna甲基转移酶抑制剂包含在单一制剂中。[4]根据[1]的药物,其中所述药物是包含所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和所述dna甲基转移酶抑制剂的药盒制剂。[5]治疗癌症的方法,包括组合施用(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂。[6]根据[5]的治疗方法,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂分别作为活性成分包含在不同的制剂中,并在相同时间或不同时间施用。[7]根据[5]的治疗方法,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂包含在单一制剂中。[8]根据[5]的治疗方法,其中施用包含所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和所述dna甲基转移酶抑制剂的药盒制剂。[9]根据[1]至[4]中任一项的药物,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺的盐是对甲苯磺酸盐。[10]根据[5]至[8]中任一项的治疗方法,其中所述(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺的盐是对甲苯磺酸盐。[11]根据[1]至[4]和[9]中任一项的药物,其中所述dna甲基转移酶抑制剂是核酸衍生物。[12]根据[5]至[8]和[10]中任一项的治疗方法,其中所述dna甲基转移酶抑制剂是核酸衍生物。[13]根据[1]至[4]和[9]中任一项的药物,其中所述dna甲基转移酶抑制剂是阿扎胞苷或地西他滨。[14]根据[5]至[8]和[10]中任一项的治疗方法,其中所述dna甲基转移酶抑制剂是阿扎胞苷或地西他滨。[15]根据[1]至[4]、[9]、[11]和[13]中任一项的药物,其中所述癌症是血癌、脑肿瘤、头/颈部癌、食道癌、胃癌、阑尾癌、结肠癌、肛门癌、胆囊癌、胆管癌、胰腺癌、胃肠道间质瘤、肺癌、肝癌、间皮瘤、甲状腺癌、前列腺癌、神经内分泌肿瘤、黑色素瘤、乳腺癌、子宫内膜癌、宫颈癌、卵巢癌、骨肉瘤、软组织肉瘤、卡波西肉瘤、肌肉瘤、肾癌、膀胱癌或睾丸癌。[16]根据[5]至[8]、[10]、[12]和[14]中任一项的治疗方法,其中所述癌症是血癌、脑肿瘤、头/颈部癌、食道癌、胃癌、阑尾癌、结肠癌、肛门癌、胆囊癌、胆管癌、胰腺癌、胃肠道间质瘤、肺癌、肝癌、间皮瘤、甲状腺癌、前列腺癌、神经内分泌肿瘤、黑色素瘤、乳腺癌、子宫内膜癌、宫颈癌、卵巢癌、骨肉瘤、软组织肉瘤、卡波西肉瘤、肌肉瘤、肾癌、膀胱癌或睾丸癌。[17]根据[1]至[4]、[9]、[11]和[13]中任一项的药物,其中所述癌症是血癌。[18]根据[5]至[8]、[10]、[12]和[14]中任一项的治疗方法,其中所述癌症是血癌。[19]根据[17]的药物,其中所述血癌是慢性淋巴细胞白血病(cll)、小淋巴细胞淋巴瘤(sll)、高危cll、非cll/sll淋巴瘤、滤泡性淋巴瘤(fl)、弥漫性大b细胞淋巴瘤(dlbcl)、套细胞淋巴瘤(mcl)、华氏巨球蛋白血症(waldenstrom'smacroglobulinemia)、多发性骨髓瘤(mm)、边缘区淋巴瘤、伯基特淋巴瘤、非伯基特高级别b细胞淋巴瘤、结外边缘区b细胞淋巴瘤、急性或慢性髓性(髓细胞)白血病、骨髓增生异常综合征或急性成淋巴细胞性白血病。[20]根据[18]的治疗方法,其中所述血癌是慢性淋巴细胞白血病(cll)、小淋巴细胞淋巴瘤(sll)、高危cll、非cll/sll淋巴瘤、滤泡性淋巴瘤(fl)、弥漫性大b细胞淋巴瘤(dlbcl)、套细胞淋巴瘤(mcl)、华氏巨球蛋白血症(waldenstrom'smacroglobulinemia)、多发性骨髓瘤(mm)、边缘区淋巴瘤、伯基特淋巴瘤、非伯基特高级别b细胞淋巴瘤、结外边缘区b细胞淋巴瘤、急性或慢性髓性(髓细胞)白血病、骨髓增生异常综合征或急性成淋巴细胞性白血病。[21]根据[17]或[19]的药物,其中所述血癌是具有野生型tp53的癌症。[22]根据[18]或[20]的治疗方法,其中所述血癌是具有野生型tp53的癌症。发明的有益效果本发明可用作治疗癌症的方法和/或抗癌剂。附图简述[图1]图1是显示组合使用的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺对甲苯磺酸盐(化合物a)和阿扎胞苷对小鼠中来源于人急性髓性白血病细胞系molm-13的皮下移植细胞的肿瘤的体内效果(图1a)和通过它们的组合施用引起的体重变化(图1b)的图。符号×描绘未处理的对照组,符号空心圆描绘2.5mg/kg阿扎胞苷,符号实心圆描绘4mg/kg阿扎胞苷,符号空心三角形描绘25mg/kg化合物a,符号空心正方形描绘25mg/kg化合物a+2.5mg/kg阿扎胞苷,和符号实心正方形描绘25mg/kg化合物a+4mg/kg阿扎胞苷。横轴显示肿瘤接种后的天数。图1a的纵轴显示由肿瘤大小计算的估计肿瘤体积。图1b的纵轴显示相对于施用第一天的体重的体重变化%。横轴上的符号空心三角形描绘化合物a的施用日,和实心三角形描绘阿扎胞苷的施用日。误差条表示上图的se和下图的sd。[图2]图2是显示组合使用的化合物a和阿扎胞苷对小鼠中来源于人急性髓性白血病细胞系molm-13的皮下移植细胞的肿瘤的体内效果(图2a)和通过它们的组合施用引起的体重变化(图2b)的图。符号×描绘未处理的对照组,符号空心圆描绘2.5mg/kg阿扎胞苷,符号实心圆描绘4mg/kg阿扎胞苷,符号实心三角形描绘50mg/kg化合物a,符号空心正方形描绘50mg/kg化合物a+2.5mg/kg阿扎胞苷,和符号实心正方形描绘50mg/kg化合物a+4mg/kg阿扎胞苷。横轴显示肿瘤接种后的天数。图2a的纵轴显示由肿瘤大小计算的估计肿瘤体积。图2b的纵轴显示相对于施用第一天的体重的体重变化%。横轴上的符号空心三角形描绘化合物a的施用日,和实心三角形描绘阿扎胞苷的施用日。误差条表示上图的se和下图的sd。[图3]图3是显示组合使用的化合物a和地西他滨对小鼠中来源于人急性髓性白血病细胞系molm-13的皮下移植细胞的肿瘤的体内效果(图3a)和通过它们的组合施用引起的体重变化(图3b)的图。符号×描绘未处理的对照组,符号空心圆描绘50mg/kg地西他滨,符号实心圆描绘1mg/kg地西他滨,符号空心三角形描绘25mg/kg化合物a,符号空心正方形描绘25mg/kg化合物a+50mg/kg地西他滨,和符号实心正方形描绘25mg/kg化合物a+1mg/kg地西他滨。横轴显示肿瘤接种后的天数。图3a的纵轴显示由肿瘤大小计算的估计肿瘤体积。图3b的纵轴显示相对于施用第一天的体重的体重变化%。横轴上的符号空心三角形描绘化合物a的施用日,实心三角形描绘1mg/kg地西他滨的施用日,和空心长菱形描绘50mg/kg地西他滨的施用日。误差条表示上图的se和下图的sd。[图4]图4是显示组合使用的化合物a和地西他滨对小鼠中来源于人急性髓性白血病细胞系molm-13的皮下移植细胞的肿瘤的体内效果(图4a)和通过它们的组合施用引起的体重变化(图4b)的图。符号×描绘未处理的对照组,符号空心圆描绘50mg/kg地西他滨,符号实心圆描绘1mg/kg地西他滨,符号实心三角形描绘50mg/kg化合物a,符号空心正方形描绘50mg/kg化合物a+50mg/kg地西他滨,和符号实心正方形描绘50mg/kg化合物a+1mg/kg地西他滨。横轴显示肿瘤接种后的天数。图4a的纵轴显示由肿瘤大小计算的估计肿瘤体积。图4b的纵轴显示相对于施用第一天的体重的体重变化%。横轴上的符号空心三角形描绘化合物a的施用日,实心三角形描绘1mg/kg地西他滨的施用日,和空心长菱形描绘50mg/kg地西他滨的施用日。误差条表示上图的se和下图的sd。实施方案描述在本发明中,(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺(ds-3032)是wo2012/121361中的实施例70的化合物。该化合物可以通过wo2012/121361中描述的方法制备(wo2012/121361的全部内容通过引用并入本文)。哺乳动物基因组中的甲基化模式在生殖细胞或胚胎发育的初始阶段期间以及在细胞产生的蛋白质发生变化的发育阶段期间发生变化。总共存在3种类型的dna甲基转移酶:dnmt3a和dnmt3b作为在dna中建立新的甲基化模式的酶,和dnmt1作为在复制过程中将曾经建立的dna甲基化模式转移到下一代细胞的酶。在本发明中,dna甲基转移酶抑制剂可以抑制任一上述酶的活性或可以抑制所有酶的活性,并且不受其抑制方式的限制。dna甲基转移酶抑制剂主要分为核酸衍生物和非核酸抑制剂。核酸衍生物的实例包括但不限于阿扎胞苷、地西他滨、折布拉林(zebularine)、硫鸟嘌呤、5-氟-2'-脱氧胞苷和4'-硫代-2'-脱氧胞苷。非核酸抑制剂的实例包括但不限于mg98、egcg、psammaplins、普鲁卡因、普鲁卡因酰胺、肼苯哒嗪、rg108、小白菊内酯、姜黄素、光神霉素a、七尾霉素a和msc14778。这些dna甲基转移酶抑制剂可以作为市售产品容易地获得,或者可以由本领域技术人员参考本领域已知的文献等合成。用于本发明的dna甲基转移酶抑制剂特别优选阿扎胞苷或地西他滨。在本发明中,阿扎胞苷(4-氨基-1-β-d-呋喃核糖基-1,3,5-三嗪-2(1h)-酮)也称为5-氮杂胞苷,并且可称为vidaza(r)。阿扎胞苷可以作为市售产品容易地获得。在本发明中,地西他滨(4-氨基-1-(2-脱氧-β-d-赤式-呋喃戊糖基)-1,3,5-三嗪-2(1h)-酮)也称为5-氮杂-2'-脱氧胞苷并且可以称为dacogen(r)。地西他滨可以作为市售产品容易地获得。在本发明中,(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺和dna甲基转移酶抑制剂可以是各种药学上可接受的盐。盐的实例可包括:氢卤酸盐,如盐酸盐和氢碘酸盐;无机酸盐,如硝酸盐、高氯酸盐、硫酸盐和磷酸盐;低级烷磺酸盐,如甲磺酸盐、三氟甲磺酸盐和乙磺酸盐;芳基磺酸盐,如苯磺酸盐和对甲苯磺酸盐;有机酸盐,如甲酸盐、乙酸盐、苹果酸盐、富马酸盐、琥珀酸盐、柠檬酸盐、酒石酸盐、草酸盐和马来酸盐;氨基酸盐,如鸟氨酸盐、谷氨酸盐和天冬氨酸盐;碱金属盐,如钠盐、钾盐和锂盐;碱土金属盐,如钙盐和镁盐;无机盐,如铵盐;和有机胺盐,如二苄胺盐、吗啉盐、苯基甘氨酸烷基酯盐、乙二胺盐、n-甲基葡糖胺盐、二乙胺盐、三乙胺盐、环己胺盐、二环己胺盐、n,n'-二苄基乙二胺盐、二乙醇胺盐、n-苄基-n-(2-苯基乙氧基)胺盐、哌嗪盐、四甲基铵盐和三(羟甲基)氨基甲烷盐。(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺的盐优选是对甲苯磺酸盐。在本发明中,(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂可各自以游离形式或溶剂化物形式存在。所述化合物或其药学上可接受的盐和dna甲基转移酶抑制剂可各自例如通过吸收空气中的水分而以水合物形式存在。溶剂化物没有特别限制,只要它是药学上可接受的。具体地,溶剂化物优选为水合物、乙醇溶剂化物等。此外,可以使用n-氧化物形式。这些溶剂化物和n-氧化物形式也包括在本发明的范围内。(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂根据其结构可具有立体异构体。所述化合物或其药学上可接受的盐和dna甲基转移酶抑制剂也包括所有这些立体异构体和这些立体异构体的任何比率的混合物。立体异构体如在1996iupc,pureandappliedchemistry68,2193-2222中所定义的。当(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂各自以互变异构体形式存在时,这些互变异构体可以以平衡状态存在或可能主要存在某一形式。所有这些情况都包括在本发明的范围内。互变异构体是指由分子的一个原子的质子转移到另一个原子产生的异构体。(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂可各自为“药学上可接受的前药化合物”,所述药学上可接受的前药化合物由于在体内生理条件下由酶、胃酸等诱导的反应,通过酶促氧化、还原、水解等或通过胃酸等诱导的水解等转化为所需化合物。前药的实例包括通过酰化、烷基化或磷酸化获得的化合物。可以根据本领域已知的方法制备化合物的前药。此外,化合物的前药还包括那些在生理条件下转化成所需化合物的化合物,如"developmentofpharmaceuticalproducts",vol.7,moleculedesign,p.163-198,hirokawa-shotenltd.(1990)中所述。在本发明中,术语“肿瘤”和“癌症”可互换使用。此外,在本发明中,肿瘤、恶性肿瘤、癌症、恶性瘤、癌、肉瘤等可统称为“肿瘤”或“癌症”。此外,术语“肿瘤”和“癌症”还包括在某些情况下分类为癌变前期的病理状况,例如骨髓增生异常综合征。本发明的一个方面涉及包括组合施用的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂的药物或治疗方法。特别是,根据本发明,获得了优异的抗肿瘤效果。因此,本发明一方面涉及用于癌症治疗的药物或用于治疗癌症的方法,包括组合施用的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂。在本发明中,“组合施用”的(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂是基于两种药物组合施用的假设。在本发明中,“组合施用”(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂是指两种药物经给定的时段掺入接受者体内。可以施用在单一制剂中含有两种药物的制剂,或者可以将药物制成单独的制剂并分别施用。在制备单独的制剂的情况下,其施用时间没有特别限制。可以同时施用单独的制剂,或者可以在不同的时间或以交错的方式在不同日期施用。在不同时间或不同日期施用(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂的情况下,其施用顺序没有特别限制。通常,这些制剂根据它们各自的施用方法施用。因此,这些制剂可以以相同的剂数施用,或者可以以不同的剂数施用。此外,在制备单独的制剂的情况下,制剂的各自的施用方法(施用途径)可以彼此相同,或者这些制剂可以通过不同的施用方法(施用途径)施用。两种药物不必同时存在于体内,并且可以经给定的时段(例如,1个月,优选1周,更优选数天,甚至更优选1天)掺入体内。在施用另一种活性成分时,一种活性成分可能已从体内消失。本发明的药物剂型的实例包括1)施用包含(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂的单一制剂,2)通过相同施用途径同时施用两种由(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂分别制备的制剂,3)通过相同施用途径以交错方式施用两种由(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂分别制备的制剂,4)通过不同施用途径同时施用两种由(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂分别制备的制剂,和5)通过不同施用途径以交错方式施用两种由(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和dna甲基转移酶抑制剂分别制备的制剂。在本发明中,两种不同的制剂可以是包含这些制剂的药盒的形式。根据本发明的药物可含有(3'r,4's,5'r)-n-[(3r,6s)-6-氨基甲酰基四氢-2h-吡喃-3-基]-6"-氯-4'-(2-氯-3-氟吡啶-4-基)-4,4-二甲基-2"-氧代-1",2"-二氢二螺[环己烷-1,2'-吡咯烷-3',3"-吲哚]-5'-甲酰胺或其药学上可接受的盐和/或dna甲基转移酶抑制剂和药学上可接受的载体,并且可以作为各种注射剂如静脉内注射剂、肌内注射剂和皮下注射剂施用,或通过各种方法如口服施用或经皮施用来施用。药学上可接受的载体是指涉及从给定器官向另一器官运输组合物的药理学上可接受的物质(例如,赋形剂、稀释剂、添加剂和溶剂)。制剂可以通过根据施用方法选择合适的制剂形式(例如口服制剂或注射剂)和使用常规用于制备制剂的各种方法来制备。口服制剂的实例可包括片剂、粉剂、颗粒剂、胶囊剂、丸剂、锭剂、溶液剂、糖浆剂、酏剂、乳剂和油性或水性混悬剂。在口服施用中,可以使用游离化合物或盐形式。水性制剂可通过与药理学上可接受的酸形成酸加合物或通过形成碱金属盐如钠盐来制备。对于注射剂,可以在制剂中使用稳定剂、防腐剂、溶解助剂等。在容器中填充可以含有这些助剂等的溶液后,可以通过冻干等将使用的制剂制备为固体制剂。此外,可以在一个容器中填充一个剂量,或者可以在一个容器中填充两个或更多个剂量。固体制剂的实例包括片剂、粉剂、颗粒剂、胶囊剂、丸剂和锭剂。这些固体制剂可含有药学上可接受的添加剂和本发明化合物。添加剂的实例包括填料、填充剂、粘合剂、崩解剂、溶解促进剂、皮肤润湿剂和润滑剂。可以根据需要选择和混合这些添加剂以制备制剂。液体制剂的实例包括溶液剂、糖浆剂、酏剂、乳剂和混悬剂。添加剂的实例包括悬浮剂和乳化剂。可以根据需要选择和混合这些添加剂以制备制剂。药用物质的实例可包括但不限于:氨基酸,例如甘氨酸、丙氨酸、谷氨酰胺、天冬酰胺、精氨酸和赖氨酸;抗微生物剂;抗氧化剂,例如抗坏血酸、硫酸钠和亚硫酸氢钠;缓冲剂,例如磷酸盐、柠檬酸盐或硼酸盐缓冲剂,碳酸氢钠和tris-hcl溶液;填料,例如甘露醇和甘氨酸;螯合剂,例如乙二胺四乙酸(edta);络合剂,例如咖啡因、聚乙烯吡咯烷、β-环糊精和羟丙基-β-环糊精;填充剂,例如葡萄糖、甘露糖和糊精;其他碳水化合物,例如单糖和二糖;着色剂;矫味剂;稀释剂;乳化剂;亲水性聚合物,例如聚乙烯吡咯烷;低分子量多肽;成盐抗衡离子;杀菌剂,例如苯扎氯铵、苯甲酸、水杨酸、硫柳汞、苯乙醇、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、氯己定、山梨酸和过氧化氢;溶剂,例如甘油、丙二醇和聚乙二醇;糖醇,例如甘露醇和山梨糖醇;悬浮剂;表面活性剂,例如脱水山梨糖醇酯、聚山梨醇酯如聚山梨醇酯20和聚山梨醇酯80、triton、氨丁三醇、卵磷脂和胆固醇;稳定性增强剂,例如蔗糖和山梨糖醇;弹性增强剂,例如氯化钠、氯化钾、甘露醇和山梨糖醇;转运剂(transportagent);赋形剂;和/或药物助剂。这些药用物质的添加量优选为药物重量的0.01至100倍,特别是0.1至10倍。制剂中优选的药物组合物的配方可由本领域技术人员根据适用的疾病、适用的施用途径等适当地确定。药物组合物中的赋形剂或载体可以是液体或固体。合适的赋形剂或载体可以是通常用于注射用水、生理盐水、人造脑脊髓液和肠胃外施用的其他物质。中性生理盐水或含有血清白蛋白的生理盐水可用作载体。药物组合物可含有ph7.0至8.5的tris缓冲剂,ph4.0至5.5的乙酸盐缓冲剂,或ph3.0至6.2的柠檬酸盐缓冲剂。这些缓冲剂还可含有山梨糖醇或其他化合物。阿扎胞苷制剂的优选实例包括但不限于补充有d-甘露醇的可注射冻干制剂。地西他滨制剂的优选实例包括但不限于含有磷酸二氢钾和氯化钠作为添加剂的可注射冻干制剂。本发明的药物可用于哺乳动物,特别是人类的癌症治疗。根据医生的判断,可以根据疾病的部位,患者的身高、体重、性别或病史来适当地选择本发明的药物的剂量和施用间隔。当向人施用本发明的药物时,相对于一种活性成分类型,剂量范围为每天约0.01至500mg/kg体重,优选约0.1至100mg/kg体重。优选地,每天一次向人施用本发明的活性成分,或者将剂量分成二至四次,并以适当的间隔重复施用。此外,如有必要,每日剂量可由医生自行决定超过上述剂量。通过皮下施用每天一次持续7天,或者通过经10分钟静脉内输注然后休药3周,以75mg/m2(体表面积)向成人施用阿扎胞苷。以该操作作为一个循环重复施用的方法是优选的实例。剂量可以根据患者的状态适当地增加或减少。通过每8小时连续静脉内输注(经3小时),以15mg/m2(体表面积)的单剂量向成人施用地西他滨,并且该施用连续进行3天。每6周重复该施用循环的方法,以及通过经1小时或更长时间的连续静脉内输注每天一次连续5天施用20mg/m2地西他滨,然后休药23天,并重复以该操作为一个循环的施用的方法是优选的实例。剂量可以根据患者的状态适当地增加或减少。待治疗的癌症类型没有特别限制,只要确认癌症对本发明的组合使用进行的治疗敏感即可。其实例包括血癌、脑肿瘤、头/颈部癌、食道癌、胃癌、阑尾癌、结肠癌、肛门癌、胆囊癌、胆管癌、胰腺癌、胃肠道间质瘤、肺癌、肝癌、间皮瘤、甲状腺癌、肾癌、前列腺癌、神经内分泌肿瘤、黑色素瘤、乳腺癌、子宫内膜癌、宫颈癌、卵巢癌、骨肉瘤、软组织肉瘤、卡波西肉瘤、肌肉瘤、膀胱癌和睾丸癌。其中,血癌是优选的。血癌的实例包括慢性淋巴细胞白血病(cll)、小淋巴细胞淋巴瘤(sll)、高危cll、非cll/sll淋巴瘤、滤泡性淋巴瘤(fl)、弥漫性大b细胞淋巴瘤(dlbcl)、套细胞淋巴瘤(mcl)、华氏巨球蛋白血症(waldenstrom'smacroglobulinemia)、多发性骨髓瘤(mm)、边缘区淋巴瘤、伯基特淋巴瘤、非伯基特高级别b细胞淋巴瘤、结外边缘区b细胞淋巴瘤、急性或慢性髓性(髓细胞)白血病、骨髓增生异常综合征和急性成淋巴细胞性白血病。其特别优选的实例包括急性髓性白血病和骨髓增生异常综合征。从另一个观点来看,待治疗的癌症类型优选对mdm2抑制剂敏感的癌症,更优选具有野生型tp53的癌症。用于确认tp53为野生型的方法的实例包括使用对突变的dna序列具有特异性的探针的微阵列方法(amplichipp53,rochemolecularsystems,inc.,etc.,http://www.ncbi.nlm.nih.gov/pubmed/21319261),使用对突变的dna序列具有特异性的探针的pcr(qbiomarkersomaticmutationpcrarrays,qiagenn.v.,etc.),使用sanger测序仪读取p53基因序列的方法(http://p53.iarc.fr/download/tp53_directsequencing_iarc.pdf),以及使用下一代测序仪读取p53基因序列的方法(truseqamplicon-cancerpanel,illuminahttp://www.illuminakk.co.jp/products/truseq_amplicon_cancer_panel.ilmn,oncomine(r)cancerresearchpanel,lifetechnologiescorp.,http://www.lifetechnologies.com/jp/ja/home/clinical/preclinical-companion-diagnostic-development/oncomine-cancer-research-panel-workflow.html,etc.)。根据本发明的药物可以与另外的抗肿瘤剂组合使用。其实例包括抗肿瘤抗生素、抗肿瘤植物成分、brm(生物反应调节剂)、激素、维生素、抗肿瘤抗体、分子靶向药物、烷化剂、代谢拮抗剂和其他抗肿瘤剂。更具体地,烷化剂的实例包括:烷化剂,例如氮芥、氮芥n-氧化物、苯达莫司汀和苯丁酸氮芥;氮杂环丙烷烷化剂,例如卡波醌和噻替派;环氧化物烷化剂,例如二溴甘露醇和二溴卫矛醇;亚硝基脲烷化剂,例如卡莫司汀、洛莫司汀、司莫司汀、盐酸尼莫司汀、链脲霉素、氯脲霉素和雷莫司汀;和白消安、二丙胺磺酯(improsulfantosylate)、替莫唑胺和达卡巴嗪。代谢拮抗剂的各种实例包括:嘌呤代谢拮抗剂,例如6-巯基嘌呤,6-硫鸟嘌呤和硫肌苷;嘧啶代谢拮抗剂,例如氟尿嘧啶、替加氟、替加氟-尿嘧啶、卡莫氟、去氧氟尿苷、溴尿苷、阿糖胞苷和依诺他滨;和叶酸代谢拮抗剂,例如甲氨蝶呤和三甲曲沙。抗肿瘤抗生素的实例包括:丝裂霉素c、博来霉素、培洛霉素、柔红霉素、阿柔比星、多柔比星、伊达比星、吡柔比星、thp-阿霉素、4'-表阿霉素和表柔比星;和色霉素a3和放线菌素d。抗肿瘤植物成分及其衍生物的实例包括:长春花生物碱,例如长春地辛、长春新碱和长春碱;紫杉烷,例如紫杉醇、多西紫杉醇和卡巴他赛;和表鬼臼毒素,例如依托泊苷和替尼泊苷。brm的实例包括肿瘤坏死因子和吲哚美辛。激素的实例包括氢化可的松、地塞米松、甲基强的松龙、强的松龙、普拉睾酮(prasterone)、倍他米松、去炎松、康复龙、诺龙、美替诺龙、磷雌酚、炔雌醇、氯地孕酮、美雄烷和甲羟孕酮。维生素的实例包括维生素c和维生素a。抗肿瘤抗体和分子靶向药物的实例包括曲妥珠单抗、利妥昔单抗、西妥昔单抗、尼妥珠单抗、地诺单抗、贝伐单抗、英夫利昔、伊匹单抗、纳武单抗(nivolumab)、派姆单抗(pembrolizumab)、阿维单抗(avelumab)、皮地珠单抗(pidilizumab)、阿特珠单抗(atezolizumab)、雷莫芦单抗、伊马替尼甲磺酸盐、达沙替尼、吉非替尼、埃罗替尼、奥希替尼、舒尼替尼、拉帕替尼、达拉非尼、曲美替尼、考比替尼、帕唑帕尼、帕博西尼、帕比司他、索拉非尼、克唑替尼、维莫非尼、奎扎替尼、硼替佐米、卡非佐米、伊莎佐米(ixazomib)、midosutaurin和吉列替尼(gilteritinib)。其它抗肿瘤剂的实例包括顺铂、卡铂、奥沙利铂、它莫西芬、来曲唑、阿那曲唑、依西美坦、托瑞米芬柠檬酸盐、氟维司群、比卡鲁胺、氟他胺、米托坦、亮丙瑞林、戈舍瑞林乙酸盐、喜树碱、异环磷酰胺、环磷酰胺、美法仑、l-天门冬酰胺酶、醋葡醛内酯(aceglatone)、西佐喃(sizofiran)、溶链菌制剂(picibanil)、丙卡巴肼、哌泊溴烷(pipobroman)、新制癌菌素、羟基脲、乌苯美司、沙利度胺、来那度胺、泊马度胺、艾瑞布林、维甲酸和云芝多糖。实施例在下文中,将参考下面给出的实施例具体说明本发明。然而,本发明不限于这些实施例,并且它们不应以任何限制性方式解释。(试验例1:化合物a和阿扎胞苷组合使用的体内效果的研究)使用磷酸盐缓冲盐水将人急性髓性白血病细胞系molm-13细胞悬浮至5×107个细胞/ml。将0.1ml制备的细胞悬液皮下移植到每只nod-scid小鼠(雄性,6周龄)。在肿瘤接种后6天,在确认平均肿瘤体积超过100mm3后,基于其肿瘤体积值对小鼠进行分组。通过强制施用于小鼠来口服施用25mg/kg或50mg/kg化合物a。将2.5mg/kg或4mg/kg阿扎胞苷静脉内施用于小鼠尾巴。对于组合使用组,相继施用25mg/kg或50mg/kg化合物a和2.5mg/kg或4mg/kg阿扎胞苷。从分组日(肿瘤接种后6天)开始,每天一次进行化合物a的施用连续5天(肿瘤接种后6至10天),并且在休药2天后,每天一次进行化合物a的施用连续4天(肿瘤接种后13至16天)。从分组日(肿瘤接种后6天)开始,每天一次进行阿扎胞苷的施用连续5天(肿瘤接种后6至10天)。使用电子数字卡尺随时间测量肿瘤的长轴(mm)和短轴(mm)。根据下面所示的计算公式(4)计算的评估日(肿瘤接种后17天)的肿瘤生长抑制%(tgi%)用于评价。此外,使用用于小动物的自动天平随时间测量体重,并且根据下面所示的计算公式(5)计算体重变化%,以研究药物施用对体重的影响。此外,最后一次体重测量的结果用于剂量计算。tgi(%)=(1-a/b)×100...(4)a:评估日化合物施用组的平均肿瘤体积(*)b:评估日未处理对照组的平均肿瘤体积(*)*:根据1/2×[肿瘤长轴]×[肿瘤短轴]×[肿瘤短轴]计算肿瘤体积。体重变化(%)=个体的平均体重变化%...(5)每个个体的体重变化%=(1-bwn/bws)×100bwn:第n日的体重bws:施用起始日的体重。结果显示在图1和2以及表1至3中。[表1]组tgi(%)化合物a25mg/kg34化合物a50mg/kg72化合物a25mg/kg+阿扎胞苷2.5mg/kg55化合物a50mg/kg+阿扎胞苷2.5mg/kg90化合物a25mg/kg+阿扎胞苷4mg/kg73化合物a50mg/kg+阿扎胞苷4mg/kg91阿扎胞苷2.5mg/kg21阿扎胞苷4mg/kg28估计肿瘤体积(mm3)。[表2]体重变化(%)。[表3](试验例2:化合物a和地西他滨组合使用的体内效果的研究)使用磷酸盐缓冲盐水将人急性髓性白血病细胞系molm-13细胞悬浮至5×107个细胞/ml。将0.1ml制备的细胞悬液皮下移植到每只nod-scid小鼠(雄性,6周龄)。在肿瘤接种后6天,在确认平均肿瘤体积超过100mm3后,基于其肿瘤体积值对小鼠进行分组。通过强制施用于小鼠来口服施用25mg/kg或50mg/kg化合物a。将1mg/kg或50mg/kg地西他滨静脉内施用于小鼠尾巴。对于组合使用组,相继施用25mg/kg或50mg/kg化合物a和1mg/kg或50mg/kg地西他滨。从分组日(肿瘤接种后6天)开始,每天一次进行化合物a的施用连续5天(肿瘤接种后6至10天),并且在休药2天后,每天一次进行化合物a的施用连续4天(肿瘤接种后13至16天)。在分组日(肿瘤接种后6天)对50mg/kg组进行地西他滨的施用,并且从分组日(肿瘤接种后6天)开始,对1mg/kg组进行地西他滨的施用,每天一次,连续5天(肿瘤接种后6-10天)。使用电子数字卡尺随时间测量肿瘤的长轴(mm)和短轴(mm)。根据下面所示的计算公式(4)计算的评估日(肿瘤接种后17天)的肿瘤生长抑制%(tgi%)用于评价。此外,使用用于小动物的自动天平随时间测量体重,并且根据下面所示的计算公式(5)计算体重变化%,以研究药物施用对体重的影响。此外,最后一次体重测量的结果用于剂量计算。tgi(%)=(1-a/b)×100...(4)a:评估日化合物施用组的平均肿瘤体积(*)b:评估日未处理对照组的平均肿瘤体积(*)*:根据1/2×[肿瘤长轴]×[肿瘤短轴]×[肿瘤短轴]计算肿瘤体积。体重变化(%)=个体的平均体重变化%...(5)每个个体的体重变化%=(1-bwn/bws)×100bwn:第n日的体重bws:施用起始日的体重。结果显示在图3和4以及表4至6中。[表4]组tgi(%)化合物a25mg/kg22化合物a50mg/kg76化合物a25mg/kg+地西他滨50mg/kg52化合物a50mg/kg+地西他滨50mg/kg83化合物a25mg/kg+地西他滨1mg/kg70化合物a50mg/kg+地西他滨1mg/kg94地西他滨50mg/kg14地西他滨1mg/kg38估计肿瘤体积(mm3)。[表5]体重变化(%)。[表6]当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种新的多肽——dna甲基化酶13和编码这种多肽的多核苷酸的制作方法
- 具有治疗活性的环亚甲基-1,2-二羧酸酰胺,制备它们的方法和含它们的药物组合物的制作方法
- 组蛋白去乙酰化酶抑制剂的制作方法
- 基于dna聚合酶链反应的甲基化dna检测方法
- 检测Cre位点特异重组酶活性的转基因报告猪及培养方法
- 一种多肽——人含胞嘧啶特异性dna甲基化酶特征性序列片段的蛋白-9.35和编码这种 ...的制作方法
- 一种多肽——脱氧核糖核酸甲基化酶-9.35和编码这种多肽的多核苷酸的制作方法
- 利用酶活性的竞争性干扰和恢复检测被分析物的制作方法
- 一种基于化学发光反应的甲基化酶检测探针、检测试剂盒及检测方法
- 编码甲基化儿茶素生物合成酶的基因的制作方法