糖基二硫代氨基甲酸盐、其制备方法和应用与流程
本发明涉及一种糖基二硫代氨基甲酸盐的制备方法及其应用。
背景技术:
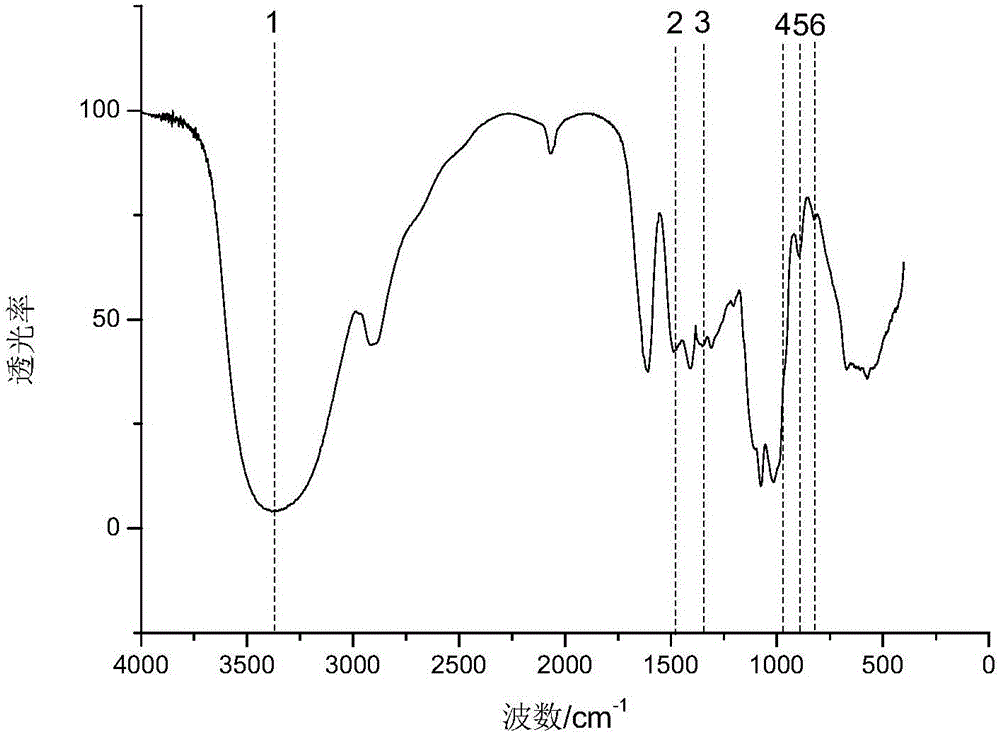
:糖类在生物体的重要功能随着生命科学的不断发展逐渐得到了广泛认可,其在生物体的功能不仅仅局限于结构物质、能量物质,它在细胞黏着与接触抑制、机体免疫保护,代谢调控,受精机制,形态发生、发育、癌变、衰老、器官移植等方面的作用逐渐被发现,在构建极其复杂的多细胞器官和生物体中发挥重要作用,机体的功能蛋白绝大多数在合成后都需要进行糖基化修饰。糖类与蛋白的特异性结合是糖生物学和糖组学的主要研究目标之一,利用糖和蛋白结合的特异性,可以将不同的糖固定在传感器表面,用于识别不同的蛋白质。近年来,由于临床诊断、环境保护、食品和医药等领域发展的实际需求,在分析过程中越来越多地需要对被分析物进行快速、在线、痕量的分析和监测。生物化学传感器作为生物技术自动化的基础,具有样品需求量小、样品可回收、重复性好、分析速度快、灵敏度高以及选择性好等优点,引起了广泛的关注。生物化学传感器是能将待测生物、化学信息按一定规律转换成可用信号(光、电信号等)输出的器件或装置。生化传感器技术融合了生物、化学、物理、医学、微纳科学、电子技术和信息科学等多门学科,是一项综合性的高新技术。生物化学识别系统作为生物化学传感器的核心,是基于生物分子的识别,设计出的某种能产生和传递特定信息的分子器件。生物化学识别系统通常涉及到待测生物或化学分子与贵金属芯片表面的特异性结合,实现光、电等物理信号的变化,从而达到对生物化学分子特异性的定量检测。通常是将生物分子例如抗体或抗原固定在传感器的表面,用于捕捉和检测目标分子。因此,通过特定的生物或化学手段对传感器表面进行修饰,使得生物或化学分子在传感器表面固定,从而实现识别的特异性是构建生物传感器识别系统的关键步骤之一。固定在传感器表面的生物化学分子应保持全活性并且有序地与待测分子接触,以实现传感器灵敏度和可重复性的最大化。通过制备自组装单分子层,将特定的分子固定在传感器表面,用于检测目标分子,简单可控,可重复性好,受到人们越来越多的关注。自组装单分子层指在稀溶液中反应性分子自发吸附到固体底物表面形成的致密有序单层膜,其基本原理是利用固-液界面间的化学作用力,使得分子自发吸附在固-液界面形成热力学稳定、结构致密、空间有序的单层膜。这种单层膜包括三个部分:一是分子的头基,它与基底表面反应点以离子键、共价键等结合;二是烷基链或其衍生物部分,是功能分子的中间部分,依靠分子链间的范德华力,使活性分子排列形成紧密有序的结构;三是分子末端基团,如巯基、羟基、氨基、卤原子等,组装不同末端基团的功能分子,所形成的自组装单分子层将具有不同的生物化学性质。通过设计自组装单分子层成膜分子的组成和结构,达到精确的化学控制,获得特定功能表面。自组装单分子膜按化学结构来分主要有六类,分别是硫醇类、有机硅烷类、脂肪酸类、磷脂类、咪唑类和希夫碱类。其中硫醇烷烃类自组装单分子膜是基于巯基与基底表面原子(金原子)的化学吸附和亚甲基链在范德华力诱导下的定向排列,从而形成的一类结合非常稳固和有序的单分子层,具有成膜条件易控,膜取向性好、排列紧密,有序稳定,组装界面功能化等优点,是目前金表面修饰与制备最主要的手段。然而硫醇类自组装膜在热、紫外线、其他硫醇和氧化剂等存在的条件下会发生脱吸附。技术实现要素:本发明旨在提供一种新的功能化糖,该功能化修饰的糖可以通过自组装固定在贵金属传感器表面,用于特异性识别蛋白,达到定量检测目标蛋白质的目的。本发明通过提供一种糖基二硫代氨基甲酸盐来实现上述目的。本发明所述的糖基二硫代氨基甲酸盐具有通式I的结构:通式I中,R为糖基;M+选自碱金属离子和铵根离子。进一步地,本发明的目的还在于提供上述糖基二硫代氨基甲酸盐的制备方法,包括如下步骤:(1)式II的化合物与碳酸铵按摩尔比1:1~3在低碳醇中于45~75℃条件下形成悬浮液,缓慢加入氨水至完全溶解,反应2~72h小时制备式III的化合物;(2)式III的化合物与碱和二硫化碳按摩尔比1:1~1.5:1~3在低碳醇/水体系中于45~75℃条件下反应2~72h制备式I的化合物。本发明再一方面的目的,在于提供上述糖基二硫代氨基甲酸盐在表面处理领域的应用,尤其是用于生物传感领域元器件的表面功能化处理。本发明进一步提供材料表面糖基化的方法,是将贵金属表面与上述本发明的糖基二硫代氨基甲酸盐的水溶液接触,于4~30℃条件下保持2~72h。当然,本发明也旨在提供经上述表面糖基化处方法处理后的材料、以及使用处理后的材料所制备的产品。本发明所提供的糖基二硫代氨基甲酸盐用于自组装程序修饰获得的表面糖基化材料在蛋白质水平有良好的的糖生物活性,实现特异性识别。所述材料的制备方法采用天然糖作为糖基化底物,方法简单、条件温和、可操作性强、重现性高、适用性广。附图说明本发明附图5幅,图1是化合物iii的紫外-可见吸收光谱;图2是化合物iii的透射红外谱图;图3是实施例2中表面糖基化的金芯片的自组装膜的射线光电子能谱;图4是实施例3糖基化的金表面的蛋白特异性吸附实验结果;图5是实施例5糖基化的金表面的蛋白特异性吸附实验结果。具体实施方式本发明公开一种糖基二硫代氨基甲酸盐,具有通式I的结构:通式I中,R为糖基;M+选自碱金属离子和铵根离子(NH4+)。具体实施方式中,所述及的碱金属离子包括但不限于Na+、K+。尤其优选Na+。通式I中,所述的R是糖基,根据本领域惯用的表达方式,可以表示为式i的结构。应当明确,该表述仅为了便于描述,该式i对R为糖基的选择并未限定作用。具体实施方式之一,本发明中所述的R是单糖基或寡糖基。包括但不限于葡萄糖基、果糖基、核糖基、半乳糖基、甘露糖基、乳糖基、阿拉伯糖基、N-乙酰氨基葡萄糖基等。本发明再一方面提供上述本发明的糖基二硫代氨基甲酸盐的制备方法,包括如下步骤:(1)式II的化合物与碳酸铵(NH4)2CO3按摩尔比1:1~3在低碳醇中于45~75℃条件下形成悬浮液,缓慢加入氨水至完全溶解,反应2~72h小时制备式III的化合物(1-氨基糖);(2)式III的化合物(1-氨基糖)与碱和二硫化碳按摩尔比1:1~1.5:1~3在低碳醇/水体系中于45~75℃条件下反应2~72h制备式I的化合物。上文所述及的C1-4低碳醇按照本领域通常的方式理解,包括碳原子数为1~4的直链或支链的低级醇,包括但不限于甲醇、乙醇、丙醇、异丙醇、丁醇、异丁醇、正丁醇。作为优选的实施方式,上述制备方法步骤(1)中,所述的式II的化合物与碳酸铵摩尔比为1:1~3,优选1:1;所述的反应温度优选45℃~60℃;所述的反应时间优选12小时;所述的低碳醇选自甲醇、乙醇、丙醇、异丙醇、丁醇,优选甲醇或乙醇。另一优选的实施方式,上述制备方法步骤(2)中,所述的式III的化合物(1-氨基糖)与碱、二硫化碳的摩尔比优选1:1:1。其中,低碳醇/水体系选自由甲醇、乙醇、丙醇、异丙醇、丁醇与水所组成的混合体系;优选甲醇或乙醇与水所组成的混合体系;尤其优选甲醇/水体系,最优选水:甲醇(v/v)=1:8的体系。所述的碱选自氢氧化钠、氢氧化钾、氨水、碳酸钠、碳酸氢钠;优选氢氧化钠和氢氧化钾。所述的反应温度优选60℃~70℃。所述的反应时间优选12小时。二硫代氨基甲酸盐(酯)是一类用途极其广泛的化合物,作为一种螯合配体广泛应用配位化学领域。相对于烷基硫醇类,二硫代氨基甲酸盐与贵金属的结合具有更加优良的化学吸附属性,耐氧化性更加优良,并且不易被其他极性硫醇化合物置换,因而可作为一种更加优良的贵金属表面修饰方法。二硫代氨基甲酸盐最主要的结构特点在于氮原子和硫原子上具有自由电子对,使得碳氮键和硫碳键形成共振结构。室温下二硫化碳能与含有氨基的化合物反应,在贵金属表面上形成二硫代氨基甲酸盐,因而含有氨基的化合物通过二硫化碳处理后即可固定在贵金属表面。基于此,本发明公开上述糖基二硫代氨基甲酸盐在表面改性,尤其是贵金属表面改性中的应用。具体方式之一,是一种材料表面糖基化的方法,该方法将材料表面与权利要求1的糖基二硫代氨基甲酸盐的水溶液接触,于4~30℃条件下保持2~72h。其中所述的材料优选贵金属。当然,也包括局部是贵金属材料的元器件产品。材料表面糖基化的方法中,所述贵金属包括但不限于金、银、钛和铜,尤其优选金和银。所述的糖基二硫代氨基甲酸盐的水溶液的浓度是1~5mmol/L,优选2mmol/L。所述的温度优选25±2℃;保持时间优选12h。经糖基化处理的贵金属材料,以金为例,糖基二硫代氨基甲酸盐通过二硫代氨基甲酸结构在贵金属表面形成配位键,形成自组装膜。其结构如式IV所示:具体实施方式的另一方面,是提供各种元器件,所述元器件具有全部或局部的表面,是经过上述本发明的方法进行表面糖基化处理的材料。本发明公开上述表面糖基化方法及产品在生物传感领域的应用。并通过表面等离子体共振仪测定了糖表面与花生凝集素(PNA)、刀豆素(ConA)以及牛血清蛋白(BSA)的特异性结合。利用糖与蛋白的特异性识别,达到目标蛋白检测的目的。以下具体实施例为进一步说明本发明,不应当理解为对本发明的任何形式的限定。实施例1化合物iii(葡萄糖基二硫代氨基甲酸盐)的制备,包括以下步骤:(1)葡萄糖(i)与碳酸铵按照摩尔比1:1加入甲醇中形成悬浮液,升温至46℃,缓慢加入氨水至全溶,继续在46℃的条件下反应12h,产物结晶洗出制备1-氨基1-脱氧葡萄糖(ii)。(2)化合物ii与二硫化碳,氢氧化钠按照摩尔比1:1:1加入甲醇中(氢氧化钠需事先配成5mol/L溶液),在46℃条件下反应12h,加入乙醇使产物析出制备化合物iii,总收率为60.7%。化合物iii采用紫外-可见光谱进行表征,紫外-可见光谱见图1,252nm处为N-C-S基团的π-π*跃迁,296nm处为S-C-S中硫原子上非键电子向共轭体系的n-π*跃迁。化合物iii采用透射红外进行表征,红外光谱见图2,特征峰归属见表1。13CNMR(100MHzD2O):δ163.1(C=S),δ95.8(CHNH),δ60.8(CH2OH),δ69.7~76.6(otherCHOH).MS(EI-):m/z[M]-254.04.表1.化合物iii透射红外特征峰编号波数(cm-1)特征峰归属13450O-H伸缩振动峰21498C-N伸缩振动峰31350C=N伸缩振动峰,共振结构4950C=S伸缩振动峰5890β构型糖苷键C-H弯曲振动峰6830α构型糖苷键C-H弯曲振动峰实施例2制备表面糖基化的金芯片。(1)制备母液:以去离子水为溶剂,充分溶解实施例1所制备的化合物iii,制得浓度为2mmol/L的自组装母液;(2)将金芯片浸泡于步骤(1)所制得的自组装母液中,于25℃条件下静置24小时;(3)所得的处理后的金芯片以乙醇冲洗,氮气吹干,避光保存。对上述制备的表面糖基化的金芯片采用X射线光电子能谱进行表征,X射线光电子能谱见图3(a),其元素比例见表2所示。未经自组装修饰的裸金表面仅检测出少量碳元素,可以归属为表面存在的少量有机沾污。经上述葡萄糖基二硫代氨基甲酸盐自组装后,表面Au元素含量明显降低,表明金芯片表面自组装有机膜的形成。所述的自组装有机膜结构中S/N比接近于2,表明表面二硫代氨基甲酸盐结构的存在。S/N比小于2是由于硫原子存在于自组装膜结构的最下层,其信号强度受到表层原子的遮蔽效应而降低。自组装膜结构中的C/N比接近于7/5,与葡萄糖基二硫代氨基甲酸盐结构中的糖结构相符。高分辨C1s谱图被用以分析上述自组装膜结构中的的有机层,结果见图3(b)。自组装膜的高分辨C1s谱图中在286.2eV附近出现明显峰,可以归属为糖分子中连接羟基和氨基的碳原子。288.2eV附近出现较弱的峰,可以归属为DTC结构中碳原子。该结果表明自组装膜结构中存在糖分子和DTC结构,表明我们通过葡萄糖基二硫代氨基甲酸盐分子自组装成功构筑了糖表面。高分辨S2p谱图见图3(c),在162.0eV附近出现含硫化合物自组装膜的经典双峰,两个峰面积比接近1:2,表明自组装结构的存在。然而该双峰的结合能差比经典硫醇自组装结构小约0.2eV,表明该自组装结构中硫原子比硫醇中的硫原子具有更多负电荷,这是由于DTC结构中共振结构造成的。高分辨N1s谱图见图3(d),与高分辨C1s、S2p谱图相符,经过自组装修饰的表面出现明显的N元素谱峰,可以归属为二硫代氨基甲酸盐结构中的N原子。综上,XPS表征结果表明,通过葡萄糖基二硫代氨基甲酸盐在金表面自组装,我们成功构筑了含有DTC结构的糖表面。表2糖基二硫代氨基甲酸盐SAM元素比例AuCONS裸金81.918.1__*__*__*SAM24.342.127.52.23.9*未检出。实施例3葡萄糖基化的金芯片的生物活性测试。按照实施例2中的方法对SPR芯片进行葡萄糖糖基化处理。将反应后的芯片置于表面等离子共振(SPR)系统中,分别通入伴刀豆球蛋白(ConA)、花生凝集素(PNA)、牛血清蛋白(BSA),发现与葡萄糖基二硫代氨基甲酸盐反应的芯片特异性结合伴刀豆球蛋白。结果如附图4所示,表明葡萄糖固定成功。实施例4化合物vi(乳糖基二硫代氨基甲酸盐)的制备,包括以下步骤:(1)乳糖(iv)与碳酸铵按照摩尔比1:1加入甲醇中形成悬浮液,升温至73℃,缓慢加入氨水至全溶,继续在73℃的条件下反应12h,产物结晶洗出制备1-氨基1-脱氧乳糖(v)。(2)化合物ii与二硫化碳,氢氧化钠按照摩尔比1:1:1加入甲醇中(氢氧化钠需事先配成5mol/L溶液),在46℃条件下反应12h,加入乙醇使产物析出制备化合物vi,总收率为50.3%。13CNMR(100MHzD2O):δ167.7(C=S),δ96.4(CHNH),δ60.8(CH2OH),δ68.5~77.8(otherCHOH).MS(EI-):m/z[M]-416.03.制备表面糖基化的金芯片。(1)制备母液:以去离子水为溶剂,充分溶解所制备的化合物vi,制得浓度为2mmol/L的自组装母液;(2)将金芯片浸泡于步骤(1)所制得的自组装母液中,于25℃条件下静置24小时;(3)所得的处理后的金芯片以乙醇冲洗,氮气吹干,避光保存。实施例5按照实施例4中的方法对SPR芯片进行乳糖糖基化处理。将反应后的芯片置于表面等离子共振(SPR)系统中系统中,分别通入伴刀豆球蛋白(ConA)、花生凝集素(PNA)、麦胚素(WGA),发现与乳糖基二硫代氨基甲酸盐反应的芯片特异性结合花生凝集素。结果如附图5所示,表明乳糖固定成功。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 检测二硫代氨基甲酸酯类农药的传感器及其制备和应用的制作方法与工艺
- 含氨基二硫代甲酸酯的刺芒柄花素衍生物、制备方法及其在抗肿瘤药物中的应用与流程
- 一种含有二硫代氨基甲酸酯类杀菌剂和生防菌的菌药组合物、制剂及其应用的制作方法与工艺
- 含二硫代氨基甲酸酯类化合物样品的前处理及检测方法与流程
- 糖基二硫代氨基甲酸盐、其制备方法和应用与流程
- 二烷基二硫代氨基甲酸酯的合成方法与流程
- 含苯甲酰胺类、二硫代氨基甲酸酯类杀菌剂和生防菌的菌药组合物、制剂及应用的制作方法与工艺
- 含二硝基苯胺类、二硫代氨基甲酸酯类杀菌剂和生防菌的菌药组合物、制剂及应用的制作方法与工艺
- 一种硫代氨基甲酸酯类次氯酸荧光探针的制备与应用的制作方法与工艺
- 包括锌、硫和农药活性成分的农业化学组合物的制作方法与工艺
- 含氨基二硫代甲酸酯的刺芒柄花素衍生物、制备方法及其在抗肿瘤药物中的应用与流程
- 一种含有二硫代氨基甲酸酯类杀菌剂和生防菌的菌药组合物、制剂及其应用的制作方法与工艺
- 含二硫代氨基甲酸酯类化合物样品的前处理及检测方法与流程
- 糖基二硫代氨基甲酸盐、其制备方法和应用与流程
- 二烷基二硫代氨基甲酸酯的合成方法与流程
- 含苯甲酰胺类、二硫代氨基甲酸酯类杀菌剂和生防菌的菌药组合物、制剂及应用的制作方法与工艺
- 一种硫代氨基甲酸酯类次氯酸荧光探针的制备与应用的制作方法与工艺
- 一种二烷基二硫代氨基甲酸酯的制备方法与流程
- 山药多糖作为二硫代氨基甲酸酯类杀菌剂增效剂的应用的制造方法与工艺
- 二硫代氨基甲酸系重金属捕捉剂的浓度测定方法以及浓度测定用试剂与流程