沃替西汀氢溴酸盐无水晶型I及其制备方法和应用与流程
本发明属药物晶型领域,涉及一种沃替西汀氢溴酸盐无水晶型i及其制备方法和应用。
背景技术:
沃替西汀(vortioxetinehydrobromide),化学名为1-[2-(2,4-二甲基苯基硫基)苯基]哌嗪氢溴酸盐,其结构式如下式i所示:
2013年9月30日,美国食品药品管理局(fda)批准沃替西汀用于治疗重度抑郁症成人患者,商品名为brintellix。该获批是基于一项全面临床开发项目中治疗重度抑郁症的疗效和安全性数据。该项目由7个关键性研究组成,包括6个为期6-8周的短期研究,以及1个为期24-64周的长期研究,这些研究结果表明,brintellix对重度抑郁症成人患者整体抑郁症状具有统计学意义的显著改善。此前,全球领先的制药与医疗保健问题研究与咨询/决策资源公司(decisionresources)发布报告预测,到2022年,brintellix在美国、日本、欧盟五大主要市场(法国、德国、意大利、西班牙、英国)中将成为重磅药物。根据迄今取得的数据,鉴于其对认知的积极影响及可耐受的副作用属性,brintellix预计将成为单相抑郁症市场中最成功的新药。
专利cn101472906b分别公开了呈晶体形态的沃替西汀的氢溴酸盐、盐酸盐、盐酸盐一水合物、甲磺酸盐、富马酸盐、马来酸盐、酒石酸盐、硫酸盐、磷酸盐、硝酸盐以及它们的制备方法和表征,并具体公开了沃替西汀氢溴酸盐的若干晶型,例如α型、β型、γ型、水合物以及乙酸乙酯溶剂化物,其中α晶型的熔点为~226℃,在水中的溶解度为2mg/ml;β晶型的熔点为~231℃,在水中的溶解度为1.2mg/ml;γ晶型在220℃下熔融,在高湿情况下易吸水。并指出氢溴酸沃替西汀β晶型最稳定,具有高熔点、较低的溶解度和良好的非吸湿性,特别适用于制备片剂。原研片brintellix中所含的沃替西汀氢溴酸盐即为β晶型。该专利将于2027年6月14日在中国到期。
为了满足药物固体制剂对于药物活性形态的严格要求(特别是晶型纯度要求和稳定性要求),扩大制剂开发所选用的原料形态并避开现有的专利保护,亟需开发一种新型的沃替西汀盐晶体或晶型。
技术实现要素:
一方面,本发明提供一种沃替西汀氢溴酸盐的无水晶型i,该无水晶型i至少具备与沃替西汀氢溴酸盐β晶型一样的溶解性、稳定性和纯度。
在本发明的一个实施方案中,采用d/max-2550pc型x射线衍射仪测定,测定条件:cukα辐射,管电压40kv,管电流250ma,所述沃替西汀氢溴酸盐无水晶型i的x-射线粉末衍射图谱以衍射角2θ°±0.2表示,具有处于3.76°、5.98°、11.96°、12.92°、18.37°、18.68°、24.62°特征峰。
在本发明的一个实施方案中,采用d/max-2550pc型x射线衍射仪测定,测定条件:cukα辐射,管电压40kv,管电流250ma,所述沃替西汀氢溴酸盐无水晶型i的x-射线粉末衍射图谱以衍射角2θ°±0.2表示,优选具有处于3.76°、5.98°、11.96°、12.64°、12.92°、17.74°、18.37°、18.68°、21.92°、24.06°、24.32°、24.62°、25.56°特征峰。
在本发明的另一个实施方案中,采用d/max-2550pc型x射线衍射仪测定,测定条件:cukα辐射,管电压40kv,管电流250ma,所述沃替西汀氢溴酸盐无水晶型i具有以衍射角2θ°±0.2表示的如图1所示的x-射线特征衍射谱图谱,具体特征谱线数据如下表1所示,其中衍射角2θ(单位:°)和晶面间距d(单位:
表1本发明的沃替西汀氢溴酸盐无水晶型i的x-射线特征衍射谱线数据
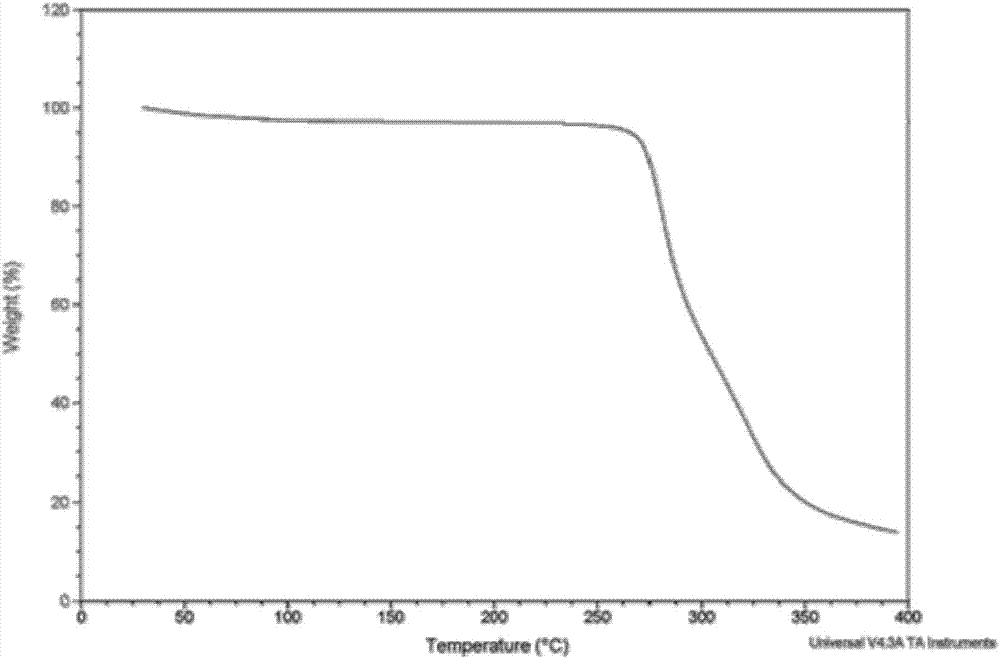
在本发明的另一个实施方案中,所述沃替西汀氢溴酸盐无水晶型i的tga分析如图2所示,显示该结构中不含溶剂(特别是水)。
在本发明的另一个实施方案中,所述沃替西汀氢溴酸盐无水晶型i的dsc分析如图3所示,显示其在127.27℃(峰顶值)处有一小的相变吸热峰,在227.41℃(峰顶值)处有一大的相变吸热峰,其熔点(峰顶值)为约233.73℃,分解温度为约260℃。
另一方面,本发明提供所述沃替西汀氢溴酸盐无水晶型i的制备方法,采用重结晶法,将任意形态的沃替西汀氢溴酸盐溶解于溶剂,特别是醇和水的混合溶剂中,搅拌回流,升温并搅拌至完全溶解,其中沃替西汀溴酸盐的重量与混合溶剂的质量体积比为1:20~100(g/ml);之后,快速降温,静置析晶,降温至0~20℃后继续静置析晶0.5~2小时;抽滤得白色沉淀,在40~50℃的温度下真空干燥,获得本发明的沃替西汀氢溴酸盐无水晶型i。
在本发明的一个实施方案中,所述溶剂优选为醇和水的混合溶剂,所述醇为甲醇、乙醇中的一种或两种,二者可以任意比例混合。
在本发明的一个实施方案中,所述醇和水的混合溶剂中,所述醇含量为约15~30%。
在本发明的一个实施方案中,优选升温至50~80℃搅拌至完全溶解。
在本发明的一个实施方案中,优选析晶温度为冰水浴至室温,更优选0-20℃,最优选10℃。
根据上述方法获得的沃替西汀氢溴酸盐无水晶型i,其具有以衍射角2θ°±0.2表示的如图1所示的x-射线特征衍射谱图谱,具体特征谱线数据如表1所示,hplc纯度≥99.9%。
第三方面,本发明提供包含所述沃替西汀氢溴酸盐无水晶型i的药物组合物。
在本发明的一个实施方案中,所述药物组合物包含作为活性成分的沃替西汀氢溴酸盐无水晶型i,以及药用赋形剂。
在本发明的一个实施方案中,所述药用赋形剂选自稀释剂、缓冲剂、助流剂、润滑剂、防腐剂、表面活性剂、润湿剂、粘合剂、崩解剂和增稠剂中的一种或多种,其用量可根据本领域常规技术进行选择,只要能够获得本发明的药物组合物即可。也可以使用制药领域已知的其他赋形剂。
在本发明的一个实施方案中,可适用于所述药物组合物的稀释剂优选选自微晶纤维素、乳糖、甘露醇、淀粉、蔗糖、碳酸钙、磷酸钙中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的崩解剂优选选自淀粉、离子交换树脂、交联聚维酮、交联羧甲基纤维素钠、羧甲基纤维素钠、羧甲淀粉钠中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的助流剂优选选自滑石粉、胶态二氧化硅、淀粉、硬脂酸镁中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的润滑剂优选选自硬脂酸镁、硬脂酸钙、硬脂酸、滑石粉中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的粘合剂优选选自烷基纤维素、羟基烷基纤维素、羧基烷基纤维素、淀粉、果胶、甲壳素衍生物、多糖、聚环氧烷、聚乙烯醇、聚乙烯吡咯烷酮中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的表面活性剂优选选自羧甲基纤维素钠、月桂酸、硬脂酸、十二烷基硫酸钠、烷基磺酸钠中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的润湿剂优选选自月桂硫酸钠、淀粉羟乙酸钠、聚乙二醇山梨坦脂肪酸酯类润湿剂(例如吐温20、60或80)中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的粘合剂优选选自烷基纤维素、羟基烷基纤维素、羧基烷基纤维素、淀粉、果胶、甲壳素衍生物、多糖、聚环氧烷中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的崩解剂优选选自淀粉、交联聚维酮、交联羧甲基纤维素钠、羧甲基纤维素钠、羧甲淀粉钠中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的增稠剂优选选自淀粉、琼脂、明胶、藻蛋白酸钠、果胶、羧甲基纤维素中的一种或多种。
在本发明的一个实施方案中,所述药物组合物可进一步包含其他任选的赋形剂如矫味剂、甜味剂和着色剂等。
在本发明的一个实施方案中,可适用于所述药物组合物的矫味剂优选选自香精、海藻酸钠、阿拉伯胶、明胶、甲基纤维素、枸橼酸、酒石酸中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的甜味剂优选选自甜菊苷、蔗糖、甘油、山梨醇、甘露醇、阿斯巴坦中的一种或多种。
在本发明的一个实施方案中,可适用于所述药物组合物的着色剂优选选自胭脂红、柠檬黄、亮蓝、钛白粉、氧化锌、氧化铁红、氧化铁黄中的一种或多种。
在本发明的一个实施方案中,所述药物组合物为片剂、胶囊、分散剂、混悬剂、口服液等剂型形式,优选片剂、口服液或胶囊;所述药物组合物可以口服和注射等方式给药,优选口服给药。
在本发明的一个实施方案中,优选所述药物组合物为片剂形式,以重量份计,其包含以下组份:
在本发明的一个实施方案中,优选所述药物组合物为片剂形式,以重量份计,其包含以下组份:
在本发明的一个实施方案中,优选所述药物组合物为口服液形式,以重量份计,由以下成分组成:
在本发明的一个实施方案中,优选所述药物组合物为口服液形式,以重量份计,由以下成分组成:
在本发明的一个实施方案中,优选所述药物组合物为胶囊形式,其包括内容物和胶囊壳,所述内容物包含本发明的沃替西汀氢溴酸盐无水晶型i、微晶纤维素、甘露醇、一水乳糖、羟丙甲基纤维素、交联聚维酮和硬脂酸镁;所述胶囊壳为明胶胶囊壳。
在本发明的一个实施方案中,以重量份计,所述胶囊包含以下组分:
第四方面,本发明提供所述沃替西汀氢溴酸盐无水晶型i以及包含该无水晶型i的药物组合物在制备治疗严重抑郁症药物中的应用,优选所述沃替西汀氢溴酸盐无水晶型i以及包含该无水晶型i的药物组合物在制备治疗认知损伤、抑郁症和焦虑症药物中的应用。
与现有技术相比较,本发明具有以下优势:
与已知的沃替西汀氢溴酸盐晶型相比较,本发明的沃替西汀氢溴酸盐无水晶型i具有更好的纯度和稳定性。平衡溶解度实验显示,本发明的沃替西汀氢溴酸盐无水晶型i在37℃水中的水溶性得到提高,明显高于β晶型,略高于α晶型(参看下表2)。溶解后可以制成更多剂型,如口服液、注射液、冲剂、糖浆剂等,丰富了沃替西汀的剂型,扩展了该药物的应用。
表2各种固体形式的沃替西汀及其氢溴酸盐在37℃水中的溶解度
附图说明
图1为本发明的沃替西汀氢溴酸盐无水晶型i的x射线衍射图谱。
图2为本发明的沃替西汀氢溴酸盐无水晶型i的tga图谱。
图3为本发明的沃替西汀氢溴酸盐无水晶型i的dsc图谱。
具体实施方式
以下通过实施例进一步阐述本发明。应理解,这些实施例仅用于举例说明目的,而不是对本发明的限制。本领域技术人员根据本发明构思对其作出的各种改变或调整,均应落入本发明的保护范围内。除注明的具体条件之外,实施例中的各试验方法均可按照常规方法来进行。
本发明的检测化合物晶型结构及性能的仪器信息如下:
粉末x射线衍射(xrpd):型号rigakud/max-2550pc,cukα辐射,功率40kv×250ma,扫描范围2θ:3~40°,步宽(stepwidth)0.02°,扫描速度5°/min。
热重分析(tg):ta公司的sdtq600,吹扫气:氮气120ml/min,升温速度:10℃/min,温度范围:室温~380℃。
差示扫描量热分析(dsc):ta公司的dscq100,吹扫气:氮气50ml/min,升温速度:10℃/min,温度范围:室温~300℃。
实施例1
取沃替西汀氢溴酸盐0.5g,加入甲醇水溶液37ml(甲醇含量15%),搅拌回流,升温至75℃,搅拌至完全溶解,降温,冷却至5~10℃,静置析晶1小时。抽滤,置于真空干燥箱(40~50℃)中烘干,得到沃替西汀氢溴酸盐无水晶型i,hplc测纯度>99.9%。
经x射线衍射仪测定,该沃替西汀氢溴酸盐无水晶型i具有如图1所示的x-射线粉末衍射图谱。
实施例2
取沃替西汀氢溴酸盐1g,加入甲醇水溶液50ml(甲醇含量25%),搅拌回流,升温至50℃,搅拌直至澄清。停止加热和搅拌,自然降温析晶,降温至10~20℃后再静置析晶1-2小时。抽滤,置于真空干燥箱(40~50℃)中烘干,得到沃替西汀氢溴酸盐无水晶型i,hplc测纯度>99.9%。
经x射线衍射仪测定,该沃替西汀氢溴酸盐无水晶型i具有如图1所示的x-射线粉末衍射图谱。
实施例3
取沃替西汀氢溴酸盐1g,加入20%的乙醇水溶液60ml,搅拌回流,升温至60℃,搅拌直至澄清。停止加热和搅拌,自然降温析晶,降温至0~5℃后再静置析晶1-2小时。抽滤,置于真空干燥箱(40~50℃)中烘干,得到沃替西汀氢溴酸盐无水晶型i,hplc测纯度>99.9%。
经x射线衍射仪测定,该沃替西汀氢溴酸盐无水晶型i具有如图1所示的x-射线粉末衍射图谱。
实施例4
取沃替西汀氢溴酸盐5g,加入25%的甲醇水溶液150ml,搅拌回流,升温至70℃,搅拌直至澄清。停止加热和搅拌,自然降温析晶,降温至5~10℃后再静置析晶1-2小时。抽滤,置于真空干燥箱(40~50℃)中烘干,得到沃替西汀氢溴酸盐无水晶型i,hplc测纯度>99.9%。
经x射线衍射仪测定,该沃替西汀氢溴酸盐无水晶型i具有如图1所示的x-射线粉末衍射图谱。
实施例5
取沃替西汀氢溴酸盐5g,加入30%的乙醇水溶液100ml,搅拌回流,升温至70℃,搅拌直至澄清。停止加热和搅拌,自然降温析晶,降温至0~5℃后再静置析晶1-2小时。抽滤,置于真空干燥箱(40~50℃)中烘干,得到沃替西汀氢溴酸盐无水晶型i,hplc测纯度>99.9%。
经x射线衍射仪测定,该沃替西汀氢溴酸盐无水晶型i具有如图1所示的x-射线粉末衍射图谱。
实施例6
按照以下配方和制备方法制备包含沃替西汀氢溴酸盐晶型i的药物片剂1000片,每片重150mg。
制备方法:将上述含量的沃替西汀氢溴酸盐无水晶型i、甘露醇、微晶纤维素、羟丙纤维素和羧甲淀粉钠在运动混合机中混合约10min,然后向该混合物中加入硬脂酸镁后再继续混合2-5min,得中间体,压片。
实施例7
按照下表配方制备包含沃替西汀氢溴酸盐无水晶型i的口服液500瓶,每瓶10ml(规格10mg/ml)。
制备方法:将蔗糖和甘油在60-90℃热水中溶解后冷却至室温,加入柠檬酸、草莓香精和苯甲酸钠搅拌使溶解,待溶液澄清后加入沃替西汀氢溴酸盐无水晶型i,继续搅拌使溶液澄清,分装得口服液。
- 还没有人留言评论。精彩留言会获得点赞!