8‑氨基喹啉‑羟基咔唑杂联体,其制备方法及其药物组合物与流程
本发明涉及合成一系列8-氨基喹啉-羟基咔唑杂联体。结构式如图1式(I)所示。既可以选择性螯合铜离子,同时又能发挥良好的神经保护作用,使它们成为治疗AD药物开发的候选化合物。
背景技术:
阿尔茨海默病(Alzheimer′s disease,AD)即老年痴呆症,是一种慢性进行性中枢神经系统疾病,其严重影响患者的认知功能、记忆功能、视空间功能和社会生活能力等。随着世界老年人口的急剧增长,AD发病人数也逐年增加,目前大约有4680万人患有AD,预计到2050年AD的患病人数将会增加到1.3亿人。AD的主要病理特征有大脑皮质弥漫性萎缩、神经元大量减少、β-淀粉样蛋白形成的老年斑(senile plaques,SPs)及tau蛋白过度磷酸化形成的神经原纤维结(neurofibrillary tangles,NFTs)。目前关于AD的发病机制尚不十分清楚,普遍认为AD是一种多病因性、多基因关联性和多环节性疾病。目前存在的假说包括Aβ级联假说、tau蛋白假说、胆碱能缺陷、金属离子紊乱假说、基因学说等多种病因假说,但任何一种假说都不能对AD的发病过程作出全面的解释。
最近的调查结果报告显示多种金属离子,包括铜、锌、铁和铝的动态变化在AD中起着重要的作用。金属铜是我们人体所必须的微量元素,是多种代谢途径的重要的过渡金属。文献报道,铜离子能抑制兴奋性神经递质受体N-甲基-D-天冬氨酸(N-Methyl-D-aspartic acid,NMDA)的过度激活,能促进Aβ聚集和淀粉样斑块的形成,还具有抗氧化损伤的作用。5-氯-7-碘-8-羟基喹啉(clioquinol)能够降低AD小鼠模型的脑Aβ沉淀,改善动物的认知功能和提高整体健康状况,成为第一个进入临床研究的抗AD金属离子螯合剂。8-羟基喹啉衍生物PBT-2可显著降低AD动物脑脊液(CSF)中Aβ42水平。8-氨基喹啉衍生物PA1673对铜离子有较高的选择性,对锌离子几乎没有螯合作用。它能够完全逆转注射或口服Aβ小鼠的记忆缺失。以8-羟基喹啉及8-氨基喹啉为核心骨架为基础开发金属离子调节剂用于AD治疗是切实可行的AD新药开发策略。
氧化应激是AD发生和发展过程中早期表现。研究发现,氧化应激是由体内产生的无规律的活性氧引起,进而导致神经元的死亡和丢失。因此,寻找外源性的抗氧剂成为AD治疗药物研中的方向之一。据报道,咔唑衍生物能够直接清除体内的活性氧,具有较强的抗氧化活性。最近研究表明,咔唑衍生物还能够抑制Aβ聚集,具有抑制胆碱酯酶的作用。咔唑衍生物卡维地洛和P7C3,具有很好的神经保护作用。以抗氧化应激为设想,引入咔唑作为抗氧化活性部位成为抗AD药物研发的重要方向。
技术实现要素:
金属离子在AD病理的发生和发展中起到关键作用,金属离子螯合剂特别是铜离子螯合剂是研发AD药物的重要策略之一。因此选择性铜离子螯合剂作为治疗AD药物的设计作为本发明的重点。基于我们的研究基础,8-氨基喹啉是良好的选择性铜离子螯合剂,在体内,8-氨基喹啉衍生物能够将二价铜离子被还原为一价铜离子,从而使二价铜离子失去与Aβ的结合能力,Aβ聚集减少。另一方面,已有的研究表明咔唑具有良好的神经神经元保护作用,具有多种治疗AD的相关特性。因此,我们设计了8-氨基喹啉与羟基咔唑杂化体,预估结合二者的治疗特性,以在AD治疗中起到一药“多靶点、多功能”的协同效果。
本发明的化合物其特征在于存在两个主要的单元:咔唑部分和8-氨基喹啉部分。一方面可以选择性螯合铜离子;另一方面,同时发挥良好的神经神经元保护作用,改善AD的症状,使得它们成为药物开发的候选物。
本发明涉及图1式(I)的化合物或其互变异构体,药用盐,前药或溶剂化物。
其中,R1=H,F,Cl,Br;R2=H,OH,OCH3;R1在咔唑的5-位,6-位,7-位或8-位;R2在喹啉的5’-位,6’-位或7’-位;-O-CH2-的氧端在咔唑的1-位,2-位,3-位或4-位。
除非另外指明,本发明的化合物还意欲包括区别仅在于存在一个或多个同位素富集的原子的化合物。例如,具有本结构的除了用氘或氚替换氢,或者用13C或14C-富集的碳原子替换碳原子,或15N-富集的氮以为的化合物属于本发明的范围内。
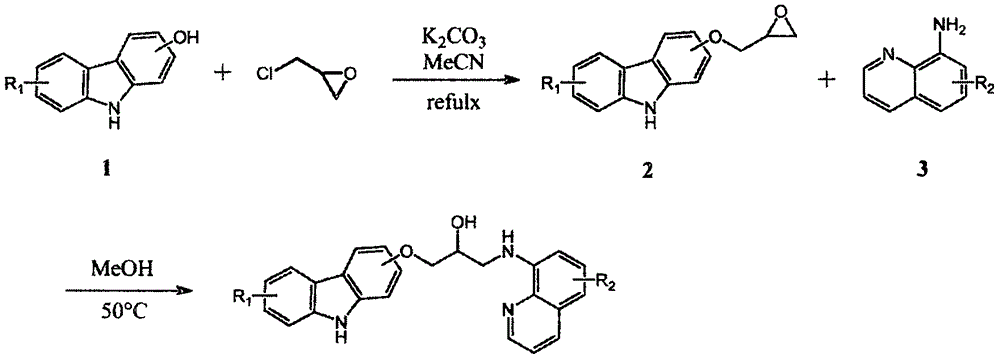
图2反应路线列举了制备本发明的化合物的方法。
具体制备方法是:
(1)将图2中化合物1溶解在乙腈中,加入催化剂碳酸钾和环氧氯丙烷,加热回流至原料反应完全,旋干溶剂,经萃取,柱层析纯化后得到中间产物2;
(2)将中间产物2溶解在甲醇中,加入化合物3,加热至50℃至原料反应完全,蒸干溶剂,粗品经柱层析纯化得到最终产物。
附图说明
图1 8-氨基喹啉-羟基咔唑杂联体结构通式(I)。
图2 8-氨基喹啉-羟基咔唑杂联体合成路线。
图3 P-Z-001的具体合成路线。
图4 化合物对L-glutamate诱导HT22细胞死亡的保护作用。
图5 化合物P-Z-001与生物体内常见金属离子(铜、铁、锌)的相互作用的紫外-可见光吸收光谱图。
实施例
提供下列实施例进一步举例说明本发明,它们不应当认为是对本发明范围的限定。
实施例1:化合物P-Z-001的合成
图3反应路线列举了合成P-Z-001的方法。
将4-羟基咔唑(1g,5.5mmol)用20mL乙腈溶解,加入催化剂碳酸钾(1.52g,11mmol)和环氧氯丙烷(5.0mL,6.4mmol),加热回流反应至原料反应完全,反应时间大约为24h。减压蒸除溶剂,剩余物用50mL乙酸乙酯溶解,用水洗3次,每次20mL。有机层被分离,并用20mL饱和食盐水洗1次,然后加入无水硫酸钠干燥,减压蒸除溶剂,得粗品。粗品经柱层析纯化(二氯甲烷∶石油醚=1∶1),得到白色固体产物a(0.86g,65%)。1H NMR(400MHz,CDCl3)δ8.36(d,J=7.9,0.9Hz,1H),8.10(s,1H),7.46-7.39(m,2H),7.35(t,J=8.0Hz,1H),7.27(dd,J=5.8,2.2Hz,1H),4.49(dd,J=11.0,3.3Hz,1H),4.30(dd,J=11.0,5.4Hz,1H),3.59(dddd,J=5.6,4.1,3.4,2.6Hz,1H),3.03(dd,J=5.0,4.1Hz,1H),2.92(dd,J=5.0,2.6Hz,1H)。13C NMR(100MHz,CDCl3)δ155.02,141.01,138.76,126.62,125.14,123.24,122.55,119.78,112.92,110.00,104.09,101.39,68.84,50.40,44.92.MS ESI:239.1。
将中间产物a(300mg,1.26mmol)用15mL甲醇溶解,加入8-氨基喹啉(222mg,1.5mmol),加热至50℃至原料反应完全,反应时间大约为16h。减压蒸除溶剂,得粗品,粗品经柱层析纯化(石油醚∶乙酸乙酯=10∶3),得淡黄色固体P-Z-001(298mg,62%)。1H NMR(400MHz,DMSO)δ11.26(s,1H),8.73(d,J=3.7Hz,1H),8.28(d,J=7.8Hz,1H),8.20(d,J=8.1Hz,1H),7.49(dd,J=8.2,4.2Hz,1H),7.44(d,J=8.1Hz,1H),7.30(dq,J=16.0,8.0,7.5Hz,3H),7.12(t,J=7.4Hz,1H),7.06(dd,J=8.0,4.0Hz,2H),6.76(d,J=7.7Hz,1H),6.70(d,J=7.9Hz,1H),5.56(s,1H),4.43-4.34(m,1H),4.26(d,J=5.1Hz,2H),3.68(d,J=10.2Hz,1H),3.48(dd,J=12.8,7.0Hz,1H)。13C NMR(100MHz,DMSO)δ155.31,147.42,145.11,141.60,139.40,138.03,136.45,128.78,128.22,126.95,125.03,122.99,122.20,122.17,119.06,113.85,112.05,110.84,104.90,104.45,100.95,70.79,68.05,55.38,46.57。
HRMS ESI(+)m/z calculated for C24H21N3O2[M+H]+:384.1713.Found:384.1707。
HPLC purity:98.4%。
实施例2:生物学评估
对L-glutamate诱导HT22细胞死亡的保护作用
小鼠海马神经元细胞株HT22,用含10%胎牛血清的DMEM完全培养基,在37℃,饱和湿度,含体积分数为5%CO2、95%空气的二氧化碳培养箱中常规培养。取对数生长期细胞,以0.25%胰酶消化后,完全培养基重悬,显微镜下细胞计数板计数并调整细胞浓度为10×104个/ml,接种96孔细胞培养板,100μL/孔,培养过夜,使细胞贴壁。将96孔板中培养基吸走,待测化合物用DMSO溶解,用完全培养基稀释,加入到96孔板中,100μL/孔。预孵育30min后,加入2μL 100mM L-glutamate。模型组不加待测化合物,直接加入2μL 100mM L-glutamate。孵育24h后,每孔加入10μL 5mg/mL MTT,孵育2h,弃去上清,加DMSO 100μL/孔,振荡使生成物formazan充分溶解,在酶标仪上测定各孔吸光度值,测定波长570nm。采用公式化合物促进细胞的存活率(%)=100%*(A待测化合物-A模型组)/(A模型组-A空白)计算细胞存活率。
实施例3:生物学评估
与生物体内常见金属离子的相互作用
反应体系总体积1ml,其中待测化合物终浓度为20μM,金属离子溶液终浓度为20μM。同时设立单独待测化合物组和空白组,各组分混匀后室温孵育30min。在紫外分光光度计上扫描各实验组在200-700nM范围内的紫外吸收光谱图,每0.5nM一个吸收点。首先在石英比色皿中加入1mL无水乙醇扫描baseline,再扫描无水乙醇为溶剂对照组,其次扫描待测化合物溶液以及化合物加金属离子溶液组。每个浓度至少进行三次独立实验。
实施例4:生物学评估
铜离子诱导的Aβ聚集的抑制作用
Aβ1-42溶入1%的氨水溶液中得储备液,分装后储存于-80℃冰箱中。Aβ储备液用20μM HEPES(含有150μM NaCl)稀释,取10μL Aβ(终浓度为25μM)加入到10μL铜离子(终浓度为25μM)和10μL测试化合物(终浓度为50μM)混合液中,37℃孵育24h。取20μL样品溶液,用50mM的glycine-NaOH缓冲液稀释至200μL混匀,采用300秒的荧光强度扫描((λexc=450nm;λem=485nm)。百分抑制率=(1-IFi/IFc)×100,IFi和IFc分别代表扣除背景之后含有和未含有抑制剂的荧光强度。
表1.Th-T荧光法测定化合物铜离子诱导的Aβ聚集的抑制作用
- 还没有人留言评论。精彩留言会获得点赞!