基于茚并芴九并稠环A‑D‑A型共轭分子及其制备方法与流程
本发明属于有机光伏技术领域,具体涉及一类基于茚并芴九并稠环环为母核,以五元芳杂环为桥联基团,末端连接缺电子单元的A-D-A型共轭分子及其制备方法,以及该类分子作为光活性层中的电子给体或者电子受体在有机光伏电池领域中的应用。
背景技术:
有机太阳能电池具有质轻、成本低、可弯曲、可溶液加工和大面积制备等优点,受到了科研工作者的兴趣和关注。近期,聚合物和小分子太阳能电池发展迅速,取得了长足的进步[Adv.Mater.,2013,25,3973;Nat.Commun.,2013,4,1446;Sci.Rep.,2014,4,6813;Nat.Commun.,2014,5,5293;Nature,2014,17,1;J.Am.Chem.Soc.2014,136,15529;Nat.Photon.,2015,9,520;Nat.Energy,2016,1,15027]。目前,基于富勒烯受体材料共混的本体异质结(BHJ)太阳能电池的光电转换效率已突破10%,预示着有机太阳能电池巨大的应用前景。
在给体材料方面,包括聚合物和小分子给体材料,得到了系统研究和快速发展,特别是近期基于聚合物给体材料与富勒烯受体材料单层电池的光电转换效率已经高达11.7%,取得了重大进展。相对于给体材料的飞速发展,受体材料的发展则相对缓慢。在受体材料方面,基于PCBM的富勒烯衍生物因其具有大的电子亲和力、优秀的电子传输性能、能与给体材料混合形成纳米尺寸的相分离等优点,在受体材料中占据主导地位[Science,1995,270,1789;Adv.Mater.,2013,25,1038]。由于该类材料在可见光区吸收较弱、能级难于调控、提纯较困难等缺点[Energy Environ.Sci.,2011,4,1558],合成新型的聚合物或小分子受体材料替代该类材料显得尤为必要。近期,基于稠环小分子受体材料呈现快速发展的势头[J.Am.Chem.Soc.,2007,129,7246;J.Am.Chem.Soc.,2016,138,375;J.Am.Chem.Soc.,2016,138,2973;J.Am.Chem.Soc.,2016,138,4955;J.Am.Chem.Soc.,2016,138,15011;Adv.Mater.,2016,28,4734;Adv.Mater.,2016,28,9243;Chem.Mater.,2016,28,6770;J.Am.Chem.Soc.,2016,138,DOI:10.1021/jacs.6b08523],光电转换效率已然突破了12%,表明小分子受体材料具有更加广阔的应用前景。
技术实现要素:
为了克服现有技术存在的不足和缺陷,本发明提供一类吸收强、电荷传输性能良好及电子能级合适的基于茚并芴九并稠环A-D-A型共轭分子,其作为电子给体或电子受体材料在有机太阳能电池中应用。
基于茚并芴九并稠环由于其刚性结构,具有强的分子间π-π作用,可获得较高的载流子迁移率。基于以上思考,本发明以基于茚并芴九并稠环为母核,五元芳杂环作为桥联基团,末端连接强拉电子基团的A-D-A型共轭分子,该类型分子可作为给体或受体材料应用于有机太阳能电池领域。
本发明提供的基于茚并芴九并稠环A-D-A型共轭分子具有以下通式结构:
其中,n为0~3;X=O,S或Se;R1~R4独立地为氢、C1~C20的烷基、C1~C20的烷氧基、4-烷基苯基、4-烷氧基苯基、5-烷基噻吩基、5-烷氧基噻吩基或5-烷硫基噻吩基;所述的4-烷基苯基、4-烷氧基苯基、5-烷基噻吩基、5-烷氧基噻吩基或5-烷硫基噻吩基分别为C1~C8的烷基、烷氧基或烷硫基。
拉电子基团A选用下列结构之一:
上述A单元中R5为C1~C8的烷基。
基于茚并芴九并稠环A-D-A型共轭分子的制备方法为:
将带有R2取代基的茚并芴双硼酸酯与2-溴-3-甲酸甲酯五元芳杂化合物(摩尔比1:2~10)在钯催化剂(醋酸钯、四(三苯基膦)钯、二(三苯基膦)二氯化钯的一种或多种)(茚并芴双硼酸酯与钯催化剂摩尔比为1:0.005~1)的作用下于甲苯和水混合溶液中(5:1,v/v)进行交叉偶联反应,所得化合物与相应活泼金属试剂(有机锂试剂、有机镁试剂、有机锰试剂的一种或多种)进行加成反应,再经关环得到所需九并稠环化合物,经溴代后金属化与N,N-二甲基甲酰胺制备得到相应的九并稠环双醛化合物。2-溴-3-甲酸甲酯五元芳杂化合物指的是2-溴-3-噻吩甲酸甲酯、2-溴-3-呋喃甲酸甲酯、2-溴-3-硒吩甲酸甲酯的一种或者多种。
将带有R1,R3,R4取代基的九并稠环双醛化合物与定量拉电子单元A(摩尔比为1:2~10)加到反应容器中,加入氯仿和64当量吡啶,进行脱氧处理,加热回流反应12小时。冷却后经萃取、干燥、浓缩、柱层析,即可以70%的分离产率得到九并稠环A-D-A型共轭分子。
本发明获得了一系列基于茚并芴九并稠环A-D-A型共轭分子及其制备方法,该方法操作简单、产物易分离纯化、易于修饰改性、易用于构建复杂A-D-A型共轭分子,在有机光电领域具有较好的应用前景。由于该类稠环A-D-A型共轭分子具有强的刚性共平面结构,末端具有强的拉电子单元,因此,该类共轭分子具有较强的吸收能力、合适的电子能级,适合作为电子给体或受体材料应用于有机太阳能电池领域。
本发明的主要优点在于:
1.合成的基于茚并芴九并稠环A-D-A型共轭分子具有良好的溶解性,能溶于大部分有机溶剂,如氯仿、二氯甲烷、四氢呋喃和氯苯等。
2.合成的基于茚并芴九并稠环A-D-A型共轭分子具有良好的光谱吸收范围,适合用于有机太阳能电池材料。
3.合成的基于茚并芴九并稠环A-D-A型共轭分子具有合适的电化学能级,适合用作电子给体或电子受体材料。
4.合成的基于茚并芴九并稠环A-D-A型共轭分子作为电子受体材料在有机太阳能电池中获得较高的能量转换效率。
附图说明
图1为基于茚并芴九并稠环A-D-A型共轭分子DTIF-IC的紫外-可见吸收光谱图。
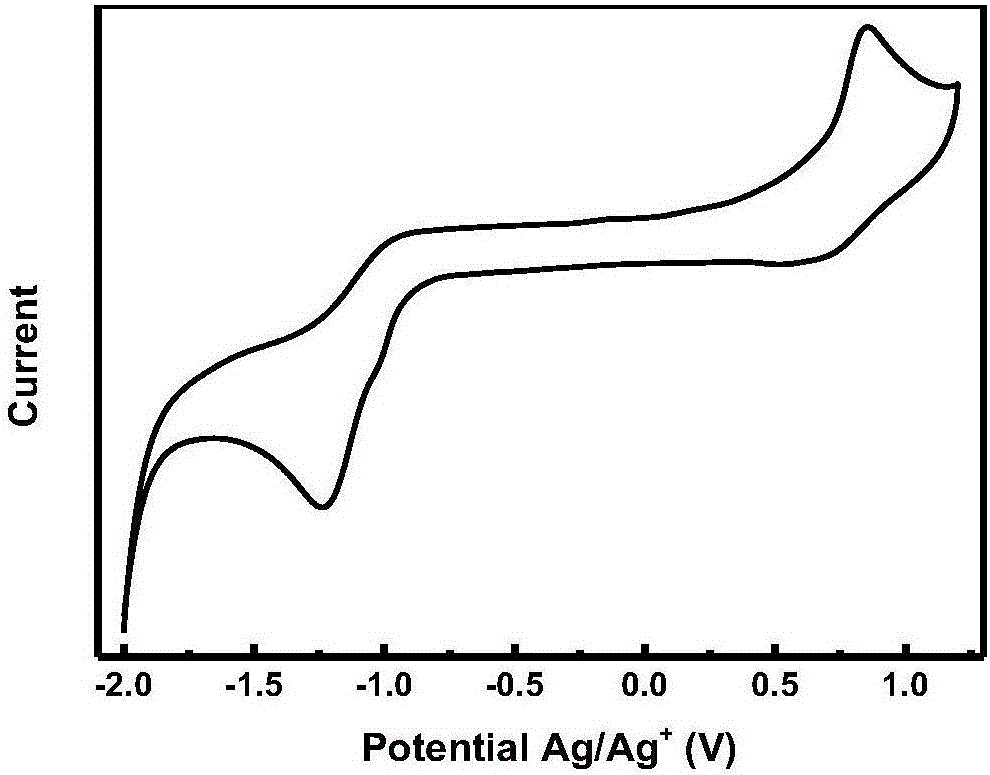
图2为基于茚并芴九并稠环A-D-A型共轭分子DTIF-IC的循环伏安曲线图。
图3为基于茚并芴九并稠环A-D-A型共轭分子DTIF-IC的有机太阳能电池的I-V曲线。
具体实施方式
下面通过具体实施例对本方面做进一步的解释说明。
基于茚并芴九并稠环A-D-A型共轭分子的制备路线如下所示,以茚并芴双频哪醇酯1为起始原料,依次经Suzuki偶联、加成、关环得到九并稠环化合物5。经锂化后DMF猝灭得到中间体7,最后在吡啶存在下与7发生Knoevenagel反应,生成基于茚并芴九并稠环A-D-A型共轭分子骨架化合物8,详见实施例1-5。
基于茚并芴九并稠环A-D-A型共轭分子的制备路线
实施例1.化合物3的合成路线如下:
氮气保护下,在250mL三口瓶中加入化合物1(2.0g,2.4mmol),化合物2(1.3g,6mmol),碳酸钾(1.7g,12mmol),336(0.5g),Pd(PPh3)4(0.23g,10%mol)溶于18mL甲苯/水(5:1),加热回流反应72h,停止反应,乙醚萃取,合并有机相,饱和食盐水洗涤,无水硫酸镁干燥,抽滤,旋干溶剂,柱色谱分离得到1.7g黄色油状物,收率86%。1H NMR(500MHz,CDCl3)δ7.77(s,1H),7.75(s,1H),7.64(d,J=1.8Hz,2H),7.54(d,J=1.1Hz,1H),7.52(d,J=1.1Hz,1H),7.50(d,J=1.6Hz,1H),7.48(d,J=1.6Hz,1H),7.44(d,J=1.4Hz,2H),7.25(s,1H),7.24(s,1H),3.71(s,J=1.2Hz,6H),2.03(t,J=8.2Hz,9H),1.22–1.00(m,45H),0.82–0.75(m,15H).13C NMR(126MHz,CDCl3)δ164.05,151.69,150.86,150.63,141.86,140.37,131.70,130.20,128.45,127.83,124.44,123.83,118.99,114.22,54.88,51.46,40.62,31.81,30.08,29.28,29.24,23.82,22.59,14.07.
实施例2.化合物4的合成路线如下:
氮气保护下,-78℃下向装有4-己基溴苯(5.0g,20.7mmol)和100mL THF的250mL三口瓶中滴加2M丁基锂10mL,保持低温反应1h。在此温度下,向反应液中滴加化合物3(1.77g,2.03mmol),恢复室温搅拌过夜,水解,乙醚萃取三次,合并有机相,饱和食盐水洗涤,无水硫酸镁干燥。抽滤,旋干溶剂,柱色谱分离得到黄绿色油状物0.8g,收率80%。1H NMR(500MHz,CDCl3)δ7.64(s,1H),7.62(s,1H),7.50(d,J=3.0Hz,2H),7.32(d,J=1.6Hz,1H),7.31(d,J=1.6Hz,1H),7.19(d,J=8.2Hz,8H),7.14(t,J=6.9Hz,8H),7.10(d,J=5.3Hz,2H),6.92(d,J=1.4Hz,2H),6.40(d,J=5.3Hz,2H),2.65–2.61(m,10H),1.63(tt,J=12.5,6.2Hz,17H),1.43–1.25(m,40H),1.19–0.96(m,61H),0.94–0.87(m,21H),0.78(dd,J=8.9,5.3Hz,18H).13C NMR(126MHz,CDCl3)δ151.35,150.41,145.89,145.77,144.19,141.91,141.75,141.39,140.18,139.24,132.87,131.62,128.97,127.98,127.92,127.62,123.93,122.25,119.58,114.02,80.80,54.69,40.16,35.67,31.90,31.83,31.79,31.59,29.96,29.25,29.11,29.04,23.69,22.71,22.66,22.61,14.15,14.07,13.81.
实施例3.化合物5的合成路线如下:
在50mL单口圆底烧瓶中加入化合物4(0.8g,0.5mmol),干燥CH2Cl2 30mL,三氟化硼乙醚溶液10mL,加热回流反应过夜。停止加热。冷却,加入水,CH2Cl2萃取三次,合并有机相,饱和食盐水洗涤,无水硫酸镁干燥。抽滤,旋除溶剂,柱色谱分离得到黄色固体0.57g,收率73%。1H NMR(500MHz,CDCl3)δ7.67(s,2H),7.44(s,2H),7.37(s,2H),7.27(s,1H),7.26(s,1H),7.21(d,J=8.3Hz,8H),7.08(d,J=8.3Hz,8H),7.02(s,1H),7.01(s,1H),2.60–2.54(m,8H),2.06–1.91(m,9H),1.65–1.52(m,9H),1.39–1.25(m,24H),1.19–1.00(m,40H),0.88(m,12H),0.78–0.74(m,12H),0.70(s,8H).13C NMR(126MHz,CDCl3)δ156.04,152.77,151.10,150.25,144.85,142.57,142.11,141.57,141.24,140.28,139.61,138.38,136.13,134.92,128.22,128.04,127.11,123.23,117.35,113.80,113.66,62.65,54.43,40.81,35.60,31.77,31.73,31.32,30.08,29.26,29.23,29.20,23.85,22.60,22.57,14.08,14.04.
实施例4.化合物6的合成路线如下:
氮气保护下,在100mL三口圆底烧瓶中加入化合物5(0.57g,0.37mmol),干燥的THF 10mL,冷却至-78℃,向反应瓶中滴加LDA(5mL,1.1mmol),保持低温反应1h。在此温度下,向反应瓶中加入DMF 1mL,缓慢恢复室温搅拌过夜。加水中止反应,乙醚萃取三次,合并有机相饱和食盐水洗涤,无水硫酸镁干燥。抽滤,旋除溶剂,柱色谱分离得到黄色固体0.23g,收率40%。1H NMR(500MHz,CDCl3)δ9.83(s,2H),7.72(s,2H),7.66(s,2H),7.51(s,2H),7.50(s,2H),7.20(d,J=8.2Hz,8H),7.11(d,J=8.3Hz,8H),2.63–2.54(m,8H),2.11–1.93(m,9H),1.65–1.53(m,9H),1.39–1.24(m,24H),1.20-1.06(m,40H),0.87(t,J=6.8Hz,12H),0.74(t,J=6.8Hz,12H),0.69(s,8H).13C NMR(126MHz,CDCl3)δ182.95,156.65,156.43,154.39,152.12,151.90,151.13,145.32,141.77,141.57,140.48,128.50,127.87,117.83,115.56,114.29,62.86,54.66,40.68,35.58,31.73,31.71,31.31,29.97,29.22,29.17,23.86,22.59,22.56,14.07,14.02.
实施例5.基于茚并芴九并稠环A-D-A型共轭分子8(DTIF-IC)的合成路线如下:
在100mL单口圆底烧瓶中加入化合物6(70mg,0.044mmol),化合物7(43mg,0.22mmol),CHCl3 10mL,吡啶 0.32mL,溶液进行脱氧处理,加热至回流反应12h。冷却至室温,水洗三次,有机相用无水硫酸镁干燥。抽滤,旋干溶剂,柱色谱分离得到蓝紫色固体60mg,收率70%。1H NMR(500MHz,CDCl3)δ8.92(s,2H),8.70(s,1H),8.69(s,1H),7.95–7.92(m,2H),7.79–7.71(m,8H),7.66(s,2H),7.54(s,2H),7.21(d,J=8.3Hz,8H),7.13(d,J=8.3Hz,8H),2.62–2.54(m,8H),2.12–1.96(m,9H),1.66–1.57(m,9H),1.35-1.29(m,24H),1.18–1.02(m,40H),0.87(t,J=6.8Hz,12H),0.76(t,J=7.0Hz,12H),0.73-0.70(m,8H).13C NMR(126MHz,CDCl3)δ188.45,161.22,152.63,143.83,142.06,141.29,137.04,134.21,128.61,127.91,63.07,54.78,35.59,31.73,31.71,31.32,30.01,29.23,29.20,29.15,22.59,22.57,14.08,14.03.
基于茚并芴九并稠环A-D-A型共轭分子DTIF-IC的紫外-可见吸收光谱图如图1所示;循环伏安曲线如图2所示;所制备的有机太阳能电池的I-V曲线如图3所示,测得器件的短路电流Jsc为13.46mA cm-2,开路电压Voc为0.94V,填充因子FF为56.5%,能量转换效率PCE为7.14%。
太阳能光伏器件的制备及性能测试:将商业购买的氧化铟锡(ITO)导电玻璃依次用去离子水、丙酮、半导体清洗液、去离子水、异丙醇超声清洗,放在真空干燥箱中干燥。在干净ITO上旋涂ZnO前驱体溶液,ZnO厚度为40nm,基片放置200℃加热台上热退火60分钟。将玻璃/ITO/ZnO衬底转移到充满氮气的手套箱中,旋涂水醇溶性阴极修饰层PFN。将实施例5的A-D-A型共轭分子DTIF-IC与聚合物给体材料PTB7-Th(重量比都为1.3:1)的共混溶液(20~30mg/ml)旋涂于ITO/ZnO(40nm)/PFN(10nm)上,70℃热退火10分钟。随后将器件转移到真空蒸镀腔中,采用真空蒸镀方法(3×10-5Pa)沉积10nm厚的MoO3和100nm厚金属Al。器件结构为:玻璃/ITO(130nm)/ZnO(40nm)/PFN(10nm)/活性层(90nm)/MoO3(10nm)/Al(100nm),光伏器件的有效面积为0.16cm2。
用配有AM1.5滤光片Newport 500W氙灯作为模拟太阳光源,在100mW/cm2光强下对器件进行光伏性能测试,光强通过标准单晶硅太阳能电池校准;I-V曲线使用Keithley 2400进行测量,通过Labview软件由计算机进行控制。
基于二苯并五元芳杂稠环A-D-A型共轭分子DTIFC-IC的有机太阳能电池的I-V曲线如图3所示。
本发明所用的聚合物给体材料PBT7-Th的结构如下:
- 还没有人留言评论。精彩留言会获得点赞!