一种检测TP53基因突变以诊断膀胱癌的方法及试剂盒与流程
本发明属于疾病临床诊断领域,具体涉及一种通过分子生物学检测手段诊断膀胱癌的技术,尤其涉及一种通过检测tp53基因突变以诊断膀胱癌的方法及试剂盒。
背景技术:
膀胱尿路上皮癌是泌尿道的最常见的恶性肿瘤。癌发病率水平在全国32个肿瘤登记处的合计为6.69/10万,占全部恶性肿瘤新发病例的2.52%。按性别统计,膀胱癌男、女性发病率分别为10.10/10万和3.20/10万,男性是女性的3.16倍。膀胱癌死亡率水平在全国32个肿瘤登记中为2.53/10万,占全部恶性肿瘤死亡总数的1.47%,此癌多数组织学表现为分化良好的乳头状病变。
tp53基因是目前发现的与肿瘤相关性最高的一种抑癌基因,是多种肿瘤的分子标志物。tp53位于人类染色体17p13上,编码393个氨基酸的蛋白,该蛋白包括3个主要的结构域:n末端反式激活位点中间的dna结合区域和c末端寡居位点,该基因的蛋白产物是细胞生长、增殖和损伤修复的重要调节因子。
tp53突变的泌尿上皮癌通常是高级别的肿瘤,倾向于肌层浸润,高复发,早期转移。tp53基因突变仅在诊断为膀胱癌的患者细胞中发现,在癌症扩散的患者中,tp53突变的检出率比在浅表癌的患者中高2.5倍,与具有较低侵袭性癌症的患者相比,tp53在高侵袭性泌尿上皮癌中的检出率高4倍以上。tp53是目前仅有的能诊断和预测膀胱癌预后的理想的评估指标之一。现有技术中针对tp53基因位点突变的检测方法例如cn103740818a、cn102146461a等,但其针对的样本通常均为临床手术获取的病变组织,难以进行膀胱癌早期无创筛查。。
目前临床上通过尿液进行膀胱癌的早期诊断的方法主要包括:尿液分析、尿脱落细胞分析,超声、ct或mri成像等。特异性膀胱肿瘤标志物是实现快速、便捷、检测的重要手段,cn106093389a、cn103018461b等致力于通过血清学方法对尿样进行检测来诊断膀胱癌;cn104620109a、cn105779641a、cn105229169a等主要在基因水平通过检测膀胱肿瘤标志物诊断膀胱癌。
然而,现有技术中膀胱癌肿瘤标记物众多,各检测指标的检测效果和检出率变异较大。一方面,为使检测结果具有临床诊断意义,必须要综合使用大量标记物,但另一方面,应用了大量标记物不但费时耗力、价格昂贵,而且各标记物的诊断结果之间往往不一致难以给出具有临床价值的诊断结论。比较成熟的无创筛查和监测膀胱癌尿基标记物,如食品和药物管理局(fda)批准的immunocy,核基质蛋白22,和荧光原位杂交(fish)具有较为确定的临床诊断意义,然而仍需要更方便、快捷,临床意义明确的诊断方法。
技术实现要素:
针对现有技术中的不足,本发明所要解决的技术问题是提供一种临床价值明确,操作简单快捷、结果直观可靠、以尿液为检测材料的无创伤膀胱癌早期临床诊断方法和试剂盒。
发明概述
本发明提供tp53基因的检测试剂在制备膀胱癌诊断试剂盒中的应用,其中所述tp53基因检测试剂选自由以下组成的组:外显子5的检测试剂、外显子7的检测试剂和外显子8的检测试剂。
如前所述本发明的应用,其中外显子5的检测试剂能够检测tp53基因外显子5中157、158、175位点的突变;外显子7的检测试剂能够检测tp53基因外显子7中244、245、248位点的突变;外显子8的检测试剂能够检测tp53基因外显子8中268、273、275、282位点的突变。
如前所述本发明的应用,其中针对每种外显子的检测试剂都包括一组探针和引物,所述探针包括供体探针和受体探针,其中供体探针3’端标记有荧光供体,所述受体探针的5’端标记有荧光受体、3’端进行磷酸化修饰;上游引物和下游引物分别位于探针结合位点的两侧。
如前所述本发明的应用,其中外显子5的检测试剂包括seqidno:1-2、外显子7的检测试剂包括seqidno:3-4、外显子8的检测试剂包括seqidno:5-6。
如前所述本发明的应用,其中外显子5的检测试剂还包括seqidno:7-8、外显子7的检测试剂还包括seqidno:9-10、外显子8的检测试剂还包括seqidno:11-12。
本发明还提供一种实时荧光pcr检测试剂盒,其特征在于包括tp53基因检测试剂,所述tp53基因检测试剂选自由以下组成的组:外显子5检测试剂、外显子7检测试剂和外显子8检测试剂,优选所述检测试剂为实时荧光pcr试剂。
如前所述本发明的试剂盒,其中外显子5的检测试剂能够检测tp53基因外显子5中157、158、175位点的突变;外显子7的检测试剂能够检测tp53基因外显子7中244、245、248位点的突变;外显子8的检测试剂能够检测tp53基因外显子8中268、273、275、282位点的突变。
如前所述本发明的试剂盒,其中针对每种外显子的检测试剂都包括一组探针和引物,所述探针包括供体探针和受体探针,其中供体探针3’端标记有荧光供体,所述受体探针的5’端标记有荧光受体、3’端进行磷酸化修饰;所述引物包括上游引物和下游引物,上游引物和下游引物分别位于探针结合位点的两侧。
如前所述本发明的试剂盒,其特征在于外显子5的检测试剂包括seqidno:1-2、外显子7的检测试剂包括seqidno:3-4、外显子8的检测试剂包括seqidno:5-6。
如前所述本发明的试剂盒,其特征在于外显子5的检测试剂还包括seqidno:7-8、外显子7的检测试剂还包括seqidno:9-10、外显子8的检测试剂还包括seqidno:11-12。
发明详述
除另有说明以外,本发明所用术语均是本领域常规的含义,对术语的解释可参考例如萨姆布鲁克等主编的《分子克隆(第三版)》。对本发明的技术内容进行详述如下:
本发明设计至少3对探针和3对引物以及mastermix,用于检测tp53基因外显子5中的位点突变、外显子7中的位点突变、外显子8中的位点突变。三型突变之和约占膀胱癌患者的85%;且检测方法试剂简单,价格低廉,而且试剂盒设计最大限度地减少了需要现场配制反应成分,所有步骤和相应试剂浓度,反应参数和判定标准均经过优化和验证;反应体系简单,最大限度地减少了影响因素。本发明提供的检测方法具有精准、操作简单以及价格低廉等特点,为临床医学上从尿液沉淀细胞中快速检测膀胱癌奠定了基础。
第一方面,本发明提供了一种检测tp53基因外显子5中的位点突变、外显子7中的位点突变、外显子8中的位点突变的试剂盒,所述试剂盒含有特异性识别tp53基因外显子突变的荧光标记探针。
本发明中,当检测tp53基因存在突变时,突变特异性探针与基因组dna特异性结合,而野生型dna则因为有单点的不配对,形成“泡”,从而显示较低的熔点。
根据本发明,所述试剂盒含有特异性识别tp53基因外显子5中的位点突变、外显子7中的位点突变、外显子8中的位点突变或其组合的荧光标记探针。
具体地,所述试剂盒可以只含有特异性识别tp53基因外显子5中的位点突变的荧光标记探针,可以只含有特异性识别tp53基因外显子7中的位点突变的荧光标记探针,也可以只含有特异性识别tp53基因外显子8中的位点突变的荧光标记探针,或者是同时含有特异性识别三种或其中两型位点突变的荧光标记探针。
本发明中,当采用同时含有识别tp53特异性三型外显子基因突变的三对荧光标记探针时,相比采用单一的荧光标记探针,其能够大大增加对膀胱癌tp53基因外显子突变的检测效率,并提高检测准确率,使检测准确率接近99%。
根据本发明,所述荧光标记探针含有供体探针和受体探针,例如特异性识别tp53基因外显子5中的位点突变的供体探针,含有特异性识别tp53基因外显子5中的位点突变的受体探针;特异性识别外显子7中的位点突变的供体探针,特异性识别外显子7中的位点突变的受体探针;含有特异性识别外显子8中的位点突变的供体探针,特异性识别外显子8中的位点突变的受体探针。
本发明中特异性识别tp53基因外显子5中的位点突变的供体探针,其核苷酸序列含有如seqidno.1所示的片段,所述特异性识别tp53基因外显子5中的位点突变的受体探针的核苷酸序列含有如seqidno.2所示的片段;
本发明中特异性识别tp53基因外显子7中的位点突变的供体探针的核苷酸序列含有如seqidno.3所示的片段,所述特异性识别外显子7中的位点突变的受体探针的核苷酸序列含有如seqidno.4所示的片段。
本发明中特异性识别tp53基因外显子8中的位点突变的供体探针的核苷酸序列含有如seqidno.5所示的片段,所述特异性识别外显子8中的位点突变的受体探针的核苷酸序列含有如seqidno.6所示的片段。
本发明中,所述seqidno.1-6荧光标记探针含有的氨基酸序列优选采用如下序列:
seqidno.1:5’-aagcgcctcacaacctccgtcatgtgct-flc-3’
seqidno.2:5’-lc640-tgcttgtagatggccatggcgcggacg-phos-3’.
seqidno.3:5’-ggagtcttccagtgtgatgatggtg-flc-3’
seqidno.4:5’-lc640-tgggcctccggttcatgccgc-phos-3’
seqidno.5:5’-gccggtctctcccaggacaggcac-flc-3’
seqidno.6:5’-lc640-cgcacctcaaagctgttccgtccc-phos-3’
此外本发明中特异性识别tp53基因外显子5中的位点突变的核苷酸序列含有如seqidno.7-8所示的片段
本发明中特异性识别tp53基因外显子7中的位点突变的核苷酸序列含有如seqidno.9-10所示的片段
本发明中特异性识别tp53基因外显子8中的位点突变的核苷酸序列含有如seqidno.11-12所示的片段
本发明中含有的检测tp53基因三型突变的特异性引物序列如下;
seqidno.7:5’-tatctgagcagcgctcatggtg-3’
seqidno.8:5’-ccctgactttcaactctgtctcc-3’
seqidno.9:5’-cctaggttggctctgactgta-3’
seqidno.10:5’-gtggcaagtggctcctga-3’
seqidno.11:5’-ccttactgcctcttgcttctc-3’
seqidno.12:5’-cttgcggagattctcttcctc-3’
根据本发明,所述试剂盒含有检测tp53的mastermix,例如还含有实时荧光定量pcr技术中涉及到的onetaqdna聚合酶、dntps。本发明中的mastermix试剂浓度和反应参数均经过优化和验证,并含有阳性和阴性对照dna样本。
本发明中,所有试剂包括荧光标记探针、特异性引物、pcr缓冲液和dntps(除酶之外)均已混合,作为“主液”,不需要单独配制,极大地方便用户操作。
本发明中所述mastermix为4×浓度,其包括优化后的pcr反应所需缓冲液、dntps和onetaqdna聚合酶。
根据本发明,所述dntps的浓度为0.05-1μm,例如可以是0.05μm、0.06μm、0.08μm、0.1μm、0.2μm、0.3μm、0.4μm、0.5μm、0.6μm、0.7μm、0.8μm、0.9μm或1μm,以及上述数值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
本发明中,所述dntps的浓度优选为0.1-0.8μm,进一步优选为0.2μm。
根据本发明,所述dna聚合酶的浓度为0.5-8u/mg,例如可以是0.5u/mg、0.6u/mg、0.7u/mg、0.8u/mg、1u/mg、1.2u/mg、1.5u/mg、2u/mg、2.5u/mg、3u/mg、3.5u/mg、4u/mg、4.5u/mg、5u/mg、5.5u/mg、6u/mg、6.5u/mg、7u/mg、7.5u/mg或8u/mg,以及上述数值之间的具体点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
本发明中,所述dna聚合酶优选为onetaqdna聚合酶,其浓度优选为0.5-8u/mg,进一步优选为1.5u/mg。
根据本发明,所述试剂盒还含有介绍该试剂盒的使用说明书。
第二方面,本发明提供了一种利用如第一方面所述的用于检测tp53基因突变的试剂盒在非疾病诊断和治疗目的中检测tp53基因突变的方法,其包括以下步骤:
(1)从筛选的病例尿液样本中离心提取尿液细胞;
(2)从尿液细胞中提取全基因组dna5-20ng,利用含有seqidno.7-8,seqidno.9-10,seqidno.11-12所示片段的特异性引物对所述模板dna进行实时pcr扩增;
(3)将步骤(2)扩增后的片段分别加入含有如seqidno.1-2,seqidno.3-4,seqidno.5-6所示片段的荧光标记探针或其混合物中进行加温熔解;
(4)通过得到的pcr产物的熔解曲线来判断tp53基因的突变情况。
根据本发明,所述检测tp53基因外显子突变的方法主要用于膀胱癌的诊断和治疗,在具体检测时,可以从尿液离心沉淀细胞中检测tp53基因外显子5、7、8的特异性突变,也可以是从膀胱组织活检标本中实现对tp53基因外显子5、7、8的特异性突变的检测,对于检测样品以及模板dna的来源也可以采用其它途径。
本发明中,步骤(1)所述待测样品优选为尿液细胞离心沉淀物和/或膀胱组织,因此,所述模板dna优选来自于尿液细胞沉淀物和/或膀胱组织活检标本。
根据本发明,步骤(2)所述实时pcr扩增的条件为:
(a)95℃预变性4min,1循环;
(b)94℃变性20s、56℃退火20s、68℃延伸40s,50个循环;
(c)37℃延伸30s,1循环。
根据本发明,步骤(3)所述加温熔解的条件为:95℃1min,62℃30s,45℃30s,40℃2min,再以0.1℃/秒的速度升高至70℃。
本发明中,所述试剂盒由特异性dna引物和荧光标记的激发探针与被激发探针构成,被激发探针3’磷酸化以防止其延伸,在pcr反应过程中,如无目标点突变,则探针与dna100%互补,从而表现为一定的温度融解。
根据本发明,步骤(4)所述判断tert基因的突变情况的方法为:
当预测熔点(55℃)±2℃范围内出现熔融曲线峰,则待测样品含有tp53三型突变或其组合突变细胞克隆。
当预测熔点(61.8℃)±2℃范围内出现熔融峰,而(55℃)±2℃缺乏熔融曲线峰时,则待测样本为含有野生型细胞群。
当多个熔融曲线峰存在,分别位于(55℃)±2℃和(61.8℃)±2℃,则待测样本含有混合细胞群,即含有相应突变细胞克隆以及野生型非突变细胞。
第三方面,本发明提供了如第一方面所述的用于检测tp53基因外显子三型突变的试剂盒在用于非疾病诊断和治疗目的的检测tp53基因外显子5中的位点突变、外显子7中的位点突变、外显子8中的位点突变或其组合突变中的应用。
本发明中,所述tp53基因外显子三型突变的试剂盒在用于非疾病诊断和治疗目的的检测tp53基因外显子5中的位点突变、外显子7中的位点突变、外显子8中的位点突变或其组合的位点突变占所有膀胱癌患者的85%以上。
第四方面,本发明提供tp53基因外显子5、7、8的序列,其中外显子5的序列包括序列表中seqidno:13、外显子7的序列包括序列表中seqidno:14、外显子8的序列包括序列表中seqidno:15。
第五方面,本发明提供tp53基因外显子5、7、8的扩增片段,在制备膀胱癌诊断试剂盒中的用途,所述基因外显子5、7、8的扩增引物分别为seqidno;7-8、seqidno:9-10、seqidno:11-12。
本发明所述tp53基因外显子5、7、8的扩增片段可以在膀胱癌诊断试剂盒中作为对照。
与现有技术相比,本发明的优点在于:
(1)经过前期大规模临床数据统计分析,选择以外显子5中157、158、175位点突变、外显子7中244、245、248位点突变、外显子8中268、273、275、282位点突变为检测靶标,开发出对上述三个外显子同时进行检测筛选膀胱癌的方法。三型突变的组合,覆盖率高,有效弥补了单一靶标荧光定量pcr的不足。本发明所述方法在膀胱癌群体中的阳性率超过了85%,阳性准确率超过98%、阴性结果准确率超过97%,针对上述位点进行检测能够有效的实现膀胱癌的筛选。
(2)融合了普通荧光pcr检测和多重荧光pcr检测的优点。引物探针的设计中采用了相同的荧光标记方案,同时使扩增产物大小相似,既避免了多重荧光pcr中采用多种荧光标记的技术复杂性,又确保了对多种靶标的同时检测。只要三个外显子中任意一个携带突变,就能获得阳性结果。(3)结果判断简单、明确。由于本申请虽然针对三个外显子靶标进行检测,三个外显子靶标中1个、2个或3个存在突变都表现为阳性结果,没有突变则为阴性结果。不需要对每个靶标的检测结果引入复杂的结果分析模型进行分析即可做出诊断,特别适用于快速筛查。
附图说明
图1:为本发明试剂盒检测原理图;
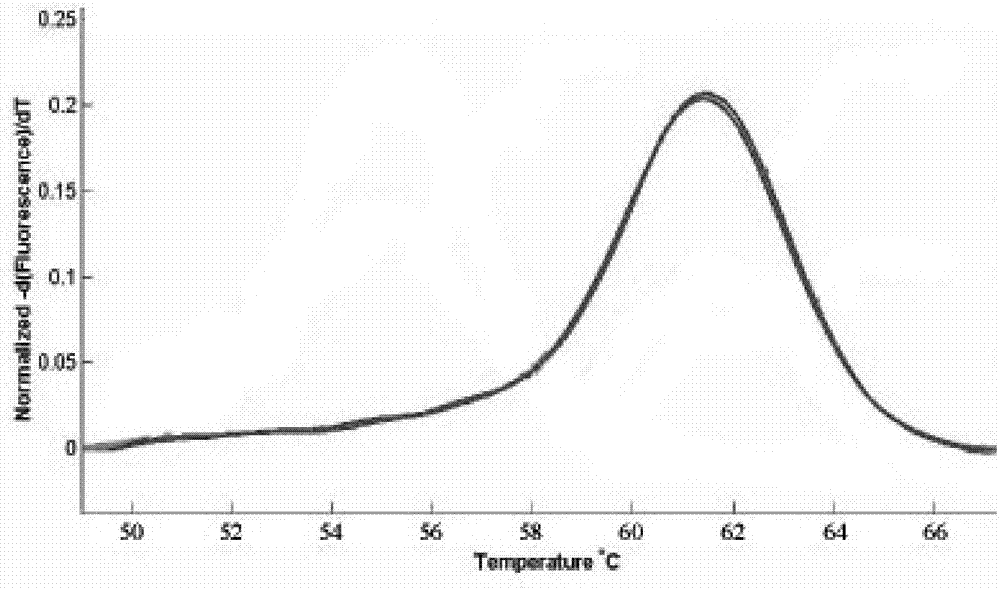
图2:阳性对照样本(膀胱癌细胞系)的检测结果,出现61.8℃的熔融曲线峰;
图3:正常尿液样本检测结果,出现55℃的熔融曲线峰;
图4:早期膀胱癌患者尿液样本检测结果,形成两个分别对应55℃、61.8℃的熔融曲线峰。
具体实施方式
以下结合具体实施例,进一步阐述本发明。这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。除非另行定义,文中所使用的所有专业与科学用语与本领域熟练人员所熟悉的意义相同。此外,任何与所记载内容相似或均等的方法及材料皆可应用于本发明方法中。文中所述的较佳实施方法与材料仅作示范之用。
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
实施例1
用于检测tp53基因启动子突变的试剂盒,其包括:
(1)特异性识别tp53基因外显子5中157、158、175位点的突变设计的荧光标记探针,其供体探针和受体探针的核苷酸序列如下:
外显子5突变的供体探针:
5’-aagcgcctcacaacctccgtcatgtgct-flc-3’
外显子5突变的受体探针:
5’-lc640-tgcttgtagatggccatggcgcggacg-phos-3’.
(2)检测tp53基因外显子5中突变的特异性引物,其核苷酸序列如下:
上游引物:5’-tatctgagcagcgctcatggtg-3’
下游引物:5’-ccctgactttcaactctgtctcc-3’
(3)mastermix,其包括:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶和10ng的dna模板;
(4)使用说明书一份。
实施例2
用于检测tp53基因外显子7中244、245、248位点突变的试剂盒,其包括:
(1)特异性识别tp53基因外显子7中244、245、248位点突变的荧光标记探针,其供体探针和受体探针的核苷酸序列如下:
外显子7的位点突变的供体探针:5’-ggagtcttccagtgtgatgatggtg-flc-3’
外显子7的位点突变的受体探针:5’-lc640-tgggcctccggttcatgccgc-phos-3’
(2)检测tp53基因外显子7中位点突变的特异性引物,其核苷酸序列如下:
上游引物:5’-cctaggttggctctgactgta-3’
下游引物:5’-gtggcaagtggctcctga-3’
(3)mastermix,其包括:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶和10ng的dna模板;
(4)使用说明书一份。
实施例3
用于检测tp53基因外显子8中268、273、275、282位点突变的试剂盒,其包括:
(1)特异性识别tp53基因外显子8中268、273、275、282的位点突变的荧光标记探针,其供体探针和受体探针的核苷酸序列如下:
外显子8的位点突变的供体探针:5’-gccggtctctcccaggacaggcac-flc-3’
外显子8的位点突变的受体探针:5’-lc640-cgcacctcaaagctgttccgtccc-phos-3’
(2)检测tp53基因外显子8中的位点突变的特异性引物,其核苷酸序列如下:
上游引物:5’-ccttactgcctcttgcttctc-3’
下游引物:5’-cttgcggagattctcttcctc-3’
(4)mastermix,其包括:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶和10ng的dna模板;
(5)使用说明书一份。
实施例4
与实施例3相比,除mastermix包括:1×pcr缓冲液、0.05μm的dntps、0.8u/mg的onetaqdna聚合酶和15ng的dna模板以外,其它与实施例3相同。
实施例5
与实施例3相比,除mastermix包括:1×pcr缓冲液、1μm的dntps、0.5u/mg的onetaqdna聚合酶和20ng的dna模板以外,其它与实施例3相同。
实施例6
与实施例3相比,除mastermix包括:1×pcr缓冲液、0.6μm的dntps、8u/mg的onetaqdna聚合酶和5ng的dna模板以外,其它与实施例3相同。
实施例7
利用实施例1的试剂盒检测tp53基因外显子5中157、158、175位点的突变,包括以下步骤:
(1)提取待测样品的尿液,离心提取尿液细胞,提取细胞全dna,利用含有seqidno.7-8所示片段的特异性引物对模板dna进行实时pcr扩增;
上游引物:5’-tatctgagcagcgctcatggtg-3’(seqidno.7);
下游引物:5’-ccctgactttcaactctgtctcc-3’(seqidno.8);
pcr扩增反应体系如下:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶、10ng的dna模板、特异性引物、供体探针和受体探针;
pcr反应条件如下:
(2)将步骤(1)扩增后的片段加入特异性识别tp53基因外显子5第157、158、175位点突变的荧光标记探针进行加温熔解;
外显子5突变的供体探针:5’-aagcgcctcacaacctccgtcatgtgct-flc-3’
外显子5突变的受体探针:5’-lc640-tgcttgtagatggccatggcgcggacg-phos-3’.
加温熔解反应条件如下:
(3)通过得到的pcr产物的熔解曲线来判断tp53基因外显子5中的位点突变情况。
检测原理如图1所示,从图1可以说明当检测tp53外显子5中的位点突变时,突变特异性探针与基因组dna特异性结合,而野生型dna则因为有单点的不配对,而形成“泡”,从而显示较低的熔点。
如果目的基因tp53外显子5无点突变存在,则在探针与dna之间出现单个非互补硷基,融解温度下降。
实施例8
利用实施例2的试剂盒检测tp53基因外显子7中244、245、248位点突变,包括以下步骤:
(1)提取待测样品的尿液,离心提取尿液细胞,提取细胞全dna,利用含有seqidno.9-10所示片段的特异性引物对模板dna进行实时pcr扩增;
上游引物:5’-cctaggttggctctgactgta-3’(seqidno.9);
下游引物:5’-gtggcaagtggctcctga-3’(seqidno.10);
pcr扩增反应体系如下:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶、10ng的dna模板、特异性引物、供体探针和受体探针;
pcr反应条件与实施例7中相同。
(2)将步骤(1)扩增后的片段加入特异性识别tp53基因外显子7中244、245、248位点突变的荧光标记探针进行加温熔解;
外显子7的突变的供体探针:5’-ggagtcttccagtgtgatgatggtg-flc-3’
外显子7的突变的受体探针:5’-lc640-tgggcctccggttcatgccgc-phos-3’
加温熔解反应条件与实施例7中相同
(3)通过得到的pcr产物的熔解曲线来判断tp53基因外显子7中的位点突变情况。
实施例9
利用实施例3的试剂盒检测tp53基因外显子8中268、273、275、282的位点突变,包括以下步骤:
(1)提取待测样品的尿液,离心提取尿液细胞,提取细胞全dna,利用含有seqidno.11-12所示片段的特异性引物对模板dna进行实时pcr扩增;
上游引物:5’-ccttactgcctcttgcttctc-3’(seqidno.11);
下游引物:5’-cttgcggagattctcttcctc-3’(seqidno.12);
pcr扩增反应体系如下:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶、10ng的dna模板、特异性引物、供体探针和受体探针;
pcr反应条件与实施例7中相同。
(2)将步骤(1)扩增后的片段加入特异性识别tp53基因外显子8中268、273、275、282的位点突变的荧光标记探针进行加温熔解;
外显子8的突变的供体探针:5’-gccggtctctcccaggacaggcac-flc-3’
外显子8的突变的受体探针:5’-lc640-cgcacctcaaagctgttccgtccc-phos-3’
加温熔解反应条件与实施例7中相同。
(3)通过得到的pcr产物的熔解曲线来判断tp53基因外显子8中的位点突变情况。
实施例10
联合检测tp53基因外显子5、7、8突变的试剂盒。
(1)特异性识别tp53基因外显子5中157、158、175位点突变、外显子7中244、245、248位点突变、外显子8中268、273、275、282位点突变的荧光标记探针。
外显子5的位点突变的供体探针:
5’-aagcgcctcacaacctccgtcatgtgct-flc-3’
外显子5的位点突变的受体探针:
5’-lc640-tgcttgtagatggccatggcgcggacg-phos-3’.
外显子7的突变的供体探针:
5’-ggagtcttccagtgtgatgatggtg-flc-3’
外显子7的突变的受体探针:
5’-lc640-tgggcctccggttcatgccgc-phos-3’
外显子8的突变的供体探针:
5’-gccggtctctcccaggacaggcac-flc-3’
外显子8的突变的受体探针:
5’-lc640-cgcacctcaaagctgttccgtccc-phos-3’
所述6种荧光标记探针混合包装于同一容器中。
(2)同时扩增tp53基因外显子7、10、15突变片段的试剂盒。
外显子5上游引物:5’-tatctgagcagcgctcatggtg-3’;
外显子5下游引物:5’-ccctgactttcaactctgtctcc-3’;
外显子7上游引物:5’-cctaggttggctctgactgta-3’
外显子7上游引物:5’-gtggcaagtggctcctga-3’
外显子8上游引物:5’-ccttactgcctcttgcttctc-3’
外显子8上游引物:5’-cttgcggagattctcttcctc-3’
所述三对引物混合包装于同一容器中。
(3)mastermix,其包括:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶和10ng的dna模板;
(4)使用说明书一份。
实施例11
利用实施例10的试剂盒检测tp53基因点突变进行检测,包括以下步骤:
(1)提取待测样品的尿液,离心提取尿液细胞,提取细胞全dna,利用含有特异性引物对模板dna进行实时pcr扩增;
pcr扩增反应体系如下:1×pcr缓冲液、0.2μm的dntps、1.5u/mg的onetaqdna聚合酶、10ng的dna模板、特异性引物、供体探针和受体探针;
pcr反应条件如下:
(2)将步骤(1)扩增后的片段加入特异性荧光标记探针进行加温熔解;
加温熔解反应条件如下:
(3)通过得到的pcr产物的熔解曲线来判断tp53基因的位点突变情况。
检测原理如图1所示,从图1可以说明当检测tp53存在位点突变时,突变特异性探针与基因组dna特异性结合,而野生型dna则因为有单点的不配对,而形成“泡”,从而显示较低的熔点。
检测结果如图2-4所示,如果目的基因tp53上存在上述点突变,探针与扩增产物之间完全配对熔解温度较高,为61.8±2℃;如果目的基因tp53无上述点突变存在,则在探针与dna之间出现单个非互补硷基,融解温度较低,为55±2℃。如果同时出现61.8℃±2的熔解峰和55±2℃的熔解峰,则表明样本中既存在tp53上述位点发生突变的癌变细胞,也存在tp53上述位点未发生突变的野生型正常细胞。
实施例12:
临床样本双盲筛检测
采集68例临床确诊患有早期膀胱癌患者的尿液样本,以35例正常人体检留存尿液样本作为对照,进行检测。以实施例7的方法进行检测,检出32例阳性样本,检出率为47.06%;以实施例8的方法进行检测,检出15例阳性样本,检出率为22.06%;以实施例9的试剂盒进行检测,检出44例阳性样本,检出率为64.70%。实施例7-9的方法,未检出假阳性结果。采用单外显子进行检测,虽然阳性准确率高,但检出率较低,难以达到临床筛查的要求。
以实施例11的方法进行检测,检出59例阳性样本,其中1例为假阳性。阳性样本检出率为85.29%(58/68),假阳性率为1.69%(1/59),阳性结果符合率/准确率为98.31%(58/59),阴性结果符合率/准确率为97.14%(34/35)。上述结果表明,实施例10-11中同时对tp53基因外显子5、7、8的突变进行检测的方法和试剂盒是最优选的技术方案,相互之间干扰小,准确率高、检出率符合临床要求,适合于膀胱癌的早期筛查。
上述说明并非对本发明的限制,本发明也并不限于上述举例。本技术领域的普通技术人员在本发明的实质范围内,作出的变化、改型、添加或替换,也应属于本发明的保护范围,本发明的保护范围以权利要求书为准。
序列表
<110>申请人名称
<120>一种检测tp53基因突变以诊断膀胱癌的方法及试剂盒
<160>15
<170>patentinversion3.5
<210>1
<211>28
<212>dna
<213>人工序列
<400>1
aagcgcctcacaacctccgtcatgtgct28
<210>2
<211>27
<212>dna
<213>人工序列
<400>2
tgcttgtagatggccatggcgcggacg27
<210>3
<211>25
<212>dna
<213>人工序列
<400>3
ggagtcttccagtgtgatgatggtg25
<210>4
<211>21
<212>dna
<213>人工序列
<400>4
tgggcctccggttcatgccgc21
<210>5
<211>24
<212>dna
<213>人工序列
<400>5
gccggtctctcccaggacaggcac24
<210>6
<211>24
<212>dna
<213>人工序列
<400>6
cgcacctcaaagctgttccgtccc24
<210>7
<211>22
<212>dna
<213>人工序列
<400>7
tatctgagcagcgctcatggtg22
<210>8
<211>23
<212>dna
<213>人工序列
<400>8
ccctgactttcaactctgtctcc23
<210>9
<211>21
<212>dna
<213>人工序列
<400>9
cctaggttggctctgactgta21
<210>10
<211>18
<212>dna
<213>人工序列
<400>10
gtggcaagtggctcctga18
<210>11
<211>21
<212>dna
<213>人工序列
<400>11
ccttactgcctcttgcttctc21
<210>12
<211>21
<212>dna
<213>人工序列
<400>12
cttgcggagattctcttcctc21
<210>13
<211>300
<212>dna
<213>外显子5
<400>13
ctgccgtcttccagttgctttatctgttcacttgtgccctgactttcaactctgtctcct60
tcctcttcctacagtactcccctgccctcaacaagatgttttgccaactggccaagacct120
gccctgtgcagctgtgggttgattccacacccccgcccggcacccgcgtccgcgccatgg180
ccatctacaagcagtcacagcacatgacggaggttgtgaggcgctgcccccaccatgagc240
gctgctcagatagcgatggtgagcagctggggctggagagacgacagggctggttgccca300
<210>14
<211>240
<212>dna
<213>外显子7
<400>14
gcttgccacaggtctccccaaggcgcactggcctcatcttgggcctgtgttatctcctag60
gttggctctgactgtaccaccatccactacaactacatgtgtaacagttcctgcatgggc120
ggcatgaaccggaggcccatcctcaccatcatcacactggaagactccaggtcaggagcc180
acttgccaccctgcacactggcctgctgtgccccagcctctgcttgcctctgacccctgg240
<210>15
<211>300
<212>dna
<213>外显子8
<400>15
ggttgggagtagatggagcctggttttttaaatgggacaggtaggacctgatttccttac60
tgcctcttgcttctcttttcctatcctgagtagtggtaatctactgggacggaacagctt120
tgaggtgcgtgtttgtgcctgtcctgggagagaccggcgcacagaggaagagaatctccg180
caagaaaggggagcctcaccacgagctgcccccagggagcactaagcgaggtaagcaagc240
aggacaagaagcggtggaggagaccaagggtgcagttatgcctcagattcacttttatca300
- 还没有人留言评论。精彩留言会获得点赞!