一种大环内酯类抗生素中空多孔型分子印迹聚合物的制备方法及应用与流程
本发明涉及分析化学前处理领域,具体说是应用于测定动物源食品中大环内酯类抗生素残留量的高选择性分离的中空多孔型分子印迹聚合物的制备方法及应用。
背景技术:
大环内酯类抗生素是一类亲脂性的抗生素,在治疗人类和动物由革兰氏阴性细菌和革兰氏阳性细菌感染所诱发的一系列疾病方面发挥着重要作用。由于其可作为动物生长促进剂,因此动物源食品中大环内酯类抗生素的滥用及残留问题非常普遍。众所周知,大环内酯类抗生素具有诸如急性中耳炎、过敏性鼻炎、肥厚型幽门梗阻等副作用。为了确保动物源食品的安全,许多国家和监管机构均建立了食品基质中大环内酯类抗生素的最大残留量限定,因此开发有效的食品中的大环内酯类抗生素的分析和定量检测技术是非常必要的。
由于食物基质非常复杂,存在着许多干扰性的组分,因此食品中痕量大环内酯类抗生素的定量测定是极为困难的,合理的样品制备方法是消除基体干扰,提高化合物响应的关键。目前已有许多用于食品基质中大环内酯类抗生素提取方法的报道,这些方法包括固相萃取(solid-phaseextraction,spe)、液膜支持萃取、基质分散固相萃取、加压液体萃取、quechers和固相微萃取等。在这些前处理方法中,spe作为一种经济实用的前处理技术尤为适合食品基质中痕量化合物的富集检测。但是传统的spe吸附剂常受到共存组分的干扰,导致萃取效率较低。如何制备化学和热稳定性高、使用寿命长、选择性好的新型固相萃取剂一直是人们所关注的热点。
分子印迹聚合物(molecularimprintingpolymers,mips)是指目标分子(模板分子)与功能单体通过共价键或非共价键作用预组装,与交联剂共聚制备得到的聚合物。mips是对模板分子具有特定识别能力的一种高选择性分离材料。mips可以特异性从复杂样品中选择性地“锁定”并富集特定目标化合物,由于其与目标化合物之间具有强烈的相互作用,使其特别适用于痕量化合物的选择性富集,而且其制备方法简单、性能稳定、环境适应性强,因此mips作为一种特效的固相萃取吸附材料为食品安全分析提供了极大的方便。近年来,科研工作者制备了许多新型的mips,如用于水样的水兼容型mips,金属离子介导mips,磁性mips,多壁碳纳米管-分子印迹聚合物(mwnts-mips),表面分子印迹聚合物(surfacemips)等。虽然表面mips可以解决传统印迹技术中存在的模板泄漏和传质慢(平衡时间为12-24h)等问题,但是没有任何识别位点的固体核,降低了分子印迹材料单位质量结合目标分子的能力。为了克服这一缺点,中空多孔型分子印迹的制备方法被提出,中空多孔印迹聚合物的中空聚合物壳很薄,降低传质阻力,并使其具有非常大的比表面积。高密度的识别位点散布在其表面,可提高其结合能力。鉴于中空多孔印迹聚合物的高选择性的识别能力和富集浓缩能力,若以大环内酯类抗生素为模板分子,制备基于中空多孔印迹聚合物的固相萃取吸附剂将有望实现对复杂食品基质中痕量大环内酯类抗生素样品的选择性富集和净化,可以最大程度的消除基质效应从而提高样品检测限。迄今为止,尚未见有关大环内酯类抗生素中空多孔印迹聚合物制备及其应用的报道。
因此,一种利用螺旋霉素为模板,介孔硅颗粒(mcm-41)为牺牲核心制备中空多孔型大环内酯类抗生素分子印迹聚合物并将其应用于分散固相萃取同时富集动物源食品中多种大环内酯类抗生素的方法被提出。
技术实现要素:
本发明的目的在于提供一种大环内酯类抗生素中空多孔型分子印迹聚合物的制备方法,该分子印迹聚合物对具有的十四至十六元内酯环结构的大环内酯类抗生素均有良好的识别性能。
本发明技术方案如下:
一种大环内酯类抗生素中空多孔型分子印迹聚合物的制备方法,其特征在于按如下步骤进行:
(1)步骤1、合成介孔硅微球:将81~405mmol的氟化铵(nh4f)和5~25mmol的十六烷基三甲基溴化铵(ctab)溶解在一定量的蒸馏水中在80℃水浴搅拌,待其完全溶解为无色透明溶液后,逐滴加入9~45ml的正硅酸四乙酯(teos),体系中各物质的物质的量比为nsio2∶nctab∶nnh4f=1∶0.125∶2,继续搅拌反应4~8h,经离心、水洗、醇洗、干燥之后,所得到的产物在空气气氛下,以5℃/min的速率升温至550℃,焙烧6h得到mcm-41样品;
(2)步骤2、表面印迹聚合物的合成:称取0.25~1.25mmol的模板分子溶于16~80ml乙腈和4~20ml甲醇组成的混合溶剂中(所述的模板分子为螺旋霉素),加入功能单体1~5mmol(所述的功能单体为非共价化合物),将此混合溶液于室温下超声,使模板分子与功能单体充分混合;然后加入交联剂5~25mmol(所述的交联剂为多烯或烯酸酯类结构的化合物),再加入步骤1得到的mcm-41介孔硅微球0.5~2.5g和热引发剂偶氮二异腈150~750mg,超声混匀、氮气脱氧,将反应液置于60℃水浴中并在1000rpm转速下搅拌加热24h,淡黄色的产物经离心水洗、醇洗后,溶于装有体积比为8∶1的甲醇-乙酸混合液的锥形瓶中,振荡洗脱聚合物中的模板分子,乙醇洗涤,干燥至恒重,得到螺旋霉素表面印迹聚合物(mmips);
(3)步骤3、中空多孔印迹材料的合成:将步骤2得到的表面印迹聚合物(mmips)置于50ml聚四氟乙烯离心管中,加入10%浓氢氟酸-乙醇溶液至浸没为止,涡旋震荡5min,静置12h,以移除mcm-41介孔硅微球,离心、水洗至中性,干燥至恒重,得到本方法对目标分子具有特异选择性的中空多孔型分子印迹聚合物(hpmips)用来富集和选择性分离动物源食品中痕量的大环内酯类药物;
所述的反应体系中加入了mcm-41介孔硅微球作为分子印迹表面聚合的核心并牺牲该核心;
所述的功能单体可以是甲基丙烯酸、甲基丙烯酰胺或4-乙烯基吡啶的任一种;
所述的硅烷化试剂交联剂为三羟甲基丙烷三丙烯酸酯、n,n’-亚甲基双丙烯酰胺或者乙二醇二甲基丙烯酸酯的任一种;
所述的模板分子∶功能单体∶交联剂的摩尔比为1∶4∶20;
所述的模板分子的洗脱溶剂每5~8h更换一次,反复9次;
与已有技术相比,本发明有益效果体现在:
1.将分子印迹聚合物和分散固相萃取(dspe)的优点有效结合起来,使该吸附剂不仅具有分子印迹聚合物的高选择性,同时具有dspe样品用量少、处理时间短、操作简单、试剂消耗少等优点。
2.以mcm-41型介孔硅为牺牲支撑模板,充分利用了其比表面积大、孔径分部均匀、孔体积大的特点,使制备所得的表面印迹聚合物具有非常大的比表面积,高密度的识别位点,可提高印迹材料的吸附能力,同时小粒径牺牲模板(~100nm)的使用,可提高聚合物层的厚度,从而降低了使用过程中机械作用对材料所产生的破坏,提高了材料的使用寿命。
3.利用hf对硅胶的腐蚀作用,移除了没有任何识别位点的固体核(mcm-41核心)后所得的中空多孔印迹聚合物具有薄壳,进一步提高了印迹材料的传质速度和单位质量结合目标分子的能力。
4.该分子印迹聚合物对具有十四至十六元内酯环结构的大环内酯类抗生素均有良好的识别性能,提取回收率高,与hplc-ms/ms联用可同时对多种目标分子进行检测,加宽了目标分子的检测范围。
附图说明
图1为hpmips和mmips的热重曲线图
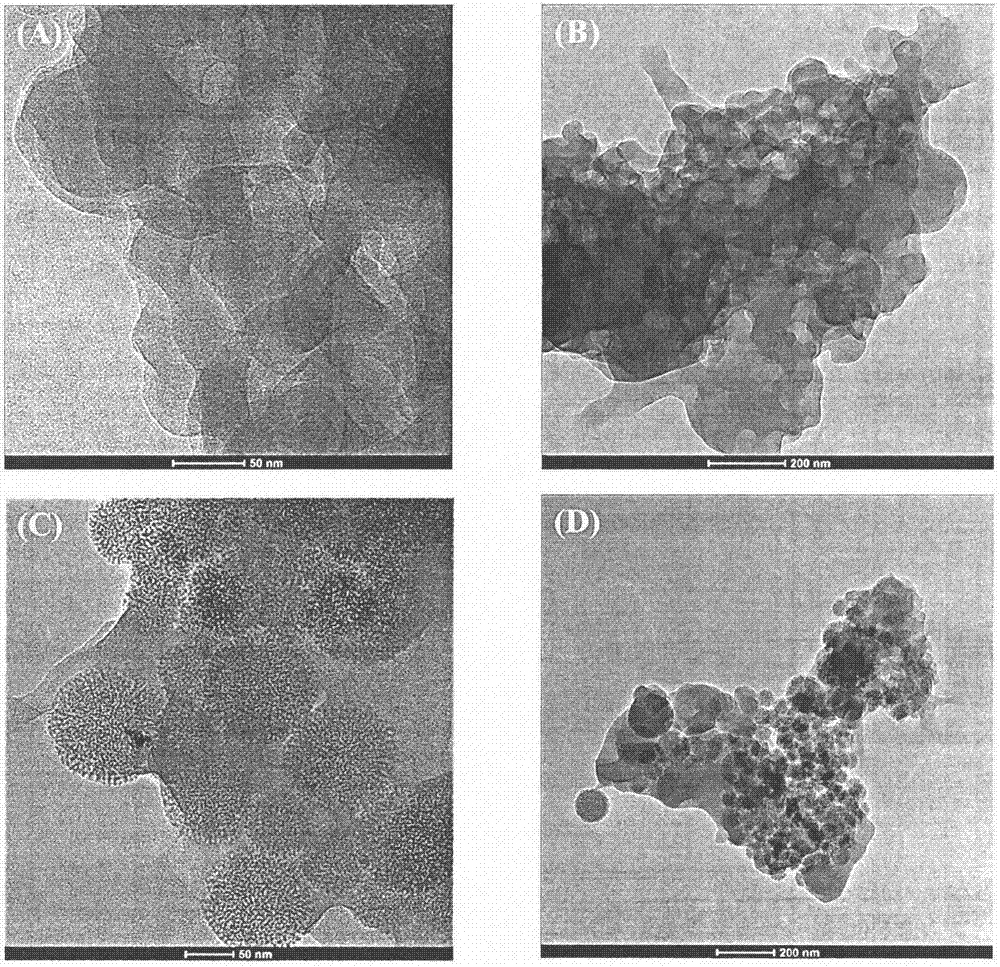
图2为hpmips(a)(b)和mmips(c)(d)的扫描电镜图
图3为hpmips、hpnips、mmips、solid-mips和solid-nips对螺旋霉素的静态吸附图
图4为hpmips与hpnips对七种大环内酯类抗生素的富集效果图
图5为hpmips对蜂蜜样品富集浓缩效果的色谱图
具体实施方式
以下通过具体实施例对本发明技术方案做进一步说明。实施例中的试验步骤和试验所用产品及试验器材,若无特别说明均为本领域常规技术手段、市购常规产品及公知仪器。
实施例1.大环内酯类抗生素中空多孔型分子印迹聚合物的制备方法
(1)步骤1、合成介孔硅微球:将40.5mmol的nh4f和2.5mmolctab溶解在250ml蒸馏水中,在80℃水浴中加热,并在1000rpm转速下搅拌,待其完全溶解为无色透明溶液后,逐滴加入4.5mlteos,继续加热搅拌反应6h,经离心、水洗、醇洗、干燥之后,所得到的产物在空气气氛下,以5℃/min的速率升温至550℃,焙烧6h得到mcm-41样品;
(2)步骤2、表面印迹聚合物的合成:称取0.25mmol的螺旋霉素溶于16ml乙腈和4ml甲醇组成的混合溶剂中,加入1mmol甲基丙烯酸,将此混合溶液于室温下超声,使模板分子与功能单体充分混合;然后加入交联剂乙二醇二甲基丙烯酸酯5mmol,再加入步骤1得到的mcm-41介孔硅微球0.5g和热引发剂偶氮二异腈150mg,超声混匀、氮气脱氧,将反应液置于60℃水浴中并在1000rpm转速下搅拌加热24h,淡黄色的产物经离心水洗、醇洗后,溶于装有体积比为8∶1的甲醇-乙酸混合液的锥形瓶中,振荡72h(每8h换一次洗脱液),洗脱聚合物中的模板分子,乙醇洗涤,干燥至恒重,得到螺旋霉素表面印迹聚合物(mmips);
(3)步骤3、中空多孔印迹材料的合成:将步骤2得到的表面印迹聚合物(mmips)置于50ml聚四氟乙烯离心管中,加入10%浓氢氟酸-乙醇溶液至浸没为止,涡旋震荡5min,静置12h,以移除mcm-41介孔硅微球,离心水洗至中性,干燥至恒重,得到本方法对目标分子具有特异选择性的中空多孔型分子印迹聚合物(hpmips)用来富集和选择性分离动物源食品中痕量的大环内酯类药物;
实施例2.hpmips对大环内酯类富集浓缩效果验证
(1)经在不同配比下测定分子印迹聚合物对模板分子的吸附性能,见表1。最终确立了以模板分子∶功能单体∶交联剂=1∶4∶20为最佳配比,其中功能单体为甲基丙烯酸时富集效果最好。所得到的分子印迹聚合物用热重分析进行表征,见图1。由热重曲线图可知在0~800℃范围内,mmips材料产生约80%的重量损失,hpmips材料产生约100%的质量的损失,说明所得到的hpmips材料中mcm-41介孔硅核心(约占mmips重量的20%)已经去除完全。
表1功能单体的类型及比例的优化
(2)hpmips和mmips的电镜照片
hpmips和mmips材料的扫描电镜图片见图2所示。可以看出mmips经氢氟酸腐蚀去除了mcm-41核心后所得的hpmips保持了原有形态并呈现出中空多孔的结构,因此具有较大的比表面积和孔径体积,从而有较高的吸附容量和传质速率。
(3)为了验证制备的中空多孔印迹材料对大环内酯类抗生素的高吸附容量,分别以hpmips、无模板中空多孔印迹材料(hpnips)、mmips以及采用未加mcm-41核心聚合制备的solid-mips和solid-nips作为分散固相萃取吸附剂,以10ml分别溶有1~100g/ml的螺旋霉素溶液样品为萃取溶液进行饱和吸附容量的平行对比实验,剩余液用液相色谱-串联质谱(hplc-ms/ms)的方法进行分析检测。结果如图3所示,在实验的浓度范围内中空多孔印迹聚合物(hpmips)的萃取量要比表面印迹聚合物(mmips)和传统的实心固体印迹聚合物(solid-mips)高。
(4)为了验证制备的中空多孔印迹材料上存在印迹位点,分别以5mg的hpmips和hpnips作为分散固相萃取材料,以分别溶有40μg/kg的阿奇霉素(azi)、螺旋霉素(spi)、替米考星(tilm)、克拉霉素(cla)、交沙霉素(jos)、罗红霉素(rox)、泰乐菌素(tyl)的2g蜂蜜样品为上样液进行萃取回收率的平行对比实验,洗脱液用hplc-ms/ms的方法进行分析检测。结果如图4所示。hpmips对阿奇霉素、螺旋霉素、替米考星、克拉霉素、交沙霉素、罗红霉素、泰乐菌素七种大环内酯类抗生素的富集回收率分别是71.5,90.8,71.6,84.3,65.3,92.2,103.8%,hpnips对阿奇霉素、螺旋霉素、替米考星、克拉霉素、交沙霉素、罗红霉素、泰乐菌素七种大环内酯类抗生素的富集回收率分别是44.4,47.1,34.1,50.2,58.4,72.2,51.0%。可见hpmips对大环内酯类抗生素具有更好的萃取效果。
实施例3.hpmips材料检测市售蜂蜜
(1)将上述得到的中空多孔印迹聚合物(hpmips)作为分散固相萃取(dspe)吸附剂。用浓度为20mmol/lk2hpo4缓冲溶液(ph=8.0)上样,1.0ml水淋洗,最后用hoac/meoh=2/98(v/v)的混合液洗脱后,氮气吹干,定容到200μl。洗脱物通过hplc-ms/ms进行分析检测。
(2)准确称取空白蜂蜜样品各2g,置于15ml聚丙烯塑料管中,再加入10ml浓度为20mmolk2hpo4(用6mol/l的hcl溶液调ph值为8.0)缓冲溶液,涡旋30s后,4500rpm下离心10min,将离心后的溶液作为固相萃取的上样液。
(3)结果
如图5为加标浓度为40mg/kg,溶有阿奇霉素、螺旋霉素、替米考星、克拉霉素、交沙霉素、罗红霉素、泰乐菌素七种大环内酯类抗生素的蜂蜜样品溶液经hpmips富集前后的对比图,从图中可以看到富集前,溶液中七种大环内酯类抗生素的信号峰响应均较弱,经hpmips材料富集浓缩后,目标化合物的响应被充分放大,完全满足定量要求,富集倍数为263.4~688.3倍。
(4)为了上述处理方法的可靠性进行了加标实验:分别向空白蜂蜜中添加浓度为1、5和20μg/kg,3个浓度水平的大环内酯类抗生素的混合标准液,按上述的方法提取、净化后用hplc-ms/ms进行分析检测,每个添加水平重复测定6次。结果见表2。
表2不同添加水平下各目标物的添加回收率和相对标准偏差(n=6)
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!