一种四环三萜类化合物及其制备方法与流程
本发明涉及植物化学领域,具体而言,涉及一种四环三萜类化合物及其制备方法。
背景技术:
苦瓜(momordicacharantial.)又称锦荔枝、凉瓜,为葫芦科(cucurbitaceae)苦瓜属(momordica)一年生攀援性草本植物,作为药食同源的瓜类蔬菜,具有增强免疫力、抗糖尿病、抗肿瘤、减肥和抑菌等功效(groverandyadav,2004;beloinetal.,2005;mauryaetal.,2009)。
与其他葫芦科作物相比,苦瓜在生长发育过程中很少被植食性昆虫危害,表现出较强的抗虫性。大量研究结果表明,苦瓜茎叶中的苦瓜素(momordicins)为主要抗虫活性物质。苦瓜素是一类葫芦烷型四环三萜类化合物(tetracyclictriterpeoids),根据其结构的差异,可以分为momordicini、momordicinii、momordicinⅲ、momordicinⅳ和momordicinⅴ等。
其中,momordicini和momordicinii对黑足黑守瓜aulacophoranigripennis、南瓜黄守瓜raphidopalpafoveicollos和粘虫pesudaletiaseparate均有强烈的拒食作用,能显著抑制斜纹夜蛾spodopteralitura、亚洲玉米螟ostriniafurnacalish和小菜蛾plutellaxylostella(l.)生长发育,并对三叶草斑潜蝇liriomyzatrifolii有显著的拒产卵作用;momordicinⅳ和momordicinⅴ对三叶草斑潜蝇也具有产卵趋避作用(chandravadanaetal.,1987,1997;陈宏,1996;yasui,1998;abeetal.,2000;boekeetal.,2004;mekuriaetal.,2005,2006;kashiwagietal.,2007;任立云等,2008;凌冰等,2008,2009;向亚林等,2009;杨舒媚,2010;骆颖等,2012)。
苦瓜素类化合物对昆虫的作用方式是多样性的,其结构与现有化学杀虫剂不同,可为创新型结构的杀虫剂提供先导化合物,因此,制备高纯度的葫芦烷型四环三萜类化合物对苦瓜素的开发应用具有重要意义。
目前国内外对苦瓜素的分离、纯化研究大部分还处于实验室研究阶段,分离纯化方法主要是采用液-液萃取和经典柱色谱相结合的方法,但这样获得的苦瓜素纯度并不是很高,往往含有其他一些结构相似的杂质,而且工艺复杂,周期长(石雪萍,2006;任立云等,2008;成兰英等,2008;王虎等,2011;李雯等,2012)。
有鉴于此,特提出本发明。
技术实现要素:
本发明的第一目的在于提供一种四环三萜类化合物。
本发明的第二目的在于提供一种所述的四环三萜类化合物的制备方法。
为了实现本发明的上述目的,特采用以下技术方案:
一种四环三萜类化合物,所述四环三萜类化合物包括如下式(i)-(iv)所示化合物:
一种四环三萜类化合物的制备方法,所述制备方法包括如下步骤:
(a)经干燥粉碎所得苦瓜叶粗粉浸提后,得到粗提物;
(b)所得粗提物以包括乙酸乙酯内的不同溶剂分别进行萃取;
(c)将乙酸乙酯萃取物以淋洗剂进行梯度洗脱,分别收集不同流分;浓缩后,以分析液相色谱进行分析,将保留出峰时间相同的流分合并后浓缩;
(d)浓缩所得固体溶解后过滤,然后以半制备液相色谱制备纯化,收集保留出峰时间相同的组分;将相应的色谱柱洗脱液合并后浓缩,得到具有不同结构的四环三萜类化合物。
与现有技术相比,本发明的有益效果为:
(1)本发明制备方法中,采用半制备高效液相色谱法对苦瓜叶乙酸乙酯萃取物洗脱液中葫芦烷型四环三萜类化合物的分离制备,操作简单且快速高效,为葫芦烷型四环三萜类化合物的分离制备与纯化提供了一种重要途径,同时也建立了一种制备样品简单,且能准确快速定性定量检测分析苦瓜素的方法。
(2)通过本发明制备方法,能够得到四种具有不同结构的高纯度葫芦烷型四环三萜类化合物,这不仅为苦瓜素类化合物杀虫机理的深入研究提供了原料基础,同时也为新结构杀虫剂的开发提供了先导化合物和研究条件。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,以下将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
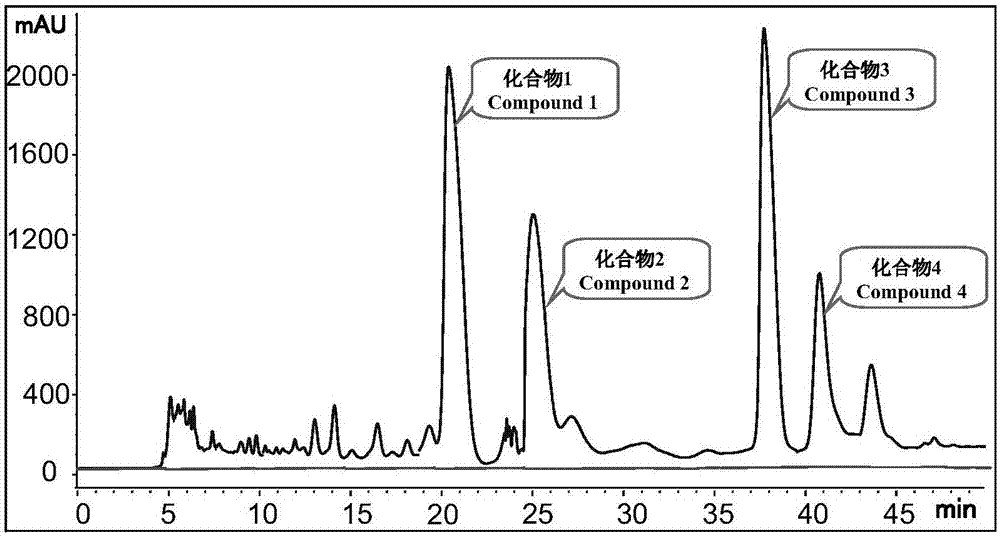
图1为本发明实施例1半制备色谱图;
图2为实施例1化合物1高效液相色谱图;
图3为实施例1化合物2高效液相色谱图;
图4为实施例1化合物3高效液相色谱图;
图5为实施例1化合物4高效液相色谱图。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
相较于传统的分离方法而言,制备型高效液相色谱是一种更为有效的分离方式,可用于天然植物活性成分的提取和纯化中(柳娜,2006;王宁等,2013)。也有研究人员采用制备型高效液相色谱对苦瓜果中的抑菌活性物质进行了分离提纯,并得到了两种对金黄色葡萄球菌有显著抑菌效果的活性成分(孟晓,2010)。然而,现有技术中,并没有针对于苦瓜叶中活性成分的提取和有效分离而提出有效的方法。本发明有鉴于此,建立了一种适用于对苦瓜叶中四种活性成分进行提取和分离的方法。
具体的,本发明方法包括如下步骤:
(a)待苦瓜成熟采收后,收集苦瓜叶片;然后,将其干燥粉碎,得苦瓜叶粗粉;
然后,将苦瓜叶粗粉按照料液比1:10~20(优选为15倍,g/ml)以乙醇溶液(优选浓度为90%,v/v)浸提提取;
提取可以采用恒温浸泡的方式进行,提取温度控制在50℃,每次提取时间控制在24h,共进行三次提取;
将每次提取后滤液合并,经浓缩(例如蒸发浓缩或减压浓缩等方式),得到乙醇粗提物(浸膏);
(b)将乙醇粗提物以常规的液-液萃取的方法,进行再次提取,其中,所用有机相分别依次为石油醚,乙酸乙酯,正丁醇,按照有机溶剂-水的“液-液”萃取法,对粗提物进一步提取纯化;
经过如上的提取,分别得到石油醚萃取物,乙酸乙酯萃取物,正丁醇萃取物,以及水萃取物。
本发明所提供的四种具体结构的四环三萜类化合物则大部分存在于乙酸乙酯萃取物中,因而进一步的提取也是以乙酸乙酯提取物作为原料。
(c)通过硅胶柱层析法,将乙酸乙酯萃取物以淋洗剂进行梯度洗脱,所用淋洗剂为不同配比的二氯甲烷-甲醇溶液;
具体的,梯度洗脱条件为,依次以二氯甲烷:甲醇(v:v)=100:1、98:1、96:1、90:1、85:1、80:1、75:1、70:1、65:1、60:1、55:1、50:1、45:1、40:1、35:1、30:1、25:1、20:1、15:1、10:1、5:1、2:1、1:1、甲醇(100%)进行梯度洗脱;
以每个梯度淋洗剂体积为1计,在洗脱过程中,每收集1/10~1/15体积的洗脱液即作为1个流分进行收集(优选的,每个梯度溶剂为1500ml,每100ml为一个流分);
然后,将所收集的各流分分别进行浓缩(无需浓缩至干),以分析色谱进行分析,分析色谱条件如下:
色谱柱:agilenttc-c18(4.6×250mm,5μm);流动相:甲醇和水,组成优选为80:20(甲醇:水,v/v);柱温:28℃;流速:0.5ml/min;检测波长dad:210nm;定量环:20μl;进样量:10μl;分析时间:50min。
葫芦烷型四环三萜类化合物极易溶于甲醇,难溶于水,甲醇极性较高,保留出峰时间短,这样就避免了与目标峰的重叠现象,并且甲醇室温下易挥发,不会引起产品纯度的降低,甲醇:水(80:20)系统溶液使主峰与杂质峰达到了基线分离。因此,本发明中,以甲醇-水体系作为流动相。
然后,将保留时间和出峰时间相同的流分合并,分别进行浓缩得到对应的固体产物。
本发明中,在进行高效液相制备色谱制备前,先将苦瓜叶乙酸乙酯粗提物通过硅胶柱层析法预处理,这样可以去除样品中大量的杂质,包括色素和黄酮类化合物。这样,一方面可以使得苦瓜素的量进一步提高,降低了半制备高效液相色谱的分离难度,简化了分离条件和提高了分离效能;另一方面也可防止半制备色谱柱污染,延长色谱柱的使用寿命。
(d)浓缩所得固体以甲醇溶解后,以0.22μm有机系微孔滤头进行过滤,然后以半制备液相色谱制备纯化,半制备色谱条件如下:
色谱柱:ultimatexb-c18(10×250mm,5μm);流动相:甲醇和水,组成优选为80:20(甲醇:水,v/v);柱温:28℃;流速:2.5ml/min;检测波长dad:210nm;定量环:1ml;进样量:100μl;半制备时间:50min。
在如上的半制品色谱制备纯化中,仍以相同的甲醇-水混合溶液作为流动相,同样也能够达到各组分有效分离的目的。同时,发明人在试验过程中发现,如果流动相流速增大会使目标峰与杂质峰分离度下降,流速过低则使样品出峰时间推迟,分离时间较长,且峰形变宽,为缩短分离时间且保持良好的分离度,在液相色谱半制备分离过程中,流动相的流速控制为2.5ml/min。
同时,与分析型色谱相比,制备色谱所选择的检测波长不一定是目标成分的最大吸收波长,而是应该选择一个可以检测到目标成分和干扰成分分离的波长更加合适。在加大进样量的情况下,如果优先选择目标成分的最大波长,很容易发生色谱柱未超载,而检测信号已经过载的情况,即色谱峰在未达到柱过载情况时即为平头峰,影响目标化合物的分离纯化。葫芦烷型四环三萜类化合物在紫外波长205-228nm之间有最大吸收峰(davidgetal.,2010),流动相甲醇在210nm处吸收峰最小,为了获得较高的检测灵敏度,减小杂质成分的干扰,使用高效液相色谱进行半制备时,其工作波长设置为210nm。
收集保留出峰时间相同的组分,进行多次制备,将对应的色谱峰洗脱液合并,浓缩干燥后,得到如下式(i)-(iv)所示的四种不同结构的葫芦烷型四环三萜类化合物,经检测,化合物的纯度达到95%以上。
其中,化合物(i)、(iv)中,glc和glu均为葡萄糖基。
在如上的多次半制备分离过程中,样品经层析柱色谱分离后,虽然苦瓜素的含量得到了大幅度提升,但溶液中仍含有一些杂质。因而,在进行高效液相半制备色谱纯化时,杂质也同步进入半制备柱中,并且在制备流动相条件下无法完全被洗脱。这既影响色谱柱寿命,也影响下一次的分离效果。因此,本发明中,优选的在每次分离纯化后以v(甲醇):v(水)=80:20,90:10,100:0梯度冲洗制备柱,然后再以v(甲醇):v(水)=80:20溶液平衡色谱柱,之后才进行下一次的分离纯化。
实施例1
(一)四环三萜类化合物制备
苦瓜种植于华南农业大学资源环境学院试验农场,待苦瓜成熟采收后,收集苦瓜叶片。
将苦瓜叶片干燥后粉碎,得到苦瓜叶粗粉,置于多功能提取器中,加入样品量15倍的90%乙醇溶液,在50℃恒温下浸泡24h,渗出滤液,共浸提3次,合并滤液。
滤液经旋转蒸发仪减压浓缩后得到乙醇粗提物,然后以常规“液-液萃取法”进行提取,分别用石油醚、乙酸乙酯和正丁醇萃取,合并萃取液,减压蒸馏分别得到石油醚、乙酸乙酯、正丁醇和水萃取物。
通过硅胶柱色谱法进一步纯化乙酸乙酯萃取物,使用开口玻璃层析柱(高:120cm;直径5cm),经处理活化过的硅胶(100-200目)作为固定相,湿法装柱。乙酸乙酯萃取物用甲醇溶解后,与硅胶(100-200目)充分拌匀、晾干、研磨成粉,装入硅胶层析柱内,然后以不同配比的二氯甲烷-甲醇溶液进行梯度洗脱,每个梯度溶剂为1500ml,每100ml为一个流分,经旋转蒸发仪浓缩后通过分析hplc进行分析,将保留出峰时间相同的流分合并,旋转减压浓缩,4℃保存;
其中,分析液相色谱条件为:色谱柱:agilenttc-c18(4.6×250mm,5μm);流动相:甲醇和水,洗脱条件:v(甲醇):v(水)=80:20;柱温:28℃;流速:0.5ml/min;检测波长dad:210nm;定量环:20μl;进样量:10μl;分析时间:50min。
然后,将不同洗脱组分浓缩所得固体分别以甲醇溶解,经0.22μm有机系微孔滤头过滤后,以半制备高效液相色谱进行半制备分离;
其中,半制备色谱条件如下:色谱柱:ultimatexb-c18(10×250mm,5μm);流动相:甲醇和水,洗脱条件:v(甲醇):v(水)=80:20;柱温:28℃,流速:2.5ml/min,检测波长dad:210nm,定量环:1ml;进样量:100μl;半制备时间:50min。
收集保留出峰时间相同的组分,进行多次制备,将相应的色谱峰洗脱液合并,将其减压浓缩后置50℃恒温干燥箱内24h,分别得到四种白色粉末状物质,记为化合物1-4。
由图1可知,在本发明制备色谱条件下,化合物1-4的保留出峰时间分别为21.1、26.3、38.4和41.2min,峰型对称,柱效较高,既保证了定性定量的准确性,又同时兼顾了分析效率的要求。
(二)四环三萜类化合物检测
(1)将所制得的化合物1-4分别以甲醇溶解后,按照如上分析液相色谱条件,采用面积归一法对制备得到的葫芦烷型四环三萜类化合物进行纯度检测,所得各组分的色谱分别如图2-图5所示。
由图2-图5可知,各组分色谱检测均为单一色谱,化合物1-4的出峰保留时间分别为:20.8、24.2、30.7和34.9min。通过采用面积归一法计算化合物1-4的纯度,其纯度均高于95%。
由此可见,由本发明方法半制备分离得到的产物中的其他成分(如色素和黄酮类化合物)对葫芦烷型四环三萜类化合物的分离干扰较小,从而保证该分析方法的重现性和稳定性。
(2)将制备得到的葫芦烷型四环三萜类化合物采用brukerav600型超导液体核磁共振谱仪进行结构鉴定。核磁共振谱(nmr)以甲醇(ch3oh)或吡啶(dmso)为溶剂,测定氢谱(1hnmr)和碳谱(13cnmr),根据氢谱(1hnmr)和碳谱(13cnmr),并参考相关文献确定化合物结构。
(i)化合物1为白色粉末,易溶于甲醇、丙酮,难溶于水,检测数据如下:
esi-msm/z:657[m+na]+。
ir
1h-nmr(cd3od)δ:10.65(1h,s,h-19),6.27(1h,d,j=4.4hz,h-6),5.61(1h,d,j=7.8hz,h-24),4.96(1h,d,j=7.8hz,glc-1),4.96(1h,d,j=7.6hz,h-23),4.46(1h,d,j=10.8hz,glc-6b),4.35(1h,d,j=10.8hz,glc-6a),4.35(1h,d,j=5.2hz,h-7),4.21(2h,brd,j=6.0hz,glc-3,4),4.01(brs,glc-2),3.88(1h,brs,glc-5),3.81(1h,brs,h-3),2.71(1h,m,h-10),2.37(1h,s,h-8),2.07(1h,m,h-20),1.75,1.71(each3h,s,h-26andh-27),1.19(3h,d,j=6.4hz,h-21),1.48,1.12,0.90,0.87(each3h,s)。
13c-nmr(100mhz,cd3od)δ:207.7(c-19),145.7(c-5),129.1(c-24),132.2(c-25),124.3(c-6),75.6(c-3),65.7(c-7),75.3(c-23),50.6(c-9),51.2(c-17),50.5(c-8),48.2(c-14),45.9(c-13),43.7(c-22),41.7(c-4),36.8(c-10),34.9(c-15),32.6(c-20),29.8(c-2),29.6(c-12),27.8(c-16),27.3(c-29),26.2(c-27),25.8(c-28),22.7(c-11),21.7(c-1),19.4(c-21),18.2(c-26),18.2(c-30),14.9(c-18),104(glc-23-1),75.6(glc-23-2),78.9(glc-23-3),71.9(glc-23-4),78.2(glc-23-5),63.0(glc-23-6)。
分子式:c36h58o9;相对分子质量为634。1hnmr和13cnmr数据与文献yasuihetal.(1998)报道一致,故可确定化合物1为momordicinii(23-o-β-d-glucopyranosyl-3,7-dihydroxycucurbita-5,24-dien-19-al),结构如下:
(ii)化合物2为白色片晶,易溶于甲醇、丙酮,难溶于水。
esi-msm/z:495[m+na]+。
mp188-191℃。
ir
1h-nmr(400mhz,cd3od)δ:9.87(1h,s,h-19),5.57(2h,brs,h-23,24),3.99(1h,brd,j=5.6hz,h-7),3.54(1h,brs,h-3),1.25(6h,s,h-26,27),0.94(3h,d,j=5.6hz,h-21),1.24,1.07,0.86,0.81(each3h,s,4×-ch3)。
13c-nmr(100mhz,cd3od)δ:209.4(c-19),147.2(c-23),140.7(c-5),125.7(c-24),123.8(c-6),77.0(c-3),71.1(c-25),66.9(c-7),51.3(c-9),51.1(c-17),50.8(c-14),46.6(c-13),42.3(c-4),40.3(c-22),37.6(c-10),35.7(c-11),30.2(c-8),30.1(c-20),29.9(c-16),29.8(c-2),28.6(c-15),27.8(c-28),27.6(c-12),26.0(c-26),23.3(c-27),22.3(c-29),21.9(c-1),19.3(c-30),18.8(c-18),15.4(c-21)。
分子式:c30h48o4;相对分子质量为472。1hnmr和13cnmr数据与文献harinanteainaletal.(2006)报道一致,故鉴定化合物2为3β,7β,25-trihydroxycucurbita-5,(23e)-dien-19-al,结构如下:
(iii)化合物3:白色粉末,易溶于甲醇、丙酮,难溶于水。
mp236-237℃。
1h-nmr(400mhz,dmso)δ::0.76(3h,s,h-30),0.86(3h,s,h-18),0.94(3h,d,j=5.5hz,h-21),1.12(3h,s,h-29),1.31(6h,s,h-26,27),1.42(3h,s,h-28),3.59(3h,s,-och3),3.78(1h,s,h-3),4.98(1h,d,j=7.8hz,h-1),5.54(1h,d,j=15.9hz,h-24),5.61(1h,m,h-23),6.17(1h,d,j=5.0hz,h-6),10.21(1h,s,h-19)。
13c-nmr(125mhz,dmso)δ:21.9(c-1),29.8(c-2),75.6(c-3),42.0(c-4),147.7(c-5),122.3(c-6),71.8(c-7),45.7(c-8),50.3(c-9),36.7(c-10),22.6(c-11),29.3(c-12),45.1(c-13),48.1(c-14),34.9(c-15),27.4(c-16),50.2(c-17),15.0(c-18),207.4(c-19),36.4(c-20),19.0(c-21),39.7(c-22),128.4(c-23),137.7(c-24),74.9(c-25),26.3(c-26),26.5(c-27),27.3(c-28),26.5(c-29),18.2(c-30),50.4(25-och3);glu:δ:101.7(d,c-1),75.0(d,c-2),78.7(d,c-3),71.6(d,c-4),78.9(d,c-5),63.0(t,c-1)。
分子式:c37h60o9;相对分子质量为648。1hnmr和13cnmr数据与参考文献okabeh,etal.(1982)一致,故鉴定化合物3为momordicosidek(3β,7β-dihydroxy-25-methoxy-cucurbita-5,23-dien-19-al),结构如下:
(iv)化合物4:白色粉末,易溶于甲醇、丙酮,难溶于水。
esi-msm/z:495[m+na]+。
mp123-125℃。
ir
1h-nmr(400mhz,cd3od)δ:0.82,0.93,1.08,1.25(each3h,s,h-18,28,29,30),1.00(3h,d,j=6.4hz,h-21),1.67(3h,s,h-26),1.70(3h,s,h-27),1.98(1h,m,h-20),2.40(1h,m,h-8),2.58(1h,m,h-10),3.55(1h,brs,h-3),4.00(1h,d,j=5.2hz,h-7),4.41(1h,m,h-23),5.16(1h,d,j=8.8hz,h-24),5.91(1h,d,j=4.0hz,h-6),9.88(1h,s,h-19)。
13c-nmr(100mhz,cd3od)δ:209.7(c-19),147.3(c-5),133.4(c-24),130.5(c-25),124.0(c-6),77.1(c-3),66.9(c-7),66.6(c-23),52.1(c-9),51.3(c-17),50.8(c-8),49.0(c-14),46.8(c-13),45.6(c-22),42.3(c-4),37.7(c-10),35.6(c-15),33.7(c-20),30.3(c-2),29.8(c-12),28.6(c-16),27.8(c-29),26.0(c-27),25.9(c-28),23.3(c-11),22.2(c-1),19.3(c-21),18.8(c-26),18.1(c-30),15.3(c-18)。
分子式:c30h48o4;相对分子质量为472。1hnmr和13cnmr数据与文献mekuriadb,etal.(2005)报道一致,故鉴定化合物4为momordicinⅰ(3,7,23-trihydroxycucurbita-5,24-dien-19-al),结构为:
由如上的检测结果可知,本发明采用半制备的分离方法,能够在较短的时间内一次可制备分离得到momordicini,momordicinii,momordicosidek和3β,7β,25-trihydroxycucurbita-5,(23e)-dien-19-al等4种葫芦烷型四环三萜类化合物,hplc分析表明所制备的4种化合物的纯度均高于95%,为葫芦烷型四环三萜类化合物的分离制备与纯化提供了一种重要途径。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以作出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!