Vγ9δ2T细胞识别与杀伤肺鳞状上皮细胞癌的新靶标抗原及其鉴别方法和应用与流程
本发明涉及生物技术领域,具体而言,涉及一种vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标及其鉴别方法和应用。
背景技术:
肺癌是世界上致死率最高的癌症,其中非小细胞性肺癌(nsclc)约占肺癌总数的80%。肺癌的高发病率、高致死率及有效治疗手段的缺乏燃起了众多研究者对新型肺癌免疫治疗策略的探索。其中,免疫关节点抑制剂及基于杀伤性t细胞的免疫过继治疗策略近年来引起了广泛关注。
vγ9δ2t细胞是人外周血γδt细胞的主要亚群(比例约为50-90%),能以mhc非限制性方式识别表达在肿瘤细胞表面的应激性内源性蛋白质抗原,对多种血液肿瘤及实体肿瘤均有直接杀伤作用。然而,vγ9δ2t细胞识别杀伤肺癌的分子机制目前尚不十分清楚,对于vγ9δ2t细胞如何在肿瘤治疗中发挥更佳作用也缺乏更好的技术手段。
有鉴于此,特提出本发明。
技术实现要素:
本发明的第一目的在于提供一种鉴别基于vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标的方法,以缓解现有技术中缺少一种可以有效鉴定发现新型靶标的方法。
本发明的第二目的在于提供利用上述方法得到的新型靶标。
本发明的第三目的在于提供上述新型靶标在制备肺鳞状上皮细胞癌免疫过继治疗药物中的应用。
为了实现本发明的上述目的,特采用以下技术方案:
一种鉴别基于vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标的方法,包括以下步骤:针对靶标分子进行如下a)-c)的操作:
a)检测vγ9δ2t细胞对靶标分子封闭的肿瘤细胞的杀伤作用;
b)检测vγ9δ2t细胞对靶标分子缺陷型的肿瘤细胞的杀伤作用;
c)检测vγ9δ2t细胞对靶标分子过表达的肿瘤细胞的杀伤作用;
所述靶标分子通过激光共聚焦显微镜方法鉴定肿瘤细胞表面异位表达得到。
进一步地,a)和b)中所述的杀伤作用显著降低,所述靶标分子为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。
进一步地,c)中所述的杀伤作用显著提升,所述靶标分子为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。
进一步地,所述检测采用cytotox96非放射杀伤试剂盒。
进一步地,所述靶标分子封闭的肿瘤细胞通过采用靶标分子抗体封闭肿瘤细胞上异位表达的靶标分子得到。
进一步地,所述肿瘤细胞包括glc-82、nci-h446或nci-h520中的至少一种,优选为nci-h520。
进一步地,所述靶标分子包括hmsh2。
进一步地,hmsh2缺陷型肿瘤细胞的构建包括采用sirna转入肿瘤细胞干扰hmsh2基因表达的步骤。
上述方法得到的新型靶标。
上述新型靶标在制备肺鳞状上皮细胞癌免疫过继治疗药物中的应用;
优选地,所述新型靶标为hmsh2。
与现有技术相比,本发明的有益效果为:
本发明提供的鉴别基于vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标的方法,靶标分子通过激光共聚焦显微镜术鉴定肿瘤细胞表面的异位表达得到,针对靶标分子进行如下a)-c)的操作:a)检测vγ9δ2t细胞对靶标分子封闭的肿瘤细胞的杀伤作用;b)检测vγ9δ2t细胞对靶标分子缺陷型的肿瘤细胞的杀伤作用;c)检测vγ9δ2t细胞对靶标分子过表达的肿瘤细胞的杀伤作用。该方法利用激光共聚焦显微镜方法来检测肿瘤细胞表面的异位表达,可以准确得到肿瘤细胞表面的异位表达分子,该分子即为靶标分子,为vγ9δ2t细胞新型靶标的候选分子,在通过对靶标分子封闭、构建缺陷型细胞和过量表达后检测vγ9δ2t细胞的杀伤作用来进一步地确定靶标分子是否为目标新型靶标。该方法可以快速准确地得到vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标,这为了解vγ9δ2t细胞的杀伤机制和肺鳞状上皮细胞癌的过继免疫治疗提供了新的思路和理论依据。
附图说明
图1为本发明实施例2中激光共聚焦显微镜术检测nci-h520细胞表面hmsh2的异位表达;
图2为本发明实施例3中抗体封闭杀伤实验验证异位表达的膜hmsh2介导vγ9δ2t细胞对nci-h520的识别杀伤;
图3a为本发明实施例4中荧光转染对照监测hmsh2基因靶向sirna的转染效率;其中,nc:nci-h520细胞自然培养对照;tc:nci-h520细胞redoligo平行转染对照;sirna:hmsh2基因靶向特异性sirna转染的nci-h520细胞;
图3b为本发明实施例4中sirnai,sirnaii显著下调hmsh2基因在nci-h520细胞中的mrna转录水平结果图;
图3c为本发明实施例4中激光共聚焦显微镜术显示sirna转染显著下调hmsh2蛋白在nci-h520细胞膜的异位表达;
图3d为本发明实施例4中sirnai,sirnaii显著下调了hmsh2介导的vγ9δ2t细胞对nci-h520的识别杀伤结果图;
图4a为本发明实施例5中用于hmsh2蛋白过表达的fugw-egfp表达载体;
图4b为本发明实施例5中流式细胞术显示fugw-egfp-hmsh2过表达nci-h520肺癌模式细胞表面hmsh2的表达较野生型显著升高;
图4c为本发明实施例5中hmsh2过表达显著增强了vγ9δ2t细胞对nci-h520肺癌模式细胞的杀伤作用;
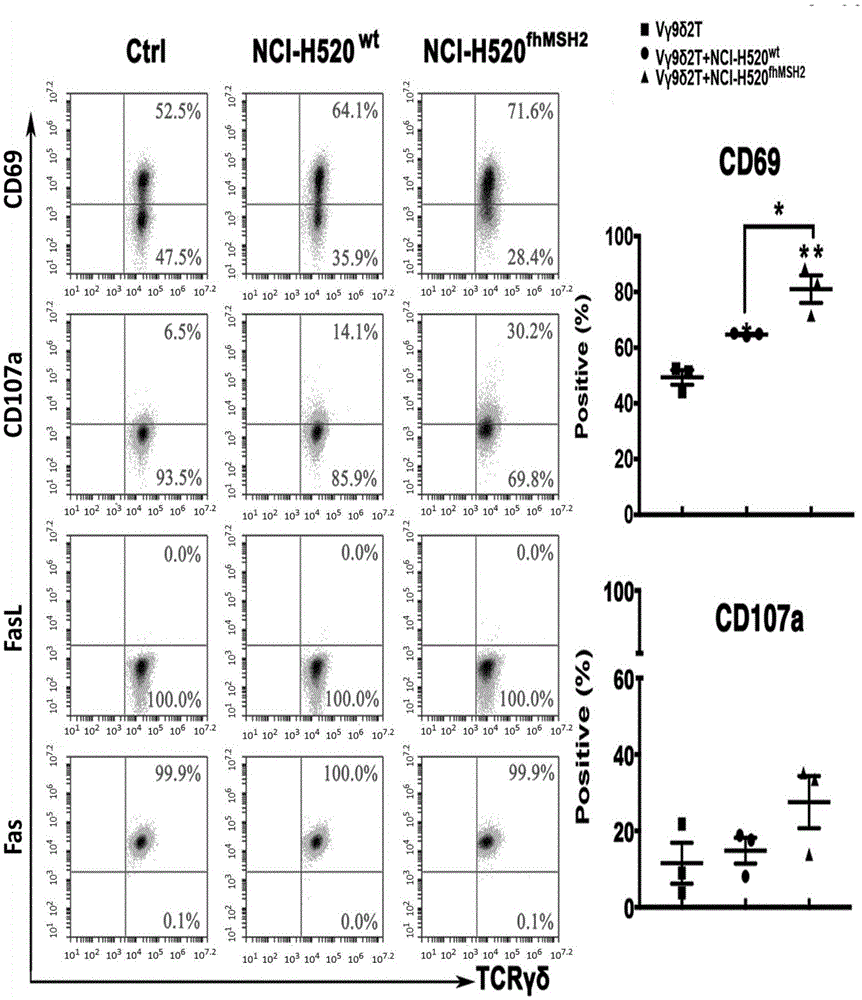
图5a为本发明实施例6中流式细胞术检测效应vγ9δ2t细胞,与野生型nci-h520及hmsh2过表达nci-h520共孵育vγ9δ2t细胞细胞表面cd69,cd107a,fas/fasl等分子的表达;
图5b为本发明实施例6中流式细胞术检测效应vγ9δ2t细胞,与野生型nci-h520及hmsh2过表达nci-h520共孵育vγ9δ2t细胞表面perforin,granzymea,granzymeb的表达;
图6a为本发明实施例6中流式细胞术检测效应vγ9δ2t细胞,与野生型nci-h520及hmsh2过表达nci-h520共孵育vγ9δ2t细胞表面ifn-γ及tnf-α的表达;
图6b为本发明实施例6中elisa检测hmsh2过表达nci-h520与vγ9δ2t细胞共孵育上清中ifn-γ及tnf-α的表达;
图6c为本发明实施例6中sirnai,sirnaii-hmsh2基因敲除对vγ9δ2t细胞分泌ifn-γ的影响。
具体实施方式
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。
一种鉴别基于vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标的方法,包括以下步骤:针对靶标分子进行如下a)-c)的操作:
a)检测vγ9δ2t细胞对靶标分子封闭的肿瘤细胞的杀伤作用;
b)检测vγ9δ2t细胞对靶标分子缺陷型的肿瘤细胞的杀伤作用;
c)检测vγ9δ2t细胞对靶标分子过表达的肿瘤细胞的杀伤作用;
靶标分子通过激光共聚焦显微镜方法鉴定肿瘤细胞表面异位表达得到。
该方法利用激光共聚焦显微镜方法来检测肿瘤细胞表面的异位表达,可以准确得到肿瘤细胞表面的异位表达分子,该分子即为靶标分子,为vγ9δ2t细胞新型靶标的候选分子,在通过对靶标分子封闭、构建缺陷型细胞和过量表达后检测vγ9δ2t细胞的杀伤作用来进一步地确定靶标分子是否为目标新型靶标。该方法可以快速准确的得到vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标,这为了解vγ9δ2t细胞的杀伤机制和肺鳞状上皮细胞癌的过继免疫治疗提供了新的思路和理论依据。
在一些实施方式中,a)和b)中的杀伤作用显著降低,说明靶标分子为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。通过封闭肿瘤细胞表面的靶标分子,使得vγ9δ2t细胞无法识别靶标分子,如果vγ9δ2t细胞的杀伤作用显著降低,这说明该靶标分子与vγ9δ2t细胞的肿瘤细胞识别有关。通过构建靶标分子缺陷型的肿瘤细胞,抑制肿瘤细胞内的靶标分子表达,降低靶标分子在肿瘤细胞表面的异位表达,使得vγ9δ2t细胞无法识别靶标分子,如果vγ9δ2t细胞的杀伤作用显著降低,说明该靶标分子与vγ9δ2t细胞的肿瘤细胞识别有关。
在一些实施方式中,c)中的杀伤作用显著提升,说明靶标分子为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。通过将靶标分子作为目标基因,构建靶标分子过表达的肿瘤细胞,使得靶标分子在肿瘤细胞表面的表达量提高,检测vγ9δ2t细胞的杀伤作用,如果显著上升,说明靶标分子的过表达提高了vγ9δ2t细胞的识别能力,进而说明该靶标分子为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。
在本发明的一些实施方式中,检测采用cytotox96非放射杀伤试剂盒。cytotox
在本发明的一些实施方式中,靶标分子封闭的肿瘤细胞通过采用靶标分子抗体封闭肿瘤细胞上异位表达的靶标分子得到。采用靶标分子抗体对靶标分子进行封闭,专一性强,可以实现对靶标分子进行封闭同时不影响其他抗原和试验的准确性。
在本发明的一些实施方式中,肿瘤细胞包括glc-82、nci-h446或nci-h520中的至少一种,优选为nci-h520。glc-82、nci-h446和nci-h520均为人肺癌细胞系,通过检测鉴定肿瘤细胞新型靶标可以对实体肿瘤的免疫治疗提供新的靶点和治疗方向。
在本发明的一些实施方式中,靶标分子包括hmsh2。hmsh2是dna错配修复蛋白家族的重要成员,正常情况下定位于细胞核。本发明通过上述方法鉴定得到hmsh2在肿瘤细胞表面异位表达,通过检测vγ9δ2t细胞对hmsh2封闭的nci-h520的杀伤作用发现杀伤效率显著降低,检测vγ9δ2t细胞对hmsh2缺陷型nci-h520的杀伤作用发现杀伤效率也显著降低,检测vγ9δ2t细胞对hmsh2过表达nci-h520的杀伤作用发现杀伤效率显著提高,说明hmsh2为vγ9δ2t细胞识别与杀伤肺鳞状上皮细胞癌的新型靶标。hmsh2可经tcr和nkg2d双重途径介导vγ9δ2t细胞对靶肿瘤细胞的识别与杀伤。hmsh2的这种膜异位表达可为氧化应激及ebv转化等因素诱导。
在本发明的一些实施方式中,hmsh2缺陷型肿瘤细胞的构建包括采用将特异性sirnas转染入肿瘤细胞靶向干扰hmsh2基因表达的步骤。
利用上述方法得到的新型靶标。利用上述方法鉴定得到vγ9δ2t细胞的新型靶标,准确性高,方法可操作性强,新型靶标为肿瘤细胞的治疗提供了新的抗原靶点,为过继免疫治疗提供了理论基础。
上述新型靶标在制备肺鳞状上皮细胞癌免疫过继治疗药物中的应用,其中,新型靶标为hmsh2。hmsh2为vγ9δ2t细胞识别与杀伤肺鳞状上皮肿瘤细胞的新型靶标,可以激活vγ9δ2t细胞,所以利用这一特性可以制备应用于过继免疫治疗的药物,针对实体肿瘤进行有效的治疗。
下面通过具体的实施例进一步说明本发明,但是,应当理解为,这些实施例仅仅是用于更详细地说明之用,而不应理解为用于以任何形式限制本发明。
实施例1肿瘤细胞的培养及效应细胞的扩增
nsclc细胞系nci-h520和正常肺成纤维细胞系mrc-5购自中国医学科学院基础医学研究所细胞培养中心,用含10%fcs的rpmi1640培养基传代培养。
分离并扩增自青年健康成人志愿者外周血pbmcs的效应vγ9δ2t细胞用含il-2的rpmi1640完全培养基传代培养。
实施例2肺癌细胞膜hmsh2的异位表达
nci-h520和mrc-5细胞分别在趴片上孵育过夜。细胞用4%多聚甲醛固定10-15min后用含0.5%bsa的pbs4℃封闭30min,依次与兔anti-hmsh2pcab或同型兔igg及fitc标记的羊抗兔二抗共孵育。用配置leicatcssp2se共聚焦成像系统的leicadmire2倒置显微镜成像。目镜为40×,数字孔径1.25(油镜)。
结果如图1所示,在激光共聚焦显微镜术检测中,nci-h520细胞膜呈现了较强的绿色荧光。说明hmsh2在nci-h520细胞膜存在异位表达。将hmsh2作为靶标分子,nci-h520作为肿瘤细胞进行验证。
实施例3vγ9δ2t细胞对hmsh2抗体封闭的肿瘤细胞的杀伤作用检测
用cytotox96非放射性杀伤分析试剂盒分析hmsh2在vγ9δ2t细胞对nci-h520靶细胞识别杀伤中的介导作用。操作按试剂盒说明书进行。正式杀伤前用anti-msh2(n-20,终浓度20μg/ml)抗体将靶细胞室温预处理1h,对照组用等量同型igg处理。适当比例的效靶细胞37℃共孵育4-5h(平行设立3个复孔)后,按试剂盒说明书计算杀伤效率。
实验结果如图2所示,从结果中可以看出,不同的效靶比中,vγ9δ2t细胞对hmsh2抗体封闭组nci-h520细胞的杀伤作用较igg对照组均显著降低。说明hmsh2为vγ9δ2t细胞识别nci-h520靶细胞的抗原靶点。
实施例4vγ9δ2t细胞对hmsh2缺陷型肿瘤细胞的杀伤作用检测
用于hmsh2基因靶向敲除的sirnai、sirnaii由上海invitrogen公司合成并逆转入nci-h520细胞,建立sirna-hmsh2-基因沉默nci-h520肺癌细胞模型,同时设立block-ittmalexa
6-12h后,sirnai、sirnaii在nci-h520细胞中的转染效率可达90-98%(图3a)。转染48-72h后,用qrt-pcr、wb、fcm及激光共聚焦显微镜术检测sirna干扰组和mock组hmsh2基因的敲除效果。从图3a-图3d结果可看出,特异性sirnai与sirnaii转染显著下调了nci-h520肺癌模式细胞中hmsh2的基因转录与蛋白质翻译水平,从而降低了肺癌细胞膜hmsh2介导的vγ9δ2t细胞对肺癌细胞的杀伤作用。说明肿瘤细胞膜表面的hmsh2下调致人vγ9δ2t细胞对hmsh2缺陷型nci-h520细胞的杀伤作用显著降低,进一步表明膜异位表达的hmsh2参与vγ9δ2t细胞对肺癌细胞的识别与杀伤作用。
实施例5vγ9δ2t细胞对hmsh2过表达肿瘤细胞的杀伤分析
将hmsh2基因的编码序列克隆并连接入fugw-egfp表达载体。构建成功的fugw-egfp-hmsh2重组质粒用lipo2000转染入nci-h520细胞建立fugw-egfp-hmsh2过表达nci-h520肺癌细胞模型。用wb和fcm检测hmsh2在fugw-egfp-hmsh2-nci-h520肺癌模式细胞中的过表达。
结果如图4a-图4c所示,hmsh2过表达肿瘤细胞构建成功。
我们将全长hmsh2基因(2805bp)连接入fugw-egfp融合蛋白表达载体并转染入nci-h520细胞以表达egfp-hmsh2融合蛋白(mw~130kda)(图4a)。fcm分析表明,fugw-egfp-hmsh2过表达nci-h520肺癌模式细胞表面hmsh2的异位表达较nci-h520-fugw(空载体转染组)、nci-h520(野生组)及同型igg对照组显著升高(图4b)。在效靶比10∶1的条件下,分别扩增自两名健康志愿者的效应vγ9δ2t细胞对膜hmsh2过表达nci-h520肺癌模式细胞的杀伤效率高达60-70%(图4c)。
实施例6vγ9δ2t细胞对hmsh2过表达nci-h520肺癌细胞的识别与杀伤机制
用cytotox96非放射性杀伤分析试剂盒分析人vγ9δ2t细胞对fugw-egfp-hmsh2-nci-h520肺癌模式细胞的杀伤效应,方法同实施例3。用fcm、elisa分析hmsh2过表达nci-h520肺癌模式细胞活化vγ9δ2t细胞的表面活化标志(cd69、cd107a等)以及杀伤相关效应分子(fas/fasl、perforin、granzymea/b、tnf-a、ifn-γ等)的表达情况。
结果如图5a-图5b所示,与野生型nci-h520细胞或fugw-egfp-hmsh2过表达nci-h520肺癌模式细胞共孵育6h后,效应vγ9δ2t细胞表面cd69的表达分别升高至60%与80%;而cd107a、fas/fasl、perforin、granzymea/b在细胞中的表达则无显著差异,说明经典的细胞毒途径在vγ9δ2t细胞介导的肺鳞癌杀伤中的作用没有我们预期的那么重要。
结果如图6a-图6c所示,本发明同时发现fugw-egfp-hmsh2过表达nci-h520肺癌模式细胞活化的vγ9δ2t细胞中ifn-γ及tnf-α分泌均增加(图6a),而特异性anti-hmsh2抗体封闭及/或sirna-hmsh2基因敲除而致的vγ9δ2t细胞ifn-γ及tnf-α分泌均降低(图6b和图6c)。ifn-γ的改变更为显著。
我们的发现不仅为ifn-γ及tnf-α参与异位表达的膜hmsh2介导的vγ9δ2t细胞对肺癌细胞的杀伤效应提供了有力证据,同时也提示ifn-γ及tnf-α信号通路在vγ9δ2t细胞介导的抗上皮细胞肿瘤免疫中的重要性。
尽管已用具体实施例来说明和描述了本发明,然而应意识到,在不背离本发明的精神和范围的情况下可以做出许多其它的更改和修改。因此,这意味着在所附权利要求中包括属于本发明范围内的所有这些变化和修改。
- 还没有人留言评论。精彩留言会获得点赞!