一种嵌合抗原受体及其应用的制作方法
本发明涉及肿瘤的细胞免疫治疗
技术领域:
,具体地,涉及一种嵌合抗原受体,编码其的核酸和表达其的细胞,以及其在制备治疗肿瘤的药物中的用途。
背景技术:
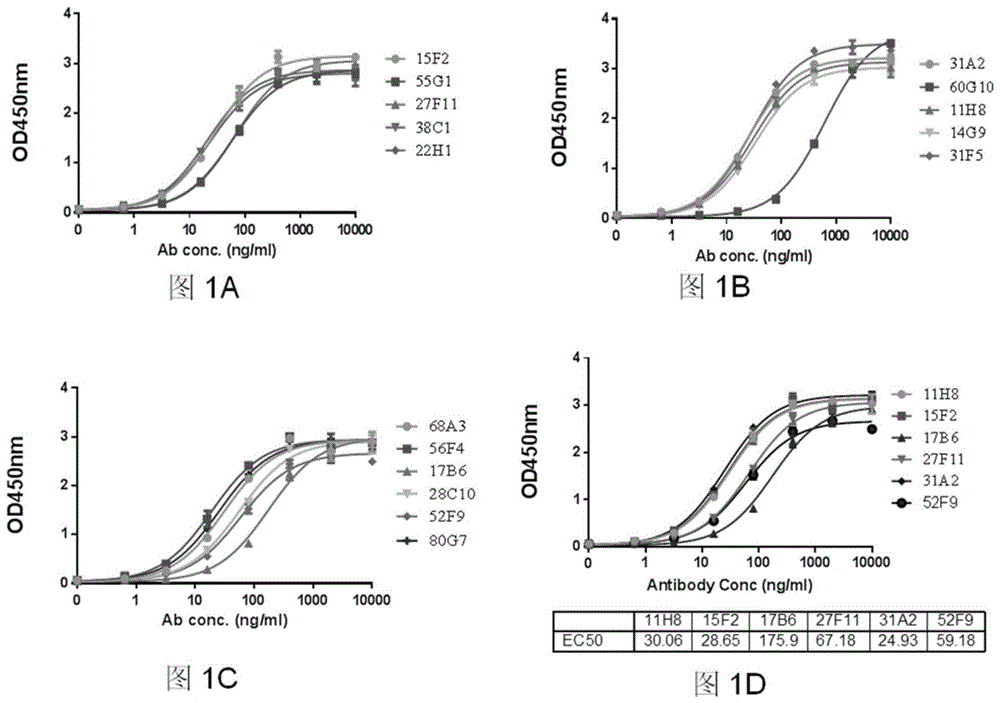
:嵌合抗原受体(car,chimericantigenreceptors)t细胞是表面表达识别特定抗原并能传递信号的嵌合型受体的t细胞。cart细胞通过表达嵌合抗原受体(car)分子而在抗肿瘤中发挥重要作用,car分子通常包括胞外段、跨膜区和胞内段:胞外段是由抗体重链和轻链可变区通过一条肽段相连接而形成的单链可变区(scfv);胞内段是各种信号传导分子的胞内段嵌合体,包括cd3zeta、cd28、ox-40、4-1bb等;跨膜区则来自其他分子(如cd8,cd4,cd28和cd3zeta)的跨膜区。单链可变片段部分的基因分离自例如产生识别靶抗原的单克隆抗体的杂交瘤。表达car分子的t细胞独立于肿瘤细胞上的主要组织相容性抗原i型的表达而直接识别肿瘤细胞表面抗原,并且在同时激活t细胞,并因此表达car的t细胞可以有效杀伤肿瘤细胞。简言之,cart细胞通过抗原-抗体识别模式对肿瘤细胞表面的特异分子进行识别,然后通过其胞内的信号传导进行激活、增殖并发挥细胞杀伤功能。人源化cd19抗体在治疗b细胞疾病如淋巴瘤、白血病或自身免疫病中的应用(参见hansen,美国专利申请公开号us2005/0070693)。尽管近年来癌症治疗取得很多进展,但b细胞恶性肿瘤,如非霍奇金淋巴瘤的b细胞亚型和慢性淋巴细胞性白血病仍然是主要的癌症相关死亡原因。因此,非常需要进一步改进的治疗方案来治疗b细胞恶性肿瘤。car-t的中文全称为嵌合抗原受体t细胞免疫疗法,是目前炙手可热的新型肿瘤治疗方式,也被认为是最可能攻克恶性肿瘤的技术之一。但car-t治疗的广泛应用也正遭遇着一系列难题和瓶颈,其中宿主免疫系统包括t细胞和抗体介导的对car分子的免疫排斥反应可能是限制car-t细胞体内持续性和长期疗效的关键阻碍和影响其应用的重要因素之一。技术实现要素:目前全球大多数临床注册的cd19car-t细胞治疗,所使用的肿瘤识别序列来源于鼠源抗体,回输人体后易被自身免疫系统识别为异种抗原,从而被宿主t细胞或抗体清除,继而影响car-t细胞体内的持续性,导致高复发率,并降低了长期临床疗效,对此,本发明的目的在于提供一种嵌合抗原受体及其应用,具体包括嵌合抗原受体以及编码其的核酸,表达其的细胞,其在制备治疗肿瘤的药物中的应用。本发明的嵌合抗原受体cd19抗体识别序列经过人源化改造,体内存活期更长,患者完全缓解期也可相应延长。本发明通过以下技术方案实现上述目的:第一方面,本发明提供了一种嵌合抗原受体,其包含至少一个胞外结构域、任选的跨膜结构域和至少一个胞内共刺激信号传导结构域,其中,所述胞外结构域包含cd19抗原识别结合结构域;其中,所述cd19抗原识别结合结构域包含具有如seqidno.1-6之一所示的序列的重链可变区或与其具有至少85%序列同一性的变体;所述cd19抗原识别结合结构域包含具有如seqidno.7-12之一所示的序列的轻链可变区或与其具有至少85%序列同一性的变体。本发明中,将人源化的cd19特异性单链抗体序列构建人源化cd19cart细胞可获得与鼠源cd19cart细胞同样的治疗效应,但却避免了鼠单链抗体的免疫排斥反应;本申请中的cd19抗原识别结合结构域经过人源化改造,不影响其对肿瘤细胞靶点抗原的识别能力,同时可能降低异种免疫排斥的发生概率,从而提升car-t细胞在人体中的持续时间,增强其对肿瘤细胞的免疫监控能力,降低肿瘤复发率,患者完全缓解期也可相应延长。在本发明的一些实施例中,所述cd19抗原识别结合结构域的重链可变区的氨基酸序列与seqidno.1-6之一所示的氨基酸序列具有至少85%,例如可以是85%、86%、88%、90%、92%、95%、98%、99%同一性的序列,且具有结合cd19和诱导t细胞信号传导的能力的变体,优选为具有至少90%,优选95%序列同一性的变体的重链可变区,且具有结合cd19和诱导t细胞信号传导的能力的变体。在本发明的一些实施例中,所述cd19抗原识别结合结构域的重链可变区的氨基酸序列与seqidno.7-12之一所示的氨基酸序列具有至少85%,例如可以是85%、86%、88%、90%、92%、95%、98%、99%同一性的序列,且具有结合cd19和诱导t细胞信号传导的能力的变体,优选为具有至少90%,优选95%序列同一性的变体的轻链可变区,且具有结合cd19和诱导t细胞信号传导的能力的变体。根据本发明,所述cd19抗原识别结合结构域包含具有如seqidno.1-6之一所示的序列的重链可变区或与其具有至少85%,优选90%,进一步优选95%序列同一性,且具有结合cd19和诱导t细胞信号传导的能力的变体。根据本发明,所述cd19抗原识别结合结构域包含具有如seqidno.7-12之一所示的序列的轻链可变区或与其具有至少85%,优选90%,进一步优选95%序列同一性,且具有结合cd19和诱导t细胞信号传导的能力的变体。本发明中,发明人发现采用这6个序列的重链和轻链的组合能够进一步提高与杂交瘤抗体的亲和力,其杀伤效果也显著提升,具体的cd19抗原识别结合结构域的重链可变区和轻链可变区可以由重链和轻链其中一条进行组合,具体如下表1所示:表1根据本发明,所述嵌合抗原受体例如可以是重链为seqidno.1和轻链为seqidno.7组成,重链为seqidno.1和轻链为seqidno.8组成,重链为seqidno.1和轻链为seqidno.9组成,重链为seqidno.1和轻链为seqidno.10组成,重链为seqidno.1和轻链为seqidno.11组成,重链为seqidno.1和轻链为seqidno.12组成,重链为seqidno.2和轻链为seqidno.7组成,重链为seqidno.2和轻链为seqidno.8组成,重链为seqidno.2和轻链为seqidno.9组成,重链为seqidno.2和轻链为seqidno.10组成,重链为seqidno.2和轻链为seqidno.11组成,重链为seqidno.2和轻链为seqidno.12组成,重链为seqidno.3和轻链为seqidno.7组成,重链为seqidno.3和轻链为seqidno.8组成,重链为seqidno.3和轻链为seqidno.9组成,重链为seqidno.3和轻链为seqidno.10组成,重链为seqidno.3和轻链为seqidno.11组成,重链为seqidno.3和轻链为seqidno.12组成,重链为seqidno.4和轻链为seqidno.7组成,重链为seqidno.4和轻链为seqidno.8组成,重链为seqidno.4和轻链为seqidno.9组成,重链为seqidno.4和轻链为seqidno.10组成,重链为seqidno.4和轻链为seqidno.11组成,重链为seqidno.4和轻链为seqidno.12组成,重链为seqidno.5和轻链为seqidno.7组成,重链为seqidno.5和轻链为seqidno.8组成,重链为seqidno.5和轻链为seqidno.9组成,重链为seqidno.5和轻链为seqidno.10组成,重链为seqidno.5和轻链为seqidno.11组成,重链为seqidno.5和轻链为seqidno.12组成,重链为seqidno.6和轻链为seqidno.7组成,重链为seqidno.6和轻链为seqidno.8组成,重链为seqidno.6和轻链为seqidno.9组成,重链为seqidno.6和轻链为seqidno.10组成,重链为seqidno.6和轻链为seqidno.11组成,或重链为seqidno.6和轻链为seqidno.12组成。在本发明的一些实施例中,所述cd19抗原识别结合结构域的重链可变区的氨基酸序列与seqidno.1-6之一所示的氨基酸序列具有至少85%,例如可以是85%、86%、88%、90%、92%、95%、98%、99%同一性的序列,且具有结合cd19和诱导t细胞信号传导的能力的变体,优选为具有至少90%,优选95%序列同一性的变体的重链可变区,且具有结合cd19和诱导t细胞信号传导的能力的变体。在本发明的一些实施例中,所述cd19抗原识别结合结构域的重链可变区的氨基酸序列与seqidno.7-12之一所示的氨基酸序列具有至少85%,例如可以是85%、86%、88%、90%、92%、95%、98%、99%同一性的序列,且具有结合cd19和诱导t细胞信号传导的能力的变体,优选为具有至少90%,优选95%序列同一性的变体的轻链可变区,且具有结合cd19和诱导t细胞信号传导的能力的变体。根据本发明,所述嵌合抗原受体的胞外结构域还包括任选的信号肽结构域,所述信号肽结构域为gm-csf信号肽、il-2信号肽或cd8α信号肽中的任意一种。根据本发明,所述胞内结构域还包括胞内共刺激信号传导域和/或cd3ζ信号传导域,所述胞内共刺激信号传导域包括人cd28胞内区、人4-1bb胞内区、人tlr1胞内区、人tlr2胞内区、人tlr3胞内区、人tlr4胞内区、人tlr5胞内区、人tlr6胞内区、人tlr7胞内区、人tlr8胞内区、人tlr9胞内区、人tlr10胞内区、人dap10胞内区、人cd27胞内区、人ox40胞内区、人cd30胞内区、人cd40胞内区、人pd-1胞内区、人ctla-4胞内区、人tim3胞内区、人lag3胞内区、人tgfβ胞内区、人icos胞内区、人淋巴细胞功能相关抗原1胞内区、人cd2胞内区、人cd7胞内区、人light胞内区、人nkg2c胞内区、人nkg2d胞内区、人nkp46胞内区、人nkp30胞内区、人nkp44胞内区、人dnam1胞内区、人b7-h3胞内区或人cd83胞内区中的任意一种或至少两种的组合,优选为人cd28胞内区、人4-1bb胞内区、人tlr2胞内区或人dap10胞内区×3、人dap10胞内区×6、人dap10胞内区×9中的任意一种或至少两种的组合(所述组合例如可以是cd28-tlr2、41bb-tlr2、41bb-cd28、41bb-cd28-tlr2、41bb-cd28-dap10×3、41bb-tlr2-dap10×3、cd28-tlr2-dap10×3、tlr2-dap10×3、cd28-dap10×3、41bb-dap10×3、tlr2-dap10×6、cd28-dap10×6、41bb-dap10×9、tlr2-dap10×9、cd28-dap10×9或41bb-dap10×9)优选为人cd28胞内区、人4-1bb胞内区、人tlr2胞内区和人dap10×3胞内区任意一种或至少两种的组合。所述跨膜结构域还包括任选的信号肽结构域,优选为cd3、cd8、cd28、ox40或icos中的任意一种,进一步优选为cd28。第二方面,本发明提供编码如第一方面所述的嵌合抗原受体的核酸。第三方面,本发明提供一种嵌合抗原受体表达细胞,其中引入了如第一方面所述的核酸。根据本发明,所述细胞为t细胞或含有t细胞的细胞群。第四方面,本发明提供制备如第三方面所述的嵌合抗原受体表达细胞的方法,其包括将如第二方面所述的核酸引入细胞的步骤。优选地,所述细胞为t细胞或含有t细胞的细胞群。第五方面,本发明提供如第一方面所述的嵌合抗原受体、如第二方面所述的核酸或如第三方面所述的嵌合抗原受体表达细胞在制备治疗肿瘤的药物中的用途。优选地,所述肿瘤为cd19阳性恶性肿瘤和/或b细胞恶性肿瘤。第六方面,本发明提供一种治疗肿瘤的药物组合,包括如第一方面所述的嵌合抗原受体、如第二方面所述的核酸或如第三方面所述的嵌合抗原受体表达细胞中的任意一种或至少两种的组合;优选地,所述药物组合还包括免疫治疗药物和/或小分子药物。本发明中,所述免疫治疗药物,例如可以是抗bcma嵌合抗原受体、抗cd20嵌合抗原受体、抗cd22嵌合抗原受体、抗cd20单克隆抗体、bcr-abl激酶抑制剂、免疫检查点抑制剂(pd-1/pd-l1单克隆抗体、ctla-4单克隆、tim3单克隆抗体、lag3单克隆抗体)、pd-1/pd-l1嵌合抗原受体、ctla-4嵌合抗原受体、tim3嵌合抗原受体或lag3嵌合抗原受体中的任意一种或至少两种的组合。本发明中,所述药物组合还包括小分子化学药物,例如可以是长春新碱、柔红霉素、左旋门冬酰胺酶、强的松、吡柔比星、地塞米松、天冬酰胺酶、阿霉素、阿糖胞苷或培门冬酶、mtor抑制剂(替西罗莫司,依维莫司,西罗莫司)、蛋白酶体抑制剂(硼替佐米、卡非佐米、伊沙佐米)或组蛋白去乙酰化酶(hdac)抑制剂(贝利司他、伏立诺他、帕比司他)中的任意一种或至少两种的组合。值得注意的是,术语“胞内结构域”是指已知在细胞中作为传输信号以引起生物过程的活化或抑制的结构域起作用的任何寡肽或多肽。值得注意的是,术语“变体”是指包含一个或几个至多个氨基酸的取代、缺失或添加的任何变体,条件是所述变体基本上保留原始序列所具有的相同功能。与现有技术相比,本申请具有如下有益效果:本申请中的cd19抗原识别结合结构域经过人源化改造,不影响其对肿瘤细胞靶点抗原的识别能力,同时可能降低异种免疫排斥的发生概率,从而提升car-t细胞在人体中的持续时间,增强其对肿瘤细胞的免疫监控能力,降低肿瘤复发率,患者完全缓解期也可相应延长。附图说明图1为杂交瘤抗体与cd19-his结合的结果图,其中,图1a为15f2、55g1、27f11、38c1和22h1与杂交瘤抗体结合的结果,图1b为31a2、60g10、11h8、14g9和31f5与杂交瘤抗体结合的结果,图1c为68a3、56f4、17b6、28c10、52f9和80g7与杂交瘤抗体结合的结果,图1d为11h8、15f2、17b6、27f11、31a2和52f9和杂交瘤抗体结合的结果;图2为cd19抗体表位结合结果图;图3为亲和度最优的cd19抗体的结合分析;图4为cd19抗体与不同抗原亲和度分析,其中,图4a为16b7、21f1、32g7、21g5、22a3、12d1、15f2、55g1、27f11、51e9、38c1、22h1、31a2、27b9和44c12抗原与cd19抗体结合的结果,图4b为60g10、11h8、14g9、31f5、16d4、31g6、32g11、55d9、16g6、80g5、68a3、56f4、17b6、28c10、52f9和80g7抗原与cd19抗体结合的结果;图5为cd19完全人源化抗体与cd19-his结合结果图;图6为cd19完全人源化抗体与nalm6/gl结合结果图;图7为嵌合抗原受体car19scfv分子结构图;图8为car(11h8/31a2/52f9/fmc63)-41bb-tlr2-cd3ζt细胞体外靶向杀伤cd19+淋巴瘤细胞系raji;图9为car(15f2/17b6/27f11/31a2/fmc63)-41bb-tlr2-cd3ζt细胞体外靶向杀伤cd19+淋巴瘤细胞系raji;图10为car(11h8/31a2/52f9/fmc63)-cd28-tlr2-cd3ζt细胞体外靶向杀伤cd19+白血病细胞系nalm6;图11为car(15f2/17b6/27f11/31a2/fmc63)-41bb-dap10×3-cd3ζt细胞体外靶向杀伤cd19+白血病细胞系nalm6;图12为car(11h8/31a2/52f9/fmc63)-41bb-tlr2-cd3ζt细胞对cd19-急性髓系白血病细胞系aml3体外杀伤结果;图13为car(15f2/17b6/27f11/31a2/fmc63)-41bb-cd28-cd3ζt细胞对cd19-急性髓系白血病细胞系aml3体外杀伤结果;图14为car(11h8/31a2/52f9/fmc63)-41bb-tlr2-cd3ζt细胞对肺癌细胞系a549体外杀伤结果;图15为car(11h8/31a2/52f9/fmc63)-cd28-tlr2-cd3ζt细胞对肺癌细胞系h460体外杀伤结果;图16为car(11h8/31a2/52f9/fmc63)-41bb-tlr2-cd3ζt细胞对胃癌细胞系mkn28体外杀伤结果;图17为car(11h8/31a2/52f9/fmc63)-cd28-tlr2-cd3ζt细胞对胃癌细胞系snu-1体外杀伤结果;图18为car(15f2/17b6/27f11/31a2/fmc63)-41bb-dap10×3-cd3ζt细胞对胃癌细胞系snu-1体外杀伤结果;图19为car(11h8/31a2/52f9/fmc63)-41bb-dap10×3-cd3ζt细胞对肝癌细胞系smmc体外杀伤结果;图20为car(15f2/17b6/27f11/31a2/fmc63)-41bb-dap10×3-cd3ζt细胞对肝癌细胞系hepg2体外杀伤结果。具体实施方式为便于理解本发明,本发明列举实施例如下。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。car质粒的构建如上所述,car分子包括胞外区域、跨膜区域、胞内区域,因此,以下实施例所用car质粒的构建步骤包括:首先,通过基因合成获得car质粒所需各基因dna,包括:抗cd19抗体免疫球蛋白重链和轻链的可变区域序列、cd28跨膜信号区域序列、tlr1信号传递区域序列、tlr2信号传递区域序列、dap10×3信号传递区域序列、cd3ζ信号传递区域序列;然后,通过酶切、连接等步骤将所需要的上述合成的各基因序列串联起来,即获得本发明的car分子。材料:hcd19-fc购于acrobiosystemscat#cd9-h5259hcd19-his购于acrobiosystemscat#cd9-h52h2;具体实施例实施例1hcd19蛋白的制备和鉴定按如下步骤制备hcd19蛋白,具体如下:hcd19-fc:在hek293细胞中表达人类cd19重组蛋白(accession#aah06338)。选择人cd19基因编码区pro20-lys291序列(c端使用fc标记)进行转染。用sds-page凝胶鉴定纯化后蛋白。hcd19-his:在hek293细胞中表达人类cd19重组蛋白(accession#p15391-1)。选择人cd19基因编码区pro20-lys291序列(c端使用his标记)进行转染。用sds-page凝胶鉴定纯化后蛋白。实施例2抗体制备(i)抗原共轭结合和免疫(1)将hcd19-fc重组蛋白与多种mabspace免疫增强肽进行免疫共轭,通过sds-page凝胶检测完成共轭蛋白质控;(2)将以上共轭hcd19-fc蛋白中以1:1比例加入弗氏完全佐剂(pierce,cat#77140)进行乳化,然后分别通过皮下和腹腔注射入h2l2小鼠进行免疫。h2l2小鼠由harbourbiomed生产,携带人类可变区域和大鼠恒定区域的基因,且不含有内源性小鼠抗体基因。使用cpg(胞嘧啶-磷硫酰-鸟嘌呤)和明矾进行了额外的免疫,以保存蛋白质的天然结构。第1次免疫后,以及免疫产生后(至少每2周一次)获取小鼠血清,采用elisa法分析抗血清中抗hcd19滴度。(ii)融合在融合前4天,每只小鼠腹腔注射未共轭hcd19-his蛋白的pbs溶液。在融合当日,无菌操作获取小鼠脾脏,并剪切、研磨、过滤成单细胞悬浮液。裂解红细胞,用dmem(gibco)冲洗脾脏细胞。将活的、对数期生长的骨髓瘤细胞(sp2/0)以1:4比例与小鼠脾脏细胞混合。在与peg(聚乙二醇)融合前清洗2次。融合后细胞用dmem培养基清洗后,用10%fbs+hfcs(氢氟烃)+opi+1×hat细胞生长培养基重悬。置于96孔细胞培养板,每孔200μl细胞生长培养基,于37℃、湿润、10%二氧化碳培养箱培养过夜。培养7天,每2-3天,吸出杂交瘤培养基上清(抗体筛选备用),更换新鲜培养基。(iii)elisa筛选抗体96孔板中加入1μg/ml人cd19-his,每孔100μl,在4℃孵育过夜;清洗后,加入100μl杂交瘤培养液上清,与人cd19-his完全结合;加入hrp(辣根过氧化物酶)标记的山羊抗大鼠fc抗体,检测结合的cd19抗体;tmb反应并h2so4终止后,在thermomultiscanfc(450nm)读数。elisa检测阳性的杂交瘤细胞继续培养,继续进一步鉴定分析。实施例3阳性杂交瘤细胞亚克隆获取和小规模抗体生产(i)阳性杂交瘤细胞亚克隆(1)在96孔板上进行elisa阳性杂交瘤细胞梯度稀释,选取具有理想亲和性和阻断活性的细胞;培养7天后,形成细胞克隆团,收集上清,通过抗原结合能力采用实施例2中的方式进一步筛选;(2)通过筛选结果选取具有最高的抗原亲和性的克隆,在杂交瘤生长培养基中扩增培养。7天后,再次检测筛选后的杂交瘤细胞培养液上清的抗原结合能力;亚克隆筛选试验至少两次以上,直到至少90个孔(96孔板);(3)当90多个井显示阳性结合信号时,鉴定出两个抗原结合活性最高的克隆,并将其转移到24孔板培养基中,允许其继续生长2天;一旦24孔板汇合,细胞被转移到6孔板;孵育5天后,部分细胞被冷冻。剩余的细胞被转移到一个烧瓶中并允许扩张;一旦烧瓶汇合,一半的细胞被冷冻(每个克隆3瓶)以作额外的备份,另一半则被允许在培养基中进一步扩大以生产抗体,使用标准方法确定同型。(ii)单克隆抗体的小规模生产(1)将杂交瘤细胞接种于滚瓶,用200-300ml杂交瘤培养基(invitrogen公司)培养14天,从杂交细胞培养中纯化cd19单克隆抗体(mabs)如下:所有净化过程均在室温下进行,采用亲和层析法纯化各种单克隆抗体;(2)离心分离寄主细胞培养液(ccf,cellculturefluid)以清除细胞碎片,然后将ccf上清液过滤、稀释,然后以柱状、蛋白g高效(bio-rad)和平衡的形式加载到蛋白g层析培养基上;(3)负载后,蛋白g柱被洗涤直到280nm处的吸光度回到基线,cd19单克隆抗体用ph值2.5甘氨酸洗脱,然后立刻加入1mtris(每1ml洗脱液)中和,以洗脱液280nm的吸光度为对照,收集含蛋白组分,使蛋白成池;(4)纯化后,通过10,000mwco膜(皮尔斯滑液裂解器或透析管)透析的cd19单克隆抗体利用pbs配置制成,配置完成后,过滤cd19单克隆抗体。实施例4elisa法纯化cd19抗体的结合分析按照实施例2,用elisa法筛选抗体。简单地,0.5μg/mlhcd19-his(acro)孵育涂层,连续稀释纯化抗体将与孵育抗原结合,利用hrp标记的山羊抗大鼠fc抗体可以检测到各抗体的结合信号。用graphpadprism软件计算拟合数据,抗体ec50汇总见图1和表2所示:表2抗体ec50(ng/ml)抗体ec50(ng/ml)16b760.555d925.921f146.616g631.532g758.880g524.621g560.068a331.222a340.931f5119.712d157.156f419.315f228.717b6175.955g159.228c1056.127f1167.252f959.251e92108.080g725.838c120.830e75286.022h123.644c9224.231a224.926c2295.029c12~21539521d532177.027b946.846e62.494e+00644c1275.947d814877.060g10608.845e9446.111h830.140d372.114g933.924e10129.031f529.219d673.716d433.015h1030791.031g626.831f11238.922g1166.6从图1和表2可以看出,抗体与hcd19-his的亲和力不同,但与hcd19-his都有一定的亲和力,选择这些抗体作为嵌合抗原受体的胞外结构域能够实现识别cd19的功能。实施例5通过fortiebio方法进行表位结合第一个cd19抗体用动力学缓冲液(pbs)稀释在装载列微型板块(greinerbio-one),250μl/孔,hcd19-his用动力学缓冲液(pbs)稀释在关联列(associationcolumn),250μl/孔;将ahc传感器放置在第一个基线中,得到第一个基线,然后在装载列中放置300秒,以捕获第一个cd19抗体,然后将传感器放置在第二个基线列中,得到第二个基线;然后将它们放入关联列300秒,让cd19/1cd19抗体完全关联,将传感器放置在第二个cd19抗体列300秒,让第二个cd19抗体与第一ab竞争/不竞争,用fortebio(octet96)分析数据,结果如图2和表3所示,具体如下:表3从图2示例性可以看出,如果第二个cd19ab不能与cd19结合,说明它与第一个具有相似的表位并与之竞争;如果第二种抗体可以不受第一抗体的影响与第一种结合而不产生任何影响,那么它们的表位是不同的,是非竞争的。根据这个结果,根据竞争结果将抗体分为两组,两组表位不同,结果如表3所示,大部分属于bin1,只有两个抗体属于bin2。实施例6用流式细胞仪(facs)对纯化的cd19抗体进行结合分析收集指数期增长cd19表达肿瘤细胞nalm6在pbs和重悬细胞密度105/孔,100μl/孔,在孔中加入稀释cd19抗体,4℃孵育1小时;利用流式细胞仪清洗缓冲液清洗细胞三次,加入抗大鼠igg-alexafluor647(abcam,cat#ab150163)4℃孵育1h;用流式细胞仪洗涤缓冲液清洗细胞3次,流式细胞仪分析样品,结果如图3和表4所示,具体如下:表4如表3所示,27f11、17b6、31a2、11h8、27b9和15f2对nalm6的结合信号最高。背景(抗大鼠igg-alexafluor647)的mfi(meanfluorescenceintensity平均荧光强度)约为450;从图3可以看出,两箱(bin)抗体的结合曲线不同:bin1的27f11、17b6、31a2和11h8结合信号较高,ec50也较高;bin2的55g1和52f9信号较低,ec50较低。实施例7特异性结合(elisa)根据实施例4中所述方法,0.5μg/mlhcd19-his、hvista-his、hpd-l1、hcd40、h41bb和hlag3分别涂层孵育,加入2μg/ml纯化抗体以绑定孵育抗原,利用hrp标记的山羊抗大鼠fc抗体可以检测抗体结合信号,结果如图4所示。如图4所示,这些抗体16b7、21f1、32g7、21g5、22a3、12d1、15f2、55g1、27f11、51e9、38c1、22h1、31a2、27b9、44c12、60g10、11h8、14g9、31f5、16d4、31g6、32g11、55d9、16g6、80g5、68a3、56f4、17b6、28c10、52f9和80g7均未与(除hcd19外)其他抗原发生交叉反应,表明抗体对cd19具有良好的特异性。实施例8杂交抗体的基因克隆和测序通过聚合酶链反应(pcr)扩增获得大鼠抗人cd19抗体轻链和重链可变区序列。利用rna提取试剂盒(takara)分别从表达11h8、17b6、31a2、27f11、15f2、19d6、52f9的杂交瘤细胞中提取总rna,用primescriptii第一链cdna合成试剂盒(takara)合成cdna(oligodt引物)。用简并正向引物和一个反向引物(由抗体同工型决定)克隆igg基因的重链可变区,用mk-f正向引物和ck-r反向引物克隆轻链可变区。每个抗体产生的条带被克隆到反式-5a克隆载体中,10多个克隆的dna使用dnastar测序仪器进行测定。测序结果表明,15f2和19d6的氨基酸序列相同,因此,这个克隆命名为15f2,序列结果如表1所示,具体如下:表1实施例9完全人源化抗体的生产测序分析和确认后,上述每一个基因的可变区克隆入重组表达载体,如轻链可变区序列(vl)融合人类免疫球蛋白iggkappa恒定区克隆到pcdna3.1(+)载体,重链可变区序列(vh)融合人类igg1恒定区克隆到pcdna3.1(+)载体,分别对抗体生产和纯化。实施例10重组完全人源化抗体的表达和纯化重组抗体蛋白的表达和纯化进行了以下步骤:(1)密度(5-6)×106细胞/ml的expicho细胞用expicho表达培养基培养,随后,使用expicho转染试剂盒在expicho细胞转染入等量的重链载体和轻链载体,载体dna最终浓度1.0μg/ml;转染细胞培养在摇动烧瓶125rpm,8%二氧化碳,37℃培养箱,转染后18-22小时添加expicho培养基;(2)于第10天收集细胞混合培养物。通过离心获得富集细胞培养液(hccf,harvestcellculturefluid),然后,将hccf加到rproteina柱(g.e.healthcare),用pbs清洗。用含有20mm柠檬酸的溶液(ph3.2)洗脱igg抗体。最后,洗脱的抗体蛋白中和后,储存在-80℃长期使用,通过sds-page和尺寸排除色谱法(tskgelg3000swxl,tosoh)分析产生的抗体以确定纯度。实施例11纯化的人源化抗体的结合特性(i)通过elisa与人类cd19蛋白结合根据实施例4所述方法,0.5μg/ml的hcd19-his涂层孵育,加入连续梯度稀释的完全人源化抗体与孵育抗原结合。利用hrp标记的山羊抗人fc抗体可以检测到每个抗体的结合信号,结果如图5和表5所示,具体如下:表511h815f217b627f1131a252f9ec502.6293.7794.5223.9954.4587.916从图5和表5可以看出,每个抗体的ec50约为2-8ng/ml,这说明抗体的结合亲和力非常高。(ⅱ)通过流式细胞技术facs检测抗体与nalm6细胞结合根据实施例6所述方法,收集处于对数增长期的nalm6细胞,离心用pbs重悬稀释,细胞密度105/100μl/孔,加入稀释的完全人源化抗体在4℃孵育1h。用流式细胞仪清洗缓冲液清洗细胞三次后,添加抗人igg-cy5(abcam,cat#ab97172)4℃孵育1h,用流式细胞仪洗涤缓冲液清洗细胞3次,流式细胞仪分析样品,结果如图6和表6所示,具体如下:表611h815f217b627f1131a252f9ec502.0564.1615.0262.8094.7631.567从图6和表6可以看出,这些完全人源化抗体11h8、15f2、1786、27f11、31a2和52f9以剂量依赖性的方式与nalm6细胞表达的cdl9结合,1786具有最高的结合信号。实施例12利用完全人源化cd19抗体序列构建嵌合抗原受体t细胞(i)嵌合抗原受体分子载体的构建通过基因合成、分子克隆等手段获得分别嵌合抗cd19完全人源化单克隆抗体scfv序列(如表1抗体序列)的puc57-car19scfv(其中对照组为fmc63),car分子结构如图7所示。通过内切酶pmei和spei对所得到的puc57-car19scfv质粒进行酶切,获得car19scfv基因,然后将car19scfv基因连接至慢病毒载体pwpxld(含gfp基因)中,构建pwpxld-car19scfv-gfp。(ii)嵌合抗原受体t细胞转染可通过病毒载体转导法、基于转座子系统的电转法、以及脂质体介导的质粒转染等方式将嵌合抗原受体分子编码基因整合或转染免疫细胞,随后这些免疫系统在载体启动子驱动下表达该基因,从而使car分子受体表达于免疫细胞表面,此处采用慢病毒转导t细胞方法,具体如下:(1)在150mm培养皿中培养处于对数增长期的293t细胞密度达80-90%时(培养基为:dmem高糖培养基+10%fbs(胎牛血清)+1%双抗(100×青霉素-链霉素混合溶液)),更换培养基:dmem高糖培养基+1%fbs+1%双抗;2-6小时后,用pei将pwpxld-car-gfp或对照质粒pwpxld-gfp、pmd2.g和pspax2三个质粒共同转化293t细胞;于转化后24、48和72小时,收集培养基上清,并加入新鲜培养基(dmem高糖培养基+1%fbs+1%双抗);培养基上清收集完毕,使用0.45umpvdf滤膜过滤,去除细胞碎片,放置在4℃冰箱待用;(2)t细胞的分离纯化:通过ficoll密度梯度法分离出血液中的单个核细胞,经红细胞裂解液裂解去除红细胞后,再通过macspan-t磁珠分选出t细胞;分选出来的t细胞用培养基aim-v加5%fbs、青霉素100u/ml和链霉素0.1mg/ml稀释至浓度2.5×106个/ml待用;通过包被cd2、cd3、cd28抗体的磁珠(美天旎)刺激t细胞,根据美天旎提供的protocol进行刺激,即磁珠与t细胞比例为1:2,t细胞密度为5×106个/ml/cm2,t细胞在37℃、5%co2培养箱培养刺激48h;(3)t细胞的慢病毒转染:将激活后的t细胞中的磁珠通过磁场作用去除,300g离心5min,去上清,用新鲜培养基重悬,分别加入car载体慢病毒和8μg/ml的polybrene和300iu/mlil-2,病毒加入量为moi=10。37℃,5%co2培养箱培养24h后,300g离心5min,去上清,用含300iu/mlil-2的新鲜培养基重悬,37℃、5%co2培养箱培养;(4)cart细胞扩增:将cart细胞密度维持在1×106个/ml左右,每2-3天进行一次半量换液。两周后,t细胞数可扩增100倍,gfp阳性的细胞为转染成功的cart细胞,gfp阳性比例通过流式进行检测,即得到cart细胞或对照t细胞的比例。实施例13完全人源化抗体cart细胞对肿瘤细胞的体外特异性杀伤试验(1)将实施例12制备的抗cd19完全人源化cart(不同scfv序列15f2、17b6、27f11、31a2、11h8、31a2、52f9)、fmc63(鼠源)cart和野生型t细胞分别以不同比例与1×104的肿瘤细胞混合,加入到96孔u型板中,每组设3个复孔,并设单独加肿瘤细胞组作为阳性对照,250g离心5min后,置于37度5%co2培养箱共培养18h;(2)荧光素酶(luciferase)定量杀伤效率检测:cart细胞与肿瘤细胞共培养或肿瘤细胞单独培养后18小时,在96孔细胞培养板中加入100μl/孔的荧光素酶底物(1×),将细胞重悬混匀,立即通过多功能酶标仪测定rlu(relativelightunit),测定时间设为1秒。杀伤比例计算公式:100%×(对照孔读数-实验孔读数)/对照孔读数(不加细胞的空白组读数可以忽略);体外比较抗cd19完全人源化cart(不同scfv序列的)、fmc63cart和野生型t细胞对表达cd19抗原的肿瘤细胞的识别杀伤功能时,肿瘤细胞选用raji-gl细胞系和nalm6-gl(荧光素酶基因luciferase),结果如图8-11所示;结果显示,与gfp-t野生型t细胞相比,表达11h8,15f2,17b6,27f11,31a2scfv的car-t细胞对cd19阳性靶细胞具有较强的体外识别和杀伤能力,且杀伤水平基本不低于鼠源fmc63scfvcar-t细胞。体外比较抗cd19完全人源化cart(不同scfv序列的)、fmc63cart和野生型t细胞对不表达cd19抗原的肿瘤细胞的识别杀伤功能(cart细胞安全性试验)时,肿瘤细胞选用不表达cd19抗原的急性髓系白血病细胞系aml3,肺癌细胞系a549-gl、h460-gl,胃癌细胞系mkn28,snu1,肝癌细胞系smmc和hepg2,结果如图12-20所示;结果显示,与gfp-t野生型t细胞相比,表达抗cd19完全人源化scfv的car-t细胞对测试的cd19阴性靶细胞基本不具有特异性识别和杀伤作用。综上所述,本申请中的cd19抗原识别结合结构域经过人源化改造,不影响其对肿瘤细胞靶点抗原的识别能力,同时可能降低异种免疫排斥的发生概率,从而提升car-t细胞在人体中的持续时间,增强其对肿瘤细胞的免疫监控能力,降低肿瘤复发率,患者完全缓解期也可相应延长。申请人声明,本发明通过上述实施例来说明本发明的产品、用途及其使用方式,但本发明并不局限于上述详细用途和使用方式,即不意味着本发明必须依赖上述详细用途和使用方式才能实施。所属
技术领域:
的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。sequencelisting<110>广东昭泰体内生物医药科技有限公司<120>一种嵌合抗原受体及其应用<130>2019<160>12<170>patentinversion3.3<210>1<211>133<212>prt<213>人工合成序列<400>1glnvalglnleuvalgluserglyglyglyvalvalglnproglyarg151015serleuargleusercysalaalaserglyphethrpheserarghis202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045alavaliletrptyraspglyserasnglntyrtyrvalaspserval505560lysglyargphethrileserargaspasnserlysasnthrleuasp65707580leuglnmetasnserleuargvalgluaspthralavaltyrtyrcys859095alaargargserilethrtrptyrglyglypheaspiletrpglygln100105110glythrmetvalthrvalserseralaglnthrthralaproserval115120125tyrproleualapro130<210>2<211>133<212>prt<213>人工合成序列<400>2glnvalglnleuvalgluserglyglyglyvalvalglnproglyarg151015serleuargleusercysglualaserglyphethrpheserarghis202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045alavalilephetyraspglyserglnasntyrtyralaaspserval505560argglyargphethrileserargaspasnserlysasnthrleuser65707580leuglnmetaspserleuargalagluaspthralavaltyrtyrcys859095alaargargserilethrtrpasnglyglypheaspiletrpglygln100105110glythrmetvalthrvalserproalaglnthrthralaproserval115120125tyrproleualapro130<210>3<211>133<212>prt<213>人工合成序列<400>3glnvalglnleuvalgluserglyglyglyvalvalglnproglyarg151015serleuargleusercysalaalaserglyphethrpheserarghis202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045alavaliletrptyraspglyserasnlystyrtyrvalaspserval505560lysglyargphethrileserargaspasnserlysasnthrleuasp65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaargargserilethrtrpaspglyalapheaspiletrpglygln100105110glythrmetvalthrvalserseralaglnthrthralaproserval115120125tyrproleualapro130<210>4<211>133<212>prt<213>人工合成序列<400>4glnvalglnleuvalgluserglyglyglyvalvalglnproglyarg151015serleuargleusercysalaalaserglyphethrpheserarghis202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045alavaliletyrtyraspglyserasnlystyrtyrvalaspserval505560lysglyargphethrileserargaspasnserlysasnthrleuasp65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaargargserilethrtrpasnglyalapheaspiletrpglygln100105110glythrmetvalthrvalserseralaglnthrthralaproserval115120125tyrproleualapro130<210>5<211>133<212>prt<213>人工合成序列<400>5glnvalglnleuvalgluserglyglyglyvalvalglnproglyarg151015serleuargleusercysalaalaserglyphethrpheserarghis202530glymethistrpvalargglnalaproglylysglyleuglutrpval354045alavaliletrptyraspglyserasnlystyrtyrvalaspserval505560lysglyargphethrileserargaspasnserlysasnthrleuasp65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaargargserilethrtrpaspglyalapheaspiletrpglygln100105110glythrmetvalthrvalserseralaglnthrthralaproserval115120125tyrproleualapro130<210>6<211>138<212>prt<213>人工合成序列<400>6glnvalglnleuvalgluserglyglyglyvalvalglnalaglyarg151015serleuargleusercysalaalaserglyphethrpheserasntyr202530glyilehistrpvalargglnalaproglylysglyleuglutrpval354045glyvaliletrphisaspglyserilelysasntyralaasppheval505560lysglyargphethrileserargaspasnsergluaspthrleutyr65707580leuglnmetasnserleuargalagluaspthralavaltyrtyrcys859095alaarggluglnglyasntyrtyrglytrpglysertyrlysalaphe100105110aspiletrpglyglnglythrmetvalthrvalserseralaglnthr115120125thralaproservaltyrproleualapro130135<210>7<211>106<212>prt<213>人工合成序列<400>7aspileglnmetthrglnserproserthrleuseralaservalgly151015aspargvalthrilethrcysargalaserglnserilesersertrp202530leualatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrlysalaserserleugluserglyvalproproargphesergly505560serglyserglythrgluphethrleuthrileserserleuglnpro65707580aspaspphealathrtyrtyrcysglnglntyrasnseralatyrthr859095pheglyglnglythrlysleugluilelys100105<210>8<211>106<212>prt<213>人工合成序列<400>8aspileglnmetthrglnserproserthrleuseralaservalgly151015aspargvalthrilethrcysargalaserglnserilesersertrp202530leualatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrlysalaserserleugluserglyvalproserargphesergly505560serglyserglythrgluphethrleualaileserserleuglnpro65707580aspaspphealathrtyrtyrcysglnglntyrasnargphetyrthr859095pheglyglnglythrlysleugluilelys100105<210>9<211>106<212>prt<213>人工合成序列<400>9aspileglnmetthrglnserproserthrleuseralaservalgly151015aspargvalthrilesercysargalaserglnserilesersertrp202530leualatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrlysalaserserleugluserglyvalproserargphesergly505560serglyserglythrgluphethrleuthrileserserleuglnpro65707580aspaspphealathrtyrtyrcysglnglntyrasnseralatyrthr859095pheglyglnglythrlysleugluilelys100105<210>10<211>106<212>prt<213>人工合成序列<400>10aspileglnmetthrglnserproserthrleuseralaservalgly151015aspargvalthrilesercysargalaserglnserilesersertrp202530leualatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrlysalaserserleugluserglyvalproserargphesergly505560serglyserglythrgluphethrleuthrileserserleuglnpro65707580aspaspphealathrtyrtyrcysglnglntyrasnseralatyrthr859095pheglyglnglythrlysleugluilelys100105<210>11<211>106<212>prt<213>人工合成序列<400>11aspileglnmetthrglnserproserthrleuseralaservalgly151015aspargvalthrvalthrcysargalaserglnserileargsertrp202530leualatrptyrglnglnlysproglylysalaprolysleuleuile354045tyrlysalaserserleugluserglyvalproserargphesergly505560serglyserglythrgluphethrleuthrileserserleuglnpro65707580aspaspphealathrtyrtyrcysglnglntyrasnseralatyrthr859095pheglyglnglythrlysleugluilelys100105<210>12<211>107<212>prt<213>人工合成序列<400>12aspileglnleuthrglnserproserpheleuservalphevalgly151015aspargvalthrilethrcysargalaserglnglyileserasntyr202530leualatrptyrglnglnlysproglylysalaprogluleuleuleu354045tyralathrserthrleuglnserglyvalproserargleusergly505560serglyserglythrgluphethrleuthrleuserserleuglnpro65707580gluaspphealathrtyrtyrcysglnglnvaltyrserpheprotyr859095thrpheglyglnglythrlysleugluilelys100105当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1