一种7-苯基-6-庚炔酸的制备方法与流程
本发明涉及有机化学领域,特别是涉及一种7-苯基-6-庚炔酸的制备方法。
背景技术:
三丁基锡(tbt)曾经被用来阻止藻类和海洋植物、贝类、海洋郁金香及类似物在船只上的生长,其原因在于这些生物的生长会使船只产生额外的摩擦力,从而必然带来大量的能源上的损耗。但是,tbt不仅影响依附在船只侧面的海洋生物,还会使与其接触的其他海洋生物中毒,具有大量环境上的副作用,已被国际海事组织(imo)禁止在船舶漆中的所有应用。
苯基辣椒碱化学名为:n-(4-羟基-3-甲氧基苯甲基)-7-苯基-6-炔庚酰胺,目前主要作为微生物防护剂用于防污漆的生产,尤其是在用于船舶装置和船只的漆和涂料中,有广泛应用。苯基辣椒碱具备防污效果好、不易流失、效力持久等特点,是目前市场上少有的优秀的tbt替代品,具有很好的市场前景,苯基辣椒碱的化学结构式如下所示:
7-苯基-6-庚炔酸是合成苯基辣椒碱的关键中间体,其合成路线对于苯基辣椒碱整体的制备起着至关重要的作用。目前,合成苯基辣椒碱的路线和方法主要如下:1)lalezari,i.等(journalofheterocyclicchemistry,1973,vol.10,p.655–658)报道的路线中,以为3-硒杂咪唑衍生物起始物料,经氢氧化钠,加热,再用二氧化硅,180℃热解方法得到7-苯基-6-庚炔酸,该方法起始原料不是常规化工产品,如需自制,含硒物质污染性较大,而且热解温度过高,危险性高,该方法不适合用于工业化生产;2)专利cn1849068a及其国际申请wo2005/025314中,采用不太稳定的5-氯戊醇为起始原料,经thp保护羟基、碘取代、与苯基炔化锂反应、脱保护、氧化共5步反应,制备得到7-苯基-6-庚炔酸,该方法路线长,成本高,第三步的苯基炔化锂需要用苯乙炔和丁基锂在超低温下自制,第五步氧化反应采用铬系氧化剂,铬系氧化剂与底物7-苯基-6-庚炔醇的摩尔用量比为2.2:1,因为大量使用到对人体、环境危害极大的铬系氧化剂,难以实现工业化生产,且由于苯乙炔基团对其他很多氧化试剂敏感,用其他方法实现这一转化很难取得满意效果;3)专利wo2015/144902报道用另外一种合成方法,以碘苯和6-庚炔酸为原料,在碘化铜和四三苯基膦钯(0)的催化下50℃反应16小时,得棕色固体产品7-苯基-6-庚炔酸,收率82%,该方法所需原料不易合成,碘化铜和钯重金属催化剂价格昂贵,总体成本过高;4)专利cn102060689a报道了用7-苯基-7-羰基庚酸为起始原料,与五氯化磷反应,再用氢氧化钠碱化后消除hcl,再酸化得到7-苯基-6-庚炔酸,该路线原料不易得,需多步反应合成,且用污染较大的五氯化磷,反应刺激性和污染性较大,还需特殊精馏、收率低,不适合工业化大生产。
技术实现要素:
鉴于以上所述现有技术的缺点,本发明的目的在于提供一种7-苯基-6-庚炔酸的制备方法,用于解决现有技术中的问题。
为实现上述目的及其他相关目的,本发明提供一种7-苯基-6-庚炔酸的制备方法,包括:
1)将苯乙炔和5-卤代戊腈在碱存在的条件下进行烷基化反应,制备获得式i化合物;
2)将式i化合物水解,以提供7-苯基-6-庚炔酸;
在本发明一些实施方式中,所述步骤1)中,5-卤代戊腈选自5-氯戊腈、5-溴戊腈、5-碘戊腈中的一种或多种的组合。
在本发明一些实施方式中,所述步骤1)中,反应在反应溶剂存在的条件下进行。
在本发明一些实施方式中,所述步骤1)中,反应在气体保护的条件下进行。
在本发明一些实施方式中,所述步骤1)中,所述碱选自dmso/nah、nanh2、na、kh中的一种或多种的组合。
在本发明一些实施方式中,所述步骤1)中,反应温度为-20~20℃,优选为-5~10℃,更优选为-1~5℃。
在本发明一些实施方式中,所述步骤1)中,苯乙炔和5-卤代戊腈的摩尔比为1~2:1,优选为1.3~1.8:1,更优选为1.5~1.7:1。
在本发明一些实施方式中,所述步骤1)中,将苯乙炔和5-卤代戊腈逐量加入包括碱的反应体系中。
在本发明一些实施方式中,所述步骤1)中,反应溶剂选自醚类溶剂。
在本发明一些实施方式中,所述步骤1)中,碱与苯乙炔的摩尔比为0.5~1:1,优选为0.55~0.65:1。
在本发明一些实施方式中,所述步骤1)中,通过惰性气体提供所述气体保护的条件。
在本发明一些实施方式中,所述步骤1)中,反应溶剂选自thf、乙二醇二甲醚、乙二醇二乙醚、dmf中的一种或多种的组合。
在本发明一些实施方式中,所述步骤1)中,所述惰性气体选自氮气、氦气、氖气、氩气、氪气、氙气中的一种或多种的组合。
在本发明一些实施方式中,所述步骤1)中,还包括:反应完成后加水淬灭,有机相脱溶。
在本发明一些实施方式中,所述步骤2)中,将式i化合物在酸性条件下水解。
在本发明一些实施方式中,所述步骤2)中,通过hcl、磷酸、硫酸中的一种或多种的组合提供所述酸性条件。
在本发明一些实施方式中,所述步骤2)中,反应在反应溶剂存在的条件下进行,反应溶剂优选包括水。
在本发明一些实施方式中,所述步骤2)中,反应温度为室温至反应溶剂的沸点温度。
在本发明一些实施方式中,所述步骤2)中,还包括:中和反应体系中的酸,有机溶剂萃取,水相酸化,固液分离获取固相物,优选的,将水相酸化至ph≤3,更优选的,将水相酸化至ph=2~3。
在本发明一些实施方式中,所述步骤2)中,将式i化合物在碱性条件下水解。
在本发明一些实施方式中,所述步骤2)中,碱与式i化合物的摩尔比为1~2:1,优选为1.3~1.8:1,更优选1.5~1.7:1,优选通过有机碱提供所述碱性条件,所述有机碱优选选自叔丁醇钾、三苯甲基钾中的一种或多种的组合。
在本发明一些实施方式中,所述步骤2)中,反应在反应溶剂存在的条件下进行,反应溶剂优选包括水和有机溶剂,所述有机溶剂优选为醇类溶剂,所述醇类溶剂选自甲醇、乙醇、丙醇、异丙醇中的一种或多种的组合。
在本发明一些实施方式中,所述步骤2)中,反应温度为室温至反应溶剂的沸点温度。
在本发明一些实施方式中,所述步骤2)中,还包括:脱溶,有机溶剂萃取,有机相酸化,固液分离获取固相物,优选的,将有机相酸化至ph≤3,更优选的,将有机相酸化至ph=2~3。
附图说明
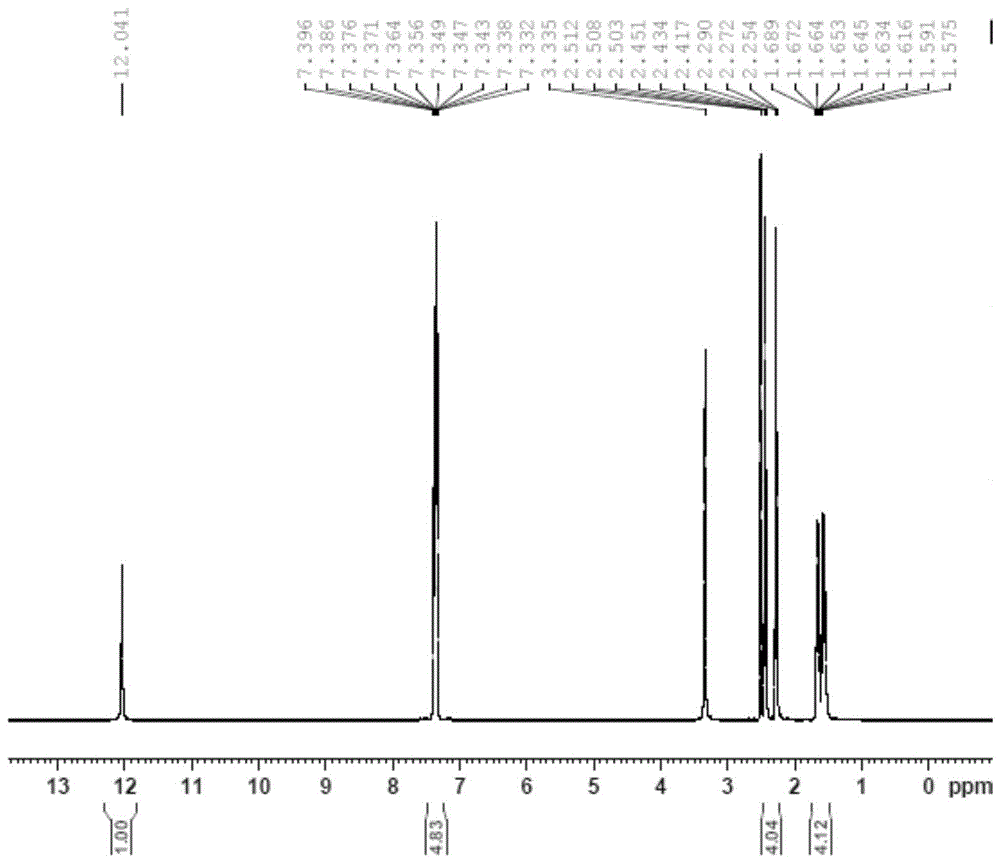
图1显示为本发明实施例3所制备的7-苯基-6-庚炔酸氢的核磁图谱示意图。
图2显示为本发明实施例3所制备的7-苯基-6-庚炔酸氢的质谱图谱示意图。
具体实施方式
本发明发明人经过大量实践研究,提供了一种新的7-苯基-6-庚炔酸的制备方法,所述7-苯基-6-庚炔酸的制备方法具有高收率、低成本、低能耗等优点,是一种更加经济、安全、环保的制备7-苯基-6-庚炔酸的方法,在此基础上完成了本发明。
本发明提供一种7-苯基-6-庚炔酸的制备方法,包括:
1)将苯乙炔和5-卤代戊腈在碱存在的条件下进行烷基化反应,制备获得式i化合物;
2)将式i化合物水解,以提供7-苯基-6-庚炔酸。
本发明所提供的7-苯基-6-庚炔酸的制备方法,可以包括:将式i化合物水解,制备获得7-苯基-6-庚炔酸,反应方程式如下:
本发明所提供的制备方法中,所述式i化合物可以在酸性条件下水解,以提供7-苯基-6-庚炔酸(式ii化合物)。式i化合物末端的氰基在酸的催化下可以水解为羧基,从而制备获得式ii化合物。可以用于提供所述酸性条件的酸可以是包括但不限于hcl(例如,浓盐酸)、磷酸、硫酸(例如,55~65wt%硫酸)等中的一种或多种的组合,酸的用量相对于式i化合物往往是过量的,例如,每1g式i化合物可以使用10~15ml酸进行水解。
本发明所提供的制备方法中,式i化合物在酸性条件下的水解反应通常可以在反应溶剂存在的条件下进行,所述反应溶剂通常为反应体系的良溶剂、且包括水,水解反应的溶剂通常包括水。本领域技术人员可选择合适的反应溶剂的用量,例如,每1g反应底物通常可以使用5~20ml反应溶剂。
本发明所提供的制备方法中,式i化合物在酸性条件下的水解反应的反应温度可以为室温至反应溶剂的沸点温度,例如,水解反应可以在80~100℃的温度条件下进行。本领域技术人员可根据反应进程调整反应时间,例如,可以通过tlc、色谱法等方法判断水解反应的反应进程,再例如,酸性条件下的水解反应的反应时间可以是为1~20小时。
本发明所提供的制备方法中,本领域技术人员可选择合适的方法,对式i化合物在酸性条件下的水解反应的产物进行后处理,例如,可以包括:中和反应体系中的酸,有机溶剂萃取,水相酸化,固液分离获取固相物。反应完成后,可以先中和体系中的酸,例如,可以将反应体系的ph调节至中性或弱碱性(例如,ph=7~8),再例如,中和体系中的酸时所使用的碱可以为碳酸氢钠等,随后可以使用合适的有机溶剂萃取,萃取后所获的水相可以进一步进行进行酸化,例如,可以将水相酸化至ph≤3,优选可以将水相酸化至ph=2~3,再例如,酸化时所使用的酸可以是hcl等,即可析出目标产物,固液分离后即可制备获得式ii化合物。
本发明所提供的制备方法中,所述式i化合物可以在碱性条件下水解,以提供7-苯基-6-庚炔酸(式ii化合物)。式i化合物末端的氰基在碱的催化下可以水解为羧基,从而制备获得式ii化合物。碱的用量相对于式i化合物往往是过量的,例如,碱与式i化合物的摩尔比可以为1~2:1,优选可以为1.3~1.8:1,更优选可以为1.5~1.7:1,可以用于提供所述碱性条件的碱可以是有机碱等,具体可以是包括但不限于叔丁醇钾、三苯甲基钾等中的一种或多种的组合。
本发明所提供的制备方法中,式i化合物在碱性条件下的水解反应通常可以在反应溶剂存在的条件下进行,所述反应溶剂通常为反应体系的良溶剂、且包括水,例如,水解反应的溶剂通常包括水和有机溶剂,所述有机溶剂优选为醇类溶剂,所述醇类溶剂选自甲醇、乙醇、丙醇、异丙醇等中的一种或多种的组合。本领域技术人员可选择合适的反应溶剂的用量,例如,每1g反应底物通常可以使用3~20ml反应溶剂。
本发明所提供的制备方法中,式i化合物在碱性条件下的水解反应的反应温度可以为室温至反应溶剂的沸点温度,例如,水解反应可以在20~40℃的温度条件下进行。本领域技术人员可根据反应进程调整反应时间,例如,可以通过tlc、色谱法等方法判断水解反应的反应进程,再例如,碱性条件下的水解反应的反应时间可以是为1~24小时。
本发明所提供的制备方法中,本领域技术人员可选择合适的方法,对式i化合物在碱性条件下的水解反应的产物进行后处理,例如,可以包括:脱溶,有机溶剂萃取,有机相酸化,固液分离获取固相物。反应完成后,可以脱除反应溶剂,随后可以使用合适的有机溶剂萃取,萃取后所获的有机相可以进一步进行酸化,例如,可以将有机相酸化至ph≤3,优选可以将有机相酸化至ph=2~3,再例如,酸化时所使用的酸可以是hcl等,即可析出目标产物,固液分离后即可制备获得式ii化合物。
本发明所提供的7-苯基-6-庚炔酸的制备方法,还可以包括:将苯乙炔和5-卤代戊腈在碱存在的条件下进行烷基化反应,制备获得式i化合物,反应方程式如下:
本发明所提供的制备方法中,所使用的碱通常可以是dmso/nah体系、nanh2、na、kh等中的一种或多种的组合,碱的使用量对于本领域技术人员来说应该是可以选择的,例如,碱与苯乙炔的摩尔比可以为0.5~1:1,优选可以为0.55~0.65:1。
本发明所提供的制备方法中,反应方程式中,x可以选自cl、br、或i,即所述5-卤代戊腈具体可以是5-氯戊腈、5-溴戊腈、5-碘戊腈等中的一种或多种的组合。苯乙炔的用量相对于5-卤代戊腈通常是基本等量或者过量的,例如,苯乙炔和5-卤代戊腈的摩尔比可以为1~2:1,优选可以为1.3~1.8:1,更优选可以为1.5~1.7:1。在投料过程中,苯乙炔和5-卤代戊腈通常可以逐量被加入包括碱的反应体系中,从而可以避免副反应的发生。
本发明所提供的制备方法中,苯乙炔和5-卤代戊腈的反应通常在溶剂存在的条件下进行,所述反应溶剂通常为反应体系的良溶剂,例如,苯乙炔和5-卤代戊腈的反应中所使用的反应溶剂可以选自醚类溶剂等,所述反应溶剂具体可以选自乙二醇二甲醚、乙二醇二乙醚、dmf、thf等中的一种或多种的组合。本领域技术人员可选择合适的反应溶剂的用量,例如,每1g反应底物通常可以使用5~20ml反应溶剂。
本发明所提供的制备方法中,苯乙炔和5-卤代戊腈的反应通常在气体保护的条件下进行。本领域技术人员可选择合适的方法提供反应的气体保护的条件,例如,可以通过使用惰性气体提供所述气体保护的条件,所述惰性气体通常可以是氮气和/或稀有气体,具体可以是氮气、氦气、氖气、氩气、氪气、氙气等中的一种或多种的组合。
本发明所提供的制备方法中,苯乙炔和5-卤代戊腈的反应通常在较低温度下进行,例如,反应可以在-20~20℃的温度条件下进行,优选可以为-5~10℃的温度条件,更优选可以为-1~5℃的温度条件。本领域技术人员可根据反应进程调整反应时间,例如,可以通过tlc、色谱法等方法判断水解反应的反应进程,再例如,苯乙炔和5-卤代戊腈的反应时间可以是为1~20小时。
本发明所提供的制备方法中,本领域技术人员可选择合适的方法,对苯乙炔和5-卤代戊腈的反应的产物进行后处理,例如,可以包括:反应完成后加水淬灭,有机相脱溶。反应完成后,可以加入水对反应体系进行淬灭,随后可以加入合适的有机溶剂萃取,萃取获得的有机相脱除溶剂,即可获得式i化合物。
本发明所提供的7-苯基-6-庚炔酸的制备方法具有原辅料均价廉易得、成本低廉,且反应条件温和、反应步骤少、反应稳定可控,特别是氰基水解的反应,活性部位少,不易发生副反应,反应完毕后,调节ph即可得到产品,后处理非常简便,整条路线的收率和质量都较好,且节约能源,环境友好。
以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。
须知,下列实施例中未具体注明的工艺设备或装置均采用本领域内的常规设备或装置。
此外应理解,本发明中提到的一个或多个方法步骤并不排斥在所述组合步骤前后还可以存在其他方法步骤或在这些明确提到的步骤之间还可以插入其他方法步骤,除非另有说明;还应理解,本发明中提到的一个或多个设备/装置之间的组合连接关系并不排斥在所述组合设备/装置前后还可以存在其他设备/装置或在这些明确提到的两个设备/装置之间还可以插入其他设备/装置,除非另有说明。而且,除非另有说明,各方法步骤的编号仅为鉴别各方法步骤的便利工具,而非为限制各方法步骤的排列次序或限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容的情况下,当亦视为本发明可实施的范畴。
实施例1
式i化合物的制备:
在反应釜里一次抽入20kgdmso,通入氮气,60%nah2.5kg,水浴温度升至50~60℃时,降温至10℃,加入36kg乙二醇二甲醚,继续降温至-1℃,滴加苯乙炔5kg,滴加5kg5-溴戊腈,3小时后滴加结束,内温3℃,控制温度0-5℃继续搅拌1小时。向反应釜中缓慢加入50kg水,形成深色溶液,降温至20℃,分出两相。将淡黄色有机相分别用水20kg,用饱和食盐水20kg洗涤。得到有机相加入3kg无水硫酸钠干燥,过滤,滤液在-0.07mpa真空和40~50℃水浴下,浓缩,得到5.3kg中间体(1),收率94%,1hnmr(400mhz,cdcl3):δ7.40~7.26(m,5h),2.43~2.47(m,2h),2.34~2.36(m,2h),1.70~1.83(m,4h).ms[m-h]-:182.39。
实施例2
式i化合物的制备:
在反应釜里一次抽入20kgdmso,通入氮气,60%nah2.5kg,水浴温度升至50~60℃时,降温至10℃,加入36kg乙二醇二甲醚,继续降温至-1℃,滴加苯乙炔5kg,滴加3.2kg5-氯戊腈,3小时后滴加结束,内温5℃,控制温度0-5℃继续搅拌12小时。向反应釜中缓慢加入50kg水,形成深色溶液,降温至20℃,分出两相。将淡黄色有机相分别用水20kg,用饱和食盐水20kg洗涤。得到有机相加入3kg无水硫酸钠干燥,过滤,滤液在-0.07mpa真空和40~50℃水浴下,浓缩,得到4.5kg中间体(1),收率80%,ms[m+h]+:184.18。
实施例3
式i化合物的制备:
在反应釜里一次抽入20kgdmso,通入氮气,30%kh4kg,水浴温度升至50~60℃时,降温至10℃,加入40kg四氢呋喃,继续降温至-1℃,滴加苯乙炔5kg,滴加5kg5-溴戊腈,1.5小时后滴加结束,内温3℃,控制温度0-5℃继续搅拌2小时。向反应釜中缓慢加入50kg水,形成深色溶液,降温至20℃,分出两相。将淡黄色有机相分别用水20kg,用饱和食盐水20kg洗涤。得到有机相加入3kg无水硫酸钠干燥,过滤,滤液在-0.07mpa真空和40~50℃水浴下,浓缩,得到5.4kg中间体(1),收率96%,ms[m-h]-:182.34。
实施例4
式ii化合物(7-苯基-6-庚炔酸)的制备:
酸水解方法:
反应釜中加入4l浓盐酸溶液,再加入0.36kg式i化合物,并将氯化氢气体鼓泡通过水10分钟,并将反应混合物加热至100℃,保持20小时。将混合物冷却至室温,加入冷的碳酸氢钠溶液直至ph为7~8。萃取水层并用二氯甲烷洗涤。将水溶液用浓hcl酸化至ph≤3,析出产物,收集为淡黄色固体(0.11kg,收率27%)。
实施例5
式ii化合物(7-苯基-6-庚炔酸)的制备:
碱水解方法:
反应釜中加入13.5kg水,13.5kg异丙醇,4.94kg叔丁醇钾,5.4kg式i化合物,在室温条件下水解,反应3小时后蒸出异丙醇,用二氯甲烷提取杂质,然后调酸至ph≤3,析出产物,得到淡黄色固体5.36kg,hplc纯度98.8%,收率90%。
1hnmr(400mhz,dmso-d6):δ12.04(s,1η),7.40~7.33(m,5h),2.45~2.25(m,4h),1.69~1.65(m,2h),1.64~1.58(m,2h)。核磁图谱具体如图1所示,质谱图谱如图2所示,ms[m-h]-:201.54。
综上所述,本发明有效克服了现有技术中的种种缺点而具高度产业利用价值。
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
- 还没有人留言评论。精彩留言会获得点赞!