一种吡虫隆的制备方法与流程
本发明涉及有机合成技术领域,特别涉及一种吡虫隆的制备方法。
背景技术:
吡虫隆,别名1-(4-氯-3-(3-氯-5-三氟甲基-2-吡啶氧基)苯基)-3-(2,6-二氟苯甲酰基)脲,分子式:c20h10cl2f5n3o3。吡虫隆为新一代高效的苯甲酰脲类昆虫生长调节剂,作为兽药主要用于动物体外寄生虫的驱杀,为广谱抗寄生虫药,具有很强的杀虫和杀卵活性。
现有技术公开了生物驱虫药吡虫隆的制备方法,申请公布号cn101209992,申请公布日20080702,该方法以2-氯-5氨基苯酚、2,6-二氯苯甲酰胺和草酰氯为原料,经三步带压反应合成吡虫隆的方法,该方法需要加压反应,且收率只有52%~62%,不利于工业化生产。
现有技术还公开了一种吡虫隆的化学合成方法,申请公布号cn101906070a,申请公布日20101208,该方法为:2-氯-5-硝基苯酚和2,3-二氯-5-三氟甲基吡啶醚化后在用硫氢化钠还原制备成2,6-二氟苯甲酰异腈酸酯;再与4-氯-3-(3-氯-5-三氟甲基-2-吡啶氧基)苯胺进行加成反应制得吡虫隆,此方法收率相对较低。
现有技术还公开了吡虫隆及其制备方法,授权公告号cn104876859b,授权公告日20180313,该方法通过一种2,6-二氟苯甲酰胺和草酰氯制备2,6-二氟苯异腈酸酯;2-氯-5-硝基苯酚与2,3-二-5-三氟甲基吡啶醚化后产物再与2,6-二氟苯异腈酸酯合成吡虫隆,此工艺步骤繁琐,催化剂价格昂贵。
技术实现要素:
本发明的目的是提供一种简化工艺步骤,提高收率的吡虫隆的制备方法。为了实现上述发明目的,本发明吡虫隆的制备方法采用的如下技术方案:
一种吡虫隆的制备方法,包括如下步骤:
(1)2,6-二氟苯甲酰胺与草酰氯反应生成式ⅰ,
(2)在溶剂中,2-氯-5-氨基苯酚与碳酸钾反应生成式ⅱ,
(3)式ⅰ和式ⅱ在催化剂的条件下反应生成式ⅲ,
(4)式ⅲ和2,3-二氯5-三氟甲基吡啶反应生成吡虫隆,
优选的,步骤(1)中的2,6-二氟苯甲酰胺与草酰氯的摩尔比为1:1.2~1.8。
优选的,所述2,6-二氟苯甲酰胺与2-氯-5-氨基苯酚的摩尔比为:1:0.95~0.99。
优选的,所述2,3-二氯5-三氟甲基吡啶与2,6-二氟苯甲酰胺的摩尔比为:1:0.95~0.99。
优选的,所述碳酸钾与2,6-二氟苯甲酰胺的摩尔比为:1:0.77~1。
优选的,步骤(2)中的溶剂为甲苯。
优选的,步骤(3)中的催化剂为dmf和四丁基溴化铵。催化剂为dmf和四丁基溴化铵,降低价格,控制成本。
与现有技术相比,本发明的有益效果在于:
本发明采用新的工艺制备吡虫隆,此工艺中间产品不需要进行处理,直接用于下一步反应并得到最终产品,不仅减少操作步骤,简化工艺,同时,提高了产品收率和纯度;并且,通过减少对中间产品的处理,从而减少降低产品能耗、减少环境污染和废液的产生。
附图说明
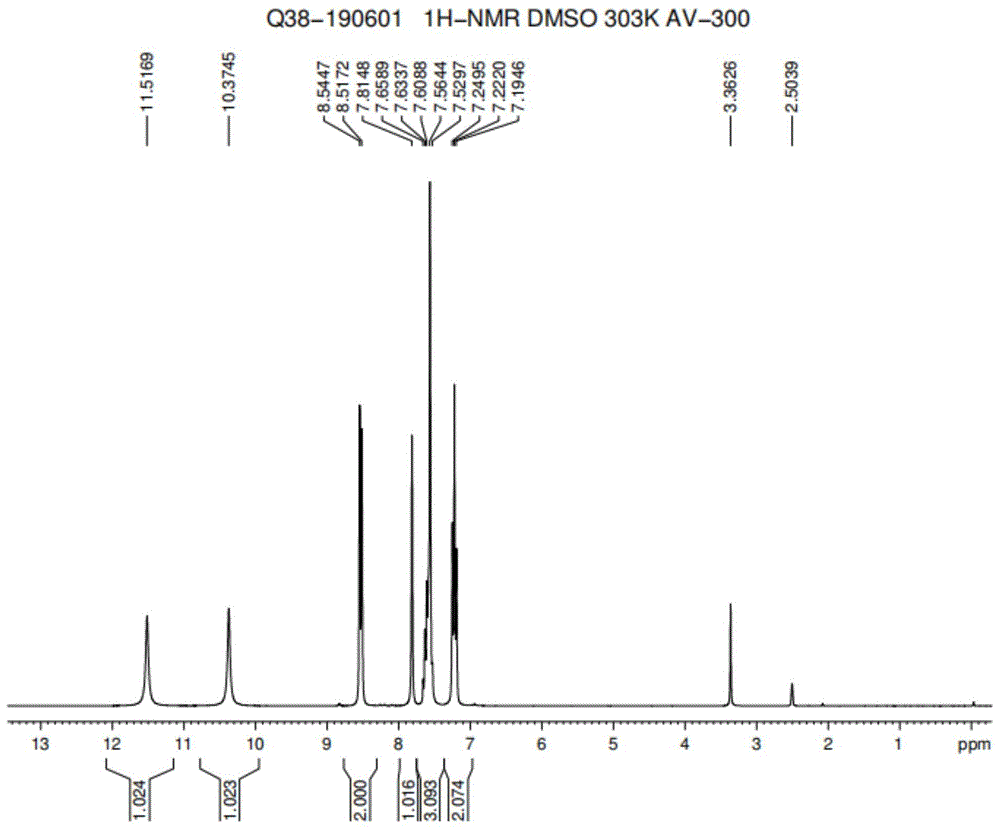
图1为本发明制备的吡虫隆的核磁共振氢谱图;
图2为本发明制备的吡虫隆的核磁共振碳谱图;
图3为本发明制备的吡虫隆的质谱图。
具体实施方式
下面结合具体实施方式,进一步阐明本发明,应理解这些实施方式仅用于说明本发明而不用于限制本发明的范围,在阅读了本发明之后,本领域技术人员对本发明的各种等价形式的修改均落于本申请所附权利要求所限定的范围。
实施例1:
(1)反应釜中投入甲苯60ml,0.1mol的2,6-二氟苯甲酰胺15.7g,25℃开始滴加0.12mol草酰氯15.2g,滴加完后,调整温度至40-50℃保温反应1小时,保温结束,缓慢升温至微回流,于100-115℃保温反应5-6小时;降温至10~30℃,制得备用液式ⅰ;
(2)向干燥洁净反应釜中投入0.095mol的2-氯-5-氨基苯酚13.7g,0.077mol的碳酸钾10.6g、甲苯60ml室温搅拌30min,得到式ⅱ;
(3)向式ⅱ中滴加备用液式ⅰ,控制温度15~35℃,滴完后加入四丁基溴化铵0.1g和dmf1.5ml,控温15~35℃搅拌24小时,得到式ⅲ;
(4)向式ⅲ中加入0.095mol的2,3-二氯5-三氟甲基吡啶20.4g,升温至回流搅拌8小时;降温至5~10℃,抽滤,用水洗涤,得吡虫隆,收率91.6%、纯度99.5%。
实施例2:
(1)反应釜中投入甲苯60ml,0.1mol的2,6-二氟苯甲酰胺15.7g,25℃左右开始滴加0.15mol草酰氯23.6g,滴加完后,调整温度至40-50℃保温反应1小时,保温结束,缓慢升温至微回流,于100-115℃保温反应5-6小时;减压蒸馏甲苯和过量的草酰氯,降温至10~30℃,制得备用液式ⅰ;
(2)向干燥洁净反应釜中投入0.097mol的2-氯-5-氨基苯酚14.0g,0.088mol的碳酸钾12.1g、甲苯60ml,室温搅拌30min,得到式ⅱ;
(3)向式ⅱ中滴加备用液式ⅰ,控制温度15~35℃;滴完后加入四丁基溴化铵0.1g和dmf1.5ml,控温15~35℃搅拌24小时,得到式ⅲ;
(4)向式ⅲ中加入0.097mol的2,3-二氯5-三氟甲基吡啶20.9g,升温至回流搅拌8小时;降温至5~10℃,抽滤,用水洗涤,得吡虫隆,收率91.1%、纯度99.7%。
实施例3:
(1)反应釜中投入甲苯60ml,0.1mol的2,6-二氟苯甲酰胺15.7g,25℃左右开始滴加0.18mol的草酰氯28.3g,滴加完后,调整温度至40-50℃保温反应1小时,保温结束,缓慢升温至微回流,于100-115℃保温反应5-6小时;降温至10~30℃,制得备用液式ⅰ;
(2)向干燥洁净反应釜中投入0.099mol的2-氯-5-氨基苯酚14.3g,0.10mol的碳酸钾13.8g、甲苯60ml,室温搅拌30min,得到式ⅱ;
(3)向式ⅱ中滴加备用液式ⅰ,控制温度15~35℃;滴完后加入四丁基溴化铵0.1g和dmf1.5ml,控温15~35℃搅拌24小时,得到式ⅲ;
(4)向式ⅲ中加入0.099mol的2,3-二氯5-三氟甲基吡啶21.3g,升温至回流搅拌8小时;降温至5~10℃,抽滤,用水洗涤,得吡虫隆,收率91.3%、纯度99.6%。
产物检测:将发明实施例制备的产物分别进行氢谱分析,碳谱分析和质谱分析,图谱分析结构如下:
根据图1氢谱分析,1hnmr(d6-dmso,d):11.52(s,br,1h,),10.37(s,br,1h,),8.54-8.52(m,2h,),7.81(m,1h,),7.66-7.53(m,3h,),7.25-7.19(m,2h),因此,本发明实施例所得产物中氢原子归属与吡虫隆相同。
根据图2碳谱分析,13cnmr(d6-dmso,d):162.55(14位碳原子),160.85-160.75(5位碳原子),160.27(16位碳原子),157.53-157.44(7位碳原子),150.45(13位碳原子),148.81(6位碳原子),143.51-143.39(3位碳原子),138.20(11位碳原子),137.74-137.70(18位碳原子),133.68-133.42(9位碳原子),130.76(8位碳原子),125.10(2位碳原子),123.07-121.75(1位碳原子),120.92(10位碳原子),119.37(15位碳原子),118.48(12位碳原子),116.05(4位碳原子),112.61-112.29(17位碳原子);因此,本发明实施例所得产物中碳原子归属与吡虫隆相同。
根据图3质谱分析,hrms:506(m),与吡虫隆的相对分子质量一致。
- 还没有人留言评论。精彩留言会获得点赞!