一种CTCF-ETO2血液病的融合基因及其检测引物和应用的制作方法
本发明具体涉及一种ctcf-eto2血液病的融合基因及其检测引物和应用。
背景技术:
eto2基因位于染色体16q24.3上,编码一个由nhr1、nhr2、nhr3和mynd结构域组成的髓系易位基因。作为一种核辅阻遏物,eto2与dna结合转录因子相互作用,并招募一系列共同抑制因子来抑制下游基因的表达,因此在造血祖细胞的细胞周期、自我更新能力和分化过程中起着至关重要的作用。eto2间接促进了白血病干细胞的转化,并引导了一个复发基因程序,导致aml的发生。据我们所知,迄今为止,在血液系统恶性肿瘤中已报道了5个eto2融合基因,包括inv(16)(p13.3q24.3)/eto2-glis2、t(1;16)(p31;q24)/nfia-eto2和t(16;21)(q22;q24)/runx1-eto2、t(9;16)(p13;q24)/pax5-eto2和淋巴瘤中的t(14;16)(q32;q24)/igh-eto2。
另外,schuback等人发现,在193例细胞遗传学正常的aml患者中,eto2-glis2融合阳性者的复发率、5年总生存率和无事件生存率明显低于阴性融合。micci等人描述了三名伴有nfia-eto2融合的aml患者的临床结果较差。相比之下,runx1-eto2患者的四年无事件生存率往往高于其他aml患者(77%对51%,p=0.06)。似乎eto2及其伴侣的协同作用将决定患者的具体结局。因此,对eto2基因重排的精确诊断将有助于提高对该类疾病的临床和生物学特征的认识和理解。
目前高通量测序是唯一可以明确未知易位位点的检测手段,然而高通量测序费用高昂,检测周期长,检测平台稀缺,对样品质量要求高,不利于普及推广,对于大多数患者来说也不是首选检测手段。依赖以往经验,针对已知的融合位点设计特异性的pcr引物组合,对肿瘤组织中提取出的rna逆转录之后进行pcr扩增并测序,检测融合基因具体易位位点,是最准确、便捷、经济的方法。因此,发现新的致病融合位点,进而设计pcr引物将有利于血液病检测准确度的进一步提高。
技术实现要素:
本发明所要解决的技术问题是提供一种ctcf-eto2血液病的融合基因及其检测引物和应用。
为解决以上技术问题,本发明采用如下技术方案:
本发明一方面提供一种ctcf-eto2血液病的融合基因,所述的融合基因由ctcf外显子5和eto2外显子2融合形成。
优选地,所述的融合基因包括seqidno.3所示的核苷酸序列,或与其具有80%以上同源性的核苷酸序列。
进一步优选地,所述的融合基因包括与seqidno.3所示的核苷酸序列具有85%以上同源性的核苷酸序列,更进一步优选具有90%以上同源性,再进一步优选具有95%以上同源性,最优选具有98%以上同源性。
优选地,所述的ctcf的基因序列在genebank中的登录号为nm_006565.4。
优选地,所述的eto2的基因序列在genebank中的登录号为nm_005187.6。
在本发明中,我们发现了第一例以急性髓细胞白血病为表现的新的ctcf-eto2血液病,该融合基因通过高通量测序技术在此病例中首次检测发现。
本发明第二方面提供一种上述ctcf-eto2血液病的融合基因作为检测靶点在制备ctcf-eto2血液病的诊断试剂中的应用。
本发明的第三方面提供一种检测上述ctcf-eto2血液病的融合基因的pcr引物,所述的引物长度在15bp-30bp之间,所述的引物gc含量在40%~60%之间,所述的引物的退火温度为70~75℃。
本发明中,所有能够检测本发明的融合基因的引物对均在本发明的保护范围内。
优选地,上游引物核苷酸序列如seqidno.1所示,或与其具有80%以上同源性,进一步优选具有85%以上同源性,更进一步优选具有90%以上同源性,再进一步优选具有95%以上同源性,最优选具有98%以上同源性。
优选地,下游引物核苷酸序列如seqidno.2所示,或与其具有80%以上同源性,进一步优选具有85%以上同源性,更进一步优选具有90%以上同源性,再进一步优选具有95%以上同源性,最优选具有98%以上同源性。
本发明中,针对本发明找到的新的融合基因,发明人在ctcf的5号外显子和eto2的2号外显子内分别设计引物,遵循引物设计原则,引物最好在模板cdna的保守区内设计,引物长度在15bp-30bp之间,引物gc含量在40%~60%之间,退火温度最好接近72℃,引物自身及引物之间不应存在互补序列,扩增条带单一特异。
经过发明人多次调试和验证,最终得到优选的上游引物如seqidno.1所示(ctcf-exon5-f:cgattacgccagtgtagaagt),下游引物如seqidno.2所示(eto2-exon2-r:tgatggctgttggtgagtg),根据发明人的实验结果,该引物组合诊断的特异性和敏感性均达到了100%,时间仅为三个工作日。采用本发明提供的探针组合进行检测ctcf-eto2易位性肿瘤,不但方便、快速、可靠而且检出率高,可用于制备ctcf-eto2易位性肿瘤诊断试剂盒,为ctcf-eto2易位性肿瘤的快速准确的诊断提供了新的工具。
本发明的第四方面是提供一种上述pcr引物在制备ctcf-eto2血液病的诊断试剂中的应用。
本发明的第五方面是提供一种ctcf-eto2血液病的诊断试剂盒,所述的诊断试剂盒包括上述pcr引物。
本发明中,我们首次发现以急性髓细胞白血病为表现的新的ctcf-eto2血液病,并且在目前的ctcf-eto2和eto2-ctcf阳性的aml病例中,存在多次复发和髓外浸润,尤其是移植后的复发给患者带来致命危险。更好地了解新型ctcf-eto2融合的分子和临床特点将有助于今后的治疗,并为肿瘤靶向治疗提供了新的视点。
由于上述技术方案的实施,本发明与现有技术相比具有如下优点:
本发明发现了ctcf-eto2血液病的新融合基因,并针对该融合基因设计了特异性的pcr引物,扩大了原有检测手段的检测范围,能够应用于临床,可提高诊断ctcf-eto2易位性血液病的检出率和准确率,为诊断分型及分子靶向治疗提供依据。
附图说明
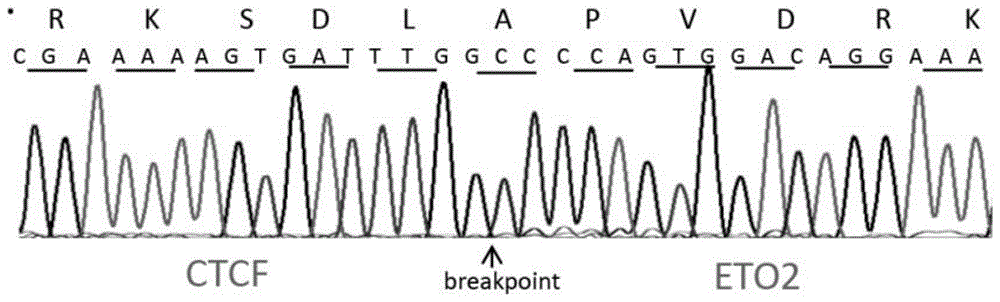
图1为在已知ctcf-eto2融合型肿瘤中应用本发明引物组合进行验证,成功检出的ctcf-eto2融合基因测序图。
具体实施方式
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例,进一步阐述本发明。
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可从商业途径获得。
实施例1针对明确诊断的病例进行验证:
本发明团队通过高通量测序技术,在一例aml病例中检测出ctcf-eto2融合基因,发现该基因由ctcf外显子5和eto2外显子2融合形成,其核苷酸序列如seqidno.3所示。对于这例高通量测序rna-seq检测出ctcfexon5-eto2exon2新融合基因的病例,使用我们设计的引物进行验证。
一、rna的提取:
严格按照rneasyffpekit操作说明进行提取。①裂红:将骨髓加入等体积的红细胞裂解液,室温裂解2min,加入含2%fbs的pbs终止反应,2000rpm离心5min;②清洗:将离心上清弃掉,加入2ml含2%fbs的pbs清洗细胞,2000rpm离心5min,弃掉上清;③加入16μldna酶缓冲液,再加入10μldnasei,混匀,室温静置15min,12000rpm离心15min,取上清;④加入320μl结合液液再加入720μl无水乙醇,混匀,分2次转移至吸附柱中,8000rpm离心1min,弃废液;⑤洗涤:加入500μl洗涤液,8000rpm离心1min;重复洗涤一次,弃废液,将吸附柱转移到一个新的2ml收集管中,12000rpm离心5min;⑥洗脱:将吸附柱转移到1.5ml的ep管中,加入100μl的洗脱液,室温静置1min,12000rpm离心1min,将收集好的洗脱液(即dna提取液)进行浓度和纯度测定,-80℃保存存待用。
二、逆转录pcrrt-pcr
采用试剂盒(k1622,revertaidfirststrandcdnasynthesiskit,mbi)对rna进行逆转录,方法详见试剂盒说明。pcr扩增引物为本专利ctcf-eto2融合基因引物组合,即上游引物如seqidno.1所示(ctcf-exon3-f:cgattacgccagtgtagaagt),下游引物如seqidno.2所示(eto2-exon4-r:tgatggctgttggtgagtg)。反应体系包括:0.125μltakaraextaqtmhs液,2.5μl10×taqbuffer(mg2+plus),2μldntp(均购自日本takara公司),引物浓度为20μmol/l,cdna模版为100ng,无菌去离子水加至25μl。pcr扩增条件为94℃变性3min后,94℃30s、60℃30s、72℃1min,共35次循环,最后72℃延伸5min。pcr产物用3%琼脂糖,电压100v,电泳,溴化乙啶染色后于紫外光下观察结果,并送测序。
结果:使用本发明引物pcr后可见单一特异的电泳条带,对扩增产物进行测序,得到ctcfexon5-eto2exon2融合基因序列(图1),扩增产物的全部序列如下:
cgattacgccagtgtagaagtcagcaaattaaaacgtcacattcgctctcatactggagagcgtccgtttcagtgcagtttgtgcagttatgccagcagggacacatacaagctgaaaaggcacatgagaacccattcaggggaaaagccttatgaatgttatatttgtcatgctcggtttacccaaagtggtaccatgaagatgcacattttacagaagcacacagaaaatgtggccaaatttcactgtccccactgtgacacagtcatagcccgaaaaagtgatttggccccagtggacaggaaagctaaggcctcagcgatgccggactccccagcggaggtgaagacgcagccccggtccacaccccccagcatgccgcccccaccgcctgccgcatcccagggggccacacgccccccctccttcacgccacacacacatcgagaggacgggcctgcgacgctgccccacggccgttttcatggctgcttaaaatggtctatggtctgtctcttgatgaacggcagcagccactcaccaacagccatca(seqidno.3),证明本项目设计的引物组合可靠且敏感,该引物可成功扩增出目的条带,条带单一、特异。
实施例2针对对照组病例进行检测
我们对30例诊断明确的对照组病例使用本发明实施例1的引物组合进行检测,rna提取、逆转录pcr和测序方法同上。
结果:使用本发明设计引物组合检测,未检测出ctcf-eto2融合基因,证明本项目设计的引物特异性高。
评价:本发明引物组合是对原有ctcf-eto2血液病融合基因引物的补充,扩展了ctcf-eto2血液病融合基因的类型,增加了rt-pcr方法诊断该肿瘤的检出率。
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
序列表
<110>苏州大学
<120>一种ctcf-eto2血液病的融合基因及其检测引物和应用
<160>3
<170>siposequencelisting1.0
<210>1
<211>21
<212>dna
<213>人工序列(rengongxulie)
<400>1
cgattacgccagtgtagaagt21
<210>2
<211>19
<212>dna
<213>人工序列(rengongxulie)
<400>2
tgatggctgttggtgagtg19
<210>3
<211>554
<212>dna
<213>人工序列(rengongxulie)
<400>3
cgattacgccagtgtagaagtcagcaaattaaaacgtcacattcgctctcatactggaga60
gcgtccgtttcagtgcagtttgtgcagttatgccagcagggacacatacaagctgaaaag120
gcacatgagaacccattcaggggaaaagccttatgaatgttatatttgtcatgctcggtt180
tacccaaagtggtaccatgaagatgcacattttacagaagcacacagaaaatgtggccaa240
atttcactgtccccactgtgacacagtcatagcccgaaaaagtgatttggccccagtgga300
caggaaagctaaggcctcagcgatgccggactccccagcggaggtgaagacgcagccccg360
gtccacaccccccagcatgccgcccccaccgcctgccgcatcccagggggccacacgccc420
cccctccttcacgccacacacacatcgagaggacgggcctgcgacgctgccccacggccg480
ttttcatggctgcttaaaatggtctatggtctgtctcttgatgaacggcagcagccactc540
accaacagccatca554
- 还没有人留言评论。精彩留言会获得点赞!