纳米结构化载体上改性胺的再生性吸附剂的制作方法
本发明涉及用于从气体混合物(包括空气)捕集和分离二氧化碳的再生性纳米结构负载型(如热解二氧化硅(fumed silica)、沉淀二氧化硅、热解氧化铝(fumed alumina)等固体)改性多胺吸收剂。
发明背景
气候变化与全球变暖被认为是当今最迫切且最严重的环境问题之一。现在通常公认,全球变暖的主要原因是所谓的温室气体被释放到大气中。一种主要的温室气体是二氧化碳(CO2),其主要由化石燃料如煤、石油和天然气的燃烧释放。这些化石燃料总计供应了世界约80%的能源需求。由于化石燃料仍然相对廉价且容易使用,并且由于尚未有可用于在所需的庞大规模上替代它们的令人满意的替代物,预期化石燃料在可预见的未来仍然是我们的主要能源来源。
一种减少CO2排放以及它们对于全球气候的影响的方式是高效且经济地从其源头(如来自燃烧化石燃料的发电厂和其他工业工厂的排放、伴随天然气的天然存在的CO2和空气)捕集CO2、以及隔离或将CO2转化成可再生燃料。
在各式各样的CO2收集或分离技术中,基于胺溶液的CO2吸收/解吸系统是最适合于从高体积气体流捕集CO2的技术之一。这种系统中常用的溶剂是烷醇胺如单乙醇胺(MEA)、二乙醇胺(DEA)、二异丙醇胺(DIPA)和甲基二乙醇胺(MEDA)的水性溶液。某些空间位阻胺,如2-氨基-2-甲基-1-丙醇(AMP),也可因其高CO2负载能力而用作吸收剂。在这些中,MEA因其高CO2吸收速率(这允许使用较短的吸收柱)而最广泛地使用。然而,MEA系统呈现主要的缺点,包括使溶剂再生需要的大量热以及由腐蚀和化学降解所造成的操作问题。为了防止过度的腐蚀,水性胺溶液中通常仅使用10至30重量%的MEA,其余为水。因为整个溶液(其中70至90%是水)需要加热来使MEA系统再生,再生过程中浪费了大量的能量。其他烷醇胺系统也呈现出不利之处。例如,受阻的仲胺(例如,DEA、DIPA、AMP)提供了比MEA更低的CO2吸收速率,并且也易于发生腐蚀和化学降解。已知MDEA仅以慢速率吸收CO2。通过共混几种烷醇胺而形成的制剂是令人感兴趣的,因为它们可以结合各种化合物的有利特性,同时部分地抑制它们的不利特性。已经开发了多种共混烷醇胺溶液,最常见的共混物是含有MEA或DEA的基于MDEA的溶液。然而,共混烷醇胺溶液并未消除基于胺溶液的系统的缺点。
CO2也可以通过吸附到固体吸附剂(sorbent)上而被捕集。固体通常用作分离CO2的物理吸附剂。这种过程是基于多孔固体可逆吸附混合物中的某些组分的能力。固体可以具有大的孔径分布,如在硅胶、氧化铝和活性碳中,或者具有通过晶体结构控制的孔径,如沸石。在低温如室温下,基于沸石的吸附剂具有高CO2吸收能力(例如,25℃下在纯CO2中,对于沸石13X为160mg CO2/g;和对于沸石4A为135mg CO2/g)。然而,这些吸附剂的吸附能力随着温度上升和在水或水汽的存在下快速下降。而且,由于气体仅仅物理吸附在吸附剂上,单种气体从气体混合物的实际分离是低的。
为了实现CO2吸附的更高选择性,可以将提供化学吸收的化合物施加到固体吸附剂上。为此目的,可以将胺或多胺沉积或接枝到固体载体上。然而,化学键合(接枝)到固体(如二氧化硅和氧化铝-二氧化硅)表面上的胺和多胺显示出低于80mg CO2/g,以及在大部分情况下低于50-60mg CO2/g吸收剂的有限吸收能力。例如,美国专利第5,087,597号(Leal等人)公开了一种使用表面积为120至240m2/g的硅胶在室温下化学吸附CO2的方法,所述硅胶用其结构中含有一个或多个氨基部分的聚烷氧基硅烷改性。该材料公开为能够吸收15至23mg干燥CO2/克吸收剂。美国专利第6,547,854号(Gray等人)公开了一种通过将胺引入到氧化固体的表面上来制备胺富集的吸附剂的方法。使用在He中的10%CO2的气体混合物,所报告的这些固体上吸收的CO2最大量为7.7mg/g吸收剂。如数据所证实的,因为其低胺覆盖率,可以吸附在各种固体载体上的接枝氨基上的CO2的量仍然相对较低。
另一个途径涉及用胺或多胺浸渍固体载体。例如,S.Satyapal等人的论文(J.Energy and Fuels 15:250(2001))描述了高表面积聚甲基丙烯酸甲酯聚合物载体上的聚乙烯亚胺(PEI)/聚乙二醇(PEG)的开发。该固体是开发用于航天飞机中以从船舱大气中除去CO2并将其释放到太空中。在50℃和0.02atm CO2下,其能力为约40mg CO2/g吸收剂。该材料及其改进公开于美国专利第6,364,938、5,876,488、5,492,683和5,376,614号(Birbara等人)中。这些专利中描述的优选载体具有聚合物性质,其中丙烯酸酯树脂如被描述为具有特别适合的特性。美国专利第5,376,614、5,492,683和5,876,488号也公开了其他可能的载体,包括氧化铝、沸石和碳分子筛。然而,根据美国专利第5,492,683和5,376,614号,吸附剂上存在的胺的量受到限制,范围在1重量%至25重量%。
美国专利第4,810,266号(Zinnen等人)公开了一种通过用胺醇处理碳分子筛来产生CO2吸附剂的方法。该专利公开了基于单乙醇胺(MEA)的材料不是稳定的,且在较高温度下的再生步骤过程中释放MEA。国际公布第WO2004/054708号公开了基于介孔二氧化硅载体的吸收剂。用于CO2吸收的活性组分是化学连接到或者物理吸附到介孔二氧化硅表面上的胺或其混合物。该公布中描述的大多数吸收剂上的吸收低于70mg CO2/g。通过使用物理吸附到载体上的二乙醇胺(DEA)获得了最好的结果(约130mg CO2/g)。然而,由于DEA在解吸条件下的挥发性,该吸收剂的效力通常随CO2吸收-解吸循环的数量增加而降低(在仅60℃的中等再生温度下,在5个循环后约16.8%)。美国专利第6,908,497号(Sirwardane等人)公开了一种通过用胺和/或醚处理具有0.72至26mg2/g的低表面积的粘土基底来制备吸附剂的方法。
醇类、聚乙二醇和其他含氧化合物也已经在数十年间用来除去酸性气体,主要是CO2和H2S。例如,来自Union Carbide(现Dow Chemicals)的和来自BASF的SEPASOLV 被用在商业方法中。作为混合物理或化学吸附剂的与胺组合的含氧化合物,在如二醇-胺方法的方法中,也已经在许多年间用来除去酸性气体(参见Kohl,A.L.和Nielsen,R.B.,GAS(Gulf Publishing Co.))。美国专利第4,044,100号(McElroy)展示了使用二异丙醇胺与聚乙二醇的二烷基醚的混合物来除去气体,包括来自气体流的CO2。J.Yeh等人(Energy and Fuels 15,pp.274-78(2001))也已经研究了使用乙二醇来改善从胺吸收和解吸CO2。虽然文献主要涉及使用液相中的胺和含氧化合物,但也已经探索了使用含氧化合物来改善固相中的气体吸附剂的特性。S.Satyapal等人(Energy and Fuels 15:250(2001))提到使用与聚合物载体上的聚乙烯亚胺结合的聚乙二醇来从太空飞船的封闭大气中除去CO2。X.Xu等人(Microporous and Mesoporous Materials62:29(2003))表明引入到介孔MCM-41/聚乙烯亚胺吸附剂中的聚乙二醇改善了测试材料的CO2吸收和解吸特性。还公开了由沉积在介孔MCM-41上的PEI组成的固体吸收剂的制备和性能(参见X.Xu等人,Energy and Fuels 16:1463(2002))。美国专利第5,376,614和5,492,683号(Birbara等人)使用多元醇来改善吸收剂的吸收和解吸性质。
另一种用于捕集二氧化碳的新材料是金属有机骨架化合物。称为MOF-177的优选化合物(J.Am.Chem.Soc.,2005,127,17998)在30巴的较高压力下具有140重量%的室温二氧化碳容量。
又一种用于此目的的吸附剂是负载型胺吸附剂,其包含沉积在纳米结构化载体上的胺或胺/多元醇组合物,该纳米结构化载体提供了结构完整性和提高的CO2吸收能力。该材料在美国专利第7,795,175号中公开。用于胺和胺/多元醇组合物的载体由纳米结构化固体组成。纳米结构化载体可以具有小于约100nm的初级粒径,并且可以是纳米二氧化硅、热解或沉淀氧化物、硅酸钙、碳纳米管或其混合物。胺可以是伯、仲或叔胺或者烷醇胺,芳族胺,混合胺,或其组合。在一个实例中,胺按吸附剂的重量计以约25%至75%的量存在。多元醇可以选自,例如甘油、乙二醇的低聚物、聚乙二醇、聚环氧乙烷及其醚、改性物和混合物,并且可以按吸附剂的重量计以至多约25%的量提供。
虽然有这些在先的公开内容,但仍然需要用于捕集CO2的改进的吸附剂,其是有效的、经济的、容易获得的以及再生性的,并且其在环境温度以及升高的温度下提供高去除能力。本发明现提供了这样的材料。
技术实现要素:
本发明提供了用于从气体混合物吸收二氧化碳的新型固体吸附剂,其包括改性多胺和纳米结构化固体载体。如本文所公开的,改性多胺是胺与醛的反应产物。
纳米结构化载体有利地具有小于约100nm和优选3至50、3至30或3至15nm的初级粒径。载体通常是二氧化硅、二氧化硅-氧化铝、硅酸钙、碳纳米管或其混合物。
改性多胺通过以下步骤作为粘性液体获得:将胺溶解于水中以形成胺溶液;伴随搅动或搅拌在加热或不加热的条件下将醛加入到胺溶液中以形成混合物,经一段时间以形成胺与醛的液体反应产物;和然后加热混合物以除去水,必要时在真空条件下进行。胺是伯、仲或叔烷基或烷醇胺,芳族胺,混合胺,多胺,多胺混合物,或其组合和/或改性物,而醛是单醛、二醛、三醛、聚合醛化合物或其混合物。优选的多胺是四亚乙基五胺、五亚乙基六胺、三亚乙基四胺、二亚乙基三胺、乙二胺、六亚乙基七胺、聚乙烯亚胺或其组合,而优选的醛是甲醛、甘醛(乙二醛)、戊二醛(戊烷-1,5-二醛)、琥珀醛(丁二醛)、邻苯二甲醛、间苯二甲醛、对苯二甲醛或其混合物。在吸附剂中,改性多胺以约25%至75%或40%至60%的量或者以按载体的重量计大致相等的量存在。
在另一个实施方式中,吸附剂还包含按吸附剂的重量计1%至至多约25%的量的多元醇。通常,多元醇选自甘油、乙二醇的低聚物、聚乙二醇、聚环氧乙烷及其醚、改性物和混合物。特别地,当纳米结构化载体是纳米二氧化硅时,改性胺按吸附剂的重量计可以以约25%至75%的量存在,和吸附剂还包含按吸附剂的重量计1%至至多25%的量的聚乙二醇。
本发明还涉及一种用于制备这些吸附剂的方法,通过伴随混合和加热使胺、醛和载体在溶剂中结合足够的时间以允许胺和醛结合且被提供到载体上,之后除去水以获得作为固体的吸附剂。
在该方法的一个实施方式中,其中纳米结构化载体分散在溶剂中以形成混悬液;胺溶解于溶剂中以形成胺溶液;醛溶解于溶剂中以形成醛溶液;和混悬液与胺和醛溶液结合。这可以通过以下步骤进行:使所述胺溶解于水中以形成胺溶液,将所述醛的水性溶液加入到所述胺溶液以形成混合物;在15至100℃温度下混合所述混合物5分钟至50小时;然后将所述混合物加热至至少100℃持续30秒至60分钟以除去部分或全部的水,任何剩余的水通过在真空下加热除去,以获得作为粘性液体的所述改性多胺。
随后,所述吸附剂通过以下步骤形成:伴随搅拌将所述粘性液体加入到载体的分散体以将所述改性多胺分散到所述载体上。
在另一个实施方式中,该方法还包括在除去水以获得所述吸附剂之前加入多元醇。特别地,该方法还包括将多元醇加入到所述混悬液;在加入所述多元醇后干燥所述混悬液以形成负载的多元醇;使所述负载的多元醇分散到所述溶剂中;和在除去所述溶剂以形成所述吸附剂之前使所述分散的负载的多元醇与所述胺溶液结合。
本发明还涉及一种通过使二氧化碳吸收于吸附剂上从气体源捕集和分离二氧化碳的方法。该吸附剂是再生性的,因为其可以通过施加热、减压、真空、气体吹扫、贫扫气(lean sweep gas)或其组合解吸和再生。对此,本发明还涉及使用改性多胺提供用于从气体混合物吸收二氧化碳的固体吸附剂,其特征在于改性多胺是胺与醛的反应产物,并且被提供到纳米结构化固体载体上。
释放的二氧化碳可用于方法中以生产可再生燃料如甲醇。在一个实施方式中,这种方法包括还原二氧化碳和水,或者在足以产生甲酸甲酯作为中间化合物的条件下还原二氧化碳,之后用氢催化氢化中间化合物以形成甲醇。
在另一个实施方式中,甲醇通过催化氢化中间化合物产生,其中用于氢化的氢是通过电解从空气获得的水来获得。在另一个实施方式中,甲醇通过以下步骤获产生在足以产生一氧化碳的条件下还原所述二氧化碳,在足以获得甲酸甲酯的条件下使所述一氧化碳与甲醇反应,和在足以产生甲醇的条件下催化氢化所述甲酸甲酯。
根据本发明产生的甲醇可以进一步加工成任何期望的衍生物或改性化合物。例如,甲醇可以脱水产生二甲基醚,其还可以在足以形成如乙烯和丙烯的化合物的条件下进一步处理。乙烯和丙烯可以转化成更高级的烯烃、合成烃、芳族化合物或相关产物,并因此可用作化学品的原料或者用作运输燃料。在进一步的实施方式中,甲醇可以进一步用于单细胞蛋白质的微生物生产。
附图说明
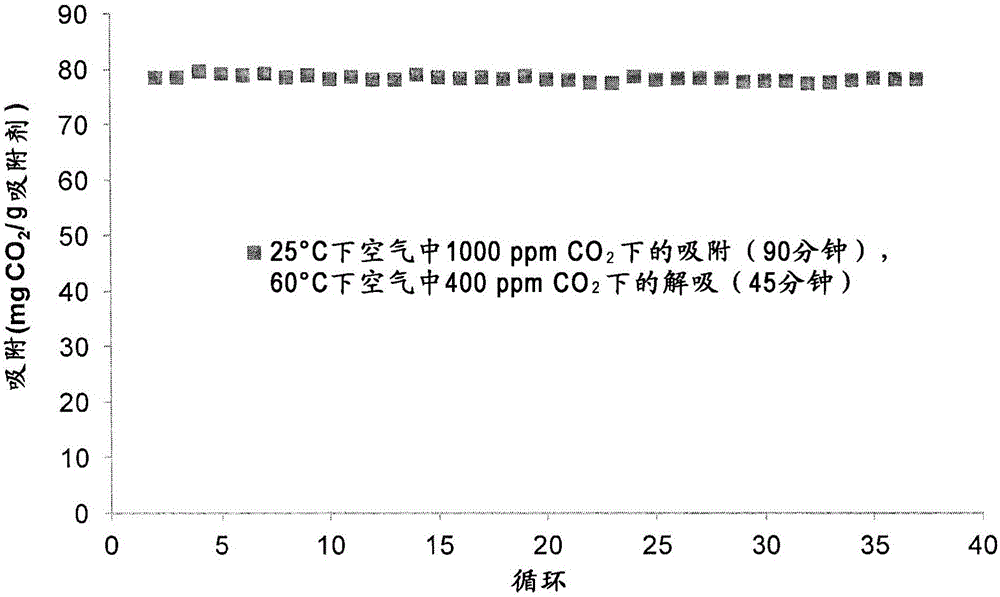
图1是CO2在基于由沉淀二氧化硅负载的被称为PEHA-HCHO-1-1的五亚乙基六胺甲醛(参见实施例1)(53/47重量%)的吸附剂上的吸附和解吸的图,吸附/解吸由热重分析仪测量。
图2是潮湿条件下CO2在基于沉淀二氧化硅上负载的被称为PEHA-HCHO-1-1的五亚乙基六胺/甲醛(参见实施例1)(53/47重量%)的吸附剂上的吸附和解吸的图,吸附/解吸在流动系统中测量。
具体实施方式
本发明涉及用于吸收CO2的再生性负载型改性多胺吸附剂。该吸附剂包括用于吸收和解吸CO2的在纳米结构化载体(例如纳米二氧化硅载体)上的改性胺。CO2可以从任何期望的来源吸收,包括工业废气、燃烧化石燃料的发电厂的烟道气以及天然来源。根据本发明的纳米结构化载体对于多胺提供了结构完整性以及为固体-气体接触提供了高表面积。
根据本发明的具有纳米级载体的改性多胺吸附剂相对于现有技术的吸收剂(例如具有聚合物载体的吸收剂)提供了显著的优势,包括在环境温度和升高的温度下的高CO2选择性和去除能力。因此,本吸附剂允许在各种各样的条件和温度下从各式各样的气体混合物选择性地捕集和分离CO2。
本吸附剂还容易在环境温度至中等温度下再生和再循环,使得在没有或具有最小活性损失的情况下进行多个吸收-解吸循环成为可能。该吸附剂还解决了现有技术吸附剂的腐蚀与挥发问题。
因此,对于从工业排气(如来自燃烧化石燃料的发电厂和其他工业工厂的那些)以及其他气体流(特别是含有较高CO2浓度的天然气)分离CO2,本吸附剂系统是实用的。重要的是,该吸附剂还可以用于从大气空气分离CO2。
根据本发明的吸附剂表明通过以下机理吸收CO2。在接触含有CO2的气体流时,负载的改性多胺通过形成氨基甲酸酯复合物而化学吸收CO2。
在水的存在下,氨基甲酸酯进一步反应形成碳酸氢盐并释放胺,其可以进一步与CO2反应,由此增加总的CO2吸收能力。
根据本发明的一个实施方式,被吸收的CO2可以容易地解吸,并且负载的改性多胺可以再生。CO2的解吸和吸附剂的再生可以通过适度加热吸附剂、施加减压或真空、气体吹扫和/或贫二氧化碳吹扫气来实现,这从吸附剂释放CO2。方便的再生使得吸附剂能够容易地经历反复的吸收-解吸循环。
种类繁多的胺可以用于本发明。适合的胺包括伯、仲和叔烷基-和烷醇胺,芳族胺,混合胺,多胺,多胺混合物及其组合和改性物。伯和仲胺对于CO2吸收是最具活性的。因此,多胺应当优选含有充足量的伯和仲氨基组分。氨基组分的具体实例包括但不限于四亚乙基五胺、五亚乙基六胺、三亚乙基四胺、二亚乙基三胺、乙二胺、六亚乙基七胺、聚乙烯亚胺,等等,包括各种各样的聚合胺化合物及其混合物。
优选的多胺包括有时称为聚亚乙基胺的各种各样的较高级的亚乙基胺类。这种多胺的通式为:H2N(NH(CH2)n)pNH2,其中n为1至4和p为2至10000。多胺优选含有充足量的重复NH(CH2CH2)单元,使得它们具有低挥发性以避免或最小化胺流失,胺流失会污染气体流并随时间降低吸收系统的效力。特别优选的线性多胺包括四亚乙基五胺(TEPA)和五亚乙基六胺(PEHA)和六亚乙基七胺(HEHA)。
可用于本发明以使胺改性的醛包括单醛以及二醛、三醛和更高级的同系物。醛组分的实例包括但不限于甲醛、甘醛(乙二醛)、戊二醛(戊烷-1,5-二醛)、琥珀醛(丁二醛)、邻苯二甲醛、间苯二甲醛、对苯二甲醛,等等,包括各种各样的聚合醛化合物及其混合物。
根据本发明的载体是具有小于1,000nm,优选小于约100nm的初级粒径的载体。优选的载体是纳米二氧化硅,特别是所谓的热解二氧化硅和沉淀二氧化硅。热解二氧化硅通常具有5至50nm范围的初级粒径和50至500m2/g的比表面积。热解二氧化硅通常通过含硅卤代物如四氯化硅(SiCl4)的气相水解来制备。可商购热解二氧化硅的实例包括来自Evonik的来自Cabot的和来自Tokuyama的沉淀二氧化硅通过使碱性硅酸盐(例如硅酸钠)与无机酸(如硫酸)在搅拌下反应而从水性溶液形成。通过该方法形成的初级颗粒通常大小为3至50nm,更特别是3至30nm和优选3至15nm。这些初级颗粒可以随后团聚以形成较大的微米级颗粒。沉淀二氧化硅的比表面积通常范围是50至500m2/g。可商购沉淀二氧化硅的实例包括来自PPG Industries的来自Evonik的以及来自Tokuyama的和
热解二氧化硅和沉淀二氧化硅具有轻质的、蓬松的、白色粉末的外观。它们的小粒径允许他们吸收和保留大量的胺,同时维持自由流散的粉末特征而不结块。热解和沉淀二氧化硅的另一个优势是它们的非毒性。非毒性允许他们用于食品加工中,例如在粉末状食品产品如代乳品中作为抗结块添加剂,以及用于化妆美容产品中,例如用于牙膏中的磨料材料。热解和沉淀二氧化硅通常是亲水性的,但它们的表面可以进行处理以产生疏水性二氧化硅。亲水性和疏水性二氧化硅二者以及其他改性二氧化硅都适合用作根据本发明的纳米结构化多胺载体。
其他适用于本多胺吸附剂的纳米结构化材料包括热解或沉淀氧化物,如热解法氧化铝、热解法氧化锆和热解法氧化钛、沉淀法氧化铝、沉淀法氧化钛、沉淀法氧化锆,硅酸钙,碳纳米管,及其混合物。
负载型多胺吸附剂可以通过浸渍或通过另外的常规技术制备。
为了增强负载型胺吸附剂的CO2吸收和解吸特性,多元醇可以以吸附剂总重量的至多25%的量引入到吸附剂组合物中。多元醇的加入改善了吸附剂的吸收和解吸并且降低了胺的粘度,允许CO2甚至在较低的温度下(<50℃)更好地接近吸附剂的活性氨基位点。本发明中使用的多元醇应当对于胺是非反应性的,并且应当具有低挥发性以避免或最小化胺流失,该流失会污染气体流并随时间降低吸收系统的效力。本吸附剂中使用的多元醇的实例包括但不限于甘油、乙二醇的低聚物、聚乙二醇、聚环氧乙烷、乙二醇低聚物的醚、聚乙二醇的醚、聚环氧乙烷的醚、环醚的低聚物或聚合物如聚四氢呋喃,及其改性物和混合物。优选的多元醇具有低于10,000的分子量。更优选的,多元醇具有低于1,000的分子量。
根据本发明的用于制备多胺负载型吸附剂的方法廉价且容易实行,但却生产出比通过此前已知的方法制备的吸附剂更优良的吸附剂。
例如,改性多胺可以通过以下步骤制备:首先将胺溶解于水中以形成胺溶液。接着,将醛的水性溶液加入到胺溶液中以形成混合物。混合物先在室温(即,15至100℃)下搅拌1分钟至50小时和优选1至30小时,然后加热到至少100℃持续30秒至300分钟,优选10至60分钟,以除去部分或全部水。可以通过真空加热除去任何剩余的水。所获得的改性胺是粘性液体。
为了形成吸附剂,粘性液体可以溶解于水中并伴随搅拌加入到水中悬浮的载体(例如,二氧化硅)中以将改性多胺分散到载体上。粘性液体的量将是粘性液体与载体的总重量的25至75%或40至60%,优选使用大约等重量的粘性液体与载体。此后,可以如上所述除去水。负载型改性多胺吸附剂可以作为固体获得,其可以压碎和过筛以产生用于吸收二氧化碳的均匀粉末。
或者,改性胺与吸附剂可以通过以下步骤共同制备:将胺与二氧化硅如上所述混合到水中,之后加入醛溶液以制备混合物。维持搅拌或搅动混合物以形成吸附剂,然后除去水以获得作为粉末状固体的吸附剂。
如上所述,可以加入多元醇来增强负载型胺吸附剂的吸收/解吸特性。当使用多元醇时,多元醇可以与胺溶液一起混合并加入到载体的悬浮液。多元醇也可以单独溶解于溶剂中并与载体的悬浮液合并。在这种情况下,多元醇溶液优选首先加入到载体的悬浮液,然后除去溶剂以获得负载的多元醇材料。然后所获得的固体分散到溶剂中,并且在搅拌下加入溶剂中胺的溶液。最后,除去溶剂以形成负载型胺/多元醇吸附剂。吸附剂可原样使用或者可以压碎和过筛以获得均匀粉末。
任何能够溶解胺和多元醇但不与之反应的溶剂都可以使用。溶剂应当优选地容易通过适度加热和/或真空与吸附剂分离。优选的溶剂包括但不限于醇类,其可以溶解胺和多元醇并且可以容易地从吸附剂除去。例如,可以使用甲醇、乙醇和异丙醇,及其各种混合物。优选的溶剂是水。
有利地,本发明使得用于各种各样的天然和工业气体源的宽范围的CO2吸收能力成为可能。吸收可以在各种各样的条件下进行,例如0至100℃的温度范围,和以任何适合的方式进行,例如在正规的流动系统中或者在固定的、运动的或流化的吸收床中。吸附剂捕获CO2的能力可以通过经吸附剂筒(cartridge)在流动系统中由使用热重分析仪(TGA)的热重法测量吸收,或者通过在静态条件下测量CO2吸收来证实。
一旦大量胺与CO2复合,吸附剂可以再生。如本文所用,术语“再生”或“再生性”理解为表示吸附剂可以通过从吸附剂释放或解吸被吸收的气体而再使用。被吸收的气体通过用实现释放的任何方法例如加热、减压、真空、气体吹扫及其组合处理吸附剂来释放。因此,根据本发明的再生的吸附剂可以在多个吸收-解吸循环中重复使用。在一个实例中,吸附剂甚至在重复的吸收-解吸循环之后保持其吸收效率。优选地,吸附剂在许多个吸收-解吸循环期间维持其吸收效率。使用平行的吸收床是便利的,其允许连续地完成吸收和解吸/再生。
例如,对于CO2吸附剂,再生是吸热的,因此吸收的CO2通过使吸收剂经历升高的温度(例如,在约25℃至约85℃的温度下加热吸附剂)、减压(例如,通过变压吸收(PSA))、气体吹扫、真空、贫气扫除(lean gas sweep)或其任何组合而释放。再生处理允许基本上大部分与吸附剂的多胺复合的CO2被释放。然后CO2可以以任何期望的方式释放、储存或使用,而没有CO2的(再生的)吸附剂在进一步的CO2吸收-解吸循环中重复使用。
CO2的用途和反应包括特别是上文提到的和共同未决美国专利7,605,293、8,212,088和8,440,729中进一步公开的那些。这三篇专利的全部内容明确地通过引用并入本文。
根据本发明的吸附剂是热稳定的并且在吸收操作的温度和/或压力范围内不释放负载的多胺。进一步,因为其能够在可以在整个方法期间容易维持的温度范围内再生和有效操作,除了CO2捕集和分离的高选择性和能力以外,吸附剂对于提供高效力和长寿命是经济的。因其灵活性和多功能性,吸附剂也可以有利地用于处理来自各种各样的来源的大体积的含CO2气体。
通常观察到,伯胺比仲胺具有对于CO2的更高反应性并且比仲胺更牢固地结合CO2。虽然这在CO2吸附步骤期间可以是有利的,但这也意味着在再生(解吸)步骤期间需要更多的能量来释放被吸附的CO2,这可能造成更缓慢的解吸动力学。为了降低再生步骤期间的能量需求,使用仅含有或主要含有仲胺的多胺因此可以是有利的。
醛优先与伯胺反应来形成亚胺。在不含有α-氢的甲醛的存在下,与伯胺的反应导致引入-CH2-OH基团和形成仲胺。进一步与来自另一多胺分子的另一伯胺反应可以通过缩合反应和消除水而导致低聚化。
多胺中部分或全部伯胺的消除或者伯胺转化成仲胺导致形成改性多胺,该改性多胺具有在再生步骤期间需求较低能量输入的改进的CO2解吸特性。因此,解吸步骤可以例如在显著较低的温度下和/或在较短的时间段内进行,从而减少方法的总体成本和时间。本专利中描述的吸附剂提供了与本领域的现有状态相比的实质性改进。
实施例
以下实施例都仅仅是说明性的,不应解释为限制本发明的范围。
实施例1:制备可再生CO2吸附剂
根据本发明的吸收剂在两个步骤中便利地制备。
步骤1:制备改性多胺物质
如下制备基于五亚乙基六胺(PEHA)H(NHCH2CH2)5NH2和甲醛的改性多胺物质。将30g的PEHA溶解于水中。然后将10.45g的稀释于20mL水中的甲醛水性溶液(水中的37%甲醛)逐滴加入到PEHA溶液。室温下搅拌混合物20小时。之后,温度逐渐提高至100℃并在该温度下保持90分钟以除去部分水。剩余的水通过在旋转蒸发仪上真空加热,之后在真空(<1mm Hg)下过夜来除去。所获产物是粘性的黄色至橙色的液体。该改性多胺命名为PEHA-HCHO-1-1。
步骤2:制备负载型多胺吸附剂
负载型改性多胺吸附剂由50重量%的PEHA-HCHO-1-1和50重量%的热解二氧化硅组成,该热解二氧化硅具有7nm的平均初级粒径和390m2/g+/-40m2/g的比表面积。
将PEHA-HCHO-1-1溶解于100mL水中。然后将该溶液在搅拌下缓慢加入到在300mL水中悬浮的等量热解二氧化硅中,以确保改性多胺良好分散在载体上。混合物在室温下再搅拌20小时,然后通过在旋转蒸发仪上真空加热、之后真空(<1mm Hg)下过夜来从混合物除去水。所获负载型多胺吸附剂是白色固体,其可被压碎和过筛以产生均匀粉末。
实施例2:制备基于改性多胺和热解二氧化硅的吸附剂
本实施例说明了在“一锅法(one pot)”中制备由53重量%的PEHA-HCHO-1-1和47重量%的热解二氧化硅组成的负载型改性多胺吸附剂,该热解二氧化硅具有7nm的平均初级粒径和390m2/g+/-40m2/g的比表面积。将30.1g(0.1295mol)PEHA溶解于120mL水中。然后在搅拌下将该溶液加入到在300mL水中悬浮的30.1g热解二氧化硅中,以确保PEHA良好分散在载体上。搅拌维持1小时,之后将10.5g(0.1295mol)甲醛水性溶液(水中的37%甲醛)在室温下逐滴加入到PEHA/热解二氧化硅溶液(加入速率为0.3mL/min)。混合物再搅拌20小时。通过在旋转蒸发仪上真空加热,之后在真空(<1mm Hg)下过夜来除去水。所获得的产物是白色粉末状固体。
实施例3:使用置于流动系统的筒中的吸附剂测量CO2吸收能力。出于空气质量的目的,从含有1000ppm CO2和50%湿度的混合物的CO2吸附。
本实施例说明了出于室内空气质量的目的,从含有1000ppm CO2的气体混合物除去CO2。所用的吸附剂是PEHA-HCHO-1-1/沉淀二氧化硅(“一锅法”中制备的53/47重量%)。
使用全玻璃无油脂流动系统获得CO2吸附数据。将通常1g的吸附剂置于两个玻璃纤维塞之间的玻璃管中。然后该U型管在85℃下排空(~30mTorr)3小时。吸附剂的重量在该处理后测量。预处理后的吸附剂重量用于之后计算CO2吸附能力。在预处理后,将含有吸附剂的U型管置于25℃恒温油浴中。为了进行吸附测量,将配有专门用于CO2测量的IR检测器的Horiba VIA-510CO2分析仪在线置于吸附装置中。所用浓度范围为0-2000ppm。在各次运行之前,用参比气体校准分析仪;空气和代表零点的超零级空气(ultra zero grade air)中的CO2。含有1000ppm CO2和50%水分的空气混合物被用于吸附测量。空气流(~335mL/min)然后在吸附床上打开。气体出口的CO2浓度几乎立刻降至0ppm,标志着从空气完全吸附CO2。CO2浓度通过Lab View 8.6随时间记录。在0ppm CO2的初始期之后,出口气体中的浓度开始上升。在吸附剂饱和后,当CO2浓度达到入口值(1000ppm)时,停止气体流。总吸附能力测定为106mg CO2/g吸附剂(2.4mmol CO2/g吸附剂)。
吸附剂上CO2的解吸是通过将含吸附剂的U型管加热至60℃、且然后使含有400ppm CO2和50%湿度的空气流通过(335ml/min)它而进行。CO2浓度通过Lab View 8.6随时间记录。打开饱和吸附剂上的空气流之后,CO2浓度立即突增至3-5%CO2,然后缓慢降低至达到入口CO2浓度(400ppm CO2)。
在这些条件(在25℃、空气中1000ppm的CO2、50%湿度、335mL/min下的吸附和在60℃、空气中400ppm的CO2、50%湿度、335mL/min下的解吸)下重复4次吸附/解吸循环。吸附能力保持稳定在约95-105mg CO2/g吸附剂。
实施例4:通过热重分析测量CO2吸收能力。出于空气质量的目的,从含有1000ppm CO2的混合物吸附CO2
使用热重分析仪(Shimadzu TGA-50)获得CO2吸收数据。将吸收剂(5-20mg)装载到铂坩埚中并放置在仪器天平上。固体吸收剂然后在期望温度下(通常为在90至110℃下)在空气流中进行预处理1小时。随后,将样品冷却到期望的吸附温度,并将气体流切换到含有空气中1000ppm的CO2的气体混合物。随时间记录样品质量的变化以测定CO2吸附能力。解吸是通过将吸附剂在含有空气中400ppm的CO2的气体混合物中加热到较高温度(通常为50至80℃)而进行。随时间记录样品质量的变化以测定CO2解吸能力。重复若干次这些吸附/解吸循环以测定吸附剂的稳定性。
对于根据“一锅法”合成制备的吸附剂(PEHA-HCHO-1-1/沉淀二氧化硅,53/47重量%),用此方法获得的吸附/解吸测量的实例在图1中展示。吸附是在含有空气中1000ppm的CO2的气体混合物中于25℃下进行90分钟。解吸是在含有400ppm CO2的气体混合物中于60℃下进行45分钟。吸附能力在超过35个吸附/解吸循环中没有降低,保持为约79mg CO2/g吸附剂。
- 还没有人留言评论。精彩留言会获得点赞!