高岑土制CHA沸石的制作方法
高岑土制cha沸石
技术领域
[0001]
本发明涉及沸石分子筛技术领域,尤其涉及一种高岑土制cha沸石。
背景技术:
[0002]
cha结构类型沸石早先发现于天然矿物,俗称菱沸石。一种sio2/al2o3摩尔比(sar)为4的ca型菱沸石,因该天然物储量少、杂质多、sar太低和稳定性热不高,限制其应用,一般只适用于制吸附剂和阳离子交换剂。
[0003]
小孔口、大空腔的结构使低硅cha沸石分子筛吸附剂在气体吸附分离和净化方面具有很突出的应用前景。例如,该沸石吸附剂具有特别强的选择吸附co2的选择性,其对ch4和n2的分离选择性分别为co2/ch4=24-51和co2/n2=127-135,可以应用于从天然气和油田气去除co2和h2s,回收甲烷和乙烷。在液化空气制氧的工业设备上,用cha沸石分子筛吸附剂的变压吸附取代13x沸石吸附剂,可以高效低能耗分离除去空气中的水和二氧化碳分子。
[0004]
cha沸石分子筛的骨架和孔道开口结构示意图见图1和图2,cha沸石分子筛的骨架是由[sio4]和[alo4]四面体共氧链接成四氧元环和六氧元环初级结构d6r笼和四氧元环八氧元环构建的cha笼,d6r笼与cha笼相互连接进一步有序相联成开口孔径0.38x0.38nm的孔道结构,cha笼的空腔很大,达到0.84x0.84x0.82nm。
[0005]
cha沸石分子筛吸附剂在焦化煤气中可以去除其中所含少量的co2、co、和ch4,制高纯h2。低硅cha沸石的另一重要应用是从空气中吸附去除小分子有毒、有害、恶臭气体。表1列举的几种典型的气体名称、化学式和分子尺寸。低硅cha沸石分子筛的骨架结构孔径是0.36
×
0.36nm,对所列的有毒、有害、恶臭气体的分子尺寸比较接近,可以通过改变吸附温度和压力,实现有效吸附。此外低硅cha沸石的硅铝摩尔比在4左右,与骨架平衡的阳离子比较多,可以通过用直径不同的金属阳离子交换制成不同阳离子型cha沸石分子筛吸附剂,精细调节其吸附孔径,以提高对特定分子的吸附选择性。
[0006]
表1
[0007]
分子名称化学式分子尺寸/nm甲醛ch3cho0.33硫化氢h2s0.36甲氰ch3cn0.42氰化氢hcn0.33二氧化硫so20.36一氧化碳co0.37二氧化碳co20.37氨nh30.38
技术实现要素:
[0008]
在发明内容部分中引入了一系列简化形式的概念,这将在具体实施例部分中进一
步详细说明。本发明的发明内容部分并不意味着要试图限定出所要求保护的技术方案的关键特征和必要技术特征,更不意味着试图确定所要求保护的技术方案的保护范围。
[0009]
为至少部分地解决上述技术问题,本发明提供了一种高岑土制cha沸石,包括:首先,对矿粉原料进行焙烧。所述矿粉选取高岭土矿粉细度为320目,所述高岭土矿粉经过650~800℃、0.5~3h焙烧使原有的晶体结构崩塌,所述偏高岭土的晶体结构为无定型。
[0010]
其次,cha沸石合成过程。所述原料、1mol/l koh溶液和所述原矿粉5%的cha晶种混合均匀组成反应混合物,所述反应混合物置于不锈钢耐压反压釜中再放入烘箱加热进行水热反应,所述水热反应温度130℃-150℃,时间48h。最终合成的产物经过滤、洗涤和烘干制成k-cha沸石。
[0011]
最后,阳离子交换。所述k-cha沸石以0.5n nacl溶液为离子交换液进行阳离子交换得到(na、k)-cha阳离子型沸石。
[0012]
进一步地,所述cha晶种与无定形偏高岭土矿粉重量之比是1-10:50-500。
[0013]
进一步地,所述交换的温度为95℃,时间2h。所述k-cha沸石:nacl溶液=1:10,交换次数为3次,每次交换后用去离子水洗涤3次,抽滤的滤饼可进行下一次离子交换。
[0014]
进一步地,所述koh溶液的浓度不限定于1.0-2.0mol/l,所述偏高岭土矿粉与koh溶液的固液比并不是限定为1:9,所述偏高岭土矿粉加入适量cha晶种的百分比也是不限于5%。所述水热反应的温度并不局限于130-150℃,反应时间也并不局限于24-48h。
[0015]
进一步地,所述阳离子型沸石(na、k)-cha可应用于co2与ch4富集、废气中co、h2s、hcn、cos、nh3、nox等有毒有害气体的吸附分离和去除,具有离子交换和吸附性质。
[0016]
进一步地,所述cha沸石的bet表面积12.4cm2/g,微孔面积0cm2/g,总孔容积0.07ml/g,微孔容积0ml/g。所述阳离子型(na、k)-cha沸石的bet表面积103.3cm2/g,微孔面积62.0cm2/g,总孔容积0.128ml/g,微孔容积0.025ml/g。显示出所述cha沸石具有丰富的晶间孔,小的微孔的吸附特征。
[0017]
进一步地,所述k-cha沸石为片状或条状晶体的聚集体晶粒,尺寸约2-3微米。
[0018]
与现有技术相比本发明的技术效果在于:本发明提出的高岑土制cha沸石是以高岭土矿粉为第一原料,此原料在我国内蒙古蒙西地区储量丰富,价格低廉。用此原料焙烧脱除其吸附和结晶水后,骨架完全被破坏而变成无定形粉,在所述无定形粉中加入适量cha晶种,在koh水溶液中通过水热反应合成k-cha沸石,所述k-cha沸石经nacl溶液交换制成的(na、k)-cha沸石显示出小孔沸石的离子交换和吸附性质。本发明所述(na、k)-cha沸石可应用于制离子交换剂和小分子,例如co2与ch4富集、废气中co、h2s、hcn、cos、nh3、nox等有毒有害气体的吸附分离和去除。同时,本发明采用的制备方法原料价格低廉,合成工艺简单,无环境污染,易于工业化。
附图说明
[0019]
为了使本发明的优点更容易理解,将通过参考在附图中示出的具体实施方式更详细地描述上文简要描述的本发明。可以理解这些附图只描绘了本发明的典型实施方式,因此不应认为是对其保护范围的限制,通过附图以附加的特性和细节描述和解释本发明。
[0020]
图1为本发明cha沸石分子筛的骨架结构示意图;
[0021]
图2为本发明cha沸石分子筛的孔道开口结构示意图;
[0022]
图3为本发明所述矿粉原料焙烧的xrd衍射谱;
[0023]
图4为本发明所述cha沸石进行xrd沸石结构作晶相鉴定示意图;
[0024]
图5为本发明所述cha沸石的晶体形貌电子显微镜照片;
[0025]
图6为本发明实施例cha沸石合成示意图。
具体实施方式
[0026]
下面描述发明的优选实施方式。本领域技术人员应当理解的是,这些实施方式仅仅用于解释发明的技术原理,并非在限制发明的保护范围。
[0027]
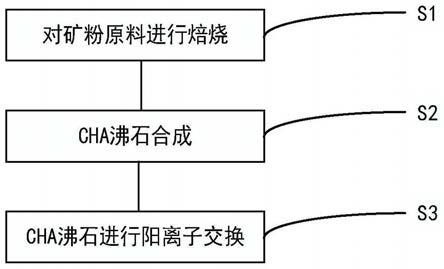
本发明实施例提供一种高岑土制cha沸石,包括如下步骤:
[0028]
步骤s1,对矿粉原料进行焙烧。所述矿粉选取高岭土矿粉细度为320目,所述高岭土矿粉经过高温焙烧破坏其晶体结构,此时偏高岭土的晶体结构为无定型,在无定型偏高岭土中加入原矿粉5%的cha晶体。
[0029]
具体而言,所述原料矿粉经650~800℃、0.5~3h焙烧使原有的晶体结构崩塌,其xrd衍射谱见图3,其中,图3中a为高岭土矿粉的xrd衍射谱,b为偏高岭土的xrd衍射谱;图中无定形粉的结构衍射峰消失,显示为背景较平坦的无定形衍射区域。
[0030]
具体而言,所述cha晶种与无定形偏高岭土矿粉重量之比是1-10:50-500。
[0031]
步骤s2,cha沸石合成过程。所述原料、1mol/l koh溶液和所述原矿粉5%的cha晶种混合均匀组成反应混合物,所述反应混合物置于不锈钢耐压反压釜中再放入烘箱加热进行水热反应,所述水热反应温度130℃-150℃,时间48h。最终合成的产物经过滤、洗涤和烘干制成k-cha沸石。
[0032]
具体而言,使用粉末x射线衍射仪对所述产物k-cha沸石进行xrd沸石结构作晶相鉴定,结果见图4。其中,图4中a为文献标准谱,图4中b为本发明制成的k-cha沸石。
[0033]
具体而言,采用北京普析通用仪器公司的xd2型x射线粉末衍射仪测试,扫描范围5-35
°
/2θ,扫描速度4
°
/2θ/min。同时,使用荷兰phenom公司的phenom prox型台式扫描电子显微镜观测合成的k-cha沸石分子筛晶体形貌以及晶粒尺寸,并拍摄照片,详细照片见图5。从而得出结论:所述k-cha沸石为片状或条状晶体的聚集体晶粒,尺寸约2-3微米。
[0034]
步骤s3,阳离子交换。所述k-cha沸石以0.5n nacl溶液为离子交换液进行阳离子交换得到(na、k)-cha阳离子型沸石。
[0035]
具体而言,采用德国bruker公司的s8 tiger x-光荧光散射仪器(xrf)测定本发明所述k-cha沸石和阳离子型(na、k)-cha沸石的化学组成与百分含量,并由其sio2、al2o3含量计算出其氧化硅与氧化铝的摩尔比(sar)。其中,所述k-cha沸石与(na、k)-cha阳离子沸石的成分分析结果如表1所示:
[0036]
表1
[0037][0038]
[0039]
从上述数据显示结果来看,在koh溶液中合成的k-cha沸石其sar明显高于偏高岭土的sar,这是因为自然形成的天然矿物na,ca-cha单晶的sar接近4,显然,该数据是低硅cha结构沸石晶相的平衡组成。
[0040]
具体而言,所述交换的温度为95℃,时间2h。所述k-cha沸石:nacl溶液=1:10,交换次数为3次,每次交换后用去离子水洗涤3次,抽滤的滤饼可进行下一次离子交换。
[0041]
具体而言,3次nacl离子交换,k-cha沸石的k2o含量从13.5下降到(k,na)-cha沸石的5.06%,交换度达到了62.5%。这说明本发明合成的低硅cha结构小孔沸石分子筛,具有良好沸石分子筛的共同特性-阳离子交换性。
[0042]
用国产贝士德仪器公司的3h-2000ps2静态容量法比表面及孔径分析仪,对k-cha沸石和(na、k)-cha沸石进行低温氮吸附测试,吸附测定结果见表2:
[0043]
表2
[0044][0045]
从上述数据分析,表明偏高岭土合成的低硅k-cha的低温氮吸附性能不突出,并不具有该结构类型沸石应该具有的微孔结构的基本性质。其原因在于,低温氮吸附所用的吸附质氮气的动力学直径是0.3nm,虽然可以进入平均孔口直径0.38nm的k-cha沸石孔内被吸附,但sar3.3左右(即si、al原子比1.7)左右的k-cha沸石属于低硅高铝沸石,与其骨架al所带负电荷平衡的k
+
含量比较高,而k
+
直径是0.26nm,k
+
必然使cha沸石孔口有效直径分别从0.38nm降低至0.12nm,这样,氮分子不能穿过孔口被吸入k-cha沸石的孔道中,使其bet表面积仅仅12cm2/g左右,但更直接反映小孔沸石结构性质的微孔表面积、微孔容积均为0。经三次nacl溶液离子交换,用直径为0.20nm的na
+
通过离子交换替代约50%的k
+
生成的(na、k)-cha沸石,其低温氮吸附性质有明显提高,bet表面积达到103cm2/g、微孔表面积和微孔容积分别提高到62.0cm2/g和0.025ml/g。该数据也提示出要将偏高岭土合成的低硅小孔k-cha沸石用于小分子气体的吸附分离,必须通过阳离子交换,用离子直径小于钾离子的其它金属阳离子部分或全部替代k-cha沸石中的钾,使其孔口开放,允许小分子气体分子被吸附和从中脱附。
[0046]
下面通过实施例对本实施例cha沸石的制成方法进行说明。
[0047]
实施例1
[0048]
选取50g焙烧后的高岭土矿粉与2.5g沸石晶体,放入到450ml浓度为1mol/l koh溶液中混合均匀组成反应混合物,该反应物倒入750ml耐压不锈钢反应釜中、密封,置于130℃的均相反应烘箱中,反应时间48h。最终合成的产物经过滤、洗涤和烘干制成k-cha沸石。用粉末x射线衍射仪对合成产物k-cha沸石进行xrd沸石结构作晶相鉴定。再将所述k-cha沸石以0.5n nacl溶液为离子交换液进行阳离子交换得到(na、k)-cha阳离子型沸石,可应用于co2与ch4富集、废气中co、h2s、hcn、cos、nh3、nox等有毒有害气体的吸附分离和去除。
[0049]
实施例2
[0050]
选取50g焙烧后的高岭土矿粉与2.5g沸石晶体,放入到450ml浓度为1mol/l koh溶液中混合均匀组成反应混合物,该反应物倒入750ml耐压不锈钢反应釜中、密封,置于150℃的均相反应烘箱中,反应时间24h。最终合成的产物经过滤、洗涤和烘干制成k-cha沸石。用粉末x射线衍射仪对合成产物k-cha沸石进行xrd沸石结构作晶相鉴定。再将所述k-cha沸石以0.5n nacl溶液为离子交换液进行阳离子交换得到(na、k)-cha阳离子型沸石,可应用于co2与ch4富集、废气中co、h2s、hcn、cos、nh3、nox等有毒有害气体的吸附分离和去除。各实施例的工艺参数见表3:
[0051]
表3
[0052][0053]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1