一种纤维蛋白溶酶原检测试剂盒的制作方法
本发明涉及临床体外检测试剂技术领域,特别涉及一种纤维蛋白溶酶原免疫比浊法检测试剂盒。
背景技术:
人纤维蛋白溶酶原(plasminogen,Pg)是一种血浆蛋白,主要由肝细胞产生,血浆中的含量为0.06~0.25mg/mL。人纤维蛋白溶酶原是人纤维蛋白溶酶的前体物质,没有活性。在正常人体内,人纤维蛋白溶酶原通过纤维蛋白溶酶原激活因子激活转变成有活性的人纤维蛋白溶酶,进而水解纤维蛋白(原)和其它的凝血因子,起到抗凝的作用。纤溶酶的作用是保持血管内的凝血、纤溶的平衡,使血流畅通。
纤维蛋白溶酶原主要生理功能是参与纤溶系统。纤维蛋白溶酶原在血清中处于非活性状态,可被尿激酶、链激酶、胰蛋白酶、凝血酶等物质激活。激活后的纤维蛋白溶酶原转变为纤溶酶,它可以水解凝固的纤维蛋白,从而使得沉淀附着于血管壁的纤维蛋白得以逐渐溶解,起到抗凝的作用。严重创伤、灼伤、外科手术、产科意外、输血反应等病理情况时,纤溶系统被过度激活,致使大量的纤维蛋白溶酶原转变为纤溶酶,其活力过强,超过了抗纤溶酶的抑制能力,这时就会导致纤溶过度而致出血。纤溶过度也是血管内弥散性凝血的重要特征。
本发明提供一种用免疫透射比浊法检测纤维蛋白溶酶原的试剂盒,优化其反应体系,使其操作简单、重复性好、稳定性好、可进行批量样本全自动化检测,从而有利于在市场中进一步推广使用。
技术实现要素:
本发明旨在提供一种稳定性好用于检测纤维蛋白溶酶原的试剂盒,该试剂盒采用免疫透射比浊法。该试剂盒与常规的试剂盒相比,稳定性和线性相关性比常规的检测试剂盒要好,有利于试剂在临床上的推广应用。
基本原理:
以免疫透射比浊法为测定原理,当样本与试剂混合后,样本中的纤维蛋白溶酶原与羊抗人纤维蛋白溶酶原抗体发生特异性结合,形成不溶性的抗原-抗体复合物,使溶液产生浊度。在340nm波长下检测,该浊度的高低在一定量抗体存在时与抗原的含量成正比。通过与同样处理的校准液比较,计算未知样本中纤维蛋白溶酶原的含量。
发明是通过以下步骤得到的:
一种纤维蛋白溶酶原检测试剂盒,其特征在于,它包含试剂R。试剂组成如下:50mmol/L pH为7.8 的磷酸盐缓冲液、1.8mg/mL羊抗人纤维蛋白溶酶原抗体、1%聚乙二醇6000、2%乳胶颗粒、20mmol/L EDTA-Na2、50mmol/L氯化钠、10mmol/L叠氮钠。
所述的纤维蛋白溶酶原检测试剂盒,其特征在于试剂R缓冲液为25℃,pH为7.8的磷酸盐缓冲液。
所述的纤维蛋白溶酶原检测试剂盒,其特征在于所述胶乳颗粒为聚苯丙烯,粒径为100-260nm。
所述的纤维蛋白溶酶原检测试剂盒,其特征在于所述稳定剂为EDTA- Na2(乙二胺四乙酸二钠)。
所述的纤维蛋白溶酶原检测试剂盒,其特征在于,使用全自动生化分析仪采用终点法进行测定,检测主波长为340nm。
本发明的试剂盒在具有双试剂功能的全自动生化分析仪上进行,其具体使用方法为:
加入生理盐水、样本或校准品3μl,再加入300μl 的试剂R,预孵育5min后读取吸光度A1,再反应5min后读取吸光度A2,并计算ΔA。
本发明的有益效果:
1)采用新的缓冲体系,改善了试剂稳定性;
2)添加EDTA-Na2,增强了试剂稳定性,而且不会对试剂准确度产生影响;
3)试剂准确度和稳定性好,价格便宜,使用方便,有利于该试剂在市场中进一步推广。
附图说明
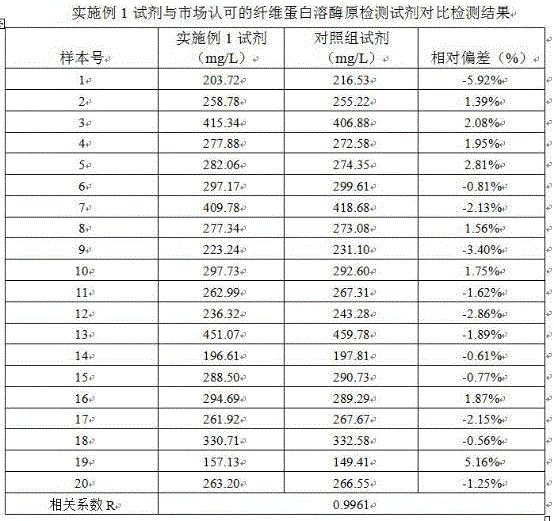
图1为本发明试剂与对照组试剂准确度实验结果;
图2为本发明试剂与对照组试剂准确度实验的相关性曲线图;
图3为本发明试剂与对照组试剂效期稳定性曲线图;
图4 为本发明试剂与对照组试剂线性相关性验证试验结果;
图5 为本发明试剂与对照组试剂线性稳定性验证试验结果。
具体实施方式
下面结合具体实施例对本发明进行进一步说明:
实施例1
一种常规的纤维蛋白溶酶原检测试剂盒,它包括试剂R。
试剂R组成为:
50mmol/L 磷酸盐缓冲液 pH为7.8
羊抗人纤维蛋白溶酶原抗体 1.8mg/mL
聚乙二醇6000 1%
乳胶颗粒 2%
EDTA-Na2 20mmol/L
氯化钠 50mmol/L
叠氮钠 10mmol/L。
本实施例所述试剂R配置时需先配制磷酸缓冲液,调到适当pH值后,再添加其它成分。本实施例所述试剂盒在使用时,其测定方法是采用迈瑞800全自动生化分析仪,利用终点法进行测定,检测主波长为340nm,操作如下:
加入生理盐水、样本或校准品3μl,再加入300μl 的试剂R,预孵育5min后读取吸光度A1,再反应5min后读取吸光度A2,并计算ΔA。
ΔA=A2- A1
纤维蛋白溶酶原含量(mg/L)=(∆A测定÷∆A标准)×C标准。
测定:检测样本 ∆A标准:标准品
实施例2
准确度验证试验:将实施例1的纤维蛋白溶酶原检测试剂作为实验组,市场上获得认可的一种准确度好、稳定性好的纤维蛋白溶酶原检测试剂作为对照组进行检测,对20个临床血清样本进行检测,检测结果如图1所示。获得了两种试剂的相关性曲线(如图2所示),结果表明,两组试剂盒的相关系数为0.9961,说明两者相关性比较好。证明本发明试剂盒添加及更改的组分对其准确性不会造成影响,试剂盒依然保持较好的准确度。
实施例3
线性相关性验证试验:选取纤维蛋白溶酶原含量为420mg/L的高值样本,用生理盐水进行系列稀释,配制6个不同浓度的样本,浓度依次为420mg/dL、336mg/dL、252mg/dL、168mg/dL、84mg/dL、0mg/dL。分别利用实施例1试剂及对照组试剂进行检测,每个浓度的样本分别测定三次,分别取平均值,检测结果如图4所示。
如上表所示,实施例1与对照组试剂检测结果相关系数均大于0.990,且实施例1试剂检测结果的相关系数略大于对照组试剂检测结果的相关系数,这表明本发明试剂具有更好的线性相关性。
实施例4
稳定性验证实验:在2℃~8℃、无腐蚀性气体的避光环境中贮存试剂,检测实施例1及对照组试剂的稳定性。每月1号分别用两组试剂测定同一混合血清样本,测定三次取平均值,检测数据如图5所示。
实验结果显示,实施例1试剂在2℃~8℃、无腐蚀性气体的避光环境中贮存15个月稳定,而对照组试剂在2℃~8℃、无腐蚀性气体的避光环境中贮存8个月后开始不稳定,说明本发明试剂更换缓冲液及添加EDTA-Na2后稳定性增强。
综上所述,本发明提供的纤维蛋白溶酶原检测试剂盒,将试剂R的缓冲液更换为pH 7.8的磷酸盐缓冲液,同时添加20mmol/L的EDTA-Na2,提高了试剂盒的稳定性,线性范围较好,试剂的准确度也较好。因此,本发明提供的纤维蛋白溶酶原检测试剂盒有利于在市场中进一步的推广使用。
- 还没有人留言评论。精彩留言会获得点赞!