壳聚糖/胶体金复合体系、制备方法及应用与流程
本发明涉及一种壳聚糖/胶体金复合体系,同时还涉及该复合体系的制备方法及应用,属于材料技术领域。
背景技术:
胶体金也称金溶胶,是把金盐还原成金后形成的稳定、均一的纳米金粒子悬液,属于多相不均匀体系,颜色从桔红色到紫红色变化。胶体金粒子以一个金核(Au)为基础,外围包覆负离子AuCl2-,最外层为H+,分散在胶体间溶液中并维持胶体呈悬浮状态。胶体金粒子的金核不是理想的球形核,颗粒较小的基本呈球形,而颗粒较大(直径30nm以上)的多呈椭球形。
胶体金粒子具有荧光光谱特性,其在可见光范围内存在单一的光吸收峰,且随着粒径的增大波长变长。另外,在胶体金的众多胶体特性中,最为显著的是对电解质的敏感性,某些大分子物质如蛋白质不仅对胶体金起到保护作用,还能提高胶体金的稳定性。一般情况下,在不破坏电解质、溶胶浓度等稳定因素时,胶体金的稳定性较好,长时间放置也不会发生凝聚现象。
目前,胶体金主要作为标记物或显色剂用于检测抗原抗体,作为一种新型的免疫标记技术在生物、医药等领域具有潜在的应用前景。由于该技术不存在内源酶干扰和放射性同位素干扰等,且采用不同颗粒大小的胶体金作为双重或多重标记,其定位更加准确。胶体金中金粒子的尺寸在1~100nm之间,除具有纳米材料的通性(如较大的比表面积、量子尺寸效应和宏观量子隧道效应等)外,其化学性质也异常活泼,可以与亲核试剂吸附生成具特殊功能的基团。例如纳米金可以与氨基发生非共价键的静电吸附,也可以与疏基产生较强的共价键作用,但结合后纳米金的光学性质并不发生变化,因此可用于生物监测。近几年,胶体金的应用主要集中在快速斑点免疫金渗滤法和胶体金快速免疫层析法。快速斑点免疫金渗滤法又叫滴金免疫法,该方法以微孔膜为固相载体,将已知的特异性抗体或抗原固定其上,并装入充满吸水材料的渗滤装置中,加入待测样本,经由滤膜的毛细管作用或渗滤作用,使标本中的抗原或抗体与膜上包被的抗体或抗原结合,最后经胶体金结合物标记而达到检测目的。而快速免疫层析法也是以微孔膜为固相载体,其上固定已知的特异性抗体或抗原作为检测带,胶体金标记物在玻璃纤维质结合释放垫上干燥,其一端与样品垫相连,另一端与膜相连,膜的另一端连有吸水垫。当加入待测样品后,样品通过毛细管向前移动,并通过含有标记物的玻璃纤维,使标记物重新水化,并与胶体金标记物相互反应一起向前,至检测线时,检测线截获标记物与待测物的复合物,从而出现红色结果。
现有技术中,传统的胶体金制备方法包括柠檬酸三钠还原法、抗坏血酸还原法、硼氢化钠还原法等。其中,柠檬酸三钠还原法的操作步骤为:取50mL 0.01%氯金酸与2mL 1%柠檬酸三钠充分混合,加热15min,冷却后用水补至原体积,即得。抗坏血酸还原法的操作步骤为:取50mL 0.01%氯金酸、0.75mL 0.2M K2CO3与0.5mL 0.7%抗坏血酸充分混合,加热10min,冷却后用水补至原体积,即得。硼氢化钠还原法的操作步骤为:取50mL 0.01%氯金酸与0.25mL 0.2M K2CO3充分混合,分3至5次向混合溶液中滴加新鲜配制的0.5mg/mL硼氢化钠,边加边振荡使其混合均匀,直至溶液变紫,最终变为橙红色,继续振荡约3min,即得。然而,上述三种方法制备出的胶体金均须于4℃下贮存。
公布号CN105665740A的发明专利公开了一种大气压空气等离子体液相下合成胶体金纳米颗粒的方法,包括:在绝缘材料容器中加入氯金酸与还原剂的混合液,向该混合液中通入大气压空气等离子体,即得胶体金纳米颗粒。该方法采用空气替代稀有气体作为激发气体,2~10min即可形成均一性良好、灵敏度高且性能稳定的胶体金纳米颗粒。公布号CN102430392A的发明专利也公开了一种复合纳米胶体金壳聚糖载体的制备方法,包括:1)取质量浓度0.01%的氯金酸溶液加热至沸腾,搅拌加入预热的1%柠檬酸三钠溶液,至氯金酸溶液由金黄色变为灰色再变为酒红色,继续搅拌煮沸至溶液呈透亮的红色,得到胶体金溶液;2)壳聚糖用0.1~1%的有机弱酸溶解成质量浓度0.01~0.1%的壳聚糖溶液,过滤备用;3)按照质量比1:0.1~1将胶体金溶液与壳聚糖溶液混合均匀,缓慢滴加0.05%的碳酸钾溶液至混合液pH值为7.0,得到复合纳米胶体金壳聚糖载体混合液。其中,复合载体的粒径分布在20~200nm之间,平均粒径80nm,可用于免疫检测或免疫诊断。然而,上述两种方法在制备胶体金时均需使用还原剂,并且制得的胶体金稳定性差,需要在低温下贮存。
技术实现要素:
本发明的目的是提供一种壳聚糖/胶体金复合体系。
同时,本发明还提供一种壳聚糖/胶体金复合体系的制备方法。
最后,本发明提供一种壳聚糖/胶体金复合体系在制备电化学生物传感器或者检测莱克多巴胺中的应用。
为了实现以上目的,本发明所采用的技术方案是:
壳聚糖/胶体金复合体系,是在含有氯金酸和壳聚糖的溶液中通入等离子体制备得到。
所述含有氯金酸和壳聚糖的溶液的组成为:氯金酸0.05~0.1g,壳聚糖0.1~0.2g,冰乙酸400~600μL,水20~30mL。配制溶液时,可先将壳聚糖溶于冰乙酸的水溶液中,再加入氯金酸即可。
所述等离子体为氮气等离子体。通入等离子体的技术参数为:脉冲射频功率源功率100~200W,通入时间5~10min。
壳聚糖/胶体金复合体系的制备方法,包括以下步骤:在含有氯金酸和壳聚糖的溶液中通入等离子体,超声混合,至溶液呈紫红色,得到壳聚糖/胶体金复合体系。
所述含有氯金酸和壳聚糖的溶液的组成为:氯金酸0.05~0.1g,壳聚糖0.1~0.2g,冰乙酸400~600μL,水20~30mL。
所述等离子体为氮气等离子体。通入等离子体的技术参数为:脉冲射频功率源功率100~200W,通入时间5~10min。制备原理为:本发明采用常温低压等离子体制备胶体金,其中壳聚糖作为稳定剂和还原剂,在等离子制备过程中,氮气等离子体引发水分子产生自由基,进而对氯金酸进行还原。
壳聚糖/胶体金复合体系在制备电化学生物传感器中的应用,具体为:将壳聚糖/胶体金复合体系滴加在电极上,干燥,得到壳聚糖/胶体金修饰的电极;将上述电极置于抗体液中,在电极表面自组装抗体,即得电化学生物传感器。在上述应用中,壳聚糖本身带有氨基基团,可为后续固定抗体(如莱克多巴胺抗体)提供结合位点,提高检测的灵敏性。
所述抗体液中含有莱克多巴胺抗体时,所得传感器即可用于检测莱克多巴胺。
本发明的有益效果:
本发明中壳聚糖/胶体金复合体系是在含有氯金酸和壳聚糖的溶液中通入等离子体制备得到,该体系中胶体金粒子为纳米尺寸,颗粒大小在50nm左右,呈不规则形状。该复合体系能作为敏感膜材料修饰电极,电极自组装RAC-anti抗体后可特异性检测RAC抗原,检测灵敏度高,选择性和稳定性好。
本发明采用等离子法制备壳聚糖/胶体金复合体系,可省去化学还原剂,在常温下快速合成稳定的胶体金,是一种“绿色”的合成方法。
附图说明
图1为复合体系中壳聚糖/胶体金的TEM图;
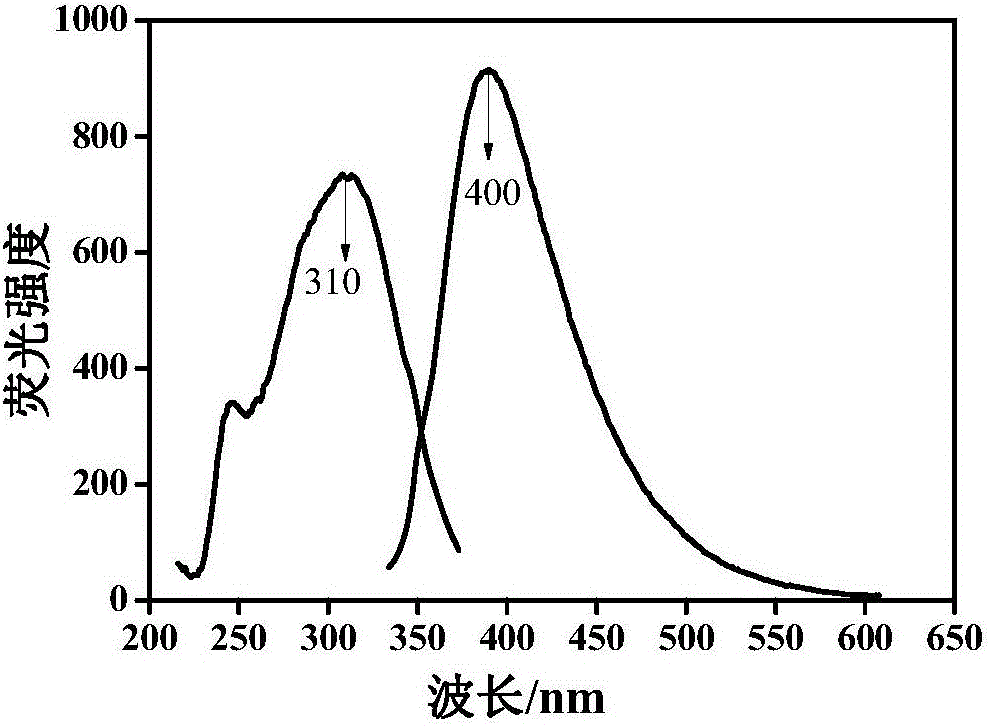
图2为复合体系中壳聚糖/胶体金的荧光测试谱图;
图3为复合体系中胶体金的紫外可见光谱图;
图4为电化学生物传感器的CV图;
图5为电化学生物传感器构筑及检测过程的电化学阻抗图;
图6为电化学生物传感器检测不同浓度RAC的EIS图及拟合曲线图;
图7为电化学生物传感器的选择性测试结果;
图8为电化学生物传感器的稳定性测试结果。
具体实施方式
下述实施例仅对本发明作进一步详细说明,但不构成对本发明的任何限制。
实施例1
壳聚糖/胶体金复合体系,其制备步骤如下:
1)用新鲜配制的王水清洗要使用的所有玻璃器皿,再用水彻底冲洗,干燥备用;
2)用1mL移液枪量取600μL 99%冰乙酸于25mL容量瓶中,加入20mL水稀释成浓度3%的冰乙酸溶液;
3)称取0.2g壳聚糖,加入到稀释好的冰乙酸溶液中,超声使壳聚糖完全溶解,静置,至气泡完全消失;
4)在去离子水中加入氯金酸至浓度100mM,再加入550μL壳聚糖溶液,在功率500W、频率40kHz下超声混合10min,静置得混合液;
5)在混合液中通入氮气等离子体,脉冲射频功率源功率200W,时间5min,再在功率500W、频率40kHz下超声混合10min,至溶液变为紫红色,得到壳聚糖/胶体金复合体系。
壳聚糖/胶体金复合体系在检测莱克多巴胺中的应用,具体步骤如下:
1)金电极的预处理
采用0.5μm和0.3μm Al2O3的浆液在麂皮上打磨抛光金电极,至电极表面无明显划痕,打磨轨迹为“8”字形,然后用去离子水清洗金电极,将残留在电极上的Al2O3洗干净;将电极置于H2O2:H2SO4体积比3:7的混合液中,于功率500W、频率40kHz下超声作用15min,去离子水冲洗干净;再将电极置于水:无水乙醇体积比1:1的混合液中,同上超声15min,再置于去离子水中超声15min;将清洗干净的金电极置于0.5M H2SO4溶液中,采用循环伏安法在0.2~1.6V电压范围内活化2遍,再用去离子水冲洗干净,吹干备用;
2)将上述制备的壳聚糖/胶体金复合体系稀释至2倍体积,超声30min使混合均匀;用10μL移液枪移取10μL稀释体系滴加在金电极上,完全干后测试其电化学阻抗(EIS),待稳定后用去离子水冲洗干净并吹干,得到壳聚糖/胶体金修饰的电极;将上述电极置于100ng/mL莱克多巴胺抗体(RAC-anti)液中浸泡2h,保证壳聚糖/胶体金复合材料有充足的时间与莱克多巴胺抗体自组装,取出冲洗干净,测试EIS,待稳定后用去离子水冲洗并吹干,即得用于检测莱克多巴胺的电化学生物传感器;
3)采用该传感器对溶液中莱克多巴胺进行检测。
实施例2
壳聚糖/胶体金复合体系,其制备步骤如下:
1)含氯金酸和壳聚糖溶液的制备
将壳聚糖溶于稀的冰乙酸溶液中,溶解完全后加入氯金酸,混匀备用;
溶液组成为:氯金酸0.05g,壳聚糖0.1g,冰乙酸400μL,水20mL;
2)在上述溶液中通入氮气等离子体,脉冲射频功率源功率100W,时间10min,反应至溶液变为紫红色,得到壳聚糖/胶体金复合体系。
壳聚糖/胶体金复合体系的应用同实施例1。
实施例3
壳聚糖/胶体金复合体系,其制备步骤如下:
1)含氯金酸和壳聚糖溶液的制备
将壳聚糖溶于稀的冰乙酸溶液中,溶解完全后加入氯金酸,混匀备用;
溶液组成为:氯金酸0.1g,壳聚糖0.2g,冰乙酸600μL,水30mL;
2)在上述溶液中通入氮气等离子体,脉冲射频功率源功率150W,时间5min,反应至溶液变为紫红色,得到壳聚糖/胶体金复合体系。
壳聚糖/胶体金复合体系的应用同实施例1。
实施例4
壳聚糖/胶体金复合体系,其制备步骤如下:
1)含氯金酸和壳聚糖溶液的制备
将壳聚糖溶于稀的冰乙酸溶液中,溶解完全后加入氯金酸,混匀备用;
溶液组成为:氯金酸0.075g,壳聚糖0.15g,冰乙酸500μL,水25mL;
2)在上述溶液中通入氮气等离子体,脉冲射频功率源功率180W,时间8min,反应至溶液变为紫红色,得到壳聚糖/胶体金复合体系。
壳聚糖/胶体金复合体系的应用同实施例1。
试验例
1)复合体系中胶体金的形貌与结构测试
测试方法:取实施例1中壳聚糖/胶体金复合体系,滴加在碳膜支撑的铜网上,用于TEM测试,结果见图1,其中图1(a)~1(c)依次为10nm、200nm、5nm标尺下的TEM图,图1(d)为电子选区衍射,1(e)为壳聚糖/胶体金的晶格条纹。
由图1可知,胶体金粒子为纳米尺寸,颗粒大小在50nm左右(呈紫红色),不规则形状,其晶格结构为对应于(310)和(400)面生长。
2)复合体系中胶体金的UV-vis和荧光测试谱图
测试方法:取实施例1中壳聚糖/胶体金复合体系,稀释10倍后加入到检测用石英比色皿中,设置仪器参数,在激发波长310nm处寻找最佳发射波长,结果见图2、3。
由图2可知,激发波长为310nm时,胶体金在400nm处有一吸收峰。
由图3可知,胶体金在543nm处出现紫外吸收峰,说明胶体金的粒径在60nm左右,与TEM测试结果基本一致。
3)电化学性质分析
测试方法:取实施例1中电化学生物传感器及一空白电极,采用上海辰华CHI600D电化学工作站,以传统的三电极工作体系,Ag/AgCl为参比电极,Pt丝为辅助电极,电化学生物传感器为工作电极,在开路电压0.22V、测试范围0.01Hz~100kHz、交流电振幅5mV条件下测试交流阻抗谱,采集数据并用Zview2处理,得到阻抗值,结果见图4。
由图4可知,与空白电极相比,实施例中电化学生物传感器的循环伏安特性曲线峰值高、面积大,说明该传感器具有较优的电化学活性。
4)电化学生物传感器检测莱克多巴胺分析
测试方法:首先在电极表面滴涂壳聚糖/胶体金复合材料,之后采用自组装的方法将电极浸泡在1ng/mL莱克多巴胺抗体液中,反应4h,再浸泡于莱克多巴胺溶液中,采用电化学阻抗谱的方法测试不同反应过程中电极表面的变化,结果见图5。
由图5可知,在电极表面依次组装壳聚糖/胶体金复合材料、RAC-anti和RAC后,EIS图中电荷转移电阻ΔRct均明显增大,CV图中循环伏安特性胶体金材料曲线面积明显增大。壳聚糖/胶体金修饰后电极吸附RAC-anti和RAC后,电荷转移电阻ΔRct增大,而循环伏安特性曲线面积变小,说明修饰后电极与RAC-anti发生非特异性吸附,而RAC-anti与RAC发生特异性吸附。
测试方法:取实施例1中电化学生物传感器,浸泡于不同浓度的莱克多巴胺溶液中,并采用电化学阻抗法测试其阻抗值,结果见图6,其中图6(a)为测试不同浓度的莱克多巴胺的Nyquist图,图6(b)为对不同浓度对应的Rct线性拟合做出的直线关系图。
通过测试不同浓度的莱克多巴胺,经拟合其交流阻抗值得到关于检测莱克多巴胺的线性方程:y=200.26LogC+529.5,线性相关系数R2=0.991,电化学生物传感器的最低检测限为2.27pg/mL。
5)电化学生物传感器的选择性和稳定性测试
测试方法:取实施例1中电化学生物传感器,分别浸泡于1μg/mL的K+、Ca2+、Na+、Mg2+、urea、UA、CLB、SAC、RAC中,测试后收集阻抗值数据,结果见图7。
由图7可知,实施例中电化学生物传感器对莱克多巴胺的检出量最高,选择性最好。
测试方法:采用实施例1中方法制备5根相同的电化学生物传感器,用于检测莱克多巴胺,结果见图8。
由图8可知,不同批次电化学生物传感器的稳定性良好。
- 还没有人留言评论。精彩留言会获得点赞!