一种基于石墨烯氧化物传感器及其对Hg2+检测的方法与流程
本发明涉及一种基于石墨烯氧化物传感器及其对hg2+检测的方法,具体涉及一种基于特异性的核酸序列结合石墨烯氧化物的传感器及其检测重金属hg2+的方法,属于重金属检测技术领域。
背景技术:
hg2+是一种剧毒的重金属,在生物的体内不断积累,即使是低浓度的汞,长期接触也会引起严重的器官损伤。在过去的十年里,基于dna构建的hg2+检测传感器可以明显提高检测限,引起了广泛的研究兴趣,如有专家学者利用电化学生物传感器在水溶液中检测汞离子,氯化血红素作为氧化还原指示剂产生电化学信号,含有5个胸腺嘧啶(t-5)的短寡核苷酸链作为探针,通过au-s键自组装在金电极上;加入汞(hg2+),形成t-hg2+-t结构,氯化血红素吸附在金电极表面产生电化学信号,用微分脉冲伏安法(dpv)对信号检测。也有相关研究者构建一种“开启”型传感器测定方法,g四联体有淬灭农历,t-hg2+-t结构对hg2+的结合能力。一个在5’-端标记的羧基荧光素(fam),3’端附近是一个富g序列形成g-四链体结构代替传统的淬灭剂。加入hg2+,序列折叠成发夹结构,使附近的fam和g-四链体接触,荧光能量发生转移,荧光淬灭;碘的加入后,碘和hg2+结合,fam荧光恢复,该方法检测极限为30nm。目前现有技术存在的问题是稳定性较差、操作繁琐、成本高、检测的特异性和灵敏性不高。
纳米颗粒对小分子物质有可观的吸附性,同时多数的颗粒对荧光会有不同程度的影响。石墨烯作为表面积大,物理、化学性能优异的新型纳米材料,一经发现就迅速被专业应用。它电子转移率高,对荧光基团影响十分明显,在生物传感器领域大显身手。用简单的方法对石墨烯氧化,修饰更多的含氧基团,衍生物go成本比较低,众多的基团可以与单链dna通过π-π效应,吸附在go表面。设计一种含有多个胸腺嘧啶(t)的dna序列,由于hg2+能特异性结合两个t,使得单链dna对折,形成发卡结构,这种构型的变化,使得dna不再是单链,go的吸附能力减弱,部分dna逐渐远离go表面,从而使标记在dna上的荧光恢复发光。
技术实现要素:
本发明目的是克服现有技术中的缺陷,提供一种基于多t核苷酸的dna传感器及其对重金属hg2+的检测方法,多t可以被hg2+特异性识别并发生连接作用,从而高灵敏、快速、低成本对汞离子进行检测。
一种基于多t核苷酸的传感器,按照以下方法制备:
(1)制备go水溶液:通过改良的hummers法大批量制备go,将go真空干燥备用,使用前,在水溶液中超声分散,使之均匀分散在水中;
(2)合成特异性的核酸序列:5’-tttgcttgttgcgcttcttgcttt-3’。
(3)对核酸序列进行荧光标记:利用sybigreeni可以与单链dna结合,使得自身荧光信号放大,且对双链的吸附效果优于单链;
(4)荧光淬灭:将核酸序列加入到go水溶液中,制备基于多t序列的检测汞的go-dna传感器;go能够对核酸序列发生吸附作用;其中核酸序列的浓度为50nm;go的浓度为10µg/ml;
(5)hg2+的检测:加入hg2+,核酸序列上多个t被hg2+连接,构成t-hg2+-t,单链dna因此形成双链结构,又因go对变化后的dna吸附能力减弱而远离,greeni的荧光恢复。
本发明的方法中,优先选择采用edc和nhs混合对go处理,活化表面的羧基基团,活化后,羧基可以与氨基相互作用,形成化学键,更加牢固的固定dna。
本发明与现有技术相比较,具有以下优点:
(1)本发明的检测成本低、灵敏性高:go制备方法成熟,实验室条件易于获得,方法简单、成本低,无需复杂步骤和昂贵的仪器,对hg2+检测具有快速,特异性、高灵敏性。
(2)本发明采用greeni插入dna作为荧光信号,属于无标记,与传统带有荧光标记(如fam)的dna不同。
(3)采用固定化dna检测hg2+,减少实验误差,提高检测的准确性:
本发明中用edc和nhs对go表面的羧基等含氧集团活化,与dna末端修饰的氨基相互作用,使得dna固定在go的表面。
附图说明
图1为实施例1的操作流程示意图。
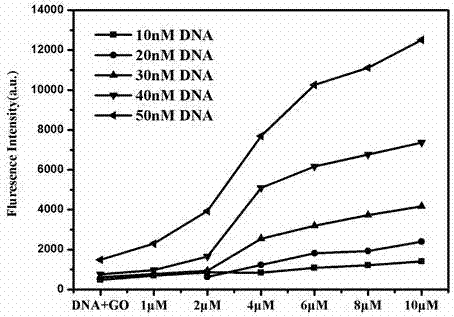
图2为不同浓度的dna构建的生物传感器对汞离子检测的影响。
图3为实施例1所制备的生物传感器加入汞离子后荧光强度随时间的变化。
图4为实施例1中基于go传感器对不同浓度的hg2+检测结果。
图5为实施例1中基于go传感器对不同金属离子选择性检测结果。
图6为实施例2的操作流程示意图。
图7为实施例2中固定化go传感器对不同浓度的hg2+灵敏性检测结果。
图8为实施例2中固定化go传感器对不同金属离子选择性检测结果。
图9实施例2中固定化go传感器对40nmhg2+检测图。
图10实施例2中固定化go传感器对4μmhg2+检测图。
具体实施方式
以下结合实施例对本发明做进一步说明,实施例是用于说明本发明而不是用于限制本发明的范围。
实施例1:
(1)制备go:通过改良的hummers法大批量制备go,在三口烧瓶中,加入3g鳞片石墨粉、1.5gnano3与69ml浓硫酸后放入恒温水浴锅中搅拌。反应1h后加入1gkmno4,35℃下反应5个小时后加入150ml去离子水。在温度98℃下反应30min后,再加入50ml的去离子水、5mlh2o2以及250ml的10%稀盐酸,将溶液倒入1000ml的大烧杯中,洗涤至ph值为5-6。将氧化产物真空干燥备用,使用前,在水溶液中1000w超声30min。
(2)合成特异的aptamer序列:5’-tttgcttgttgcgcttcttgcttt-3’,该序列在生工生物工程(上海)股份有限公司合成。
(3)荧光淬灭:向10μg/mlgo溶液中加入50nm的aptamer,同时加入1*greeni,随着时间的增加,染料会标记dna,但由于go对单链的吸附作用,大部分荧光被淬灭,20min后荧光强度趋于稳定。
(4)dna浓度的选择:在检测体系中分别加入不同浓度的dna(10nm,20nm,30nm,40nm,50nm),探究dna的最佳浓度,如图2。图2中为分别用10nm,20nm,30nm,40nm,50nmdna构建生物传感器对重金属hg检测效果不同;dna浓度越高,效果越好。
(5)基于go传感器对hg2+进行检测:含10μg/mlgo及50nmaptamer混合物在室温下放置30min。加入不同浓度(40nm—2μm)hg2+后,greeni荧光强度增加,20min后对aptamer上标记的greeni进行扫描,如图3为加入汞后荧光强度随时间的变化,用50nmdna和10μg/mlgo构建生物传感器,随着重金属浓度hg2+浓度的增加,在短时间引起荧光变化,并稳定;如图4为基于go传感器对hg2+灵敏性检测结果,图中greeni标记的aptamer的浓度为50nm,go浓度为10μg/ml;检测发现,灵敏度可达到22.5nm。
其中图1为本发明的流程示意图,图中与hg2+结合的核酸适配体是单链结构,当核酸适配体与go吸附后,标记的greeni荧光淬灭,当结合hg2+后,核酸适配体构象变化,形成双链,脱离go表面而使greeni发光。图1中可见,石墨烯氧化物对单链dna具有吸附作用,dna末端修饰上荧光基团由于靠近石墨烯氧化物,荧光能量共振转移使得荧光强度减弱,加入重金属hg2+,由于hg2+可以连接t-hg-t,发生错配,引起单链dna构成发卡结构,石墨烯氧化物对发卡结构的双链dna吸附效果减弱,dna远离材料表面,荧光基团强度恢复。
(5)选取其他与aptamer没有特异性作用的多种重金属如镉、钙、镍、锌、钴、铁、钴、铁、钾、铅、镁、锰等进行选择性检测,在同一实验条件下,发现go-aptamer能特异结合hg2+,而不能与其他金属结合,能明显区分出与其他几个重金属的差别,如图5,用50nmdna和10μg/mlgo构建生物传感器,加入各种重金属,不会引起荧光恢复现象,说明该生物传感器具有很好的选择性;证明该检测方法对hg2+具有良好地选择性。
实施例2:
(1)制备go:通过改良的hummers法大批量制备go,在三口烧瓶中,加入3g鳞片石墨粉、1.5gnano3与69ml浓硫酸后放入恒温水浴锅中搅拌。反应1h后加入1gkmno4,35℃下反应5个小时后加入150ml去离子水。在温度98℃下反应30min后,再加入50ml的去离子水、5mlh2o2以及250ml的10%稀盐酸,将溶液倒入1000ml的大烧杯中,洗涤至ph值为5-6。将氧化产物真空干燥备用,使用前,在水溶液中1000w超声30min。
(2)合成特异的核酸序列:5’-tttgcttgttgcgcttcttgctttnh2-3’,该序列在生工生物工程(上海)股份有限公司合成。
(3)go活化:0.5ml含50mmnhs和200mmedc与1ml2mg/mlgo,再加入0.5ml超纯水,室温下反应0.5小时后,10000rpm20min离心,去除上清,加入1ml超纯水,储存备用。
(4)构建go-dna传感器:向10μg/mlgo溶液中加入50nm的dna,过夜处理,使得dna与活化的go充分作用。
(5)基于go传感器对hg2+进行检测:含10μg/mlgo及50nm核酸序列混合物,加入1*sybrgreeni,静置10min,荧光标记。加入不同浓度(0nm—1000nm)hg2+,20min后对核酸序列上标记的sybrgreeni进行扫描,如图6,用edc/nhs活化石墨烯氧化物上的羧基,使它可以与dna末端修饰的氨基相互作用,紧密的拉近了荧光基团与石墨烯氧化物表面的距离,荧光强度减弱。离心去除未固定上的单链dna,加入重金属hg,同样引起单链dna构成双链发卡结构,核酸序列离开表面一定距离,荧光恢复,图中sybrgreeni标记的核酸序列的浓度为50nm,go浓度为10μg/ml。检测发现,灵敏度可达到17.1nm。
图7为固定化go传感器对hg2+灵敏性检测结果;用50nmdna和10μg/mlgo过夜混合,通过氨基化固定构建生物传感器,随着重金属浓度hg浓度的增加,荧光逐渐恢复。
图8为固定化go传感器对hg2+选择性检测结果;用50nmdna和10μg/mlgo过夜混合,通过氨基化固定构建生物传感器,加入各种重金属,不会引起荧光恢复现象,说明该生物传感器具有很好的选择性。
本实施例中的固定化使得dna和go间结合更加紧密,且由于离心,去除了没有结合上的dna,有效提高了检测的灵敏性。
其中图1为本实施例的流程示意图,图中与hg2+结合的核酸序列是单链结构,当核酸序列与go吸附后,标记的sybrgreeni荧光淬灭,当结合hg2+后,核酸序列形成双链,远离go表面,sybrgreeni发光。
实施例3:
步骤(1)~(4)同实施例1中。
(5)基于go传感器对hg2+进行检测:含10μg/mlgo及50nm核酸序列混合物,加入1*sybrgreeni,静置10min,荧光标记。加入40nm浓度hg2+,20min后对核酸序列上标记的sybrgreeni进行扫描。
图9为固定化go传感器对hg2+检测的实例;图中曲线由上至下依次为dna、dna-go-40nmhg2+、dna-go检测结果曲线。
实施例4:
步骤(1)~(4)同实施例1中。
(5)基于go传感器对hg2+进行检测:含10μg/mlgo及50nm核酸序列混合物,加入1*sybrgreeni,静置10min,荧光标记。加入4μm浓度hg2+,20min后对核酸序列上标记的sybrgreeni进行扫描。
图10为固定化go传感器对hg2+检测的实例;图中曲线由上至下依次为dna、dna-go-4μmhg2+、dna-go检测结果曲线。
sequencelisting
<110>江苏大学
<120>一种基于石墨烯氧化物传感器及其对hg2+检测的方法
<130>一种基于石墨烯氧化物传感器及其对hg2+检测的方法
<160>1
<170>patentinversion3.3
<210>1
<211>24
<212>dna
<213>人工序列
<400>1
tttgcttgttgcgcttcttgcttt24
- 还没有人留言评论。精彩留言会获得点赞!