基于SPR的角蛋白18‑3A9的检测方法与流程
本发明属于角蛋白检测技术领域,具体涉及一种基于spr的角蛋白18-3a9的检测方法。
背景技术:
尽管已有化学法、色谱法、光谱法、免疫法、毛细管电泳法和离子迁移谱法等方法应用到生物样本检测中,但化学法灵敏度低,色谱法、毛细管电泳法和离子迁移谱法前处理过程时间较长,需要专门技术人员和大规模昂贵仪器,光谱法灵敏度低以及对待测样品纯度要求较高,免疫法操作时间过长。目前应用于检测中最广泛的为胶体金试纸,但其以结肠癌易感人群血液为检测对象,且其灵敏度只有300-1000ng/ml。而本技术以其高灵敏度,可实现对结肠癌易感人群的血液中癌症标志物进行检测,从而避免了对客体隐私的侵犯,并大大提高了工作效率。
表面等离子体共振(surfaceplasmonresonance,spr)技术是基于物理光学现象的一种分析技术。当偏振光以共振角入射照在金属和电介质的界面上时,发生全反射,入射光的一部分能量与表面等离子体波发生耦合,引起表面等离子体共振,产生光强急剧减少的反射光。利用光学spr技术测定时,一般是将一种功能反应物(如配体)固定在传感芯片表面金属膜上,当加入待测样品(受体)并使其与传感芯片上的功能反应物相互作用时,引起体系的折射率变化,从而引起spr光学信号的改变。由于spr技术的高识别性、高灵敏性、快速、原位(无需标记)、便捷、实时等优点,spr传感技术现已被广泛应用于生命科学研究、药物筛选、食品分析、环境监测、农业生产等领域。目前,国内外未见将角蛋白18-3a9检测与spr技术结合在一起的报道。
技术实现要素:
本发明的目的是为了解决现有技术的不足,而提供一种基于spr的角蛋白18-3a9的检测方法,该检测方法可实时、快速、高灵敏度的检测角蛋白18-3a9,大大降低结肠癌易感人群检测的漏检率,可应用于结直肠癌的早期筛查,具有一定的临床应用价值。
本发明采用如下技术方案:
基于spr的角蛋白18-3a9的检测方法,包括以下步骤:
步骤一:将spr芯片放置到spr仪器中作为传感芯片,仪器温度设定为20~30℃,spr为表面等离子共振的简称;
步骤二:以10~30μl/min的流速往spr芯片表面通入200~300μledc和nhs的混合液,活化该芯片面的羧基基团,该spr芯片经edc/nhs活化后的羧基基团可以偶联bsa上的氨基;
步骤三:在步骤二活化表面羧基后的spr芯片上以10~30μl/min的流速通入0.5~2mg/mlbsa-methamphetamine溶液,使其偶联到活化过的羧基上,要求目标响应值(ru)达到2000~3000;
步骤四:在步骤三bsa-methamphetamine偶联后的spr芯片上以10~30μl/min的流速通入75~100μl乙醇胺盐酸盐溶液,用以封闭未反应的活化过的羧基位点;
步骤五:在步骤四处理后的spr芯片上以10~30μl/min的流速通入30~50μl梯度浓度的角蛋白18-3a9抗体,确定合适的抗体浓度;
步骤六:将一系列不同浓度的30~50μl的角蛋白18-3a9标准品分别与步骤五确定的浓度抗体混合后,以10~30μl/min的流速依次通入spr芯片,建立标准曲线;其中角蛋白18-3a9抗原与步骤五确定的浓度抗体等体积;
步骤七:将30~50μl的待检测样品与步骤五确定的浓度抗体等体积混合后,以10~30μl/min的流速通入spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量。
更进一步地,步骤一中所述spr芯片是先在玻璃基底上表面镀一层2~3nm厚的铬层,再在铬层上表面镀一层40~50nm厚的金膜;金膜表面生成巯基烷醇后用环氧氯丙烷处理生成环氧基,环氧基共价结合葡聚糖后用溴乙酸处理使葡聚糖羧基化,从而得到羧基化的葡聚糖表面。
更进一步地,步骤二中所述edc和nhs的混合液为edc和nhs的等体积混合溶液,所述edc为n-(3-二甲基氨丙基)-n’-乙基碳二亚胺,浓度为0.2~0.4m;nhs为n-羟基琥珀酰亚胺,浓度为0.1~0.2m。
更进一步地,步骤三中所述bsa-methamphetamine为人工合成的角蛋白18-3a9完全抗原,即在bsa(牛血清白蛋白)表面偶联了methamphetamine(角蛋白18-3a9)分子,可购买获得;ph值为4.5~5.5;
更进一步地,步骤四中所述乙醇胺盐酸盐溶液的浓度为1~2m。
更进一步地,步骤五中所述的角蛋白18-3a9抗体为对bsa-methamphetamine具有特异性识别的鼠源单克隆抗体。
更进一步地,步骤五中每个角蛋白18-3a9抗体反应完成后以10~30μl/min的流速通入naoh溶液,使抗原抗体解离,完成芯片再生后再加入下一个浓度的抗体;所述的氢氧化钠溶液为50~100mm。
更进一步地,在进入步骤六前,可进行多次注射步骤五确定的最合适浓度抗体,验证实验的重复性。
更进一步地,步骤七中的待测样品为血液或唾液。
本发明与现有技术相比,其有益效果为:
(1)本发明所述检测方法操作简便,实时、快速,只需将抗原抗体混合通入芯片,便可实时观测结果;
(2)本发明所述的芯片制备方案成熟,已经商业化,购买方便,并可重复使用上百次,是一种非常经济的检测方法;
(3)本发明检测方法所达到的灵敏度较高,时间较短,是其他任何技术都没法比拟的;
(4)由于胶体金试纸的灵敏度只有300-1000ng/ml,当待检样品含量低于其灵敏度时,胶体金试纸将无法检测,而本发明正好解决了这一问题。
附图说明
图1为不同浓度抗体与spr响应信号间的关系,其中,抗体浓度依次为6.25μg/ml、12.5μg/ml、25μg/ml、50μg/ml、100μg/ml抗角蛋白18-3a9;
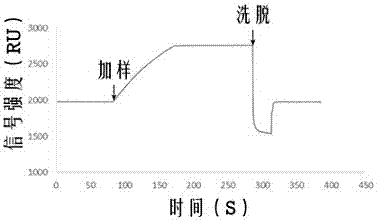
图2为spr芯片的再生示意图,注射氢氧化钠后spr信号骤降,并逐渐恢复至初始基线状态;
图3为分别注射5次恒定浓度抗体的spr响应图;
图4中为角蛋白18-3a9检测的标准曲线。
具体实施方式
下面结合实施例对本发明作进一步的详细描述。
本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。
基于spr的角蛋白18-3a9的检测方法,包括以下步骤:
步骤一:将spr芯片放置到spr仪器中作为传感芯片,仪器温度设定为20~30℃,spr为表面等离子共振的简称;
步骤二:以10~30μl/min的流速往spr芯片表面通入200~300μledc和nhs的混合液,活化该芯片面的羧基基团,该spr芯片经edc/nhs活化后的羧基基团可以偶联bsa上的氨基;
步骤三:在步骤二活化表面羧基后的spr芯片上以10~30μl/min的流速通入0.5~2mg/mlbsa-methamphetamine溶液,使其偶联到活化过的羧基上,要求目标响应值(ru)达到2000~3000;
步骤四:在步骤三bsa-methamphetamine偶联后的spr芯片上以10~30μl/min的流速通入75~100μl乙醇胺盐酸盐溶液,用以封闭未反应的活化过的羧基位点;
步骤五:在步骤四处理后的spr芯片上以10~30μl/min的流速通入30~50μl梯度浓度的角蛋白18-3a9抗体,确定合适的抗体浓度;
步骤六:将一系列不同浓度的30~50μl的角蛋白18-3a9标准品分别与步骤五确定的浓度抗体混合后,以10~30μl/min的流速依次通入spr芯片,建立标准曲线;其中角蛋白18-3a9抗原与步骤五确定的浓度抗体等体积;
步骤七:将30~50μl的待检测样品与步骤五确定的浓度抗体等体积混合后,以10~30μl/min的流速通入spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量。
更进一步地,步骤一中所述spr芯片是先在玻璃基底上表面镀一层2~3nm厚的铬层,再在铬层上表面镀一层40~50nm厚的金膜;金膜表面生成巯基烷醇后用环氧氯丙烷处理生成环氧基,环氧基共价结合葡聚糖后用溴乙酸处理使葡聚糖羧基化,从而得到羧基化的葡聚糖表面。
更进一步地,步骤二中所述edc和nhs的混合液为edc和nhs的等体积混合溶液,所述edc为n-(3-二甲基氨丙基)-n’-乙基碳二亚胺,浓度为0.2~0.4m;nhs为n-羟基琥珀酰亚胺,浓度为0.1~0.2m。
更进一步地,步骤三中所述bsa-methamphetamine为人工合成的角蛋白18-3a9完全抗原,即在bsa(牛血清白蛋白)表面偶联了methamphetamine(角蛋白18-3a9)分子,可购买获得;ph值为4.5~5.5;
更进一步地,步骤四中所述乙醇胺盐酸盐溶液的浓度为1~2m。
更进一步地,步骤五中所述的角蛋白18-3a9抗体为对bsa-methamphetamine具有特异性识别的鼠源单克隆抗体。
更进一步地,步骤五中每个角蛋白18-3a9抗体反应完成后以10~30μl/min的流速通入naoh溶液,使抗原抗体解离,完成芯片再生后再加入下一个浓度的抗体;所述的氢氧化钠溶液为50~100mm。
更进一步地,在进入步骤六前,可进行多次注射步骤(5)确定的最合适浓度抗体,验证实验的重复性。
以下实施例中提到的主要试剂信息见表1;主要仪器与设备信息见表2。
表1
表2
以下实施例所采用的spr芯片为kei公司生产的cm5芯片,该芯片的表面为羧甲基化葡聚糖,易偶联bsa上的氨基;所使用的spr仪器为kei公司生产的esprit;胶体金试纸购自艾博生物医药(杭州)有限公司。
实施例1
(1)打开spr仪器,解锁spr芯片插槽,将spr芯片放置到插槽中,锁上芯片插槽;spr仪器温度设定为25℃;
(2)以20μl/min的流速往在spr芯片表面通入注射250μl的edc和nhs等体积比混合液,活化该芯片表面的羧基基团;其中edc浓度为0.4m,nhs浓度为0.1m;
(3)在活化表面羧基后的spr芯片上以20μl/min的流速通入1mg/ml的ph5.0的bsa-methamphetamine溶液,使其偶联到活化过的羧基上,要求目标响应值(ru)达到3000;
(4)在偶联bsa-methamphetamine的spr芯片上以20μl/min的流速通入100μl的1m的乙醇胺盐酸盐溶液,用以封闭未反应的活化过的羧基位点;
(5)以20μl/min的流速通入40μl的6.25μg/ml,12.5μg/ml,25μg/ml,50μg/ml,100μg/ml梯度浓度的角蛋白18-3a9抗体,结果如图1所示,结果表明6.25μg/ml和12.5μg/ml的抗体浓度下的ru值过小,标曲梯度较窄,降低灵敏度;50μg/ml和100μg/ml的抗体浓度下的ru值较高,但是会耗费掉过多的抗体,不利于成本控制,综合比较下,25μg/ml的抗体浓度最为合适,确定后续测试中的抗体浓度为25μg/ml;
(6)每个样品反应完成后以20μl/min的流速通入10μl50mm的naoh溶液,使抗原抗体解离,完成芯片再生后再加入下一个浓度的抗体,如图2所示,起始基线为1980ru,再生后基线回到1978ru,cv(变异系数)仅为0.07%,表明芯片再生效果较好;
(7)以20μl/min的流速通入25μg/ml的抗体40μl共5次,验证实验的重复性,结果如图3所示;5次重复的ru分别为1039.5ru,1065.0ru,1062.3ru,1047.1ru,1006.2ru,cv仅为2.26%,表明实验的重复性较好;
(8)将一系列不同浓度的40μl的角蛋白18-3a9标准品(125ng/ml、62.5ng/ml、31.25ng/ml、15.63ng/ml、7.81ng/ml、3.91ng/ml、1.95ng/ml、0.98ng/ml、0.49ng/ml、0.24ng/ml、0.12ng/ml、0.06ng/ml、0ng/ml)与25μg/ml抗体等体积依混合后以20μl/min的流速依次通入40μl到spr芯片获取spr响应信号,建立标准曲线,结果如图4所示,在0.06~7.81ng/ml范围内,角蛋白18-3a9的浓度与spr响应信号成线性关系,最低检测浓度在0.06-0.12ng/ml范围,当角蛋白18-3a9浓度超过7.81ng/ml或低于0.06ng/ml时,角蛋白18-3a9的浓度与spr信号不再成线性关系。
(9)待检测人(甲)的基本情况:性别男,年龄31,其血液经胶体金试纸检测结果为角蛋白18-3a9阳性。
将甲的血液12000pm离心10min后,取40μl的样品与等体积的抗体混合后,以20μl/min的流速依次通入30μl到spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量为超出标曲,大于7.18ng/ml。
验证下本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得甲血液中角蛋白18-3a9含量为1042.12ng/ml,与本发明测得的结果一致。
实施例2
(1)打开spr仪器,解锁spr芯片插槽,将spr芯片放置到插槽中,锁上芯片插槽;spr仪器温度设定为25℃;
(2)以约10μl/min的流速往spr芯片表面通入100μl0.2medc和100μl0.1mnhs的混合液,活化该芯片表面的羧基基团;
(3)在步骤(2)活化表面羧基后的spr芯片上以10μl/min的流速通入0.5mg/mlbsa-methamphetamine溶液(ph值为4.5),使其偶联到活化过的羧基上,要求目标响应值(ru)达到约2000;
(4)在步骤(3)bsa-methamphetamine偶联后的spr芯片上以10μl/min的流速通入75μl2m乙醇胺盐酸盐溶液,用以封闭未反应的活化过的羧基位点;
(5)以10μl/min的流速通入30μl的6.25μg/ml,12.5μg/ml,25μg/ml,50μg/ml,100μg/ml梯度浓度的角蛋白18-3a9抗体,结果如图1所示,结果表明6.25μg/ml和12.5μg/ml的抗体浓度下的ru值过小,标曲梯度较窄,降低灵敏度;50μg/ml和100μg/ml的抗体浓度下的ru值较高,但是会耗费掉过多的抗体,不利于成本控制,综合比较下,25μg/ml的抗体浓度最为合适,确定后续测试中的抗体浓度为25μg/ml;
(6)每个样品反应完成后以10μl/min的流速通入10μl50mm的naoh溶液,使抗原抗体解离,完成芯片再生后再加入下一个浓度的抗体,如图2所示,起始基线为1980ru,再生后基线回到1978ru,cv(变异系数)仅为0.07%,表明芯片再生效果较好;
(7)以10μl/min的流速通入25μg/ml的抗体30μl共5次,验证实验的重复性,结果如图3所示;5次重复的ru分别为1039.5ru,1065.0ru,1062.3ru,1047.1ru,1006.2ru,cv仅为2.26%,表明实验的重复性较好;
(8)将一系列不同浓度的30μl的角蛋白18-3a9标准品(125ng/ml、62.5ng/ml、31.25ng/ml、15.63ng/ml、7.81ng/ml、3.91ng/ml、1.95ng/ml、0.98ng/ml、0.49ng/ml、0.24ng/ml、0.12ng/ml、0.06ng/ml、0ng/ml)与25μg/ml抗体等体积依混合后以20μl/min的流速依次通入30μl到spr芯片获取spr响应信号,建立标准曲线,结果如图4所示,在0.06~7.81ng/ml范围内,角蛋白18-3a9的浓度与spr响应信号成线性关系,最低检测浓度在0.06-0.12ng/ml范围,当角蛋白18-3a9浓度超过7.81ng/ml或低于0.06ng/ml时,角蛋白18-3a9的浓度与spr信号不再成线性关系。
(9)待检测人(乙)的基本情况:性别男,年龄43,其血液经胶体金试纸检测结果为角蛋白18-3a9阴性。
将乙的血液12000pm离心10min后,取30μl的样品与步骤(5)确定的浓度抗体等体积混合后,以10μl/min的流速通入30μl到spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量超出标曲,大于7.81ng/ml。
验证下本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得乙血液中角蛋白18-3a9含量为142.47ng/ml,与本发明测得的结果一致。
实施例3
(1)打开spr仪器,解锁spr芯片插槽,将spr芯片放置到插槽中,锁上芯片插槽;spr仪器温度设定为30℃;
(2)以约30μl/min的流速往spr芯片表面通入150μl0.2medc和150μl0.2mnhs的混合液,活化该芯片表面的羧基基团;
(3)在步骤(2)活化表面羧基后的spr芯片上以30μl/min的流速通入2mg/mlbsa-methamphetamine溶液(ph值为5.5),使其偶联到活化过的羧基上,要求目标响应值(ru)达到约3000;
(4)在步骤(3)bsa-methamphetamine偶联后的spr芯片上以30μl/min的流速通入100μl2m乙醇胺盐酸盐溶液,用以封闭未反应的活化过的羧基位点;
(5)以30μl/min的流速通入50μl的6.25μg/ml,12.5μg/ml,25μg/ml,50μg/ml,100μg/ml梯度浓度的角蛋白18-3a9抗体,结果如图1所示,结果表明6.25μg/ml和12.5μg/ml的抗体浓度下的ru值过小,标曲梯度较窄,降低灵敏度;50μg/ml和100μg/ml的抗体浓度下的ru值较高,但是会耗费掉过多的抗体,不利于成本控制,综合比较下,25μg/ml的抗体浓度最为合适,确定后续测试中的抗体浓度为25μg/ml;
(6)每个样品反应完成后以30μl/min的流速通入10μl50mm的naoh溶液,使抗原抗体解离,完成芯片再生后再加入下一个浓度的抗体,如图2所示,起始基线为1980ru,再生后基线回到1978ru,cv(变异系数)仅为0.07%,表明芯片再生效果较好;
(7)以30μl/min的流速通入25μg/ml的抗体50μl共5次,验证实验的重复性,结果如图3所示;5次重复的ru分别为1039.5ru,1065.0ru,1062.3ru,1047.1ru,1006.2ru,cv仅为2.26%,表明实验的重复性较好;
(8)将一系列不同浓度的50μl的角蛋白18-3a9标准品(125ng/ml、62.5ng/ml、31.25ng/ml、15.63ng/ml、7.81ng/ml、3.91ng/ml、1.95ng/ml、0.98ng/ml、0.49ng/ml、0.24ng/ml、0.12ng/ml、0.06ng/ml、0ng/ml)与25μg/ml抗体等体积依混合后以20μl/min的流速依次通入40μl到spr芯片获取spr响应信号,建立标准曲线,结果如图4所示,在0.06~7.81ng/ml范围内,角蛋白18-3a9的浓度与spr响应信号成线性关系,最低检测浓度在0.06-0.12ng/ml范围,当角蛋白18-3a9浓度超过7.81ng/ml或低于0.06ng/ml时,角蛋白18-3a9的浓度与spr信号不再成线性关系。
(9)待检测人(丙)的基本情况:性别男,年龄22,其血液经胶体金试纸检测结果为角蛋白18-3a9阴性。
将乙的血液12000pm离心10min后,取50μl的样品与步骤(5)确定的浓度抗体等体积混合后,以30μl/min的流速通入50μl到spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量为6.11ng/ml。
验证下本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得丙血液中角蛋白18-3a9含量为6.02ng/ml,与本发明测得的结果一致。
实施例4
待检测人(丁)的基本情况:性别男,年龄21,其血液经胶体金试纸检测结果为角蛋白18-3a9阳性。
取40μl丁的血液样品与等体积的抗体混合后,以20μl/min的流速依次通入30μl到spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量为超出标曲,大于7.18ng/ml。
验证下本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得丁血液中角蛋白18-3a9含量为3219.65ng/ml,与本发明测得的结果一致。
实施例5
待检测人(戊)的基本情况:性别男,年龄37,其血液经胶体金试纸检测结果为角蛋白18-3a9阳性。
取30μl戊的血液样品与等体积的抗体混合后,以10μl/min的流速通入30μl到spr芯片,记录响应信号,代入标准曲线,求得血液中角蛋白18-3a9含量超出标曲,大于7.81ng/ml。
验证下本实施例检测结果的真实性:以气相色谱-质谱联用技术(gc/ms)和固相萃取技术(spe)相结合测得戊血液中角蛋白18-3a9含量为2613.72ng/ml,与本发明测得的结果一致。
本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!