一种全氟丁基改性聚乙烯亚胺大分子含氟表面活性剂及其制备与在农药缓释中的应用的制作方法
本发明属于农药缓释技术领域,具体涉及一种全氟丁基改性聚乙烯亚胺大分子含氟表面活性剂及其制备方法与其在农药缓释中的应用。
背景技术:
联合国粮食及农业组织(fao)预测到2050年世界人口将增至98亿,如何保证粮食的可持续供应是一个严峻的问题。然而,由于害虫、疾病和杂草的危害,农作物的产量和质量急剧下滑。比如,全球大约有9000多种昆虫和螨虫,50000多种植物病原体和8000多种杂草,对农作物造成了巨大的损害。因此,为了保护农作物,增加农业生产积极性,农药的使用必不可少。据农业部门报道,如果不使用农药,水果每年减产约78%,蔬菜每年减产约54%,谷类作物每年减产约32%。
按《中国农业百科全书·农药卷》的定义,农药是指用来防治危害农林牧业生产的有害生物(害虫、害螨、线虫、病原菌、杂草及鼠类)和调节植物生长的化学药品。农药的使用主要面临着三个问题(int.j.environ.sci.technol.2016,13,2977-2994):一是农药活性成分水溶解性低造成的生物可利用度低的问题,比如杀虫剂辣椒素在水中的溶解度为60mg/l,鱼藤酮的溶解度只有0.002mg/l;除草剂异丙甲草胺的溶解度为530mg/l,咪鲜胺的溶解度为340mg/l;除草剂莠去津的溶解度为28mg/l。二是选择性差,对非靶标生物具有药害行为,比如除草剂百草枯通过接触可以杀灭非靶标绿色植物;杀虫剂苄氯菊酯也能作用于非靶标节肢动物,如蜘蛛等。三是无控制释放到环境,多数情况下农药的实际使用量大大超过杀灭有害生物所需要的农药剂量,因为其中60~70%的农药活性成分通过渗析、挥发、固定或浸出等方式迁移到环境中,无法到达靶标位点,没有发挥应有的作用,比如除草剂甲草胺和杀虫剂吡虫啉通过增大浓度弥补其因为无控制释放行为的损失。
在当前新农药创制存在投入大、周期长的情况下,高效利用现有优秀农药品种是保障粮食作物安全,实现稳产增收的有效途径。控制释放是农药有效利用的核心科学问题之一,对于发展有效、安全和绿色农药剂型具有重要意义。农药控释体系由农药活性成分和基质材料组成,这些基质材料包括有机溶剂、表面活性剂、乳化剂、粘土、推进剂等,称为农药助剂,可以有效提高农药剂型中活性成分的药效和性能,延长活性成分保质期,保护活性成分不受光照等自然因素而分解。
农药缓释体系中基质材料种类很多,主要分为无机材料和有机材料两大类。无机材料主要分为粘土材料和硅质材料,其中粘土材料主要包括膨润土、高岭石、蒙脱土和海泡石等;硅质材料主要包括玻璃、珍珠岩和沸石等。无机材料的结构多为层状或多孔结构,具有高比表面积、高化学稳定性和高机械性能稳定性,通过吸附或包夹等作用来负载活性农药分子,但这些负载体系存在不容易分散、造成光合作用受阻等缺陷。有机材料主要包括天然高分子材料和生物相容性合成高分子材料。天然高分子材料一般是一些聚合物基质,如纤维素、木质素、壳聚糖、淀粉和环糊精等。生物相容性合成高分子材料一般是由聚合物单体通过聚合反应合成而得到,比如聚乙烯亚胺(pei)、聚乙二醇(peg)、聚氧乙烯-聚氧丙烯-聚氧乙烯(peo-ppo-peo)等,这些合成高分子材料与天然高分子材料一样,具有良好的生物相容性(int.j.environ.sci.technol.2016,13,2977–2994)。但这些高分子材料存在分散性差、对农药分子的包结效率低、以及包结稳定性差等缺点。在亲水性高分子结构中引入疏水链,使之具有两亲性,是提高载药效率和稳定性的有效方法。这类两亲性高分子能够在水溶液中自组装形成以疏水链为内核、亲水基为外壳的聚合物胶束,其疏水内核通过疏水作用包载疏水性农药活性分子,形成载药胶束。常见的疏水链主要是普通c-h链(j.agric.foodchem.2016,64,1447-1483)。近年来,采用含氟成分作为疏水链的两亲性高分子进行医药药物控制释放的文献报道较多(polymer2011,52,4727-4735),这些含氟两亲性高分子材料主要利用了含氟成分的“三高两憎”特性,即高表面活性、高化学稳定性、高热力学稳定性、憎水、憎油,并且易于生成稳定的胶束结构进行载药(prog.polym.sci.2007,32,509–533)。另外,含氟成分化学性质稳定,不与医药药物分子发生化学反应,并且形成一层保护层,避免环境因素破坏活性成分分子结构,维持药物活性。上述报道的这些含氟高分子材料的c-f链长度普遍较长(≥8),长全氟碳链具有生物累积性、生物毒性和环境持久性,已被列入《关于持久性有机污染物的斯德哥尔摩公约》持久性有机污染物(pops)受控名单限制使用(acssustainablechem.eng.2016,4,387-391)。目前,还没有采用含氟两亲性高分子材料作为农药载体的报道。
苯噻菌酯(试验代号y5247)是2005年发现的新型杀菌剂农药品种,为线粒体呼吸链细胞色素bc1复合物抑制剂。该杀菌剂可广泛用于防治蔬菜和瓜果类白粉病、霜霉病、灰霉病、褐斑病、黑星病、玉米小斑病、水稻稻曲病、柑橘地腐病、油菜菌核病等。苯噻菌酯使用的主要剂型是乳油,持效期比较短,而且使用大量的有机溶剂,容易造成环境污染和资源浪费。为了克服此缺点,提高苯噻菌酯的使用效率,有必要研发苯噻菌酯及其杀菌剂组合物的缓释剂型。
技术实现要素:
为了解决现有技术存在的问题,本发明的首要目的在于提供一种可以作为农药缓释剂型载体材料的全氟丁基改性聚乙烯亚胺(pei)大分子含氟表面活性剂。
本发明的另一目的在于提供上述全氟丁基改性pei大分子含氟表面活性剂的制备方法,即以对羟基苯甲醛为起始原料,与全氟丁基磺酰氟进行磺酸酯化得到中间体,中间体再与pei进行还原胺化反应,得到全氟丁基改性pei大分子含氟表面活性剂。
本发明的再一目的在于提供上述全氟丁基改性pei大分子含氟表面活性剂在农药缓蚀中的应用。
本发明的目的通过下述技术方案实现:
一种全氟丁基改性pei大分子含氟表面活性剂,以pei为亲水性骨架、以全氟丁基为疏水基团的大分子含氟表面活性剂,其分子结构如下式所示:
其中,pei为商品化的超支化聚乙烯亚胺大分子,l、m和n表示统计意义上的结构单元数,其伯、仲、叔胺的比例为1:2:1;可以使用的pei分子量在600-10000的范围,优选为分子量1800。
上述全氟丁基改性pei大分子含氟表面活性剂的制备方法,包括如下步骤:
(1)对羟基苯甲醛在缚酸剂存在下,于溶剂中与全氟丁基磺酰氟发生亲核取代反应,得到全氟丁基磺酰氧基苯甲醛中间体。
(2)中间体在还原剂存在下,于溶剂中与pei发生还原胺化反应,得到全氟丁基改性pei大分子含氟表面活性剂。
步骤(1)中:所述的缚酸剂优选为碳酸钾;所述的溶剂优选为乙腈。
步骤(2)中:所述的还原剂优选为硼氢化钠;所述的溶剂优选为甲醇;所述的pei的分子量可以为600-10000,优选为1800;所述的中间体m1的用量优选为pei中伯胺与仲胺总摩尔数的1-10%,更优选为5%。
上述全氟丁基改性pei大分子含氟表面活性剂具有如下特征:最低表面张力为22.6mn/m,临界胶束浓度(cmc)为3.0mg/ml,水合粒径约为80nm左右,tem粒径约为50nm左右,且呈球形胶束均匀分布在水溶液中。基于该特征,上述全氟丁基改性pei大分子含氟表面活性剂能够作为农药缓释剂载体材料,可用于农药缓释领域,制备农药缓释剂型。
一种农药缓释剂型,包含作为载体的上述全氟丁基改性pei大分子含氟表面活性剂和农药活性成分,优选以一种杀菌剂或两种以上的杀菌剂混配得到的杀菌剂组合物作为农药活性成分。将杀菌剂混配可以达到杀灭各种类型有害病菌的目的,通过制备杀菌剂组合物的缓释剂型,将会具有更好的综合杀菌效果。所述的杀菌剂包括苯噻菌酯、苯醚甲环唑、三唑酮、三唑醇、吲唑磺菌胺等。
优选的,载体与农药活性成分的质量比为2.5:1,即全氟丁基改性pei大分子含氟表面活性剂与杀菌剂或杀菌剂组合物的质量比为2.5:1。在该比例下,农药缓释剂型的载药量达27%以上,包封率可达100%。
优选的,所述的农药缓释剂型,包含上述全氟丁基改性pei大分子含氟表面活性剂、苯噻菌酯或由苯噻菌酯和一种或两种以上的其它杀菌剂混配得到的杀菌剂组合物。
上述农药缓释剂型可通过溶剂挥发法来制备,具体可包括如下步骤:分别取适量全氟丁基改性pei大分子含氟表面活性剂和适量农药活性成分用丙酮溶解,得到有机相,搅拌条件下缓慢滴加水,直至有机相变澄清,继续搅拌10-30分钟,除去丙酮,即可得农药缓释剂型溶液。
本发明以生物相容性的聚乙烯亚胺(pei)为基质材料,通过还原胺化反应引入全氟丁基,合成一种全氟丁基改性的pei大分子含氟表面活性剂。全氟丁基链具有疏水疏油特性,通过适当的分子设计,可以与pei连接,得到的全氟丁基改性pei大分子含氟表面活性剂具有表面活性高、临界胶束浓度(cmc)低的特点,并且在亲水性pei的作用下,易形成球形胶束的包结体系,可以适用于农药缓释体系。另外,全氟丁基具有碳氟链短,无生物累积性,不受pops公约限制。本发明通过溶剂挥发法对苯噻菌酯或其杀菌剂组合物进行包载,形成载药胶束,优化胶束形貌、粒径大小、稳定性、缓释性能,得到苯噻菌酯缓释剂型及其杀菌剂组合物缓释剂型。生物活性测试表明,这些剂型具有优良的使用效果。
本发明相对于现有技术具有如下优点和效果:
本发明的全氟丁基改性pei大分子含氟表面活性剂不含有持久有机污染物特征的全氟辛基类基团,具有优异的表面活性,其最低表面张力可达22mn/m左右,临界胶束浓度(cmc)值在3mg/ml左右。与商品化的全氟辛基磺酸钠(最小表面张力22mn/m,cmc值为8.5×10-3mol/l)(j.phys.chem.c2008,112,16850)、十二烷基磺酸钠(最小表面张力34mn/m,cmc值为8.7×10-3mol/l)(j.colloidinterf.sci.2012,370,102)等相比,具有显著的优势。并且本发明地合成路线短,产率高,原料廉价易得,具有很高地工业应用价值。
本发明的全氟丁基改性pei大分子含氟表面活性剂具有较好的水溶性,直接溶解于水中便可自组装形成球形胶束,粒径大小约为50nm左右,具有较好的胶束形成能力,适用于农药剂型中的载体材料。
本发明的全氟丁基改性pei大分子含氟表面活性剂溶解于水溶液中,可通过溶剂挥发法包载苯噻菌酯及其组合物,形成球形载药胶束,粒径在200nm左右,且在极稀溶液中也能稳定存在,并且对苯噻菌酯及其组合物具有一定增溶作用,提高并长时间维持苯噻菌酯及其组合物的药效,具有一定的缓释效果,能够大大降低其对斑马鱼的毒性。苯噻菌酯及其组合物载药胶束剂型的制备方法简单有效,具有很高的实用价值。
附图说明
图1是全氟丁基改性pei大分子含氟表面活性剂的结构图。
图2是中间体m1以及全氟丁基改性pei大分子含氟表面活性剂的合成路线图。
图3是全氟丁基改性pei大分子含氟表面活性剂1hnmr(a)和19fnmr(b)谱图。
图4是全氟丁基改性pei大分子含氟表面活性剂表面张力随浓度变化图。
图5是全氟丁基改性pei大分子含氟表面活性剂粒径随浓度变化图(a)和tem图(b)。
图6是全氟丁基改性pei大分子含氟表面活性剂胶束载药示意图。
图7是载药胶束红外谱图。
图8是苯噻菌酯原药标准浓度曲线(a)和苯噻菌酯载药最佳质量比(b)结果图。
图9是载药胶束粒径及稀释稳定性dls图(a)和载药胶束tem图(b)。
图10是载药胶束体外释放累积释放率结果图。
图11第七天对柑橘炭疽病病菌抑制效果图,a-d分别为空白对照、原药苯噻菌酯、载药胶束、载体材料的抑制效果图。
图12第五天对水稻纹枯病病菌抑制效果图,a-d分别为空白对照、原药苯噻菌酯、载药胶束、载体材料的抑制效果图。
图13是载药胶束对柑橘炭疽病抑制率(a)和水稻纹枯病抑制率(b)结果图。
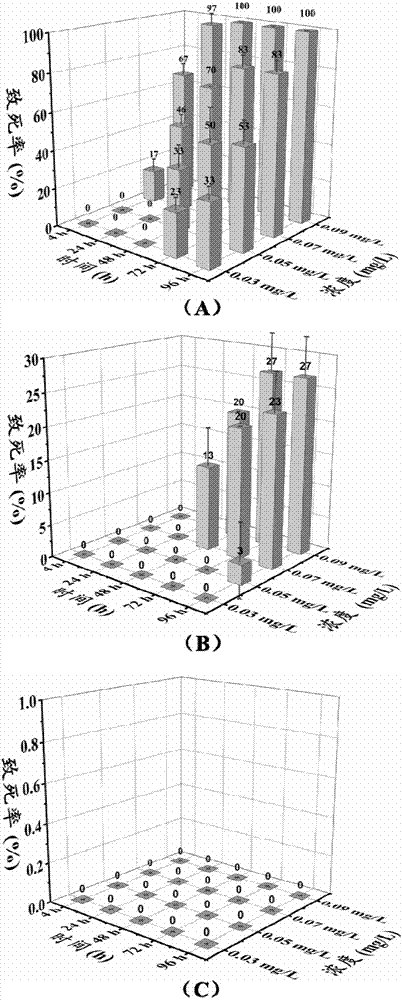
图14是鱼毒活性测试结果图,a-c分别为原药苯噻菌酯、载药胶束及载体的测试结果图。
具体实施方式
下面结合实施例及附图对本发明做进一步详细的描述,但本发明的实施方式不限于此。
实施例1中间体(m1)的制备
合成路线如图2所示,在干燥的250ml烧瓶中加入12.2g(0.1mol)对羟基苯甲醛,用150ml乙腈溶解,搅拌下加入缚酸剂碳酸钾27.6g(0.2mol),回流半小时,然后缓慢滴加含氟前体原料全氟丁基磺酰氟36.2g(0.12mol),tlc监测反应终点。向反应液中加入100ml乙酸乙酯,用饱和氯化钠溶液洗3次,有机层用无水硫酸钠干燥并低温结晶,过滤得到白色固体中间体全氟丁基磺酰氧基苯甲醛(m1),39.2g,收率为97%。
1hnmr(600mhz,dmso):δ10.08(s,1h,-cho),8.13(d,j=8.0hz,2h,phh),7.75(d,j=8.0hz,2h,phh);
19fnmr(376mhz,dmso):δ-82.01(3f),-112.34(2f),-121.84(2f),-126.76(2f);
ms(ei):404.09(m+)(计算值:404.20)。
实施例2全氟丁基改性pei大分子含氟表面活性剂的制备
合成路线如图2所示,在干燥的250ml烧瓶中加入8g(0.02mol,下述pei中伯胺与仲胺总摩尔数的5%)全氟丁基磺酰氧基苯甲醛(m1)、100ml无水甲醇,再加入22.6gpei(m.w.1800),室温下搅拌2h,然后分批加入硼氢化钠0.75g(0.02mol),继续反应10min,tlc监测反应终点。反应完成后脱溶,加入丙酮重新溶解,有白色固体杂质析出,过滤得滤液,滤液用正己烷反复沉淀,得到黄色油状产物,标记为全氟丁基改性pei大分子含氟表面活性剂c4f-pei-b,产率为92%。通过1hnmr中中间体苯环上质子峰积分面积和pei中亚甲基上质子峰及分面积之比计算全氟丁基链在pei上的取代度,为1.38%,通过19fnmr确定其结构,谱图如图3所示。
通过改变全氟丁基磺酰氧基苯甲醛(m1)的用量(使m1用量为pei中伯胺与仲胺总摩尔数的1-10%),采用相同的合成方法,可以得到不同全氟丁基链取代的全氟丁基改性pei大分子含氟表面活性剂。
实施例3全氟丁基改性pei大分子含氟表面活性剂表面张力和临界胶束浓度(cmc)的测试
取一定量的上述c4f-pei-b,用蒸馏水分别配成以下浓度梯度(单位:mg/ml)的溶液:0.1、0.5、0.7、0.9、1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0、12.0,用oca20接触角测量仪在25℃进行表面张力的测定(悬滴法),其最低表面张力为22.6mn/m,临界胶束浓度(cmc)为3.0mg/ml,测试结果图如图4所示。
实施例4全氟丁基改性pei大分子含氟表面活性剂粒径测试
取一定量的上述c4f-pei-b,用蒸馏水分别配成以下浓度梯度(单位:mg/ml)的溶液:0.1、0.5、0.7、0.9、1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0、11.0、12.0,采用粒度仪动态光散射(dls,zen3690,英国)测量每个浓度下的粒径大小,结果如图5(a)所示。从图5(a)可以看出,在浓度为3mg/l左右开始出现单峰,粒径发生明显变化,粒径变得均一,平均水合粒径在80nm左右,开始形成胶束,临界胶束浓度在3mg/l左右,与表面张力测定的结论(图4)一致。另外,在大于临界胶束浓度3mg/l的情况下均呈现单峰,说明形成的胶束在大于cmc的浓度下具有很好的稳定性。当浓度为6mg/l时,通过场发射高分辨透射电子显微镜(tem)(jem-2100f,日本)可以观察到胶束呈球形,分散均匀,胶束粒径约为50nm,如图5(b)所示。
实施例5溶剂挥发法制备苯噻菌酯载药胶束
胶束载药示意图如图6所示,称取3g全氟丁基改性pei大分子含氟表面活性剂(c4f-pei-b)和1g苯噻菌酯(y5247),分别溶于10ml丙酮中,将两者混合得到有机相。搅拌下向有机相中滴加蒸馏水约20ml,继续搅拌10分钟,得到澄清混合溶液;将混合溶液旋转蒸发脱溶除去丙酮,加蒸馏水定容至30ml;经微孔膜过滤除掉未包载的苯噻菌酯,得到载药胶束溶液。载药胶束溶液经冷冻干燥后,进行红外测试,确认载药情况,红外谱图如图7所示。载药后的红外谱图出现原药(y5247)的特有羰基吸收峰(1750cm-1)和载体材料(c4f-pei-b)特有氨基吸收峰(3300cm-1),说明苯噻菌酯成功地被全氟丁基改性pei大分子含氟表面活性剂胶束包载。
实施例6载药量和包封率的优化
取苯噻菌酯原药用乙腈配制1-10mmol/l系列浓度梯度,通过高效液相色谱绘制苯噻菌酯标准浓度曲线,如图8(a)所示,线性方程为y=881.72x-431.54,相关系数r2为0.999。以质量比分别为载体材料(c4f-pei-b):原药(y5247)=5.0:1、3.3:1、2.5:1、2.0:1制备载药胶束溶液,通过标准曲线确定载药胶束溶液中原药质量,计算不同比例下载药量及包封率,确定最佳比例,结果如图8(b)所示。从图8(b)看出,当质量比为2.5:1时,载药量和包封率达到最优,分别为27%、100%。
实施例7载药胶束粒径测试及稀释稳定性测试
以最佳质量比2.5:1制备的载药胶束定容至2mg/ml,采用dls和tem测量载药胶束粒径,如图9(a)和图9(b)所示。dls显示载药胶束平均粒径为250nm左右,tem显示在载药胶束粒径在200nm左右,同样因为tem测量的是干燥之后的载药胶束粒径,低于dls所测水合粒径。同时,将载药胶束浓度依次稀释10倍(0.2mg/ml)、20倍(0.1mg/ml)、40倍(0.05mg/ml)、100倍(0.02mg/ml),其粒径大小保持不变,只有一个单峰,说明载药胶束在极稀溶液中也能稳定存在,具有很好的稳定性。
实施例8载药胶束体外释放实验
参照文献方法(colloidssurfbbiointerfaces85(2011)86–91)测试。取实施例6优化制备的载药胶束溶液5ml(包载原药质量折算2.7mg),放入截留分子量为1000的透析袋中;以2.7mg苯噻菌酯原药作为空白对照,用乙腈溶解,放入截留分子量为1000的透析袋中;以体积为200ml的30%的乙醇溶液为释放介质,将透析袋置入,室温搅拌,分别取样分析释放情况。前12个小时取样间隔2小时,之后取样间隔5小时。每次取样2ml,并补充相同体积的新鲜30%乙醇介质溶液。取样通过hplc确定释放出的苯噻菌酯含量,绘制累积释放曲线,如图10所示。苯噻菌酯原药在10小时左右累计释放率达到50%,在15小时左右累计释放率趋于平缓,达到平衡;载药胶束也在15小时左右释放趋于平缓,累计释放率不足40%,相比原药空白对照,具有明显缓释作用。
实施例9载药胶束杀菌活性测试
以原药苯噻菌酯(y5247)的浓度15ppm为基准,取含有等量原药成分的载药胶束(y5247-loaded)溶液,以及等量载体材料(c4f-pei-b)作为对照,采用琼脂平板培养法,通过测量琼脂培养基上菌落直径,计算得到载药胶束对柑橘炭疽病和水稻纹枯病病菌的杀菌活性,杀菌效果如图11和图12所示,计算结果如图13所示。从这些图可以看出,载药胶束对柑橘炭疽病和水稻纹枯病病菌的抑制率高于原药苯噻菌酯,是因为载药胶束对苯噻菌酯具有一定的缓释作用,能够长时间维持苯噻菌酯的药效。载药胶束对于柑橘炭疽病病菌,6天后抑制率趋于平缓,维持在45%左右;而原药苯噻菌酯随着时间的增长的抑制率下降,7天后抑制率低于30%;对于水稻纹枯病病菌,载药胶束4天后抑制率趋于平缓,维持在47%左右,原药苯噻菌酯随着时间的增长的抑制率呈直线下降,5天后抑制率降为32%。载体材料本身对柑橘炭疽病病菌的抑制率很低(不超过10%),对水稻纹枯病病菌的抑制率为0。
实施例10载药胶束鱼毒活性测试
配制苯噻菌酯(y5247)原药的浓度分别为:0.03mg/l、0.05mg/l、0.07mg/l、0.09mg/l,同时配制含有等量原药成分的载药胶束(y5247-loaded)溶液和含有等量载体材料(c4f-pei-b)的溶液,按照国家标准gb/t13267-91测试对斑马鱼的急性毒性。实验结果如图14所示。在时间为96小时、浓度为0.05mg/l时,苯噻菌酯对斑马鱼的致死率达到53%(文献报道:斑马鱼的急性毒性试验ld50(96小时):0.043mg/l,属于剧毒型),在高浓度0.09mg/l下,对斑马鱼的致死率为100%。载药胶束在96小时,浓度为0.05mg/l时,对斑马鱼的致死率为3%,可大大降低苯噻菌酯原药对斑马鱼的毒性,在高浓度0.09mg/l下,对斑马鱼的致死率不超过30%,载体材料对斑马鱼没有毒性,可见载体材料(c4f-pei-b)形成的胶束对苯噻菌酯进行包载,形成载药胶束之后可以大幅度降低苯噻菌酯对鱼的毒性。
实施例11苯噻菌酯组合物载药胶束杀菌活性测试
以苯噻菌酯与苯醚甲环唑按照质量比1:1混合得到其组合物,以相同的方法用c4f-pei-b制备组合物的载药胶束。以组合物总浓度15ppm为基准,取含有等质量组合物的载药胶束溶液为测试样,以及含等量载体材料(c4f-pei-b)的溶液作为空白对照,采用琼脂平板培养法,测试载药胶束对柑橘炭疽病和水稻纹枯病病菌的杀菌活性。实验结果表明,苯噻菌酯组合物载药胶束同样对柑橘炭疽病和水稻纹枯病病菌有优良的抑制效果。载药胶束对于柑橘炭疽病病菌,6天后抑制率趋于平缓,维持在65%左右;而组合物随着时间的增长抑制率下降,7天后抑制率低于30%。对于水稻纹枯病病菌,载药胶束4天后抑制率趋于平缓,维持在58%左右;组合物随着时间的增长抑制率也呈直线下降,5天后抑制率降为32%。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!