一种吡唑醚菌酯农药微乳液制剂及制备方法与流程
本发明属于农药制剂领域,具体涉及一种环境友好型的吡唑醚菌酯的农药微乳液及其制备方法。
背景技术:
传统农药剂型以乳油和可湿性粉剂为主,其中约一半是乳油,产品中的大量甲苯、二甲苯等芳香烃有机溶剂易造成环境污染和资源浪费。随着人们对环境安全愈加重视,对农药的安全性也提出了更为严格的要求。因此,开发高效、低毒、低残留、对环境友好的农药新剂型,以水相部分或全部代替乳油中有机溶剂的水基性制剂便成了国内外农药新剂型研究的热点。
微乳液是由油(o)、水(w)、表面活性剂(s)和助表面活性剂(cs)组成的有序多元体系,具有较大的界面面积,超低界面张力,热力学稳定等性质。具有油包水(w/o)、双连续(b.c.)、水包油(o/w)等丰富的微观结构。微乳剂以水作为分散介质,不用或仅用少量有机溶剂,在表面活性剂的作用下,将油溶性原药以超微细状态(粒径0.01-0.1μm)均匀分散于水中,形成热力学稳定的透明均体系,属于纳米级技术范畴的绿色剂型。并具其增溶能力强、传递效率高,能促进向动植物组织内部的渗透,可以提高农药的药效,有效的减少农药污染问题,因此微乳液作为农药的载体具有重要的研究意义,为农药的发展提供了新的途径。
tween-20,化学名为聚氧乙烯失水山梨醇单月桂酸酯,是山梨醇及其一失水、双失水化合物与月桂酸酯按每摩尔山梨醇及其脱水化合物与约20摩尔的环氧乙烷在碱性条件下缩合而制得。
tween-80,化学名为聚氧乙烯失水山梨醇单油酸酯,为淡黄色至橙黄色的粘稠液体。由于其结构中具有较长的碳链结构,对亲脂性药物有较好的助溶作用,在制备难溶性药物制剂时,常用作助溶剂、乳化剂和稳定剂等。分子式为c24h44o6(c2h4o)n。生产上用山梨醇及其它的失水、双失水化合物的单油酸酯与约20摩尔的环氧乙烷在碱性条件下缩合而制得。
吡唑醚菌酯为新型广谱杀菌剂。线粒体呼吸抑制剂.具有保护、治疗、叶片渗透传导作用。纯品为白色至浅米色无味结晶体。溶解度(20℃,g/100ml):水(蒸馏水)中溶解度为0.00019,乙酸乙酯中≥65,为一种油溶性农药。
技术实现要素:
为了解决以上技术问题,本申请利用低毒物质tween-20、tween-80,异丙醇,乙酸乙酯等构筑微乳液,来包载农药吡唑醚菌酯,微乳液载体对农药吡唑醚菌酯的载药能力及农药微乳液的稳定性进行了研究,并提供了一种具有均匀粒径、良好稳定性的吡唑醚菌酯微乳液制剂。
本领域公知,微乳液是一种溶胀的胶团。当表面活性剂在水中的浓度大于临界胶束浓度,两亲性分子自发组装形成胶团,当油相比例与胶束属于一定范围内时,在一定的可能下,油相溶剂分子填充至胶束之间,自发组装成为胶团,并且根据溶剂分子之间排列关系的不同,其稳定性也存在一定的差异。
本申请研究筛选得到了一种微乳液系统,采用tween-80或tween-20为表面活性剂,异丙醇为助表面活性剂,乙酸乙酯为油相,实验证明上述试剂在一定比例能够形成微乳液区域,微乳液被称之为“溶胀的胶束”,可用于提高疏水性分子溶解度,具有良好的应用价值。
为了实现以上技术目的,本发明提供以下技术方案:
本发明第一方面,提供一种微乳液系统,该微乳液系统包括表面活性剂、异丙醇、乙酸乙酯及水;其中,表面活性剂为吐温-80或吐温-20,异丙醇为助表面活性剂,乙酸乙酯为油相,水为水相。
优选的,上述微乳液系统中表面活性剂,异丙醇,乙酸乙酯和水的质量分数为0-10%,0-20%,0-20%和60%-100%,其中表面活性剂、异丙醇、乙酸乙酯的质量分数不为0%。
优选的,所述水为二次蒸馏水。
本发明第二方面,提供上述微乳液系统在药物制剂领域的应用。
优选的,所述药物制剂为农药制剂。
优选的,所述在药物制剂领域的应用为作为药物载体的应用。
本发明第三方面,提供一种吡唑醚菌酯微乳液制剂,该吡唑醚菌酯微乳液制剂以上述微乳液系统为载体。
本申请提供的微乳液系统,其原料试剂均为环境友好型的有机试剂,应用于作物及土壤中,对环境的危害性大大降低。另外,本研究发现上述试剂组成的微乳系统具有良好的粒径及稳定性,适应长期放置及高温、寒冷环境。
优选的,上述吡唑醚菌酯微乳液制剂中,吡唑醚菌酯的载药量为0.2%~0.5%,所述表面活性剂与助表面活性剂共同构成辅助相,其中表面活性剂与助表面活性剂的质量比为1:2。农药微乳液不同于人体使用的药物微乳液,农药在使用过程中需要加水稀释后使用,其剂型研发更加侧重乳剂的稳定性,并且要求具有良好的贮存性能。微乳剂性质相对稳定,可以以任何比例对水稀释,其应用于农药制剂效果良好。
微乳液的稳定性,与胶束的分布状态相关,与油相分子与胶束的插接状态也有关,除溶剂系统之外,药物与溶剂系统的配合也会影响药剂的稳定性。当外界温度升高,溶液中分子活跃度增加,分子引力关系改变,有可能会影响胶束或胶团的组装情况;温度降低时,溶剂分子固化析出,其稳定性有可能被破坏。当溶剂系统中各分子处于一定比例状态时,胶团结合紧密甚至复配之后改善了胶团整体的熔点,足以对抗外界温度变化,得到一种能对抗高温及寒冷环境的微乳液系统。介于农药微乳液的应用形式,能够获得具有良好稳定性微乳液具有不可预见性,且对于农药制剂具有重要的意义。
优选的,上述吡唑醚菌酯微乳液中,表面活性剂为tween-80,吡唑醚菌酯载药量为0.5%,油相与辅助相的质量比为9:1。
当载药量为0.5%时,上述试剂配比条件下制备的微乳,离心状态下不分层,平均粒径可达到19.93nm,载药能力良好,并且具有良好的放置稳定性及热贮稳定性。
优选的,上述吡唑醚菌酯微乳液中,表面活性剂为tween-80,吡唑醚菌酯载药量为0.2%,油相与辅助相的质量比为6:4或7:3或8:2或9:1。
经筛选证明,该试剂配比下的吡唑醚菌酯能够形成稳定性良好的微乳,平均粒径分别为34.58nm、18.56nm、19.38nm、30.44nm,长时间放置后粒径基本不发生变化。
进一步优选的,油相与辅助相的质量比为9:1或7:3或8:2。
冷贮实验结果表明,上述三种配比下的微乳剂具有更为优良的冷贮稳定性。
优选的,上述吡唑醚菌酯微乳液中,表面活性剂为tween-20,吡唑醚菌酯载药量为0.2%,油相与辅助相的质量比为7:3或8:2或9:1。
通过观察微乳状态,上述配比下的吡唑醚菌酯能够形成澄清透明的微乳状态,平均粒径为27.73nm、16.23nm、20.17nm,复合生物制剂的要求。
进一步优选的,油相与辅助相的质量比为9:1或8:2。冷贮存实验结果表明,该配比下的吡唑醚菌酯微乳液具有更优良的冷贮稳定性。
更进一步的,油相与辅助相的质量比为9:1。载药量考察表明,当油相与辅助相质量比为9:1时,具有更好的载药效果。
本发明第四方面,提供一种吡唑醚菌酯微乳液的制备方法,根据表1,准确称取各物质于小烧杯中,将该混合物充分搅拌,混匀,利用离心机将混合液中气泡离去,静置保存。
本发明第五方面,提供上述吡唑醚菌酯微乳液作为农药杀菌剂的应用。
本发明的有益效果
1.本申请提供了一种吡唑醚菌酯微乳液,以tween-80或tween-20为表面活性剂,异丙醇为助表面活性剂,乙酸乙酯为油相,蒸馏水为水相。本申请中提供的吡唑醚菌酯微乳液采用环境友好型试剂作为原料,应用于农作物及土壤中,可以大大降低危害性。
2.本申请提供的吡唑醚菌酯微乳液,平均粒径均在100nm以下,外观澄清透明,具有良好的放置稳定性及高温、低温贮存稳定性,适应多种气候及多种运输、储存条件,应用于工业生产,具有良好的技术效果。
附图说明
构成本申请的一部分的说明书附图用来提供对本申请的进一步理解,本申请的示意性实施例及其说明用于解释本申请,并不构成对本申请的不当限定。
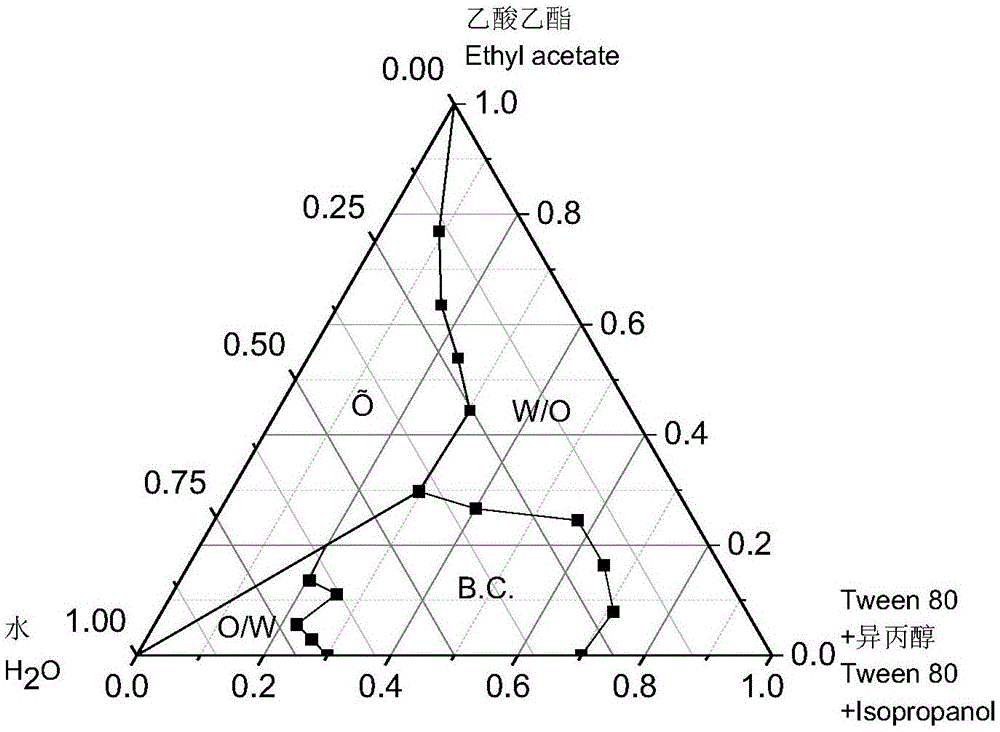
图1为tween-80/异丙醇/乙酸乙酯/水拟三元体系相图;
其中,水浴温度为25℃,me为微乳区,ⅱ为多相区,o/w为水包油型微乳液,b.c.为双连续型微乳液,w/o为油包水型微乳液。
图2为tween-20/异丙醇/乙酸乙酯/水拟三元体系相图;
其中,水浴温度为25℃,me为微乳区,ⅱ为多相区,o/w为水包油型微乳液,b.c.为双连续型微乳液,w/o为油包水型微乳液。
图3为tween-80/异丙醇/乙酸乙酯/水体系微乳电导率随水的质量分数变化关系图;
其中,水浴温度为25℃。
图4为tween-20/异丙醇/乙酸乙酯/水体系微乳电导率随盐水的质量分数变化关系图;
其中,水浴温度为25℃。
具体实施方式
应该指出,以下详细说明都是例示性的,旨在对本申请提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本申请所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本申请的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”和/或“包括”时,其指明存在特征、步骤、操作、器件、组件和/或它们的组合。
正如背景技术所介绍的,传统农药剂型中含有大量甲苯、二甲苯等芳香烃有机溶剂,造成环境污染和资源浪费。本申请提供了一种吡唑醚菌酯的微乳液制剂,采用tween-20、tween-80,异丙醇,乙酸乙酯作为制剂制备原料,对环境更加友好,并且本申请研究得到吡唑醚菌酯微乳剂具有良好的药剂学性质,应用于农作物疾病防治,具有重要的实用意义。
为了使得本领域技术人员能够更加清楚地了解本申请的技术方案,以下将结合具体的实施例与对比例详细说明本申请的技术方案。
实施例1
吡唑醚菌酯载药量为0.5%,表面活性剂为tween-80时:称取吡唑醚菌酯0.0249g、乙酸乙酯0.0999g、吐温-800.3742、异丙醇0.75g,水3.75g于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径具有良好的高温稳定性第
实施例2
吡唑醚菌酯载药量为0.2%,tween-80与乙酸乙酯的体积比为6:4时:称取吡唑醚菌酯0.0262g、乙酸乙酯0.4746g、吐温-800.2488、异丙醇0.5001g,水3.7393g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为30.44nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例4
吡唑醚菌酯载药量为0.2%,tween-80与乙酸乙酯的体积比为7:3时:称取吡唑醚菌酯0.0093g、乙酸乙酯0.3637g、吐温-800.2925、异丙醇0.5822g,水3.7524g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为19.38nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例5
吡唑醚菌酯载药量为0.2%,tween-80与乙酸乙酯的体积比为8:2时:称取吡唑醚菌酯0.0112g、乙酸乙酯0.2400g、吐温-800.3310、异丙醇0.6664g,水3.7479g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为18.56nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例6
吡唑醚菌酯载药量为0.2%,tween-20与乙酸乙酯的体积比为7:3时:称取吡唑醚菌酯0.0093g、乙酸乙酯0.3645g、吐温-200.2902、异丙醇0.5840g,水3.7512g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为82.72nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例7
吡唑醚菌酯载药量为0.2%,tween-20与乙酸乙酯的体积比为8:2时:称取吡唑醚菌酯0.0106g、乙酸乙酯0.2483g、吐温-200.3319、异丙醇0.6730g,水3.7551g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为85.09nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例8
吡唑醚菌酯载药量为0.2%,tween-20与乙酸乙酯的体积比为9:1时:称取吡唑醚菌酯0.0109g、乙酸乙酯0.1171g、吐温-200.3748、异丙醇0.7511g,水3.7618g,于具塞比色管中,充分搅拌混匀制成吡唑醚菌酯微乳液,该条件下制备的微乳液澄清透明,平均粒径为33.39nm,具备良好的载药能力及高温、低温贮存稳定性。
实施例9
本实施对微乳液载体及农药吡唑醚菌酯的载药能力及农药微乳液的稳定性进行了研究。
1.实验部分
1.1试剂
tween-80(化学纯,国药集团化学试剂);tween-20(化学纯,国药集团化学试剂);异丙醇(分析纯,国药集团化学试剂);乙酸乙酯(分析纯,国药集团化学试剂);二次蒸馏水;吡唑醚菌酯原药(纯度95.6%)
1.2拟三元相图的绘制
研究选取的表面活性剂(s)为tween-80、tween-20,助表面活性剂(cs)为异丙醇,油相(o)为乙酸乙酯,水相(w)为二次蒸馏水,构建拟三元体系相图。tween-80/异丙醇/乙酸乙酯/水拟三元相图的绘制:采用本实验室前期工作方法—水稀释法。将tween-80与异丙醇按w(tween-80):w(异丙醇)=1:2组成的体系视为一个组分,准确称量总量约0.5g不同比例s和o[s/o(w/w)]分别为10:0,9:1,8:2,7:3,6:4,5:5,4:6,3:7,2:8,1:9,0:10,置于15ml具塞比色管,磁力搅拌5min使s和o混合均匀,放置于25.0±0.1℃的恒温水浴中搅拌5~10min,至体系的状态不随时间变化。之后,采用水稀释法向上述拟二组分体系中滴加第3个组分,边滴加边搅拌,观察并记录发生相变时水的质量分数。通过目测观察体系的相转变点,初步确定相界限。在相转变点附近的样品置于恒温槽中24h,确定体系达到平衡后,再根据物相的状态初步确定相界限,结果如图1所示。tween-20/异丙醇/乙酸乙酯/水拟三元相图的绘制同上,结果如图2所示。
1.3微乳相结构的研究
1.3.1电导率法
在体系相图中,测定微乳区表面活性剂与油为一定比例时不同水相浓度下的电导率。s/o(w/w)分别为10:0,9:1,8:2,7:3,6:4。恒定实验温度为25.0±0.1℃。电导率仪参数为0.995。做出电导率随水相浓度的变化曲线,并按照曲线斜率划分为w/o型微乳区、o/w型微乳区和b.c.型微乳区。
1.3.2粒径的测定
采用动态光散射法测定z-averagesize,该结果是基于动态光散射(dynamiclightscattering,dls)测量得到的光强分布(intensitypsd)粒径。将准备好的待测样品置于清洁的石英比色皿中,25℃条件下测定微乳液的粒径。判断是否形成稳定的微乳液,粒径在1-100nm之间。在o/w型微乳区选点,总质量固定5g的条件下,配置表面活性剂、油与水不同比例的微乳液,使用粒径仪测定o/w型微乳液的粒径,3次测量取平均值,测定粒径的微乳样品的配方见表2-3。
表1o/w型微乳理论成分表
表2tween-80/异丙醇/乙酸乙酯/水体系o/w型微乳组分表
表3tween-20/异丙醇/乙酸乙酯/水体系o/w型微乳组分表
1.4微乳液作为农药吡唑醚菌酯载体的研究
1.4.1吡唑醚菌酯o/w型微乳的制备
将吡唑醚菌酯溶于乙酸乙酯中,作为油相。在微乳体系水包油(o/w)区域选点并配制微乳,置于25℃下待用,配方见表5-6。
表4载药微乳理论成分表
表5tween-80/异丙醇/乙酸乙酯/水体系o/w型载药微乳样品组分表
表6tween-20/异丙醇/乙酸乙酯/水体系o/w型载药微乳样品组分表
1.4.2吡唑醚菌酯o/w型微乳液粒径的测定
采用动态光散射法测定。将准备好的待测样品置于清洁的10mm石英比色皿中,25℃条件下测定微乳液的粒径。判断是否形成稳定的微乳液,粒径在1-100nm之间。
测试包载了不同质量分数吡唑醚菌酯o/w型微乳液的粒径。本实验选取2个质量分数:0.2%,0.5%。配方见表5-6。测试每种质量分数的吡唑醚菌酯o/w型微乳液的粒径,探究吡唑醚菌酯的加载对微乳液粒径的影响,分析不同结构的表面活性剂构筑的微乳载体的载药能力。
1.4.3吡唑醚菌酯o/w型微乳液稳定性的测定
测试包载了不同质量分数吡唑醚菌酯和不同s/o比例的o/w型农药微乳液的稳定性。在微乳体系o/w型微乳区域选点并配制微乳,配方见表5-6,延用2.3.1中配制的微乳。首先,将配制好的微乳液编号,采用离心机离心,转速为2000r/min离心30分钟,观察微乳是否分层、是否透明。之后,将载药微乳液置于常温下密闭保存观察7天,观察微乳液是否分层、是否透明,并测量对比微乳液前后粒径。若微乳液不分层、透明则农药微乳液稳定。
1.4.4温度、水质对吡唑醚菌酯o/w型微乳液稳定性的影响
研究温度对吡唑醚菌酯o/w型微乳液稳定性的影响。将载药微乳分别置于-2-10℃的冰箱和55℃的高温水浴中各12h,观察微乳液是否分层、是否透明,并测量对比前后微乳液的粒径。若微乳液不分层、透明则农药微乳液稳定。若微乳液粒径未发生较大变动,说明农药微乳液稳定。载药微乳配方见表4。
研究不同水质对吡唑醚菌酯o/w型微乳液稳定性的影响。分别用二次蒸馏水、去离子水和自来水配制载药微乳液,载药微乳配方见表4。观察微乳液是否分层、是否透明,并测量对比三种微乳液的粒径。若微乳液不分层、透明则农药微乳液稳定。若三种微乳液粒径皆处于1-100nm之间,且与二次蒸馏水配制的农药微乳液差别不大,说明水质对农药微乳液的稳定性影响不大。
通过对tween-20/异丙醇/乙酸乙酯/水体系和tween-80/异丙醇/乙酸乙酯/水体系的拟三元相图的对比发现:
相同点:微乳结构在较小含水量下形成w/o型微乳,在中等含水量时转变为b.c.型微乳,在高含水量时转变为o/w型微乳。
不同点:tween-20/异丙醇/乙酸乙酯/水拟三元体系相图中总微乳区较大,即tween-20较tween-80更易形成微乳。tween-20相图中双连续型微乳区和w/o型微乳区较大,tween-80相图中o/w型微乳区较大,tween-80更易形成o/w型微乳液。
2.2微乳相结构转变
2.2.1微乳结构与电导率
在水稀释法电导率(用κ表示)曲线(25℃)中,根据微乳电导率曲线斜率的不同,可以将整个微乳单相区划分为w/o区,双连续区和o/w区。由图1-2可以发现:微乳区可大致分区为水质量分数<20%时,体系为w/o型微乳;水质量分数>75%时,体系为o/w型微乳;水质量分数处于20%~75%范围内时为微乳的过渡区,即双连续区。电导率曲线分区点即微乳相结构转变点见表7(按水的质量分数划分)。
表7水稀释法电导率曲线分区点(水的质量分数w%)
注:w%(1)为w/o型微乳区与b.c.微乳区的分界点;w%(2)为b.c.微乳区与o/w型微乳区的分解点。
2.2.2微乳结构与粒径
所配制的样品的粒径处于1-100nm之间,符合微乳液的粒径要求,所以配制的样品是o/w型微乳液。不同表面活性剂与油相比例微乳液的粒径数据见表8。
表8不同表面活性剂与油相比例的微乳液的粒径(水的质量分数为75%)
2.3吡唑醚菌酯o/w型微乳剂配制及稳定性的研究
2.3.1载药微乳的外观
tween-80/异丙醇/乙酸乙酯/水体系与tween-20/异丙醇/乙酸乙酯/水构建的o/w型微乳液包载质量分数为0.2%的农药吡唑醚菌酯后,仍然是澄清透明的体系,说明包载0.2%的农药,易形成农药o/w型微乳液;微乳液包载质量分数为0.5%的农药吡唑醚菌酯后,体系易变为浑浊,且离心后分层,说明包载吡唑醚菌酯过量,o/w型微乳结构被农药吡唑醚菌酯破坏,不易形成微乳剂。若包载相同含量的吡唑醚菌酯,对比两个体系可以发现,tween-80/异丙醇/乙酸乙酯/水体系构建的o/w型微乳液不易变浑浊,其微乳结构更稳定,载药能力更强。微乳载体包载农药吡唑醚菌酯后的外观见表9-10。
表9tween-80/异丙醇/乙酸乙酯/水体系载药微乳的外观
表10.tween-20/异丙醇/乙酸乙酯/水体系载药微乳的状态
2.3.2载药微乳的粒径
吡唑醚菌酯溶解度(20℃,g/100ml):水(蒸馏水)0.00019,tween-80与tween-20构建的o/w型微乳载体对农药吡唑醚菌酯都具有增溶作用。从o/w型微乳载体的载药能力方面,相同条件下,tween-80构建的o/w型微乳液的载药能力优于tween-20,tweeen20构建的微乳液包载农药后粒径较大,微乳结构易被破坏。包载农药吡唑醚菌酯的微乳载体的粒径及载药能力分析见表11-12.
表11tween-80/异丙醇/乙酸乙酯/水/吡唑醚菌酯载药微乳粒径及载药能力分析
表12tween-20/异丙醇/乙酸乙酯/水/吡唑醚菌酯载药微乳粒径及载药能力分析
2.3.3载药微乳的稳定性
tween-20/异丙醇/乙酸乙酯/水体系与tween-80/异丙醇/乙酸乙酯/水体系构建的包载农药吡唑醚菌酯的o/w型微乳液稳定性皆较好。将包载农药的微乳液采用高速离心机离心后,均未分层,保持澄清透明。在常温下放置7天后,载药微乳皆未出现分层现象,吡唑醚菌酯未析出,农药微乳澄清透明,微乳粒径变化不大。说明由tween-20和tween-80构建的o/w型微乳载体包载农药吡唑醚菌酯后农药微乳液稳定性皆较好,符合农药制剂的常规要求,具体检测结果见表13-14。但tween-80构建的微乳载体能够包载质量分数为0.5%的吡唑醚菌酯,载药微乳液稳定性较好,且在表面活性剂比例较小时,tween-80构建的载药微乳稳定性好,由此可得,tween-80/异丙醇/乙酸乙酯/水体系构建的载药微乳的稳定性优于tween-20。
表13.载药微乳体系的稳定性
表14.载药微乳体系放置7d前后粒径数据对比
2.3.4吡唑醚菌酯o/w型微乳的冷贮、热贮稳定性分析
包载质量分数0.5%的吡唑醚菌酯o/w型微乳液在冷贮12h后,出现析出药品的现象,吡唑醚菌酯析出,静置一段时间,吡唑醚菌酯会沉淀于具塞比色管底部,说明吡唑醚菌酯质量分数为0.5%的载药微乳冷贮稳定性差,不适用于低温环境。在tween-80构建的载药微乳体系中,包载质量分数0.2%的农药微乳液在s/o(w/w)为6:4时,在冷贮12h后,出现浑浊现象,在tween-20构建的载药微乳体系中,包载质量分数0.2%的农药微乳液在s/o(w/w)为7:3时,在冷贮12h后,出现浑浊现象,说明在冷贮条件下,农药微乳剂的微乳结构被破坏,其冷贮稳定性较差。而其余s/o(w/w)比例的载药微乳冷贮稳定性较好。吡唑醚菌酯o/w型微乳冷贮后微乳外观见表15.
表15冷贮后吡唑醚菌酯o/w型微乳的外观
包载质量分数0.5%、0.2%的吡唑醚菌酯o/w型微乳液在热贮12h后,仍保持澄清透明,说明吡唑醚菌酯o/w型微乳热贮稳定性好,适用于高温环境。吡唑醚菌酯o/w型微乳热贮前后微乳外观及粒径数据见表16.
表16热贮后吡唑醚菌酯o/w型微乳外观
2.3.5水质对吡唑醚菌酯o/w型微乳稳定性的影响
研究不同水质对吡唑醚菌酯o/w型微乳液稳定性的影响。分别用二次蒸馏水、去离子水和自来水配制载药微乳液。由tween-80与tween-20构建的包载质量分数0.2%吡唑醚菌酯的微乳液,在s/o为6:4时,采用去离子水的载药体系呈现浑浊状态,不能形成o/w型微乳液。而由自来水配制的载药体系皆为澄清透明,可以构建吡唑醚菌酯o/w型微乳液。不同水质构建的o/w型载药微乳的外观及粒径数据见表17,表18.
表17.去离子水构建的载药体系的外观及粒径数据
表18自来水构建的载药体系的外观及粒径数据
2.3.6结果与讨论:
tween-80/异丙醇/乙酸乙酯/水体系构建的o/w型微乳液可以包载质量分数为0.5%的吡唑醚菌酯,热贮稳定性好,不同水质对微乳液稳定性影响小,但载药微乳的冷贮稳定性差,低温下会析出农药,不适用于低温环境。包载质量分数为0.2%的吡唑醚菌酯时,当s/o(w/w)为9:1,8:2,7:3时,载药微乳冷贮、热贮稳定性好,水质影响小,载药微乳应用范围广;当s/o(w/w)为6:4时,载药体系初始状态为浑浊体系,放置12h后,体系变为澄清透明,形成o/w型微乳液,但该载药微乳冷贮稳定性差,受水质影响大,应用范围较小。
tween-20/异丙醇/乙酸乙酯/水/体系构建的o/w型微乳液不能包载质量分数为0.5%的吡唑醚菌酯,不能构建吡唑醚菌酯o/w型微乳液。包载质量分数为0.2%的吡唑醚菌酯时,s/o(w/w)为7:3时,载药微乳冷贮稳定性差,但微乳液稳定性受水质影响小;s/o(w/w)为9:1,8:2时,载药微乳冷贮、热贮稳定性好,微乳稳定性受水质影响小。
tween-80/异丙醇/乙酸乙酯/水体系构建的o/w型微乳液的载药能力优于tween-20,且载药微乳稳定性优于tween-20。
以上所述仅为本申请的优选实施例而已,并不用于限制本申请,对于本领域的技术人员来说,本申请可以有各种更改和变化。凡在本申请的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本申请的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!