一种MRS造影剂及其制备方法和应用与流程
本发明属于医用造影剂技术领域,具体涉及一种新的MRS造影剂及其制备方法和应用。
背景技术:
现有技术公开了MRS成像即磁共振波谱成像技术,是目前唯一能无创性观察活体组织代谢及生化变化的技术。其原理是在相同的磁场环境下,处于不同化学环境中的同一种原子核,由于受到原子核周围不同电子云的磁屏蔽作用,而具有不同的共振频率。有关波谱分析就是利用化学位移研究分子结构,其优势在于:由于代谢异常通常早于结构变化,MRS可以检测到常规MR不能检测到的异常,其敏感性更高。然而,传统的MRS成像技术利用体内内源性代谢物进行诊断疾病,无法可靠地鉴别某些特殊病变,如无法可靠地鉴别脑胶质瘤及脑内其他肿瘤如淋巴瘤等,甚至一些非肿瘤性肿块如脱髓鞘斑块等。鉴于此,本申请的发明人拟采用引入外源性造影剂进行MRS增强显像,具体涉及提供一种MRS造影剂及其制备方法和应用,而至目前为止,业内尚无MRS造影剂概念的提出。
技术实现要素:
本发明的目的在于,针对现有临床实践的需求,提供一种MRS造影剂及其制备方法和应用。本发明合成的简单结构的纳米颗粒,能实现高效能MRS增强显像。
本发明提供了一种新型磁共振波谱(MRS)成像造影剂。
具体的,本发明提供了一种新型医用MRS造影剂,其中的探针材料为ALA担载的HMSNs纳米颗粒;较佳地,所述探针材料的纳米颗粒尺寸为50-300nm。
本发明基于:(1)HMSNs表面易修饰,生物安全性好,载药量高,(2)β-ALA是肝脏生成的一种非蛋白源性氨基酸,转运到肌肉组织中形成肌肽且中枢神经系统不存在β-ALA,且MRS波谱存在特异峰于2.562ppm及3.177ppm,(3)Angiopep-2(ANG)有助于纳米颗粒穿过血脑屏障并靶向脑胶质瘤,将ALA担载入ANG修饰的HMSNs中,形成AMSNs,制成MRS造影剂,尤其是脑胶质瘤特异性MRS造影剂。
本发明中,所述造影剂适用于MRS造影成像。
本发明中MRS造影剂概念的提出,将打破目前常规MRS成像技术发展的禁锢,对临床影像诊断技术的发展和应用具有重要意义,可线束提高脑胶质瘤影像学诊断的信心。
本发明所述的MRS造影剂的概念不仅适用于脑胶质瘤,同样也适用于其他疾病如乳腺癌等。
本发明进一步提供了上述MRS造影剂的制备方法,其包括:首先制备合成空心介孔氧化硅纳米颗粒(Hollow Mesoporous Silica Nanoparticles,HMSNs),然后再在其表面修饰Angiopep-2(ANG)以使得纳米颗粒能够更好地通过血脑屏障,继而将β-丙氨酸(ALA)担载入HMSNs的空腔及孔道内,形成AMSNs(Alanine Loaded Hollow Mesoporous Silica Nanoparticles)。
本发明上述MRS造影剂的制备方法,包括下述步骤:
1)将ANG-HMSNs纳米颗粒分散于PBS或去离子水中,并加入ALA的PBS或去离子水溶液,得到第一混合液;
2)常温下搅拌步骤1)制备的第一混合液24~72h;
3)分离步骤2)溶液中所含ALA担载的HMSNs纳米颗粒。
本发明中,所述步骤1)中使用的ANG-HMSNs纳米颗粒通过下述方法制备:
a)将NH2-HMSNs纳米颗粒、EDC、NHS及ANG配成第二混合液中,搅拌24-72h;
b)离心收集步骤a)的第二混合液,并将其分散至水中,得到ANG-HMSNs。
本发明的步骤1)中,ALA与ANG-HMSNs的质量比为1∶(1-200);
本发明所述的步骤a)中,NH2-HMSNs纳米颗粒、EDC、NHS及ANG的质量比为(10~100)∶(10~100)∶(10~130)∶1。
本发明对所制得的HMSNs纳米颗粒进行了性能测试,获得分散于去离子水中的透射结果,和制得的HMSNs纳米颗粒的粒径分布;制得的HMSNs纳米颗粒的N2吸附试验,制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的数码照片及水溶液的DLS水和动力学直径图和zeta电位图以及FT-IR图,和不同浓度游离ALA的MRS谱线图及所得的ALA标准曲线,ALA药物释放曲线,和制得的AMSNs纳米颗粒瘤内注入大鼠皮下脑胶质瘤模型的MRS谱线图,及注射后脑胶质瘤的生物电镜图及能谱图,制得ANG-HMSNs及AMSNs纳米颗粒分别与BCEC及C6细胞共培养24小时后的细胞毒性评价图,制得的ANG-HMSNs及AMSNs纳米颗粒与C6细胞共培养后的MRS谱线图,制得的ANG-HMSNs纳米颗粒连接FITC后与C6细胞共培养2小时后共聚焦所观察到的细胞吞噬纳米颗粒的情况以及实验鼠注射入所制得的AMSNs纳米颗粒后的体重变化情况结果图和心、肝、脾、肺、肾、脑等各器官的组织切片图,结果表明,本发明所述的AMSNs纳米颗粒可用于MRS增强成像,进一步制备MRS造影剂,所述的MRS造影剂,造影效果优异,且无毒副作用,可成功实现皮下脑胶质瘤及原位脑胶质瘤的MRS增强显像,生物相容性好,对于医学疾病的诊断具有重要价值和意义。
本发明的优点有:
HMSNs安全性好,表面易于修饰,其大空腔结构使其能够担载更多的成像介质;ALA具有特征性MRS谱线,于2.562ppm及3.177ppm处存在两个峰,其中2.562ppm处的峰不受脑内其他物质峰的影响,为AMSNs的特征峰;
所述的合成的MRS造影剂的制备方法,制备工艺简易,成像效果优异,灵敏度高,生物相容性好,对临床影像诊断技术的发展和应用具有重要意义。
附图说明
图1为实施例1制得的HMSNs纳米颗粒分散于去离子水中的透射电镜(TEM)照片。
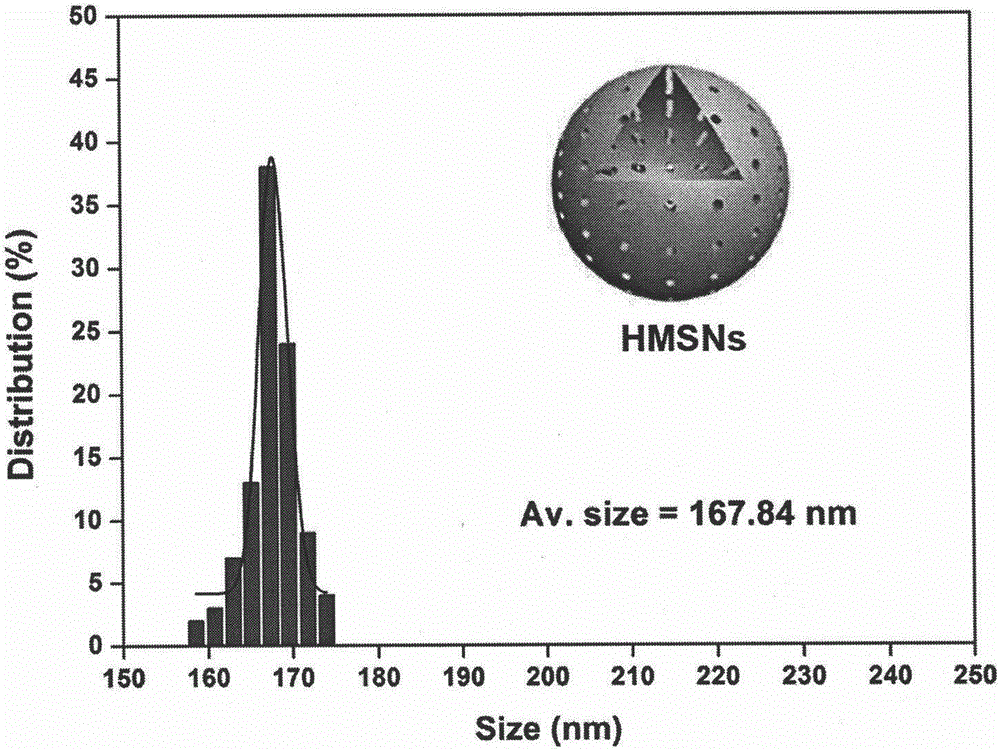
图2为实施例1制得的HMSNs纳米颗粒的粒径分布图。
图3为明实施例1制得的HMSNs纳米颗粒的N2吸附试验结果。
图4为实施例1制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的数码照片。
图5为实施例1制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的DLS水和动力学直径图。
图6为实施例1制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的zeta电位图。
图7为实施例1制得的HMSNs、ANG-HMSNs及AMSNs纳米颗粒的FT-IR图。
图8为实施例1不同浓度游离ALA的MRS谱线图及所得的ALA标准曲线。
图9为实施例1制得的AMSNs纳米颗粒的ALA药物释放曲线。
图10为实施例1制得的AMSNs纳米颗粒瘤内注入大鼠皮下脑胶质瘤模型的MRS谱线图。
图11为实施例1制得的AMSNs纳米颗粒静脉注射入大鼠原位脑胶质瘤模型的MRS谱线图及注射后脑胶质瘤的生物电镜图及能谱图。
图12为实施例1制得ANG-HMSNs及AMSNs纳米颗粒分别与BCEC及C6细胞共培养24小时后的细胞毒性评价图。
图13为实施例1制得的ANG-HMSNs及AMSNs纳米颗粒与C6细胞共培养后的MRS谱线图。
图14为实施例1制得的ANG-HMSNs纳米颗粒连接FITC后与C6细胞共培养2小时后共聚焦所观察到的细胞吞噬纳米颗粒的情况。
图15为昆明鼠注射入所制得的AMSNs纳米颗粒后的体重变化情况结果图。
图16为昆明鼠注射入所制得的AMSNs纳米颗粒后,心、肝、脾、肺、肾、脑等各器官的组织切片图。
具体实施方式
以下结合附图和下述实施方式进一步说明本发明,应理解,附图及下述实施方式仅用于说明本发明,而非限制本发明。本领域的技术人员根据本发明的上述内容作出的一些非本质的改进和调整均属于本发明的保护范围。另外,下述工艺参数中的具体配比、时间、温度等也仅是示例性,本领域技术人员可以在上述限定的范围内选择合适的值。
实施例1
将100mg实心SiO2颗粒超声分散到20mL去离子水中,备用;将100mg C16TAB,30mL去离子水,30mL乙醇及0.55mL氨水预先配成混合溶液,向其中滴加实心SiO2的水溶液,搅拌0.5h。随后,迅速向其中加入0.25mL TEOS,继续搅拌6h;产物通过离心收集后,分散到Na2CO3的水溶液中(0.848gNa2CO3+20mL水),并在50℃水浴条件下搅拌10h以刻蚀掉中间的实心SiO2层,得到HMSNs;产物离心收集后,用大量的去离子水及酒精反复洗涤,分散到盐酸的乙醇溶液中(50mL盐酸+500mL乙醇)78℃回流12h,回流重复4次,最后回流结束后用大量的去离子水及酒精反复洗涤,离心收集材料分散至水中,即得HMSNs水溶液;取50mg HMSNs分散至50mL乙醇中,再加入100μLAPTES于80℃回流4小时,产物用离心收集即得NH2-HMSNs。取NH2-HMSNs 10mg,EDC 37mg,NHS 48mg,ANG 10mg,分散在20mL去离子水中,常温搅拌24h,即获得ANG-HMSNs;取上述ANG-HMSNs 50mg,加入50mM ALA水溶液中,常温下搅拌48h,离心收集材料,即得AMSNs。图1显示了所制得的HMSNs纳米颗粒分散于去离子水中的透射电镜(TEM)照片,表明HMSNs的成功合成,粒径分布均一且具有良好的单分散性;图2显示了所制得的HMSNs纳米颗粒的粒径分布图,所合成的HMSNs纳米颗粒粒径约168nm;图3显示了所制得的HMSNs纳米颗粒的N2吸附试验结果,所合成的HMSNs比表面为880m2/g,孔径为4.2nm,孔容为1.16cm2/g;图4显示了制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的数码照片,均未见明显沉淀,分散性良好;图5显示了制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的DLS水和动力学直径图,证实NH2-HMSNs及ANG-HMSNs纳米颗粒成功制备;图6显示了制得的HMSNs、NH2-HMSNs及ANG-HMSNs纳米颗粒水溶液的zeta电位图,证实NH2-HMSNs及ANG-HMSNs纳米颗粒成功制备;图7显示了制得的HMSNs、ANG-HMSNs及AMSNs纳米颗粒的FT-IR图,证实ANG-HMSNs纳米颗粒的成功制备;图8显示了不同浓度游离ALA的MRS谱线图及所得的ALA标准曲线;图9显示了制得的AMSNs纳米颗粒的ALA药物释放曲线,表明AMSNs纳米颗粒药物释放量较少。
实施例2 医用成像应用效果实验
1、MRS成像
1.1实验材料及仪器:
采用实施例1制得的AMSNs纳米颗粒;
MRS成像检测仪器型号:7.0T小动物磁共振成像系统Agilent Technologies Inc,U.S.A.
1.2实验动物:雄性Sprague-Dawley大鼠皮下胶质瘤模型及原位脑胶质瘤模型,平均年龄2个月,平均体重200g,购自上海斯莱克实验动物公司;
1.3实验方法:SD大鼠用水合氯醛进行腹腔麻醉后,采用实施例1制得的AMSNs水溶液10mg/mL,40mg/kg通过瘤内注射至皮下脑胶质瘤内,尾静脉注射至原位脑胶质瘤模型鼠内,行MRS成像,并在不同的时间点观察感兴趣区波谱变化情况;
实验结果显示:制得的AMSNs纳米颗粒瘤内注入大鼠皮下脑胶质瘤模型的MRS谱线图,可见打药后胶质瘤区域MRS显著的AMSNs峰出现,在2.562ppm及3.177ppm,表明AMSMs可用于体内MRS成像(如图10所示),图11显示了制得的AMSNs纳米颗粒静脉注射入大鼠原位脑胶质瘤模型的MRS谱线图及注射后脑胶质瘤的生物电镜图及能谱图,显示注药后正常脑区域未见明显的AMSNs峰,而胶质瘤区域可见到AMSNs峰于2.562ppm(用药前胶质瘤区域的波谱2.562ppm位置没有峰),表明AMSNs可穿透血脑屏障靶向胶质瘤,可用作脑内原位胶质瘤的特异性MRS造影剂。
实施例3 毒性评价实验
1.体外细胞毒性实验
1.1实验材料:采用实施例1所制得的ANG-HMSNs及AMSNs纳米颗粒;
1.2实验方法:采用MTT(3-(4,5-dimethylthiazol-2-y1)-2,5-diphenyltetrazolium bromide)方法评价细胞存活率,具体实验方法为:(1)接种细胞:用含10%胎小牛血清得培养液配成单个细胞悬液,以每孔105-106个细胞接种到96孔板,每孔体积100微升(2)培养细胞:加入纳米颗粒后与细胞共培养24小时后,每孔加MTT溶液(5mg/ml,用PBS配制,pH=7.4)50微升,继续共培养4h,小心吸弃孔内培养上清液,对于悬浮细胞需要离心后再吸弃孔内培养上清液。(3)定量:每孔加150微升DMSO,脱色摇床振荡10min,使结晶物充分融解,选择570nm波长,在酶联免疫监测仪上测定各孔光吸收值,记录结果;
实验结果显示:制得ANG-HMSNs及AMSNs纳米颗粒在1000μg/mL的较高浓度下,共培养24小时后细胞仍有高达85%以上的存活率;表明ANG-HMSNs及AMSNs纳米颗粒的低细胞毒性(如图12所示);MRS谱线图表明仅有AMSNs与细胞共培养后才可表现出特征峰(如图13所示);细胞吞噬纳米颗粒的结果表明AMSNs可被C6细胞吞噬(如图14所示);
2.体内组织毒性实验
2.1实验材料采用实施例1制得的AMSNs纳米颗粒;
2.2实验动物:昆明小鼠,平均体重20g,5~6周龄,购自复旦大学医学院动物房;
2.2.3实验方法:尾静脉注射AMSNs纳米颗粒水溶液(剂量为40mg/kg);尾静脉注射所述AMSNs纳米颗粒的生理盐水溶液(剂量为40mg/kg),通过常规的H&E染色观察注射前、注射30天后的组织切片;并记录小鼠体重变化情况;
图15显示了昆明鼠注射入所制得的AMSNs纳米颗粒后的体重变化情况结果图;图16显示了昆明鼠注射入所制得的AMSNs纳米颗粒后,心、肝、脾、肺、肾、脑等各器官的组织切片图,实验结果表明:昆明鼠在注射nCAs前后,心肝脾肺肾和脑各器官均无明显毒性反应,表明该材料在活体水平的低毒性。
- 还没有人留言评论。精彩留言会获得点赞!