达巴万星在制备治疗艾滋病的药物中的应用的制作方法
本发明属于药物技术领域,具体涉及化合物达巴万星(Dalbavancin)在制备治疗艾滋病的药物中的应用。
技术背景
艾滋病,是一种由人类免疫缺陷病毒(Human Immunodeficiency Virus,HIV)感染引起的一种严重传染病。作为一种可以直接破坏人体免疫系统的慢性传染病,艾滋病已经成为世界上严重威胁人类健康的疾病之一。联合国艾滋病规划署(UNAIDS)的数据显示,截至2011年年末,全球共有3420万人感染了HIV。目前我国艾滋病流行正处于快速增长期,感染人数逾78万(UNAIDS,2011)。因此,对HIV/AIDS的防治已成为不容忽视的社会问题和重大科研课题。研发新型的抗HIV药物是治疗和防控艾滋病的主要途径。20世纪90年代以来,随着人类对病毒及其感染过程的分子生物学研究的不断深入,以及药物研发技术的不断创新,抗病毒药物有了突飞猛进的发展,尤其是抗HIV的药物。许多大型国际制药公司,如辉瑞、默克、葛兰素史克、罗氏、雅培、百时美施贵宝等,投入大量资源用于抗HIV的药物研发。其中,部分公司已经拥有多种抗HIV药物,并借此获得丰厚的收益和回报。自1987年第一个治疗HIV感染的药物齐多夫定(zidovudine,AZT)被美国FDA批准上市以来,截止2013年已有33种抗HIV病毒的化学实体药物被美国FDA批准上市,其中包括18种逆转录酶抑制剂,11种蛋白酶抑制剂,2种整合酶抑制剂,1种CCR5协同受体拮抗剂和1种膜融合抑制剂(USFDA,2013)。这些不断涌现出来的抗HIV新药能够有效地抑制人体内HIV病毒的复制,减缓艾滋病发展进程,大大提高了艾滋病人的平均存活时间。但是,由于这些药物主要靶向逆转录酶、蛋白酶、Gp41和整合酶等有限的几个病毒蛋白,病毒通过频繁变异极易适应和逃避药物施加的选择压力。随着这些药物的广泛使用,很容易产生交叉耐药性及严重的毒副作用,使其临床应用受到很大限制。而且目前使用的抗HIV感染药物还存在其他种种弊病,诸如价格昂贵、使用不方便、毒性高,服药繁琐、不能清除体内病毒等。综合以上原因,开发新药势在必行,需要不断地创制出新的、高效的、价廉的抗HIV药物。
药物重定位(Drug Repositioning)是快速发现抗癌药物的优选策略。药物重定位,也称为旧药新用,是指利用相关的技术方法对已有的药物进行重新筛选、组合或改造从而发现其未知新用途的过程。相比于从零开始的新药研发,药物重定位基于已有药物的重新开发能够节省大量前期研发投入(如药靶发现、化合物筛选、安全性测试等)。因此,系统地发掘和评价所有上市药物的抗HIV潜力对于新颖抗HIV药物发现和药物重定位用于艾滋病治疗具有重要意义和重大价值。但是通过实验来筛选所有的上市药物是一个艰难的、花费昂贵而又耗时的过程。
因此本发明利用新开发的预测化合物抗HIV活性的方法发现并验证达巴万星具有抗HIV活性,可在制备治疗艾滋病的药物中进行应用。目前,现有技术中未见有快速准确地预测和发现已有药物具有抗HIV活性的方法的报道,也未见有化合物达巴万星具有抗HIV活性的报道。
技术实现要素:
本发明的目的在于开辟达巴万星(Dalbavancin)药物的新用途,提供达巴万星(Dalbavancin)在制备治疗艾滋病的药物中的应用。
为了实现本发明的上述目的,本发明提供了如下的技术方案:
达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其中达巴万星具有显著的抗HIV活性且细胞毒性较低。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其中所述达巴万星对细胞的毒性很小,CC50>200μM;在浓度等于EC50时,达巴万星对细胞C8166完全没有毒性。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其中达巴万星对HIV-1诱导C8166细胞形成合胞体的抑制作用的EC50为8.694μM,治疗指数TI大于23.0;在HIV-1p24抗原定量结果显示达巴万星抑制p24抗原作用的EC50为1.296μM,治疗指数TI大于135.1。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其特征在于所述药物中有效成分达巴万星及其药学上可接受的盐占0.5-90%。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其中检测达巴万星及其药学上可接受的盐抗HIV活性是选用人T淋巴细胞系C8166和HIV-1实验株HIV-1NL4-3对达巴万星进行体外的细胞毒性和抗HIV活性实验,其中细胞毒性使用MTT比色法检测,抗HIV活性利用合胞体抑制试验和HIV-1p24抗原定量两者方法进行检测。
如所述的达巴万星及其药学上可接受的盐在制备治疗艾滋病药物中的应用,其中所述的达巴万星的药学上可接受的盐是指与有机酸形成的盐,所述的有机酸为酒石酸、甲酸、乙酸、乙二酸、丁酸、马来酸、琥珀酸、己二酸、藻酸、柠檬酸、天冬氨酸、苯磺酸、樟脑酸、樟脑磺酸、二葡糖酸、环戊烷丙酸、十二烷基硫酸、乙磺酸、葡庚糖酸、甘油磷酸、庚酸、己酸、延胡索酸、2‐羟基乙磺酸、乳酸、甲磺酸、烟酸、2‐萘磺酸、扑酸、果胶酯酸、3‐苯基丙酸、新戊酸、丙酸、对‐甲苯磺酸和十一烷酸。
达巴万星作为药物时,可直接使用,或者以药物组合物的形式使用。该药物组合物中含有0.1-99%的达巴万星化合物,优选为0.5-90%的有效成分达巴万星,其余为药物学和药剂学上可接受的,对人和动物无毒的药用辅料或载体。
所述的药用载体为一种或多种固体、半固体和/或液体稀释剂,填料以及药物制品辅料。本发明的药物组合物以单位体重服用量的形式使用。本发明的药物可经注射(肌注和静注)和口服两种形式给药。
与现有技术相比,本发明优益性在于:
为了预测和找出具有抗HIV活性的药物化合物,本发明首次采用如下的技术来进行操作。目前还没有只利用化合物的结构就可以直接预测化合物抗HIV活性的方法。本发明通过利用大量的抗HIV活性数据并整合相对频率权重的分子指纹方法以及机器学习方法(向量机和随机森林)来实现对化合物的抗HIV活性的预测。该技术只需要输入化合物的结构就可以快速而准确的预测出该化合物是否具有抗HIV活性。利用该技术我们发现达巴万星具有显著的抗HIV活性且细胞毒性较低,可以在制备治疗艾滋病的药物中应用。达巴万星目前是用于制备治疗由革兰氏阳性菌导致的急性细菌性皮肤和皮肤结构感染的药物。因此,现有技术中还未有任何下述机理和方法的记载:
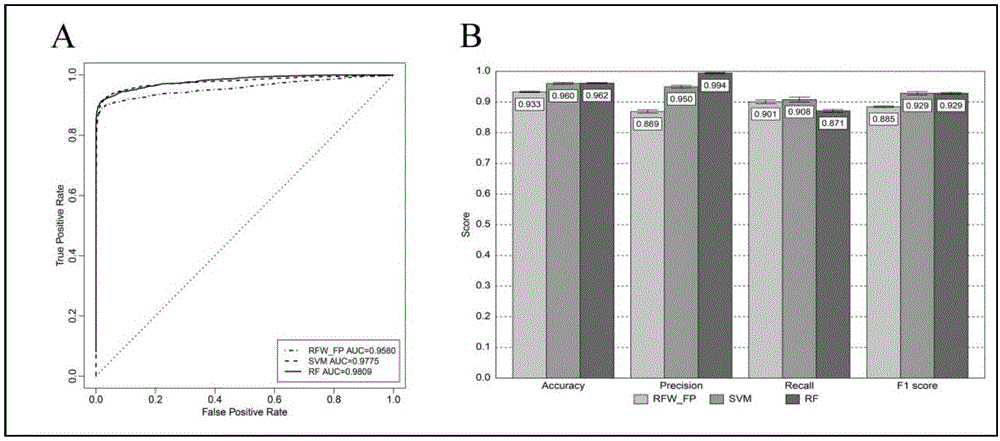
本发明利用首先建立了一个称为“Anti-HIV-Predictor”的抗HIV化合物预测和发掘平台(http://bsb.kiz.ac.cn/Anti-HIV-Predictor)。该平台的建立过程见图1。该平台整合3种方法(相对频率权重的分子指纹方法、支持向量机方法和随机森林方法)来预测化合物的抗HIV活性。该平台的ROC曲线线下面积大于0.95并且准确率超过93%(图2)。因此该平台可以快速准确地预测指定化合物是否具有抗HIV活性。本发明利用该平对已经上市的1835个药物进行预测和筛选,以便对这些药物进行药物重定位用于抗HIV治疗。本发明预测出来若干新的抗HIV化合物,这些化合物到目前为止都没做过任何的抗HIV活性实验。因此,本发明对这些化合物进行了一系列的体外抗HIV活性实验。实验结果发现化合物达巴万星(Dalbavancin)具有显著的抗HIV活性且细胞毒性较低。因此达巴万星对艾滋病具有很高的治疗指数。达巴万星是一种新型半合成糖肽抗生素,其作用机制与万古霉素相同,是抑制G+菌细胞壁的生物合成。达巴万星被批准用于治疗由革兰氏阳性菌(包括耐甲氧西林金黄色葡萄球菌)导致的急性细菌性皮肤和皮肤结构感染。因此,本发明开辟了达巴万星的新的用途即作为制备治疗艾滋病药物的应用。
达巴万星(Dalbavancin)对HIV-1NL4-3病毒株的抗HIV活性实验结果显示了不同浓度的达巴万星对HIV-1NL4-3病毒株的抑制作用。达巴万星对HIV-1诱导C8166细胞形成合胞体的抑制作用的EC50为8.694μM,治疗指数TI大于23.0。在HIV-1p24抗原定量结果显示达巴万星抑制p24抗原作用的EC50为1.296μM,治疗指数TI大于135.1。以上实验结果表明达巴万星的细胞毒性较小或无,具有显著的抗HIV活性和较高的治疗指数,可作为制备治疗艾滋病药物的应用。
附图说明
图1显示:抗HIV化合物预测和发掘平台“Anti-HIV-Predictor”的建立过程和在药物重定位中的应用;
图2显示:抗HIV化合物预测和发掘平台“Anti-HIV-Predictor”的预测性能;
图3显示:达巴万星对C8166的毒性作用(方块曲线所示)和对HIV-1p24的抑制作用(圆点曲线所示)。
具体实施方式
下面结合附图,用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
实施例1
测试达巴万星(Dalbavancin)的抗HIV作用:
1、实验目的:测试达巴万星(Dalbavancin)的抗HIV作用
2、实验材料
2.1.测定药物和化合物
待测样品达巴万星购自北京乐博生物科技有限公司。阳性对照化合物叠氮胸苷(3’-Azido-3’-deoxythymidine,AZT)购自Sigma公司。待测样品根据溶解性溶解于RPMI-1640完全培养基或DMSO中,溶解于DMSO中的样品储液浓度为50mM,溶解于RPMI-1640完全培养基的样品储液浓度为10mM、5mM或2mM(根据溶解度确定),储存条件为:-20℃;AZT溶解于RPMI-1640完全培养基中,0.22μm滤膜过滤除菌,贮存液浓度为6mg/ml,分装后-20℃保存。
2.2.试剂和溶液
2.2.1.试剂
HEPES(N-2(2-Hydroxyothyl)piperazine-N'-(2-ethanesufonic acid)、MTT(3,(4,5-Dimethylthiazol-2-yl)-2,5-diphenyl tetrazolium bromide)、DMF(N,N’-Dimethyl formamine)、青霉素(Penicillin)、硫酸链霉素(Streptomycin sulfate)、谷氨酰胺(Glutamine)均购自Sigma公司;2-巯基乙醇(2-ME,2-Mercaptoethanol)为Bio-Rad公司产品。RPMI-1640和胎牛血清为Invitrogen公司产品。
2.2.2.培养基
RPMI-1640完全培养基,含有10%胎牛血清,2mM谷氨酰胺,10mM HEPES,50μM2-巯基乙醇,100,000IU青霉素,100μg/ml链霉素。
2.3.细胞和病毒
人T淋巴细胞系C8166、HIV-1实验株HIV-1ⅢB由英国Medical Research Council,AIDS Reagent Project惠赠。HIV-1实验株HIV-1NL4-3由NIH惠赠。所有细胞和病毒均以含10%胎牛血清的RPMI-1640完全培养基进行培养。按常规方法制备HIV-1ⅢB和HIV-1NL4-3,滴定并计算出病毒的TCID50。病毒贮存液分装后,置-70℃保存。细胞和病毒按常规方法冻存和复苏。
3、HIV-1感染性滴定
HIV-1NL4-3按Johnson&Byington(1990)所述方法改良进行滴定,简述如下:将HIV-1贮存液在96孔板上作4倍稀释,10个梯度,每梯度6个重复孔,同时设置对照孔6孔。每孔加入C8166细胞50μl,每孔终体积为200μl。37℃,5%CO2培养。第3天补加新鲜RPMI-1640完全培养基100μl,第7天在倒置显微镜下观察每孔中HIV-1诱导的细胞病变效应(Cytopathic Effect,CPE),以每孔是否有合胞体(Syncytium)的形成确定;按Reed&Muench方法计算病毒的TCID50(50%Tissue Culture Infection Dose)。
4、对C8166细胞的毒性实验
4×105/ml C8166细胞悬液100μl与不同的待测药物溶液混合,设3个重复孔。同时设置不含药物的对照孔,37℃,5%CO2培养3天,采用MTT比色法检测细胞毒性。ELx800酶标仪测定OD值,测定波长为570nm,参考波长为630nm。计算得到CC50值(50%Cytotoxic Concentration),即对50%的正常T淋巴细胞系C8166产生毒性时的药物浓度。
5、对HIV-1NL4-3致细胞病变(CPE)的抑制实验
将8×105/ml C8166细胞50μl/孔接种到含有100μl/孔梯度倍比稀释药物的96孔细胞培养板上,然后加入50μl的HIV-1NL4-3稀释上清,1300TCID50/孔。设3个重复孔。同时设置不含药物的正常细胞对照孔。AZT为阳性药物对照。37℃,5%CO2培养3天,倒置显微镜下(100×)计数合胞体的形成。EC50(50%Effective Concentration)为抑制合胞体形成50%时的药物浓度。
6、对HIV-1NL4-3急性感染C8166细胞中病毒复制的抑制实验
将4×105个/mL的C8166细胞与HIV-1NL4-3(MOI=0.04)在37℃下感染2小时,用PBS离心洗涤2次,去除游离的病毒离子,取100μL细胞接种到含有100μL不同稀释度待测化合物的96孔板上,37℃,5%CO2培养3天。培养上清离心后收集,用终浓度0.5%Triton X-100裂解灭活。检测药物对HIV-1复制的抑制作用采用捕捉p24抗原ELISA方法。
7、ELISA检测p24抗原
1μL/板抗鼠IgG-Fc抗体4℃铺板过夜;5%脱脂奶粉4℃封板过夜;加入100μl/孔鼠抗p24单抗(利用Liu G J等人建立的方法制备,Liu G J,Wang J P,Xiao J C,et al.Preparation and characterization of three monoclonal antibodies against HIV-1p24capsid protein[J].Cell MolImmunol,2007,4(3):203-208.)37℃,1小时;加入100μl/孔裂解感染细胞培养上清,37℃,2小时;加入100μl/孔1∶100稀释的兔抗p24多抗(利用Liu G J等人建立的方法制备,Liu G J,Wang J P,Xiao J C,et al.Preparation and characterization of three monoclonal antibodies against HIV-1p24capsid protein[J].Cell MolImmunol,2007,4(3):203-208.),37℃,1小时;加入100μl/孔1∶20000稀释的羊抗兔IgG-HRP(Sigma),37℃,1小时;加入OPD底物反应液。10分钟后,2M硫酸终止反应。Elx800ELISA仪测定OD值,测定波长490nm,参考波长630nm。计算出药物对HIV-1复制表达p24抗原的抑制率和EC50,即抑制50%HIV-1p24抗原表达的药物浓度。
8、计算公式
根据实验结果绘制剂量反应曲线,按Reed&Muench法计算出化合物抑制病毒的50%有效浓度(EC50),50%抑制细胞生长浓度(CC50)及抗HIV-1活性的治疗指数TI值(Therapeutic index)为:TI=CC50/EC50。
1)、细胞生长存活率(%)=实验孔OD值/对照孔OD值×100
2)、HIV-1致细胞病变的抑制率(%)=(1-实验孔合胞体数/对照孔合胞体数)×100
3)、HIV-1p24抗原表达的抑制率(%)=(1-实验孔OD值/对照孔OD值)×100
9、实验结果和评价
9.1.达巴万星(Dalbavancin)对C8166细胞的毒性实验结果
表1列出了达巴万星的CC50,本发明的图3(方块曲线所示)显示了不同浓度的达巴万星对细胞C8166的毒性作用。实验结果表明达巴万星对细胞的毒性很小,CC50>200μM(CC50越大表示毒性越小)。在浓度等于EC50(1.296μM)时,达巴万星对细胞C8166完全没有毒性(图3)。
9.2.达巴万星(Dalbavancin)对HIV-1NL4-3病毒株的抗HIV活性实验结果
表1列出了达巴万星的EC50,本发明的图3(圆点曲线所示)显示了不同浓度的达巴万星对HIV-1NL4-3病毒株的抑制作用。达巴万星对HIV-1诱导C8166细胞形成合胞体的抑制作用的EC50为8.694μM,治疗指数TI大于23.0。在HIV-1p24抗原定量结果显示达巴万星抑制p24抗原作用的EC50为1.296μM,治疗指数TI大于135.1。
以上实验结果表明达巴万星的细胞毒性较小或无,具有显著的抗HIV活性和较高的治疗指数,可作为制备治疗艾滋病药物的应用。
表1.达巴万星(Dalbavancin)对HIV-1NL4-3病毒株的抑制作用及对C8166细胞的毒性作用
实施例2:
按达巴万星(Dalbavancin)与赋形剂重量比1:1或1:2的比例加入赋形剂,制粒压片。
实施例3:
达巴万星(Dalbavancin)为有效成分,按常规胶囊制剂方法制成胶囊。
实施例4:
片剂:达巴万星(Dalbavancin)10mg
淀粉适量
玉米浆适量
硬脂酸镁适量
制备方法:将按达巴万星(Dalbavancin)与助剂混合,过筛,在合适的容器中均匀混合,把得到的混合物制粒压片。
实施例5:
胶囊剂:达巴万星(Dalbavancin)10mg
淀粉适量
硬脂酸镁适量
制备方法:将达巴万星(Dalbavancin)与助剂混合,过筛,在合适的容器中均匀混合,把得到的混合物装入硬明胶胶囊。
实施例6:
片剂:达巴万星(Dalbavancin)10mg,乳糖180mg,淀粉55mg,硬脂酸镁5mg。
制备方法:将达巴万星(Dalbavancin)、乳糖和淀粉混合,用水均匀湿润,把湿润后的混合物过筛并干燥,再过筛,加入硬脂酸镁,然后将混合物压片,每片重250mg,化合物含量为10mg。
实施例7:
安瓿剂:达巴万星(Dalbavancin)2mg,氯化钠10mg;
制备方法:将达巴万星(Dalbavancin)和氯化钠溶解于适量的注射用水中,过滤所得溶液,在无菌条件下装入安瓿瓶中。
实施例8:
胶囊剂:达巴万星(Dalbavancin)10mg,乳糖187mg,硬脂酸镁3mg;
制备方法:将达巴万星(Dalbavancin)与助剂混合,过筛,均匀混合,把得到的混合物装入硬明胶胶囊,每个胶囊重200mg,活性成分含量为10mg。
- 还没有人留言评论。精彩留言会获得点赞!