卡托普利等血管紧张素转化酶抑制剂在牙本质粘结上的用途及卡托普利牙本质粘结剂的制作方法
本发明涉及卡托普利等血管紧张素转化酶抑制剂在牙本质粘结上的用途及含卡托普利的牙本质粘结剂。
背景技术:
牙本质是一个由富含胶原基质的羟基磷灰石和含流动液体的牙本质小管所构成的生物复合体。建立在这种异质性结构和内源性富水基质上的牙本质粘结,有赖于牙本质粘结剂树脂单体渗透进入到牙本质中,固化后产生的微机械锁合。然而,树脂单体不可能完全取代胶原纤维间及胶原内部空间的水分,因此,牙本质粘结层很可能在胶原纤维间存在残留水分,阻止树脂和胶原纤维的紧密连接,形成微渗漏或纳米渗漏,引起树脂成分的水解降解,破坏牙本质粘结。而且,牙本质脱矿的深度和树脂渗透浸润的深度有可能不匹配,会在混合层底部产生不完全浸润区。体外及体内实验证实,牙本质粘结的混合层中来自于该未完全浸润区的胶原基质的降解,与内源性牙本质酶的释放和激活有关。其中,最主要的牙本质内源性酶是基质金属蛋白酶(mmps)。暴露的胶原易受内源性mmps的酶解,牙本质中有机基质的酶解破坏会威胁牙本质-修复体粘结的长期稳定性。
mmps是一组依赖于锌离子和钙离子的宿主源性蛋白酶,并且存在于矿化的牙本质中。mmps分为胶原酶,明胶酶,基质降解酶,基质溶解因子,膜型mmps等及其他。人牙本质主要包含明胶酶a(mmp-2)、明胶酶b(mmp-9)和胶原酶2(mmp-8),这些都能降解牙本质中最主要的i型胶原纤维。mmp-2和mmp-9还能降解基底膜及其他间质结缔组织中的细胞外基质。在牙本质中存在的mmps,在酸脱矿前处于未激活状态。在牙本质酸蚀或牙本质龋的低ph值环境下,它们能被激活和释放,会引起牙本质中暴露的胶原纤维的降解,从而影响牙本质粘结的长期稳定性。
无活性的酶原要转变成有活性的mmps,经典的方法是切断前肽区来实现。以mmp-9为例,其激活机制是裂解蛋白分子中半胱氨酸与锌离子间的配位键。当外界因素(致病因素,酸等)直接或者间接切断了蛋白分子内部半胱氨酸与锌离子之间的配位键,暴露了活性位点,从而激活mmp-9。所以,如有化学物质能与mmp-9活性位点的锌离子螯合,能抑制mmp-9的活性。与mmp-9类似,所有的mmps都依赖于锌离子,其激活均需要与锌离子螯合。
牙本质粘结中应用基质金属蛋白酶抑制剂(mmps)能减缓牙本质混合层中胶原蛋白的降解,从而提高牙本质粘结的稳定性。mmps抑制剂有多种,如天然的mmps抑制剂原花色素、葡萄籽提取物,生理性mmps抑制剂(tissueinhibitorofmetalloproteinase,timp)以及合成的mmps抑制剂如氯己定(chlorhexidine,chx)、乙二胺四乙酸(ethylenediaminetetraaceticacid,edta)、戊二醛、四环素等均可增加牙本质粘接的耐久性。
氯己定(chx)是目前研究较多的用于口腔环境的非特异性mmp抑制剂。氯己定是一种广谱的抗菌剂,也是阳离子型表面活性剂,同时是有效的胶原酶抑制剂,能直接抑制mmp-2,mmp-8,mmp-9的活性。氯己定对mmp-8(胶原酶ii)的抑制作用主要由阳离子螯合作用引起的。氯己定能在很低的浓度(0.02%)抑制mmp-8的活性。氯己定易溶于乙醇,但微溶于水(0.08g/100ml)。为了提高氯己定在水中的溶解度,通常在氯己定中加入酸来形成可溶于水的盐,比如氯己定醋酸盐和氯己定葡糖酸盐。学者们将不同浓度的chx加入粘接剂中或作为牙科树脂的组分和底涂剂用于牙本质粘接,期望增加牙本质粘结的稳定性。但chx具有副作用,并可能会干扰粘接剂和牙本质基质的有效结合,尚存在争议。
卡托普利是人工合成的非肤类血管紧张素转化酶(ace)抑制剂,化学成分是巯甲丙脯酸,化学组成是1-(3-巯基-2-甲基-1-丙酰)-l-脯氨酸(c9h15no3s)。结构式为:
主要作用于肾素-血管紧张素-醛固酮(raa)系统。卡托普利抑制raa系统的血管紧张素转换酶,阻止血管紧张素ⅰ转换或血管紧张素ⅱ,并能抑制醛固酮分泌,减少水钠潴留。卡托普利能和ace活性位点中的zn2+螯合,从而起到抑制ace活性的作用。卡托普利从1979年起应用于高血压的治疗,对多种类型高血压均有明显降压作用,并能改善充血性心力衰竭患者的心脏功能,同时也作为肾保护剂在使用。
有很多研究报道卡托普利对mmps具有抑制作用。从卡托普利的分子结构上看,其末端的一个羧基能和酶的精氨酸离子键结合,其巯基能和酶的zn2+结合,而中间的羰基能与酶的氢键结合,从而达到抑制胶原酶的目的。
目前,对卡托普利作用于mmps的研究并没有将目光关注到牙本质粘结领域。牙本质粘结持久性研究是一个研究热点,并没有完全解决。而mmps是影响牙本质粘结持久性的重要因素之一。前期研究发现,在牙本质粘结中,卡托普利能发挥其抑制mmps的作用。而具体机制有待进一步研究。现研究最多的氯己定是一种广谱抗菌剂,纯氯己定在水中的溶解度很低,氯己定的盐类在牙本质粘结中具有不稳定性。相反,卡托普利的水溶性好(0.1g/ml),也易溶于其他溶剂,如乙醇、丙酮等,具有良好的理化性质,其作用机理也与氯己定不尽相同。卡托普利具有良好的mmps抑制特性,在牙本质粘结中引入卡托普利等,是全新的尝试。在前期的实验中有确切的效果,有望成为改善牙本质粘结持久性的新一代产品。
技术实现要素:
牙本质胶原基质(主要是胶原纤维)在粘结中会降解,牙本质粘结的稳定性与持久性问题还没有完全解决。本发明在牙本质粘结的稳定性、持久性研究中引入卡托普利等,是全新的尝试,这基于卡托普利等血管紧张素转化酶抑制剂同时具有抑制基质金属蛋白酶(mmps)的作用,且因其分子量小、溶解性好,理化性质更出色,相较于氯己定等能更便利的应用于牙本质粘结。
本发明主要解决的技术问题是在牙本质粘结体外实验中应用卡托普利并与传统的mmps抑制剂氯己定作对比研究,来确定在牙本质粘结中应用卡托普利是否有利于维持粘结的稳定性与持久性。在此基础上研制出相关的含卡托普利等的牙本质粘结剂,并验证其有效性,最终在临床推广应用。
为了达到此目的,本发明的技术方案是,将血管紧张素转化酶抑制剂应用在牙本质粘结上。
为了达到此目的,根据一个实施方案,本发明的特征在于选取一种血管紧张素转化酶抑制剂—卡托普利,其化学成分是巯甲丙脯酸,化学组成是1-(3-巯基-2-甲基-1-丙酰)-l-脯氨酸(c9h15no3s)。
卡托普利仅是血管紧张素转化酶抑制剂的一种,血管紧张素转化酶抑制剂中的其他形式制剂,如依那普利、西拉普利、奎那普利、苯那普利、福辛普利、雷米普利等,也具有类似的作用和效果,优选分子量小、溶解性好的血管紧张素转化酶抑制剂。也可以采用它们的任意比例、任意组分的混合物。
包括卡托普利在内的血管紧张素转化酶抑制剂可以制成溶试剂,其溶剂为水、乙醇、丙酮等;也可以制成粘结剂,包括卡托普利在内的血管紧张素转化酶抑制剂作为粘结剂的其中一种组分。
本发明采用的技术方案是在牙本质粘结的体外实验研究中,卡托普利与研究较成熟的mmps抑制剂—氯己定相比较。在完成粘结后,本发明通过测量牙本质粘结强度的变化、sem、tem等研究方法评价卡托普利应用于牙本质粘结中的效果。
在卡托普利与氯己定的对比实验研究中:葡萄糖酸氯己定的浓度为2%;卡托普利溶于水,制备成浓度为0.5%、1%、2%的溶液;对照组则为蒸馏水。
离体牙制备标准的牙本质粘结面,分组,分别为2%氯己定组、卡托普利组(0.5%、1%、2%)以及对照组(去离子水)。相同条件下牙本质粘结面经过酸蚀后,上述溶液分别处理各自组的牙本质粘结面,完成粘结。然后制备微拉伸试件,进行水贮存的老化试验。分别测定即刻(24小时)、6个月以及12个月后的粘结强度,粘结面的变化用扫描电镜(sem)观察。
根据粘结强度以及扫描电镜的结果对比卡托普利与氯己定的作用,推断卡托普利在牙本质粘结中的应用效果。
在此实验基础上,作进一步的研究。因为牙本质粘结剂的溶媒通常为乙醇、丙酮等,本发明采用的技术方案是在牙本质粘结的体外实验研究中,卡托普利溶于乙醇、丙酮,制备成一定浓度的卡托普利乙醇溶液、卡托普利丙酮溶液。以该溶液处理牙本质粘结面,完成粘结。然后进行老化试验。最后测定粘结强度,以扫描电镜、透射电镜等为辅助研究手段。评定卡托普利以乙醇、丙酮作为溶媒,在牙本质粘结中的应用效果。
本发明采用的进一步的技术方案是,卡托普利作为一种组分直接加入牙本质粘结剂中,制备含卡托普利的牙本质粘结剂。在体外实验研究中,应用此粘结剂完成牙本质的粘结。然后进行老化试验。最后测定粘结强度,以扫描电镜、透射电镜等为辅助研究手段。评定含卡托普利的牙本质粘结剂,在牙本质粘结中的应用效果。
通过上述体外实验,确定制备出一定浓度的含卡托普利水溶液、乙醇溶液、丙酮溶液等制剂;确定制备出含一定量卡托普利的牙本质粘结剂。通过临床试验,评定卡托普利制剂、卡托普利粘结剂的临床应用效果。
通过本发明提供的用途、方法、粘结剂,可以保护牙本质基质中的胶原纤维不被分解破坏,提高牙本质粘结的强度,维持牙本质粘结的稳定性与持久性。
附图说明
表1是本发明的不同牙本质处理剂(去离子水、2%葡萄糖酸氯己定、0.5%卡托普利、1%卡托普利、2%卡托普利)处理后即刻(24小时)、6个月、12个月的牙本质粘结强度值。
图1是本发明的不同牙本质处理剂(去离子水、2%葡萄糖酸氯己定、0.5%卡托普利、1%卡托普利、2%卡托普利)处理后即刻(24小时)、6个月、12个月的牙本质粘结强度的柱状图。
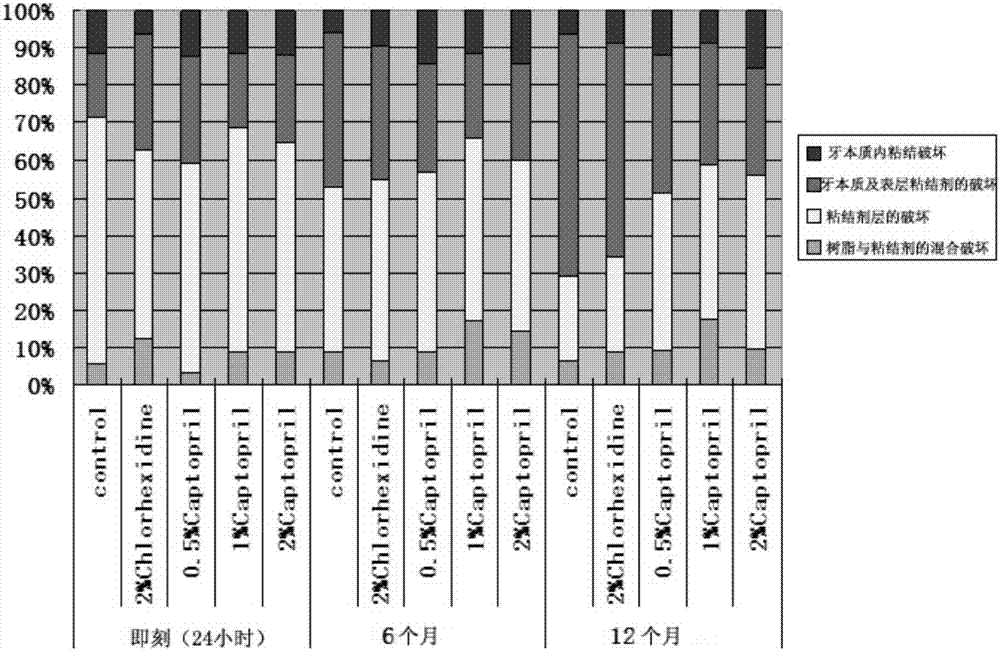
图2是本发明的不同牙本质处理剂(去离子水、2%葡萄糖酸氯己定、0.5%卡托普利、1%卡托普利、2%卡托普利)处理后牙本质粘结测试试件经过微拉伸试验,牙本质粘结断裂面断裂的部位分析图。
图3是本发明的不同牙本质处理剂(去离子水、2%葡萄糖酸氯己定、0.5%卡托普利、1%卡托普利、2%卡托普利)处理后,在即刻(24小时)、6个月、12个月牙本质粘结测试试件经过微拉伸试验后断裂面的扫描电镜图。
具体实施方式
下面结合附图对本发明的较佳实施例进行详细阐述,以使本发明的优点和特征能更易于被本领域技术人员理解,从而对本发明的保护范围作出更为清楚明确的界定。
请参阅附图,本发明实施例包括:
实施例1
本实施例为基础实验,比较卡托普利与传统的mmps抑制剂氯己定在牙本质粘结中的作用效果。具体方法如下:
卡托普利(sigma)制备成0.5%、1%、2%的水溶液,氯己定为2%的葡萄糖酸氯己定(alfaaesar,usa)水溶液。
无龋第三磨牙40颗,随机分成5组,每组8颗。第一组:以去离子水处理,作为对照组;第二组:以2%氯己定处理;第三组:0.5%卡托普利处理;第四组:1%卡托普利处理;第五组:2%卡托普利处理。
每颗牙在喷水下垂直于牙体长轴切去冠方牙釉质,暴露牙本质,表面用800目碳化硅砂纸湿抛光制备牙本质粘结面,平行于牙体长轴磨除周围轴壁牙釉质。
牙本质粘结面先用酸蚀剂酸蚀20秒,随后大量喷水冲洗30秒,空气吹干(10秒)后。每组牙本质粘结面分别以不同溶液进行再湿处理60秒:第一组涂去离子水,第二组涂布2%氯己定溶液,第三组涂布0.5%卡托普利溶液,第四组涂布1%卡托普利溶液,第五组涂布2%卡托普利溶液。
用吸潮纸吸去多余溶液,使其成为微湿润状态,再均匀涂布粘结剂(3m,adpertmsinglebond2,美国)20秒,空气轻吹10秒,光照20秒后进行树脂(3m,z250)分层充填,树脂充填高度约为4-5mm。
树脂充填完毕的牙齿在慢速牙切片机上沿牙长轴进行切割,形成横截面积约为0.9mm*0.9mm的牙本质测试试件,长度约为8mm~12mm,每牙约制备16个测试试件。
将每颗牙的牙本质测试试件分别储存于去离子水的密闭瓶中。去离子水每周更换一次。
24小时后每组每颗牙所制备的样品中随机选取4个样本,每组共32个样品,进行即刻组的微拉伸粘结强度测定。
其余牙本质测试试件储存于密闭瓶中的去离子水中进行老化试验,去离子水每周更换一次。6个月后和12个月后分别随机取同样数量的牙本质测试试件(32个)进行微拉伸试验(方法同24小时即刻组)。
微拉伸粘结强度测定的仪器:万能材料试验机(zwick/roellmodelbz2.5/tn1s,zwickgmbh&co,ulm,德国)预载0.5n,拉伸试验速度1mm/min,直至牙本质试件粘结面断裂,计算机自动记录样本拉伸断裂时的峰值(n)。同时分别记录被测量试件的宽度和厚度。根据断裂时的峰值(n)和粘结面的面积(mm2),计算各组各试件的微拉伸黏结强度值(mpa=n/mm2)。
各组微拉伸粘结强度测试数值采用spss16.0统计软件统计分析,各组均数之间的总体差异采用单因素方差分析(one—wayanova)比较,均数间两两比较用lsd法进行。
牙本质测试试件断裂面的sem观察:每个时间段中样本进行微拉伸试验后,喷铂金处理后,sem在不同放大倍数下(90,500,1.5k,3k,10k,20k)观察断裂面牙本质小管、胶原纤维网、树脂突等结构。
各实验组粘结强度值见表1:
统计结果显示:即刻组(24小时)各组之间的平均微拉伸粘结强度值没有显著性差异(p>0.05)。随时间的推移,各组的微拉伸粘结强度值均有所下降,对照组与2%氯己定组下降明显,而卡托普利各组粘结强度下降程度没有对照组与2%氯己定组明显。6个月组:2%氯己定组的微拉伸强度平均值比对照组高,但是两者间没有显著性差异;1%卡托普利组微拉伸强度平均值比对照组高,且有显著性差异(p<0.05);2%卡托普利组微拉伸强度平均值分别高于对照组和2%氯己定组,且均有显著性差异(p<0.05)。12个月组:对照组微拉伸强度平均值与2%氯己定组比较没有显著性差异(p>0.05);0.5%、1%和2%卡托普利组的微拉伸强度平均值与对照组、1%氯己定组比较都有显著性差异(p<0.05);0.5%、1%和2%卡托普利组的微拉伸强度平均值组间没有显著性差异(p>0.05)。
对照组即刻(24小时)、6个月、12个月的平均微拉伸粘结强度值的比较:随时间的推移平均微拉伸粘结强度均下降,6个月为29.89±14.55mpa,12个月降为23.90±14.56mpa,与即刻平均微拉伸粘结强度比较均有显著性差异(p<0.05),而6个月与12个月的粘结强度比较没有显著性差异(p>0.05)。2%氯己定组6个月、12个月的平均微拉伸粘结强度值同样均有下降,其中12个月后的平均微拉伸粘结强度值下降很明显(降为20.12±13.61mpa),6个月时的平均微拉伸粘结强度值和即刻组比较没有显著性差异(p>0.05),而12个月时的平均微拉伸粘结强度值与即刻组比较有显著性差异,且与6个月时的平均微拉伸粘结强度值比较也有显著性差异(p<0.05)。0.5%卡托普利组、1%卡托普利组、2%卡托普利组的平均微拉伸粘结强度值随时间的推移虽均有所下降,但下降不明显(表1),在24小时、6个月、12个月三个时间段中三者间的平均微拉伸粘结强度值比较均没有显著性差异(p>0.05)。
三个时间段的平均微拉伸粘结强度结果显示,与氯己定相比较,卡托普利更有利于维持稳定的牙本质粘结强度。图2为不同组粘结强度变化的柱状图,直观地说明了本实验的结论。
微拉伸测试试件断裂面分析结果见附图2。在即刻(24小时)时,5组粘结面断裂的部位基本相同,以树脂、粘结层为主;6个月后,5组粘结面的断裂部位稍有改变,相互间比较变化不明显;12个月后,去离子水处理的对照组与2%氯己定组断裂部位的部位改变明显,主要的断裂面部位在粘结面的基底层,涉及牙本质、胶原纤维层,而3组卡托普利处理的实验组粘结面断裂部位变化不明显,与即刻组相似。结果提示卡托普利更有利于牙本质粘结,能够维持其稳定性与持久性。
sem结果,见图3。
即刻组(24小时):各组断裂面形貌相似,树脂突与牙本质小管结合紧密,管间牙本质中有较多的树脂成分,包绕胶原纤维网,胶原网状结构不清晰。
6个月组:对照组牙本质小管内树脂突与小管壁间出现明显间隙(a2白色箭头),管间牙本质中树脂成分有降解迹象,暴露较多的裸露胶原(a2黑色箭头)。2%氯己定组中树脂突与牙本质小管大多数结合紧密,少许出现裂隙,管间牙本质中可见较多树脂成分,胶原纤维网状结构少量暴露。卡托普利三组中,形貌结构均相似,树脂突大多数仍然充满整个牙本质小管且结合紧密,管间牙本质中仍结合大量树脂成分,胶原纤维网因结合树脂成分,胶原网状结构仍旧不清晰。
12个月组:与即刻组相比较,12个月后的对照组与2%氯己定组形貌变化较大,树脂突与牙本质小管之间的间隙变得较大(a3,b3白色箭头),树脂突本身有降解,部分小管中树脂突缺失。管间牙本质中因树脂成分降解较多,裸露的胶原纤维多见(a3,b3黑色箭头),胶原网状结构清晰。卡托普利三组中,形貌相似,与即刻组比较大多数牙本质小管中仍有树脂突,且其中大多数树脂突与牙本质小管壁结合紧密,少数出现裂隙;管间牙本质中仍然保留较多树脂成分,因而胶原网状结构大多数依旧不清晰。
sem实验结果显示卡托普利能维持牙本质粘结的稳定性与持久性,在本实验中其效果要优于氯己定。
微拉伸粘结强度与sem结果表明卡托普利更能维持稳定的牙本质粘结,在牙本质的粘结修复中具有应用价值。
实施例2
牙本质粘结剂的溶剂通常有乙醇、丙酮等,卡托普利易溶于乙醇、丙酮,以乙醇、丙酮为溶媒制备一定浓度的卡托普利乙醇溶液、卡托普利丙酮溶液。然后应用于牙本质粘结,通过实验测试其对牙本质粘结强度的影响。实验的方法步骤参照实施例1,实施的方法为微拉伸粘结强度的测定、扫描电镜、透射电镜等。
实施例3
本发明采用的进一步的技术方案是,卡托普利直接加入牙本质粘结剂中,制备含卡托普利的牙本质粘结剂。以离体牙作牙本质粘结的体外实验研究。同样制备牙本质粘结面,牙本质粘结面经过酸蚀、冲洗后,涂布含卡托普利的粘结剂,光照,再完成树脂分层充填。并与不含卡托普利的牙本质粘结剂、含其他成分(如氯己定)的牙本质粘结剂作对比研究。测试的方法有微拉伸粘结强度的测定、粘结断裂面的sem观测以及透射电镜等。评定含卡托普利的牙本质粘结剂,在牙本质粘结中的应用效果。
实施例4
本发明的最终目的是临床应用。通过上述体外实验,确定制备出一定浓度的含卡托普利的水溶液、乙醇溶液、丙酮溶液等制剂;确定制备出含一定量卡托普利的牙本质粘结剂。通过临床试验,评定卡托普利制剂、卡托普利粘结剂的临床应用效果。实施的方法选择合适的病例(如v类洞),完成粘结充填,遵照一定的标准,通过长期随访,以保留率或脱落率、边缘分析等方法,对比研究卡托普利制剂、卡托普利粘结剂应用的临床效果。
实施例1为本发明的基础实验,本实验结果表明卡托普利在维持牙本质粘结的稳定性与持久性上要优于氯己定,说明卡托普利在牙本质粘结中具有应用价值。其余实施例是在此实验基础上的引申,同时也可能有其他的实施方式。所以任何有关卡托普利等血管紧张素转化酶抑制剂直接或间接在牙本质粘结相关的技术领域中的应用,均包括在本发明的专利保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!