一种基于埃洛石和精氨酸改性聚酯脲氨酯复合材料及其制备与应用的制作方法
本发明属于组织工程技术和再生医学材料领域,具体涉及一种基于埃洛石纳米管和精氨酸改性的聚酯脲氨酯复合材料及其制备方法与应用。所述复合材料用作复合补片,用于骨组织工程材料领域。
背景技术:
临床上,由外伤、癌症、免疫性疾病等造成的骨组织损伤时有发生,且呈现日益增长趋势。尽管骨组织有一定的再生能力,但是如果损伤严重,由于损伤处适于细胞生长的基质缺失,细胞会难以被募集到大面积的骨缺损部位,骨修复过程极为漫长,并且伴随着损伤部位微环境的改变,骨组织往往不能完全再生,仅是疤痕修复。现在临床上多采用自体骨移植来应对大范围缺损,但其来源有限,拆东墙补西墙的方法需要多次手术来完成,会给患者带来很多痛苦和额外的损伤。
组织工程和再生医学的发展则为骨修复提供了解决思路,组织工程支架植入体内,通过募集细胞,支持细胞的粘附、生长、增殖,诱导干细胞分化,可构建出利于组织再生的微环境,促进组织的再生和修复。组织工程支架材料是其中的重要的组成部分,优异的组织工程支架材料不仅要具有良好的生物相容性,能支持细胞生长,还需要有一定的功能性和生物活性,可在体内降解。常用的骨粉、羟基磷灰石、β-磷酸三钙等支架材料虽能在较小范围的骨缺损上取得良好的治疗效果,但它们在体内只起到骨传导的作用,自身并不能诱导骨再生,骨修复进程缓慢。天然材料和其相关水凝胶支架则往往受限于较低的力学性能和不匹配的降解,骨修复效果有限。
聚氨酯是一种具有高结构可调性的多嵌段聚合物,相对天然材料具有更好的机械性能,性质更稳定,更易于调控。适当的软硬段结构可制备具有良好生物相容性的生物医用聚氨酯材料,可降解软段如pcl的选用也可合成具有生物降解性的聚氨酯材料。这类聚氨酯可被制成多孔支架,用于骨组织的修复,但实际应用中,由于材料疏水的结构和分子间氢键作用力,使得材料降解极为缓慢,与组织的修复不匹配,支架未经过体外矿化处理的疏水表面也难以支持细胞的粘附和生长,且生物活性较差,难以诱导骨组织的再生修复。如何改善聚氨酯的亲水性,提高生物降解性,保证材料的生物相容性和安全性,赋予材料一定生物活性和骨诱导性,并且同时兼顾可加工性仍是亟待解决的问题。
技术实现要素:
本发明为解决现有技术的缺陷和不足,提供一种基于埃洛石和精氨酸改性聚酯脲氨酯复合材料的制备方法。本发明的方法所制备的复合材料具有一定的亲水性和生物活性,具备良好的细胞相容性,可支持细胞粘附、生长和增殖、诱导干细胞成骨分化,促进骨再生和修复,同时具备生物降解性,可随新骨的生成最终降解。
本发明另一个目的在于提供由上述方法制备的复合材料。
本发明再一个目的在于提供上述复合材料的应用。
本发明的目的通过以下技术方案实现:
一种基于埃洛石和精氨酸改性聚酯脲氨酯复合材料的制备方法,包括以下步骤:
1)在惰性氛围和搅拌的条件下,将聚己内酯二醇与六亚甲基二异氰酸酯在引发剂的作用下进行预聚反应,降温至40~70℃,加入l-精氨酸-1,8-辛二醇酯溶液,继续反应5~10h,稀释,透析,冷冻干燥,获得聚酯脲氨酯材料;所述六亚甲基二异氰酸酯与聚己内酯二醇的摩尔比为(1.2~2):1;所述预聚反应的温度为60~90℃,预聚反应的时间为0.5~2h;
2)将聚酯脲氨酯材料溶解于有机溶剂中,加入埃洛石纳米管,分散均匀,成膜,获得复合材料。
步骤1)中所述引发剂为辛酸亚锡或异辛酸锡;引发剂的用量为聚己内酯二醇和六亚甲基二异氰酸酯总质量的0.01%~0.05%。
步骤1)中所述l-精氨酸-1,8-辛二醇酯溶液是指将l-精氨酸-1,8-辛二醇酯溶于有机溶剂中得到;所述有机溶剂为二甲基亚砜(dmso)或n,n-二甲基甲酰胺dmf;所述l-精氨酸-1,8-辛二醇酯:有机溶剂的摩尔体积比为0.25mol:(400~500)ml;
步骤1)中所述聚己内酯二醇的数均分子量为500~3000,优选为530~2000;
步骤1)中所述搅拌的转速为100~300r/min;步骤1)中l-精氨酸-1,8-辛二醇酯与聚己内酯二醇pcl摩尔比为(0.2~1):1;
步骤1)中所述稀释是指采用dmso稀释反应溶液,所述透析是指在截留分子量3500的透析袋中进行透析后;
聚己内酯二醇使用前进行真空干燥处理。
步骤2)中所述有机溶剂为二氯甲烷、二甲基亚砜dmso,n,n-二甲基甲酰胺dmf;所述埃洛石纳米管的用量占复合材料总质量的2%~10%,优选为6%。
所述聚酯脲氨酯膜材料的水接触角为50o~80o。聚酯脲氨酯膜材料表面zeta电位在ph<10的宽范围内显示正电性,其正电性大小随l-精氨酸-1,8-辛二醇酯用量增加而增大,ph~7.0,zeta电位为33mv~90mv。
步骤2)中所述埃洛石纳米管的直径为30~70nm,长度为300nm~3μm。
本发明的复合材料的弹性模量为2~24mpa,拉伸强度为0.6~10mpa。
所述复合材料在骨组织工程材料中的应用。
所述骨组织工程材料为骨填充材料、骨修复用生物医用材料或骨再生用生物医用材料。
所述聚酯脲氨酯材料即精氨酸改性聚酯脲氨酯具有以下化学结构:
式i中,精氨酸二醇酯链段b与pcl链段a的摩尔比为0.2~1:1。
与现有技术相比,本发明具有以下优点和有益效果:
1、相比于传统聚氨酯材料,本发明制备的基于埃洛石和精氨酸改性聚酯脲氨酯复合材料中,带正电的精氨酸改性聚酯脲氨酯材料无细胞毒性,细胞相容性良好,可促进胶原的沉积、支持细胞的生长和促进细胞增殖。
2、本发明中使用的扩链剂为l-精氨酸-1,8-辛二醇酯,异氰酸酯为脂肪族的六亚甲基二异氰酸酯,软段选用了fda批准的医用高分子材料pcl链段,降解产物无毒、可吸收,且降解产物精氨酸还有利于创口的修复,减少炎症反应。材料的正电性和降解性可通过控制扩链剂精氨酸二醇酯的比例来进行控制,精氨酸链段可增强材料与水的相互作用,改善材料亲水性,同时解决pcl型聚氨酯实际降解速率过慢的问题。
3.具有高长径比的埃洛石纳米管则作为复合材料进一步增强了材料机械性能,同时增强了材料诱导干细胞成骨分化的能力,制备的复合材料具有良好的理化性能和生物学性能,可促进新骨的生成和骨缺损的修复并实现自身降解,并且易于加工制备成骨修复支架,用于临床上骨损伤的修复。
附图说明
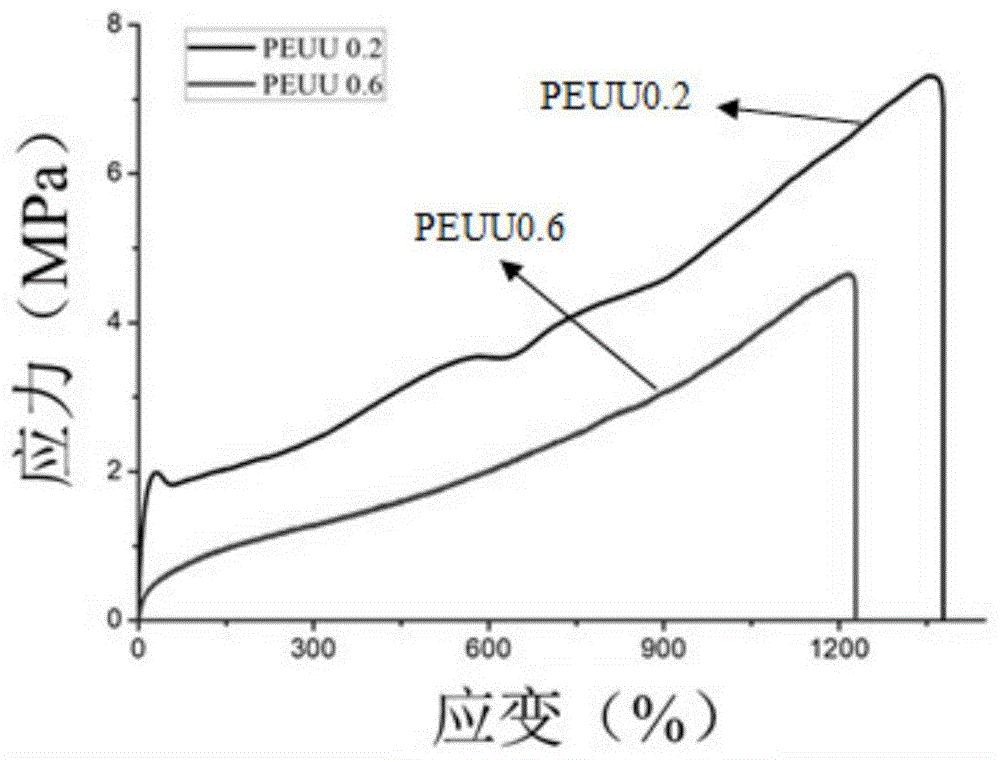
图1为实施例1中聚酯脲氨酯膜材料(peuu0.2,peuu0.6)的应力-应变曲线;
图2为实施例1中聚酯脲氨酯(peuu0.2,peuu0.6,peuu1.0)和聚氨酯膜材料(pu-bdo)的表面zeta电位曲线图;
图3为聚氨酯(pu-bdo)、实施例1中未复合的聚酯脲氨酯材料peuu(即peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)在1,4,7天的calcein-am/pi活死细胞染色荧光图像;
图4为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织micro-ct图像;其中无补片即空白组,未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料;
图5为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织的切片h&e染色图;其中无补片即空白组,未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料;
图6为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织的切片masson染色图;右下角的图中nb表示新生骨组织;其中无补片即空白组,未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料;
图7为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)横截面的sem图;图a为实施例1中未复合的聚酯脲氨酯材料(peuu0.2),图b为实施例3中复合膜材料。
具体实施方式
下面结合具体实施例来进一步说明本发明。以下实施例为本发明较佳的实施方式,但并不对本发明的保护范围做任何形式的限定。
聚己内酯(pcl)二醇(cas:36890-68-3,sigma,189405mn~530;sigma,189421mn~2000)。
实施例1精氨酸改性聚酯脲氨酯的制备
一种基于聚己内酯、六亚甲基异氰酸酯和精氨酸二醇酯的精氨酸改性聚酯脲氨酯的制备,由以下步骤制备而成:
(1)将l-精氨酸-1,8-辛二醇酯冷冻干燥72h,用二甲基亚砜进行溶解,每0.25moll-精氨酸-1,8-辛二醇酯溶解至400ml二甲基亚砜,加入分子筛,备用,获得l-精氨酸-1,8-辛二醇酯溶液;
(2)聚己内酯(pcl)二醇(mn~530)抽真空除水3h后,在惰性气体(氮气)保护下,加热至70℃,机械搅拌,搅拌速率150r/min,加入六亚甲基二异氰酸酯(hdi)(hdi与pcl二醇的摩尔比为1.2:1,1.6:1,2.0:1),待搅拌均匀,滴入pcl与hdi总质量0.05%的异辛酸锡(用甲苯配成0.5mg/ml的引发剂溶液),进行1h预聚;预聚结束后,降低反应温度至60℃,滴加l-精氨酸-1,8-辛二醇酯溶液(l-精氨酸-1,8-辛二醇酯与pcl二醇的摩尔比为0.2:1,0.6:1,1:1)进行扩链,继续反应8h,加入dmso稀释反应溶液(hdi,pcl和l-精氨酸-1,8-辛二醇酯与反应液中溶剂的质量体积比为(5~10)g:100ml),在截留分子量3500的透析袋中进行透析后,-20℃冷冻干燥72h,得到聚酯脲氨酯材料peuu0.2、peuu0.6和peuu1.0,具体配方见表1。
将得到的聚酯脲聚氨酯材料用二氯甲烷溶解,每1g材料加入10ml二氯甲烷,在5cm×5cm或10cm×10cm的聚四氟乙烯模具中流延成膜。本发明制备的精氨酸改性聚酯脲氨酯均易流延成膜片。
其中,精氨酸二醇酯(l-精氨酸-1,8-辛二醇酯)由l-精氨酸和1,8-辛二醇在对甲苯磺酸保护下进行脱水缩合后,所得产物通过调ph至9.5脱除保护基团,通入co2中和,过滤,冷冻干燥得到。
聚氨酯(对比例)的制备:
将聚己内酯(pcl)二醇(mn~530)抽真空除水3h后,在惰性气体(氮气)保护下,加热至70℃,机械搅拌,搅拌速率150r/min,加入六亚甲基二异氰酸酯(hdi)(hdi与pcl二醇的摩尔比为1.2:1),待搅拌均匀,滴入pcl与hdi总质量0.05%的异辛酸锡(用甲苯配成0.5mg/ml的引发剂溶液),进行1h预聚;预聚结束后,降低反应温度至60℃,滴加1,4-丁二醇进行扩链(1,4-丁二醇与pcl二醇的摩尔比为0.2:1),在反应的过程中分两次加入dmso,使反应过程中产物充分溶解,以防爆聚,继续反应8h,截留分子量3500的透析袋中进行透析后,-20℃冷冻干燥72h,得到聚氨酯材料pu-bdo。聚氨酯材料pu-bdo的配方见表1.
每1g聚氨酯材料pu-bdo加入10mldmf溶解,在5cm×5cm或10cm×10cm的聚四氟乙烯模具中流延成膜。
表1聚酯脲氨酯材料以及聚氨酯的配方
hdi为六亚甲基二异氰酸酯,pcl530为聚己内酯(pcl)二醇(mn~530),l-arg-8为l-精氨酸-1,8-辛二醇酯,bdo为1,4-丁二醇。
将聚氨酯pu-bdo与精氨酸改性的聚酯脲氨酯(peuu0.2,peuu0.6,peuu1.0)相比,材料降解极为缓慢,疏水性强,细胞难以粘附,难以用作骨修复材料。
实施例2不同分子量pcl制备聚酯脲氨酯
本实施例选用分子量为530和2000的pcl分别制备聚酯脲氨酯,其制备步骤和反应条件同实施例1。本实施例的配方如表2。
表2聚酯脲氨酯材料的配方
hdi为六亚甲基二异氰酸酯,pcl530为聚己内酯(pcl)二醇(mn~530),pcl2000为聚己内酯二醇(mn~2000),l-arg-8为l-精氨酸-1,8-辛二醇酯。
所制备的几种聚酯脲氨酯中,选用pcl2000制备的材料中因精氨酸质量占比较少,较疏水。相对于pcl2000制备的材料,pcl530制备的材料更亲水,pcl530制备的材料随精氨酸醇酯与pcl的比值n(摩尔比)的增加,水接触角不断减小,膜表面正电性逐步增强,n=1.0的材料机械性能较差,软段为pcl530以及投料比n=0.2和n=0.6的材料具有更好的机械性能,且更适于细胞的粘附和生长。
实施例3埃洛石纳米管与精氨酸改性聚酯脲氨酯复合材料的制备
将实施例1中制备的聚酯脲氨酯peuu0.2溶解于二氯甲烷中,分别加入不同量埃洛石纳米管(埃洛石纳米管占复合材料总质量2%,4%,6%,8%,10%),搅拌分散,由于聚酯脲氨酯的正电特性和埃洛石外管壁的负电特性,埃洛石纳米管可以很容易在溶液中均匀分散而不沉降,流延成膜,用冲子切割成直为径5mm的复合补片(即复合材料)。
相对于未添加埃洛石的聚酯脲氨酯,本实施例的复合材料(埃洛石纳米管复合后的聚酯脲氨酯材料)亲水性、机械性能略有增强,ph=7时的表面zeta电位和降解性无明显差异,同样可支持细胞生长,添加6%埃洛石的埃洛石纳米管复合聚酯脲氨酯补片骨缺损修复效果最佳,2个月的大鼠颅骨缺损修复结果显示,缺损中心有大量新骨生成。
性能测试:
(1)亲水性测试:
将实施例1中聚酯脲氨酯材料以及聚氨酯进行亲水性测试,测试结果如表3所示。
表3聚酯脲氨酯材料以及聚氨酯的水接触角
从表3中可以看出,相较于聚氨酯pu-bdo,精氨酸改性聚酯脲氨酯的亲水性显著提高。
(2)力学性能测试
将实施例1中聚酯脲氨酯膜材料(peuu0.2,peuu0.6)进行力学性能测试,测试结果如图1所示。图1为实施例1中聚酯脲氨酯膜材料(peuu0.2,peuu0.6)的应力-应变曲线。从图1可知,本发明制备的聚酯脲氨酯具备良好的机械性能,弹性佳。
(3)将实施例1中聚酯脲氨酯膜材料(peuu0.2,peuu0.6,peuu1.0)以及聚氨酯(pu-bdo)进行zeta电位性能测试,测试结果如图2所示。
图2为实施例1中聚酯脲氨酯(peuu0.2,peuu0.6,peuu1.0)和聚氨酯膜材料(pu-bdo)的表面zeta电位曲线。从图2可知,膜表面zeta电位显示精氨酸改性聚酯脲氨酯材料(即聚酯脲氨酯)呈现稳定的正电性,并且电位随精氨酸醇酯含量增加而增大。
(4)将聚氨酯(pu-bdo)、实施例1中未复合的聚酯脲氨酯材料peuu(即peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)进行骨细胞培养的测试,测试结果如图3所示。
图3为聚氨酯(pu-bdo)、实施例1中未复合的聚酯脲氨酯材料peuu(即peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)在1,4,7天的calcein-am/pi活死细胞染色荧光图像。
从图3可知,在实施例1中未复合的聚酯脲氨酯材料以及实施例3中复合膜材料上接种骨细胞培养1,4,7天进行活死染色后在倒置荧光显微镜下观察,可见骨细胞铺展完全,材料可支持细胞生长和增殖,且对活细胞数的统计结果显示材料具有促进细胞增殖的作用。
另外,当精氨酸二醇酯与pcl摩尔比在0.2~0.6时,材料更利于细胞生长、铺展和增殖。
(5)、体内实验
(5-1)颅骨缺损模型的构建:spf级sd大鼠,以3%戊巴比妥钠通过腹腔注射麻醉,剔除头部毛发,清洁表面皮肤,切开皮肤及皮下组织,剥离骨膜后于大鼠颅骨上用骨钻制造2个5mm左右对称的骨缺损模型。在骨缺损处植入复合补片(实施例1中未复合的聚酯脲氨酯材料以及实施例3中复合膜材料),缝合,用碘伏消毒创口部位。术后定时观察记录其生理状况。在1、2、3月用二氧化碳窒息法处死实验组大鼠,取出颅骨,生理盐水清洗周围血液,4%多聚甲醛固定48h后对取得的骨组织样品进行ct扫描和组织学分析,评估补片对颅骨缺损修复的效果。测试结果如图4~6所示。
图4为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织micro-ct图像;其中无补片即空白组、未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料;
图5为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织的切片h&e染色图;其中无补片即空白组、未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料;
图6为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)植入大鼠颅骨缺损部位2个月后的骨组织的切片masson染色图;图中nb表示新生骨组织;其中无补片即空白组、未复合的聚酯脲氨酯peuu即实施例1中peuu0.2,peuu-hnt即为实施例3中埃洛石的含量为6%的复合材料。
(5-2)结果:
如图4、图5和图6所示,相对于空白缺损,peuu补片(peuu0.2,peuu-hnt)植入周围胶原沉积,在大鼠颅骨植入聚酯脲氨酯补片组的大鼠颅骨缺损边缘有部分新骨的生成,带正电的补片可能起到了吸附胶原和蛋白,募集细胞,支持细胞生长的作用,而pu-bdo因强疏水作用易滑动,难以固定至缺损处作为补片材料。
(6)材料的结构表征
图7为实施例1中未复合的聚酯脲氨酯材料(peuu0.2)以及实施例3中复合膜材料(peuu-hnt,埃洛石的含量为6%,hdi:pcl530:l-arg-8摩尔比为1.2:1.0:0.2)横截面的sem图;图a为实施例1中未复合的聚酯脲氨酯材料(peuu0.2),图b为实施例3中复合膜材料。
本发明的上述实施例仅仅是为清楚地说明本发明所作的举例,而并非是对本发明的实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!