胰高血糖素、GLP-1和GIP三重激动剂的长效缀合物的液体制剂的制作方法
胰高血糖素、glp-1和gip三重激动剂的长效缀合物的液体制剂
技术领域
1.本发明涉及胰高血糖素/glp-1/gip三重激动剂的长效缀合物的液体制剂和制备该液体制剂的方法。
背景技术:
2.肥胖症和糖尿病(包括2型糖尿病)是现代社会中发生的代表性代谢疾病。这些疾病在世界上被视为威胁健康的因素,并且目前由于这些疾病的发生而带来的经济成本正在迅速增加。
3.胰高血糖素样肽-1(glp-1)和葡萄糖依赖性促胰岛素多肽(gip)是代表性的胃肠激素和神经激素,并且是根据食物摄入量控制血糖水平的物质。胰高血糖素是一种由胰腺分泌的肽激素,并且与上述两种物质一起参与控制血糖水平。
4.glp-1是一种由食物摄入刺激小肠分泌的激素。glp-1以血糖依赖性方式促进胰腺中的胰岛素分泌,并抑制胰高血糖素的分泌,因此有助于降低血糖水平的作用。此外,glp-1具有通过充当饱腹因子来减缓胃肠道中的消化作用和通过延迟排空胃肠道中消化食物的时间来减少食物摄入量的作用。此外,据报道,向大鼠施用glp-1具有抑制食物摄入和减轻体重的作用,并且这些作用在正常和肥胖状态下都同样发生,因此显示了glp-1作为治疗肥胖症的药物的潜力。
5.gip(由食物摄入的刺激分泌的胃肠激素之一,glp-1也是如此)是由肠k细胞分泌的42个氨基酸组成的激素。据报道,gip以血糖依赖性方式发挥促进胰腺胰岛素分泌的功能,并有助于降低血糖水平,从而展现出增加glp-1激活、抗炎等作用。
6.当由于药物、疾病、激素或酶缺乏等原因导致血糖水平下降时,胰腺中会产生胰高血糖素。胰高血糖素发出肝脏糖原分解的信号以诱导葡萄糖释放,并将血糖水平升高至正常水平。除了增加血糖水平的作用外,胰高血糖素还抑制动物和人类的食欲,并激活脂肪细胞的激素敏感脂肪酶,以促进脂肪分解和能量消耗,从而显示出抗肥胖效果。
7.因此,基于glp-1在控制血糖水平和减轻体重方面的作用,正在积极研究以开发glp-1作为治疗糖尿病和肥胖症的治疗剂。目前,正在开发由蜥蜴毒液制备并且与glp-1具有约50%的氨基酸同源性的毒蜥外泌肽-4作为治疗相同疾病类型的治疗剂。然而,据报道,含有glp-1和毒蜥外泌肽-4的治疗剂显示副作用,比如呕吐和恶心(syed y.y.,drugs,2015july;75(10):1141
–
52)。
8.因此,目前正在开发一种新物质,该物质可以高度激活glp-1、gip和胰高血糖素受体,并具有控制血糖水平和减轻体重的效果,而不会引起任何副作用,比如呕吐和恶心。此外,目前有一种新物质正在开发中,它与glp-1、gip和胰高血糖素受体具有不同的活性比率。例如,这种物质:其具有减轻体重的效果,但是由于高glp-1和gip活性而具有显著更高的控制血糖水平的效果,但是具有相对较低的胰高血糖素活性以达到降血糖效果;或这种物质:其对glp-1、gip和胰高血糖素中全部都具有高活性,因此具有显著高的减轻体重的效
果。
技术实现要素:
9.技术问题
10.需要开发一种稳定的液体制剂,其能够长期储存对已开发的胰高血糖素受体、glp-1受体和gip受体中全部都具有活性的肽的长效缀合物而不担心病毒污染。
11.技术方案
12.本发明的一个目的是提供一种胰高血糖素、glp-1和gip三重激动剂的长效缀合物的液体制剂。
13.本发明的另一个目的是提供一种用于制备液体制剂的方法。
14.有益效果
15.根据本发明的液体制剂具有通过在简单制剂中为具有大分子量的本发明的缀合物提供储存稳定性的经济优势。
附图说明
16.图1a和1b是基于实施例3的液体制剂(柠檬酸钠(ph 5.5)、甘露糖醇、聚山梨醇酯20、甲硫氨酸)确认根据缓冲剂类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性的结果。具体而言,将表9中所示的每种组成用作胰高血糖素、glp-1和gip三重激动剂的长效缀合物的液体制剂,并在25℃下储存6周后显示稳定性结果。
具体实施方式
17.实施本发明的一个方面提供了胰高血糖素、glp-1(胰高血糖素样肽-1)和gip(葡萄糖依赖性促胰岛素多肽)三重激动剂的长效缀合物的液体制剂。长效缀合物指其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽与免疫球蛋白fc片段通过接头共价结合的物质。
18.在一个实施方式中,本发明涉及对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物的液体制剂,其中液体制剂包括:药理学有效量的对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物;和i)缓冲剂,和ii)不含白蛋白的稳定剂,其包括糖醇、糖或其组合。长效缀合物可以指其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽与免疫球蛋白fc片段通过接头共价结合的物质。
19.在一个实施方式中,液体制剂是包括下述化学式1的长效缀合物;缓冲剂;和糖醇、糖或其组合的液体制剂:
20.[化学式1]
[0021]q–
la–z[0022]
在上述化学式1中,
[0023]
q是下述通式1的肽;
[0024]
l是包含乙二醇重复单元的接头;
[0025]
a是0或自然数,条件是当a是2或更大时,每个l是彼此独立的;
[0026]
z是免疫球蛋白fc片段;和
[0027]
–
表示共价键:
[0028]
[通式1]
[0029]
xaa1
–
aib
–
xaa3
–
gly
–
thr
–
phe
–
thr
–
ser
–
asp
–
xaa10
–
ser
–
xaa12
–
xaa13
–
xaa14
–
xaa15
–
glu
–
xaa17
–
xaa18
–
xaa19
–
lys
–
xaa21
–
phe
–
val
–
xaa24
–
trp
–
leu
–
leu
–
xaa28
–
xaa29
–
xaa30
–
r1(通式1,seq id no:47)
[0030]
在上述通式1中,
[0031]
在从n-末端开始第16位加下划线的谷氨酸(glu)和第20位加下划线的赖氨酸(lys)残基之间形成内酰胺环,
[0032]
xaa1是组氨酸、4-咪唑并乙酰基(ca)或酪氨酸;
[0033]
xaa3是谷氨酸或谷氨酰胺;
[0034]
xaa10是酪氨酸或半胱氨酸;
[0035]
xaa12是赖氨酸或异亮氨酸;
[0036]
xaa13是酪氨酸、丙氨酸或半胱氨酸;
[0037]
xaa14是亮氨酸或甲硫氨酸;
[0038]
xaa15是半胱氨酸或天冬氨酸;
[0039]
xaa17是精氨酸、异亮氨酸、半胱氨酸或赖氨酸;
[0040]
xaa18是丙氨酸、精氨酸或组氨酸;
[0041]
xaa19是丙氨酸、谷氨酰胺或半胱氨酸;
[0042]
xaa21是谷氨酸或天冬氨酸;
[0043]
xaa24是谷氨酰胺、天冬酰胺或天冬氨酸;
[0044]
xaa28是丙氨酸、天冬酰胺或天冬氨酸;
[0045]
xaa29是半胱氨酸、甘氨酸、谷氨酰胺、苏氨酸、谷氨酸或组氨酸;
[0046]
xaa30是半胱氨酸、甘氨酸、赖氨酸或组氨酸,或不存在;和
[0047]
r1是半胱氨酸、m
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:48)或m
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:49)或不存在,
[0048]
其中:
[0049]
m是cys或pro;和
[0050]
n是cys或gly,或不存在。aib是指氨基异丁酸。
[0051]
在根据前述任一个实施方式所述的液体制剂中,液体制剂是特征在于其包括下列的液体制剂:18nmol/ml至920nmol/ml的下述化学式1的长效缀合物;将液体制剂的ph维持在5.0至7.0的范围内的量的缓冲剂;和0.5%(w/v)至10%(w/v)的糖醇、糖或其组合。
[0052]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其可以进一步包括选自等渗剂、非离子表面活性剂和氨基酸的一种或多种组分。
[0053]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其不包括等渗剂。
[0054]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其不进一步包括选自非离子表面活性剂和氨基酸的一种或多种组分。
[0055]
在根据前述任一个实施方式所述的液体制剂中,肽的特征在于其包括选自seq id no:1至46的任一种氨基酸序列。
[0056]
在根据前述任一个实施方式所述的液体制剂中,肽的特征在于其包括选自seq id no:1、2、9、19、21至27、30至32或40至46的任一种氨基酸序列。
[0057]
在根据前述任一个实施方式所述的液体制剂中,肽的特征在于其包括选自seq id no:9、30至32或42至46的任一种氨基酸序列。
[0058]
在根据前述任一个实施方式所述的液体制剂中,肽的特征在于其进一步包括seq id no:9的氨基酸序列。
[0059]
在根据前述任一个实施方式所述的液体制剂中,r1的特征在于其是半胱氨酸、cys
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser(seq id no:50)、
[0060]
pro
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser(seq id no:51)、
[0061]
pro
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser
–
gly(seq id no:52)、pro
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser(seq id no:53)或
[0062]
pro
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser
–
cys(seq id no:54)或不存在。
[0063]
在根据前述任一个实施方式所述的液体制剂中,l的特征在于其是聚乙二醇。
[0064]
在根据前述任一个实施方式所述的液体制剂中,l中乙二醇重复单元部分的分子量的特征在于其在1kda至100kda的范围内。
[0065]
在根据前述任一个实施方式所述的液体制剂中,上述化学式1的结构的特征在于其由下述化学式2的结构表示:
[0066]
[化学式2]
[0067][0068]
这里,q和z如化学式1中所定义。
[0069]
在根据前述任一个实施方式所述的液体制剂中,乙二醇重复单元的特征在于其具有式[och2ch2]n,其中n为自然数,并且肽中[och2ch2]n区的平均分子量,例如数均分子量被确定为1kda至100kda。
[0070]
在根据前述任一个实施方式所述的液体制剂中,n值的特征在于其被确定为使肽中[och2ch2]n区的平均分子量,例如数均分子量为10kda。
[0071]
在根据前述任一个实施方式所述的液体制剂中,q的特征在于其在其c-末端被酰胺化。
[0072]
在根据前述任一个实施方式所述的液体制剂中,q的特征在于其经由肽中半胱氨酸的硫原子被连接。
[0073]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的特征在于其源自igg4。
[0074]
在根据前述任一个实施方式所述的液体制剂中,z的特征在于其具有其中两条多肽链通过分子间二硫键连接并且仅通过两条链中的一条中的氮原子连接的结构。
[0075]
在根据前述任一个实施方式所述的液体制剂中,z的特征在于其包括seq id no:
76的氨基酸序列的单体。
[0076]
在根据前述任一个实施方式所述的液体制剂中,z的特征在于其为seq id no:76的氨基酸序列的单体的同源二聚体。
[0077]
在根据前述任一个实施方式所述的液体制剂中,z的特征在于其通过在其n-末端的脯氨酸的氮原子连接。
[0078]
在根据前述任一个实施方式所述的液体制剂中,z(其为免疫球蛋白fc片段)和q的特征在于它们不是糖基化的。
[0079]
在根据前述任一个实施方式所述的液体制剂中,缓冲剂的特征在于其选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合。
[0080]
在根据前述任一个实施方式所述的液体制剂中,缓冲剂的特征在于其选自柠檬酸盐缓冲溶液、乙酸盐缓冲溶液、组氨酸缓冲溶液,以及其组合。
[0081]
在根据前述任一个实施方式所述的液体制剂中,缓冲剂的特征在于其是乙酸及其盐。
[0082]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的ph的特征在于其为5.0至5.5。
[0083]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的ph的特征在于其为5.0至6.5。
[0084]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的ph的特征在于其为5.1至6.0。
[0085]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的ph的特征在于其为5.1至5.5。
[0086]
在根据前述任一个实施方式所述的液体制剂中,缓冲剂的浓度的特征在于其为5mm至100mm,用于将液体制剂的ph维持在5.0至7.0的范围内。
[0087]
在根据前述任一个实施方式所述的液体制剂中,糖或糖醇的特征在于其是选自蔗糖、甘露糖醇和山梨糖醇中的一种或多种。
[0088]
在根据前述任一个实施方式所述的液体制剂中,糖或糖醇的特征在于其在制剂中以1%(w/v)至20%(w/v)的浓度存在。
[0089]
在根据前述任一个实施方式所述的液体制剂中,长效缀合物的特征在于其在制剂中以18nmol/ml至2,757nmol/ml、18nmol/ml至920nmol/ml、18nmol/ml至919nmol/ml、90nmol/ml至552nmol/ml、150nmol/ml至600nmol/ml、183nmol/ml至552nmol/ml、400nmol/ml至550nmol/ml或150nmol/ml至200nmol/ml的浓度存在。
[0090]
在根据前述任一个实施方式所述的液体制剂中,糖的特征在于其为葡萄糖、果糖、半乳糖、乳糖、麦芽糖、蔗糖或其组合。
[0091]
在根据前述任一个实施方式所述的液体制剂中,糖的特征在于其为蔗糖。
[0092]
在根据前述任一个实施方式所述的液体制剂中,糖醇的特征在于其为选自甘露糖醇和山梨糖醇中的一种或多种。
[0093]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其进一步包括选自非离子表面活性剂和氨基酸的一种或多种组分。
[0094]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其进一步包
括等渗剂。
[0095]
在根据前述任一个实施方式所述的液体制剂中,等渗剂的特征在于其是氯化钠。
[0096]
在根据前述任一个实施方式所述的液体制剂中,非离子表面活性剂的特征在于其以0.01%(w/v)至0.1%(w/v)的浓度包含。
[0097]
在根据前述任一个实施方式所述的液体制剂中,非离子表面活性剂的特征在于其为泊洛沙姆、聚山梨醇酯或其组合。
[0098]
在根据前述任一个实施方式所述的液体制剂中,非离子表面活性剂的特征在于其选自泊洛沙姆188、聚山梨醇酯20、聚山梨醇酯40、聚山梨醇酯60、聚山梨醇酯80,以及其组合。
[0099]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其进一步包括作为稳定剂的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的氨基酸。
[0100]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0101]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0102]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至6.5;
[0103]
1%(w/v)至10%(w/v)的糖醇、糖或其组合;
[0104]
0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和
[0105]
0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0106]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0107]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0108]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;
[0109]
4%(w/v)至10%(w/v)的糖;
[0110]
0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和
[0111]
0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0112]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0113]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0114]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.1至5.5;
[0115]
4%(w/v)至10%(w/v)的糖;和
[0116]
0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0117]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0118]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0119]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.1至5.5;和
[0120]
4%(w/v)至10%(w/v)的糖。
[0121]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0122]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0123]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;和
[0124]
4%(w/v)至10%(w/v)的糖。
[0125]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0126]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0127]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;
[0128]
4%(w/v)至10%(w/v)的糖;和
[0129]
0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0130]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0131]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0132]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;
[0133]
4%(w/v)至10%(w/v)的糖;和
[0134]
0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和
[0135]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于其包括:
[0136]
90nmol/ml至552nmol/ml的化学式1的肽缀合物;
[0137]
5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;
[0138]
4%(w/v)至10%(w/v)的糖;
[0139]
0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂;和
[0140]
0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂。
[0141]
在根据前述任一个实施方式所述的液体制剂中,氨基酸的特征在于其是甲硫氨酸。
[0142]
在根据前述任一个实施方式所述的液体制剂中,甲硫氨酸的特征在于其在制剂中以0.01mg/ml至1mg/ml的浓度存在。
[0143]
在根据前述任一个实施方式所述的液体制剂中,氨基酸的特征在于其是甲硫氨酸或精氨酸。
[0144]
在根据前述任一个实施方式所述的液体制剂中,甲硫氨酸或精氨酸的特征在于其在制剂中以0.01mg/ml至1mg/ml的浓度存在。
[0145]
在根据前述任一个实施方式所述的液体制剂中,液体制剂的特征在于当其在40℃
±
2℃和相对湿度75%
±
5%的苛刻试验条件下储存一周时具有透明外观。
[0146]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc区的特征在于其为igg-、iga-、igd-、ige-或igm-衍生的fc片段。
[0147]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc区的特征在于其选自(a)ch1结构域、ch2结构域、ch3结构域和ch4结构域;(b)ch1结构域和ch2结构域;(c)ch1
结构域和ch3结构域;(d)ch2结构域和ch3结构域;(e)ch1结构域、ch2结构域、ch3结构域和ch4结构域中的一个或两个或更多个结构域与免疫球蛋白铰链区或铰链区的一部分之间的组合,和(f)重链恒定区和轻链恒定区的每个结构域之间的二聚体。
[0148]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的每个结构域的特征在于其为具有不同来源的结构域的杂合体,所述不同来源源自选自igg、iga、igd、ige和igm的免疫球蛋白。
[0149]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的特征在于其为由单链免疫球蛋白组成的二聚体或多聚体的形式,该单链免疫球蛋白由相同来源的结构域组成。
[0150]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的特征在于其为igg4 fc片段。
[0151]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的特征在于其为人无糖基化的igg4 fc片段。
[0152]
在根据前述任一个实施方式所述的液体制剂中,免疫球蛋白fc片段的特征在于其为天然fc衍生物,包括:其中除去能够形成分子间二硫键的位点的修饰;除去其中天然fc的几个n-末端氨基酸的修饰;其中将甲硫氨酸残基添加到天然fc的n-末端的修饰;其中除去补体结合位点的修饰;其中除去抗体依赖性细胞介导的细胞毒性(adcc)位点的修饰,或其组合。
[0153]
实施本发明的另一个方面提供了用于制备液体制剂的方法。
[0154]
在一个实施方式中,本发明涉及用于制备长效缀合物的液体制剂的方法,其为根据前述任一个实施方式所述的液体制剂,方法包括:混合(a)对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物,其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc片段彼此连接,与(b)i)缓冲剂和ii)糖或糖醇。
[0155]
在根据前述任一个实施方式所述的方法中,液体制剂的特征在于其进一步包括选自等渗剂、非离子表面活性剂和氨基酸的一种或多种组分。具体实施方式
[0156][0157]
下文将对本发明进行更详细的描述。
[0158]
同时,本文公开的每个解释和示例性实施方式都可以适用于其他每个解释和示例性实施方式。即,本文公开的各种因素的所有组合属于本发明的范围。此外,本发明的范围不应受到下文提供的具体公开内容的限制。
[0159]
此外,本领域普通技术人员只需使用常规实验就能认识或证实本文所述的本发明的许多特定方面的等效物。此外,还意欲将这些等效物包括在本发明中。
[0160]
在本发明的整篇说明书中,不仅使用了天然存在的氨基酸的常规单字母和三字母编码,而且还使用了其他氨基酸通常允许的那些三字母编码,比如α-氨基异丁酸(aib)、sar(n-甲基甘氨酸)和α-甲基-谷氨酸等。此外,根据iupac-iub命名规则,本文提到的氨基酸被缩写如下:
[0161]
丙氨酸ala、a
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
精氨酸arg、r
[0162]
天冬酰胺asn、n
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
天冬氨酸asp、d
[0163]
半胱氨酸cys、c
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
谷氨酸glu、e
[0164]
谷氨酰胺gln、q
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
甘氨酸gly、g
[0165]
组氨酸his、h
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
异亮氨酸ile、i
[0166]
亮氨酸leu、l
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
赖氨酸lys、k
[0167]
甲硫氨酸met、m
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
苯丙氨酸phe、f
[0168]
脯氨酸pro、p
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
丝氨酸ser、s
[0169]
苏氨酸thr、t
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
色氨酸trp、w
[0170]
酪氨酸tyr、y
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
缬氨酸val、v
[0171]
实施本发明的一个方面提供胰高血糖素、glp-1(胰高血糖素样肽-1)和gip(葡萄糖依赖性促胰岛素多肽)三重激动剂的长效缀合物的液体制剂。
[0172]
具体地,本发明涉及对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物的液体制剂,包括:对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物,其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc片段以药学上有效的量连接;以及缓冲剂;以及糖醇、糖或其组合。
[0173]
具体地,本发明提供了一种液体制剂,其包括:下述化学式1的长效缀合物;缓冲剂;和糖醇、糖或其组合:
[0174]
[化学式1]
[0175]q–
la–z[0176]
在上述化学式1中,
[0177]
q是下述通式1的肽;
[0178]
l是包含乙二醇重复单元的接头;
[0179]
a是0或自然数,条件是当a是2或更大时,每个l是彼此独立的;
[0180]
z是免疫球蛋白fc片段;和
[0181]
–
表示共价键:
[0182]
[通式1]
[0183]
xaa1
–
aib
–
xaa3
–
gly
–
thr
–
phe
–
thr
–
ser
–
asp
–
xaa10
–
ser
–
xaa12
–
xaa13
–
xaa14
–
xaa15
–
glu
–
xaa17
–
xaa18
–
xaa19
–
lys
–
xaa21
–
phe
–
val
–
xaa24
–
trp
–
leu
–
leu
–
xaa28
–
xaa29
–
xaa30
–
r1(通式1,seq id no:47)
[0184]
在上述通式1中,
[0185]
在从n-末端开始第16位加下划线的谷氨酸(glu)和第20位加下划线的赖氨酸(lys)残基之间形成内酰胺环,其中
[0186]
xaa1是组氨酸、4-咪唑并乙酰基(ca)或酪氨酸;
[0187]
xaa3是谷氨酸或谷氨酰胺;
[0188]
xaa10是酪氨酸或半胱氨酸;
[0189]
xaa12是赖氨酸或异亮氨酸;
[0190]
xaa13是酪氨酸、丙氨酸或半胱氨酸;
[0191]
xaa14是亮氨酸或甲硫氨酸;
[0192]
xaa15是半胱氨酸或天冬氨酸;
[0193]
xaa17是精氨酸、异亮氨酸、半胱氨酸或赖氨酸;
[0194]
xaa18是丙氨酸、精氨酸或组氨酸;
[0195]
xaa19是丙氨酸、谷氨酰胺或半胱氨酸;
[0196]
xaa21是谷氨酸或天冬氨酸;
[0197]
xaa24是谷氨酰胺、天冬酰胺或天冬氨酸;
[0198]
xaa28是丙氨酸、天冬酰胺或天冬氨酸;
[0199]
xaa29是半胱氨酸、甘氨酸、谷氨酰胺、苏氨酸、谷氨酸或组氨酸;
[0200]
xaa30是半胱氨酸、甘氨酸、赖氨酸或组氨酸,或不存在;和
[0201]
r1是半胱氨酸、m
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:48)或m
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:49)或不存在,
[0202]
其中:
[0203]
m是cys或pro;和
[0204]
n是cys或gly,或不存在。
[0205]
如在本文中使用的,术语“液体制剂”是指配制成液体形式的药物,并且旨在包括所有内部使用的液体制剂和外部使用的制剂。
[0206]
本发明的液体制剂包括显示药理作用的化学式1的长效缀合物,和当其被配制为液体形式时能够将显示药理作用的缀合物稳定维持和/或储存一定时间段的物质。除了化学式1的长效缀合物之外,还可以将所包括的展现液体制剂的药理作用的组分与稳定剂互换使用。
[0207]
在本发明的化学式1的长效缀合物的液体制剂中,储存稳定性对于确保精确的剂量很重要。
[0208]
证实了通过包括特定浓度的化学式1的长效缀合物(其为展现出药理作用的物质);将ph维持在5.0至7.0的范围内的量的缓冲剂;和0.5%(w/v)至10%(w/v)的糖醇、糖或其组合,化学式1的长效缀合物即使在长时间储存时也是稳定的,从而提供本发明的新型制剂。
[0209]
包括在本发明的液体制剂中的对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物的浓度可以是18nmol/ml至1,840nmol/ml,但不限于此。
[0210]
在一个实施方式中,长效缀合物的浓度可以是18nmol/ml至920nmol/ml,但不限于此。
[0211]
如在本文中使用的,术语“稳定剂”是指将制剂中诸如活性成分的组分稳定地维持特定时间段的物质。本发明的稳定剂优选地不含白蛋白。可用作蛋白质稳定剂的人血清白蛋白由人血液制备,并且因此可能被人类致病病毒污染,并且明胶或牛血清白蛋白可能会在一些患者中引起疾病或可能会引起过敏反应。本发明的无白蛋白稳定剂不含外源蛋白比如人或动物血清白蛋白或纯化的明胶,并且因此不容易受到病毒感染。
[0212]
在本发明中,稳定剂具体是指使胰高血糖素、glp-1和gip三重激动剂的长效缀合物稳定地储存的物质。在胰高血糖素、glp-1和gip三重激动剂的长效缀合物中,储存稳定性不仅对确保精确很重要,而且对于抑制针对胰高血糖素、glp-1和gip三重激动剂的缀合物的抗原物质的潜在生成也很重要。
[0213]
缓冲剂(其为包括在本发明的液体制剂中的一种组分)可以维持溶液的ph,使得液体制剂的ph不快速改变,以使化学式1的长效缀合物稳定。缓冲剂也可以被称为缓冲系统,
并且缓冲剂或缓冲系统用于维持液体制剂的ph。可以没有限制地使用能够维持可以稳定化学式1的长效缀合物的ph的缓冲剂,该缀合物为稳定的目标材料。
[0214]
缓冲剂可以是ph缓冲液,包括磷酸和其共轭碱(即,碱金属盐比如磷酸盐:磷酸钠、磷酸钾或其氢盐或二氢盐)、柠檬酸及其盐(例如,柠檬酸钠)、乙酸及其盐(例如,乙酸钠)或组氨酸及其盐,并且还可以使用这些缓冲液的混合物,但是缓冲剂不限于此。
[0215]
本发明的液体制剂可以包括含有缓冲剂的缓冲溶液作为液体制剂的溶剂,具体地,缓冲溶液可以选自柠檬酸盐缓冲溶液(例如,柠檬酸钠缓冲溶液)、乙酸盐缓冲溶液(例如,乙酸钠缓冲溶液)、磷酸盐缓冲溶液(例如,磷酸钠缓冲溶液)、组氨酸缓冲溶液,以及其组合。此外,可以以足以维持液体制剂的目标ph的浓度包含液体制剂中的缓冲溶液或缓冲剂(柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐、或其组合)。
[0216]
液体制剂的ph可以在约5.0至约7.0,例如约5.0至约6.8、约5.0至约6.7、约5.0至约6.6、约5.0至约6.5、约5.0至约6.4、约5.0至约6.3、约5.0至约6.2、约5.0至约6.1、约5.0至6.0、约5.0至约5.9、约5.0至5.8、约5.0至约5.7、约5.0至约5.6、约5.0至约5.5、约5.0至约5.4、约5.0至约5.3、约5.0至约5.2、约5.1至约7.0,例如约5.1至约6.8、约5.1至约6.7、约5.1至约6.6、约5.1至约6.5、约5.1至约6.4、约5.1至约6.3、约5.1至约6.2、约5.1至约6.1、约5.1至6.0、约5.1至约5.9、约5.1至5.8、约5.1至约5.7、约5.1至约5.6、约5.1至约5.5、约5.1至约5.4、约5.1至约5.3、约5.1至约5.2,或约5.0、5.1、5.2、5.3、5.4、5.5、5.6、5.7、5.8、5.9、6.0、6.1、6.2、6.3、6.4、6.5、6.6、6.7、6.8、6.9或7.0的范围内,但不特别限于此。
[0217]
达到目标ph的液体制剂的浓度可以为约1mm至约200mm,更具体地约5mm至约100mm、约5mm至约80mm、约5mm至约40mm、约8mm至约40mm、约5mm至约30mm或约5mm至约25mm、约10mm至约25mm、约15mm至约25mm、约18mm至约24mm、约18mm至约22mm或约20mm,但不特别限于此。
[0218]
在一个实施方式中,缓冲剂可以是乙酸及其盐,但不限于此。
[0219]
在另一个实施方式中,缓冲溶液可以是乙酸盐缓冲溶液(例如,乙酸钠缓冲溶液)或柠檬酸盐缓冲溶液(例如,柠檬酸钠缓冲溶液),但不特别限于此。
[0220]
同时,在制备液体制剂中,将各组分溶解在水(例如,wfi)中,并且可以使用hcl和/或naoh等将缓冲溶液或制剂的ph调解至所需的ph,这是本领域已经常用的方法。因此,即使权利要求书中没有另外提及ph调节剂,本领域技术人员也会理解,通过这种方法,制剂可以具有调节的ph。
[0221]
糖醇(其为包括在本发明的稳定剂中的一种组分)是指含有多个羟基的物质,并且可以以包括其中糖的醛基和/或酮基被醇基取代的物质,以及含有多个羟基的糖。糖或糖醇可以增加胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。例如,糖醇可以是选自甘露糖醇和山梨糖醇的一种或多种,但不限于此。
[0222]
糖(其为包括在本发明的液体制剂中的一种组分)指单糖、二糖、多糖、寡糖等,并且可以增加对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物的稳定性。具体实例可以包括单糖比如甘露糖、葡萄糖、果糖、半乳糖、岩藻糖和木糖;二糖比如乳糖、麦芽糖和蔗糖;和多糖比如棉子糖和葡聚糖,但不限于此。
[0223]
在一个实施方式中,糖可以是葡萄糖、果糖、半乳糖、乳糖、麦芽糖、蔗糖或其组合,但不限于此。
[0224]
例如,糖可以是蔗糖,但不特别限于此。
[0225]
相对于液体制剂的总溶液,糖醇、糖或其组合可以以约0.5%(w/v)至约20%(w/v)、约0.5%(w/v)至约10%(w/v)、约0.5%(w/v)至约6%(w/v)、约1%(w/v)至约20%(w/v)、约1%(w/v)至15%(w/v)、约2%(w/v)至约15%(w/v)、约2%(w/v)至约12%(w/v)、约2%(w/v)至约12%(w/v)、约3%(w/v)至约10%(w/v)、约4%(w/v)至约10%(w/v)、约4%(w/v)至约6%(w/v),约5%(w/v)至约10%(w/v)、约6%(w/v)至约10%(w/v)、约7%(w/v)至约10%(w/v)、约7%(w/v)至约9%(w/v)、约8%(w/v)至约9%(w/v)或约1.0%(w/v)、约3.0%(w/v)、约5.0%(w/v)或约8.0%(w/v)的浓度存在,但不特别限于此。
[0226]
此外,液体制剂可以进一步包括选自等渗剂、非离子表面活性剂和氨基酸的一种或多种组分,但不特别限于此。
[0227]
因此,液体制剂的稳定剂可以基本上由i)缓冲剂和ii)糖或糖醇组成,而且还可以基本上由以下组成:i)缓冲剂、ii)糖或糖醇和iii)非离子表面活性剂;i)缓冲剂、ii)糖或糖醇和iii)等渗剂;i)缓冲剂、ii)糖或糖醇、iii)氨基酸和iv)非离子表面活性剂;i)缓冲剂、ii)糖或糖醇和iii)氨基酸;i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂和iv)等渗剂;i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂和iv)氨基酸;i)缓冲剂、ii)糖或糖醇、iii)等渗剂和iv)氨基酸;或i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂、iv)等渗剂和v)氨基酸、但不特别限于此。这里,很明显上面或下面描述的所有内容都适用于构成稳定剂的每种组分的类型、浓度或ph。
[0228]
尽管不特别限于此,非离子表面活性剂(其为包括在液体制剂中的一种组分)降低蛋白质溶液的表面张力,从而防止蛋白质在疏水表面的吸附或聚集。
[0229]
可用于本发明的非离子表面活性剂的具体实例可以包括聚山梨醇酯(例如,聚山梨醇酯20(聚氧乙烯(20)失水山梨醇单月桂酸酯)、聚山梨醇酯40(聚氧乙烯(20)失水山梨醇单棕榈酸酯)、聚山梨醇酯60(聚氧乙烯(20)失水山梨醇单硬脂酸酯)、聚山梨醇酯80(聚氧乙烯(20)失水山梨醇单油酸酯)(聚氧乙烯基团后面的数值20是指氧乙烯基团
–
(ch2ch2o)
–
)的总数);泊洛沙姆(peo
–
ppo
–
peo共聚物;peo:聚(环氧乙烷),ppo:聚(环氧丙烷))、聚乙二醇
–
聚丙二醇、聚氧乙烯化合物(例如,聚氧乙烯
–
硬脂酸酯,聚氧乙烯烷基醚(烷基:c1–c30
)、聚氧乙烯单烯丙基醚、烷基苯基聚氧乙烯共聚物(烷基:c1–c30
)等)、十二烷基硫酸钠(sds)等、或聚山梨醇酯或泊洛沙姆。这些也可以单独使用或其两种或更多种组合使用。
[0230]
具体地,非离子表面活性剂可以是聚山梨醇酯80、聚山梨醇酯60、聚山梨醇酯40、聚山梨醇酯20或泊洛沙姆188,并且这些可以组合使用,但不特别限于此。
[0231]
在本发明中,优选地不包含高浓度的非离子表面活性剂,并且具体地,在本发明的制剂中所包含的非离子表面活性剂的浓度可以为约0.2%(w/v)或更低,例如约0.001%(w/v)至约0.2%(w/v)、约0.001%(w/v)至约0.1%(w/v)、约0.001%(w/v)至约0.05%(w/v)、约0.005%(w/v)至约0.08%(w/v)、约0.002%(w/v)至约0.05%(w/v)、约0.005%(w/v)至约0.05%(w/v)、约0.01%(w/v)至约0.05%(w/v)、约0.01%(w/v)至约0.04%(w/v)、约0.01%(w/v)至约0.03%(w/v)、约0.01%(w/v)至约0.1%(w/v)或约0.02%(w/v),但是浓度不特别限于此。
[0232]
氨基酸(作为可以添加到液体制剂的任选组分的稳定剂类型)可以是甲硫氨酸、精
氨酸、甘氨酸或其组合,但不限于此。此外,氨基酸可以是l-形式,但不特别限于此。氨基酸可以是甲硫氨酸或精氨酸。此外,甲硫氨酸可以是l-甲硫氨酸,并且精氨酸可以是l-精氨酸,但不特别限于此。
[0233]
氨基酸可以抑制由于蛋白质的氧化反应而可能发生的杂质生成,但不特别限于此。
[0234]
氨基酸可以以约0.01mg/ml至约1mg/ml、约0.01mg/ml至约0.8mg/ml、约0.01mg/ml至约0.5mg/ml、约0.02mg/ml至约0.5mg/ml或约0.02mg/ml至约0.4mg/ml或约0.1mg/ml的浓度存在于制剂中,但不特别限于此。
[0235]
在一个实施方式中,液体制剂包括缓冲剂,并且糖或糖醇可以包括或可以不包括等渗剂,并且可以不进一步包括选自非离子表面活性剂和氨基酸的一种或多种组分,但不限于此。
[0236]
等渗剂是指可以控制渗透压的物质。当将根据本发明的液体制剂施用到身体时,等渗剂可用于适当地维持渗透压。
[0237]
等渗剂的代表性实例可以包括作为水溶性无机盐的氯化钠、硫酸钠或柠檬酸钠,具体地氯化钠,但不特别限于此。这种无机盐可以是进一步包括在上述稳定剂中的任选的组分,并且不特别限于此。此外,上述稳定剂可用作等渗剂。
[0238]
根据本发明的制剂中的等渗剂的浓度可以是0mm至约200mm、0mm至约150mm、0mm至约100mm、约10mm至约200mm、约10mm至约150mm、约10mm至约100mm、约10mm至约50mm、约20mm至约100mm、约40mm至约110mm、约20mm至约80mm、约20mm至约50mm、约20mm至约30mm或约40mm至约50mm、约40mm至约60mm或约90mm至约110mm,但不特别限于此。
[0239]
同时,除了糖醇、糖或其组合;和缓冲剂(其为上述液体制剂的基本组分);和非离子表面活性剂和氨基酸(其为任选地组分)之外,本发明的液体制剂可以任选地进一步包括在不损害本发明的效果的范围内的本领域已知的其他组分或材料,但不限于此。
[0240]
同时,液体制剂可以进一步包括多元醇,但不特别限于此。
[0241]
例如,液体制剂可以包括i)缓冲剂和ii)糖或糖醇以及多元醇,并且可以进一步在基本上由以下组成的稳定剂中包括多元醇:i)缓冲剂、ii)糖或糖醇和iii)非离子表面活性剂;i)缓冲剂、ii)糖或糖醇和iii)等渗剂;i)缓冲剂、ii)糖或糖醇、iii)氨基酸和iv)非离子表面活性剂;i)缓冲剂、ii)糖或糖醇和iii)氨基酸;i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂和iv)等渗剂;i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂和iv)氨基酸;i)缓冲剂、ii)糖或糖醇、iii)等渗剂和iv)氨基酸;或i)缓冲剂、ii)糖或糖醇、iii)非离子表面活性剂、iv)等渗剂和v)氨基酸,但不特别限于此。
[0242]
可以进一步包括在本发明的液体制剂中的多元醇的实例可以包括丙二醇和低分子量聚乙二醇、甘油、低分子量聚丙二醇等,并且这些可以以其一种或两种或更多种组合使用,但不限于此。
[0243]
在本发明中,化学式1的长效缀合物为包括在本发明的液体制剂中的活性成分,并且可以以药学上有效的量包括在其中。例如,制剂中的长效缀合物的浓度可以为约18nmol/ml至约2,800nmol/ml、约18nmol/ml至约2,757nmol/ml、约18nmol/ml至约2,576nmol/ml、约18nmol/ml至约2,392nmol/ml、约18nmol/ml至约2,208nmol/ml、约18nmol/ml至约2,024nmol/ml、约18nmol/ml至约1,840nmol/ml、约18nmol/ml至约1,656nmol/ml、约18nmol/
ml至约1,472nmol/ml、约18nmol/ml至约1,288nmol/ml、约18nmol/ml至约1,104nmol/ml、约18nmol/ml至约920nmol/ml、约18nmol/ml至约919nmol/ml、约18nmol/ml至约828nmol/ml、约18nmol/ml至约740nmol/ml、约18nmol/ml至约736nmol/ml、约18nmol/ml至约644nmol/ml、约18nmol/ml至约552nmol/ml、约18nmol/ml至约460nmol/ml、约18nmol/ml至约368nmol/ml、约18nmol/ml至约276nmol/ml、约18nmol/ml至约184nmol/ml、约18nmol/ml至约92nmol/ml、约90nmol/ml、约552nmol/ml、约90nmol/ml、约600nmol/ml、约450nmol/ml、约600nmol/ml、约500nmol/ml、约600nmol/ml、约530nmol/ml、约580nmol/ml、约183nmol/ml、约184nmol/ml、约183.79nmol/ml、约183.8nmol/ml、约183nmol/ml至约276nmol/ml、约183nmol/ml至约386nmol/ml、约183nmol/ml至约460nmol/ml、约183nmol/ml至约552nmol/ml、约183nmol/ml至约560nmol/ml、约183nmol/ml至约644nmol/ml、约183nmol/ml至约736nmol/ml、约183nmol/ml至约740nmol/ml、约551nmol/ml、约552nmol/ml、约551.37nmol/ml、约551.4nmol/ml、约150nmol/ml至约200nmol/ml、约170nmol/ml至约200nmol/ml,但不特别限于此。
[0244]
如在本文中使用的,术语“约”是指包括所有的
±
0.5、
±
0.4、
±
0.3、
±
0.2、
±
0.1等的范围,并且包括与这些值后面的值相当或相似的所有值,但是范围不限于此。
[0245]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:化学式1的肽缀合物;选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;糖;选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0246]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至6.5;1%(w/v)至10%(w/v)的糖醇、糖或其组合;0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0247]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;4%(w/v)至10%(w/v)的糖;0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂;和0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0248]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.1至5.5;4%(w/v)至10%(w/v)的糖;和0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0249]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.1至5.5;和4%(w/v)至10%(w/v)的糖。
[0250]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/
ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.1至5.5;和4%(w/v)至10%(w/v)的糖。
[0251]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;和4%(w/v)至10%(w/v)的糖。
[0252]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;4%(w/v)至10%(w/v)的糖;和0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂。
[0253]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;4%(w/v)至10%(w/v)的糖;和0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂。
[0254]
在一个实施方式中,液体制剂可以是含有以下的液体制剂:90nmol/ml至552nmol/ml的化学式1的肽缀合物;5mm至25mm的选自柠檬酸及其盐、乙酸及其盐、组氨酸及其盐、磷酸及其盐以及其组合的缓冲剂,使得液体制剂的ph为5.0至5.5;4%(w/v)至10%(w/v)的糖;0.01mg/ml至1mg/ml的选自精氨酸、甘氨酸、甲硫氨酸以及其组合的稳定剂;和0.01%(w/v)至0.1%(w/v)的选自泊洛沙姆、聚山梨醇酯或其组合的非离子表面活性剂。
[0255]
当在40℃
±
2℃和相对湿度75%
±
5%的苛刻试验条件下储存一周时,液体制剂可以具有透明的外观。
[0256]
如在本文中使用的,术语“压力测试”是指旨在确定药物稳定性基本特征的测试。它是在药物开发期间进行的,并且在比加速测试更苛刻的条件下进行,并且有助于确定药物的预期降解产物和物理变化。
[0257]
同时,下文将更详细地描述对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物,其为包括在本发明的液体制剂中的活性成分。
[0258]
如在本文中使用的,术语“对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物”为包括在本发明的液体制剂中的活性成分,并且可以以药理学有效量包括在制剂中。长效缀合物可以是其中免疫球蛋白fc片段与对胰高血糖素受体、glp-1受体和gip受体具有活性的肽缀合的形式。
[0259]
与没有与免疫球蛋白缀合的肽相比,缀合物可以展现出增加的药效持续时间,并且在本发明中,根据通式1的肽的化学式1的缀合物被称为“长效缀合物”,并且可以与“长效三重激动剂缀合物”、“肽缀合物”或“化学式1的长效缀合物”互换使用。
[0260]
在一个实施方式中,免疫球蛋白fc片段和q可以不是糖基化的,但不限于此。
[0261]
同时,缀合物可以是非天然存在的。
[0262]
本发明的长效缀合物可以是其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc片段彼此连接的形式,并且连接方法不特别限于此,但是肽和免疫
球蛋白fc片段可以通过接头彼此连接。
[0263]
在一个实施方式中,本发明的长效缀合物具有下述化学式1的结构。
[0264]
[化学式1]
[0265]q–
la–z[0266]
在上述化学式1中,
[0267]
q是下述通式1的肽;
[0268]
l是包含乙二醇重复单元的接头;
[0269]
a是0或自然数,条件是当a是2或更大时,每个l是彼此独立的;
[0270]
z是免疫球蛋白fc片段;和
[0271]
–
表示共价键。
[0272]
化学式1的长效缀合物的q可以是对胰高血糖素受体、glp-1受体和gip受体具有活性的肽。“对胰高血糖素受体、glp-1受体和gip受体具有活性的肽”包括对胰高血糖素受体、glp-1受体和gip受体具有显著活性水平的各种物质,例如,各种肽。
[0273]
尽管其不特别限于此,对胰高血糖素受体、glp-1受体和gip受体具有显著活性水平的肽可以与“三重激动剂”互换使用。
[0274]
更具体地,上述化学式1的q(其为对胰高血糖素受体、glp-1受体和gip受体具有活性的肽)可以是包括下述通式1的序列的对胰高血糖素受体、glp-1受体和gip受体具有活性的肽:
[0275]
[通式1]
[0276]
xaa1
–
aib
–
xaa3
–
gly
–
thr
–
phe
–
thr
–
ser
–
asp
–
xaa10
–
ser
–
xaa12
–
xaa13
–
xaa14
–
xaa15
–
glu
–
xaa17
–
xaa18
–
xaa19
–
lys
–
xaa21
–
phe
–
val
–
xaa24
–
trp
–
leu
–
leu
–
xaa28
–
xaa29
–
xaa30
–
r1(通式1,seq id no:47)
[0277]
在上述通式1中,
[0278]
在从n-末端开始第16位加下划线的谷氨酸(glu)和第20位加下划线的赖氨酸(lys)残基之间形成内酰胺环,其中
[0279]
xaa1是组氨酸、4-咪唑并乙酰基(ca)或酪氨酸;
[0280]
xaa3是谷氨酸或谷氨酰胺;
[0281]
xaa10是酪氨酸或半胱氨酸;
[0282]
xaa12是赖氨酸或异亮氨酸;
[0283]
xaa13是酪氨酸、丙氨酸或半胱氨酸;
[0284]
xaa14是亮氨酸或甲硫氨酸;
[0285]
xaa15是半胱氨酸或天冬氨酸;
[0286]
xaa17是精氨酸、异亮氨酸、半胱氨酸或赖氨酸;
[0287]
xaa18是丙氨酸、精氨酸或组氨酸;
[0288]
xaa19是丙氨酸、谷氨酰胺或半胱氨酸;
[0289]
xaa21是谷氨酸或天冬氨酸;
[0290]
xaa24是谷氨酰胺、天冬酰胺或天冬氨酸;
[0291]
xaa28是丙氨酸、天冬酰胺或天冬氨酸;
[0292]
xaa29是半胱氨酸、甘氨酸、谷氨酰胺、苏氨酸、谷氨酸或组氨酸;
[0293]
xaa30是半胱氨酸、甘氨酸、赖氨酸或组氨酸,或不存在;和
[0294]
r1是半胱氨酸、m
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:48)或m
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser
–
n(seq id no:49)或不存在,
[0295]
其中:
[0296]
m是cys或pro;和
[0297]
n是cys或gly,或不存在。
[0298]
上述通式1的aib是指氨基异丁酸。
[0299]
在本说明书中,“aib”可以与“2-氨基异丁酸”或“氨基异丁酸”互换使用,并且2-氨基异丁酸和氨基异丁酸可以彼此互换使用。
[0300]
肽可以包括选自seq id no:1至46的氨基酸序列或(基本上)由选自seq id no:1至46的氨基酸序列组成,但不限于此。
[0301]
这种肽的实例包括包含选自seq id no:1、2、9、19、21至27、30至32或40至46的氨基酸序列或(基本上)由其组成的肽,但是不特别限于此。在另一个实例中,肽可以是包括选自seq id no:9、30至32或42至46的氨基酸序列或(基本上)由其组成的肽,或它可以是包括seq id no:9的氨基酸序列或(基本上)由其组成的肽,但不特别限于此。
[0302]
此外,上述通式1中的r1可以是cys
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser(seq id no:50)、pro
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser(seq id no:51)、pro
–
ser
–
ser
–
gly
–
ala
–
pro
–
pro
–
pro
–
ser
–
gly(seq id no:52)、pro
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser(seq id no:53)或pro
–
ser
–
ser
–
gly
–
gln
–
pro
–
pro
–
pro
–
ser
–
cys(seq id no:54)或可以不存在,但是不特别限于此。
[0303]
此外,对胰高血糖素受体、glp-1受体和gip受体具有活性的肽可以包括分子内桥,例如,共价桥或非共价桥,并且具体地,可以是包括环的形式。它可以是其中在第16位的谷氨酸和第20位的赖氨酸残基之间形成环的形式,其在上述通式1中加了下划线,但不特别限于此。环的非限制性实例可以包括内酰胺桥(或内酰胺环)。
[0304]
此外,根据本发明的肽可以包括肽本身、其盐(例如,肽的药学上可接受的盐)或其溶剂化物的形式的所有那些。此外,肽可以是任何药学上可接受的形式。
[0305]
盐的种类没有特别限制。然而,盐优选地为对受试者(例如,哺乳动物)安全且有效的盐,但不特别限于此。
[0306]
术语“药学上可接受的”是指在药物医学决策的范围内可有效地用于预定用途,而不会引起过度的毒性、刺激、过敏反应等的材料。
[0307]
如在本文中使用的,术语“药学上可接受的盐”是指源自药学上可接受的无机酸、有机酸或碱的盐。合适的盐的实例可以包括盐酸、溴酸、硫酸、硝酸、高氯酸、富马酸、马来酸、磷酸、乙醇酸、乳酸、水杨酸、琥珀酸、甲苯-对-磺酸、酒石酸、乙酸、柠檬酸、甲烷磺酸、甲酸、苯甲酸、丙二酸、萘-2-磺酸、苯磺酸等。源自合适的碱的盐的实例可以包括碱金属比如钠、钾等;碱土金属比如镁;铵等。
[0308]
如在本文中使用的,术语“溶剂化物”是指根据本发明的肽或其盐与溶剂分子之间形成的复合物。
[0309]
此外,尽管在本发明中被描述为“由特定seq id no组成的肽”,但是不排除相应的seq id no的氨基酸序列的上游或下游的无意义的序列,或可能天然发生的突变,或其沉默
突变,只要该肽具有与由相应seq id no的氨基酸序列组成的肽相同或相应的活性,并且即使在存在序列添加或突变时也显然属于本发明的范围。
[0310]
同时,肽可以是非天然存在的。
[0311]
肽的c-末端可以是酰胺化的肽或具有游离羧基(
–
cooh)的肽或可以包括具有未修饰的c-末端的肽,但不限于此。
[0312]
在一个实施方式中,q可以在c-末端被酰胺化,但不限于此。
[0313]
在一个实施方式中,q可以是非糖基化的,但不限于此。
[0314]
本发明的通式1的肽可以通过固相合成方法合成,可以通过重组方法生产,并且可以通过商业上生产,但不限于此。
[0315]
如在本文中使用的,术语“化学式1的长效缀合物”为包括在本发明的液体制剂中的活性成分,可以以药理学有效的量包括在液体制剂中。具体地,缀合物为其中对对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc区通过接头彼此连接的形式,并且可以展现出与没有与免疫球蛋白fc区连接的对胰高血糖素受体、glp-1受体和gip受体具有活性的肽相比增强的药效持续时间。
[0316]
此外,在化学式1的长效缀合物中,q(对胰高血糖素受体、glp-1受体和gip受体具有活性的肽)和免疫球蛋白fc片段之间的连接可以通过物理或化学键、非共价或共价键,并且具体地共价键来实现,但不限于此。
[0317]
此外,在化学式1的肽缀合物中,连接q(对胰高血糖素受体、glp-1受体和gip受体具有活性的肽)和免疫球蛋白fc片段的方法没有特别限制,但是对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc片段可以通过接头彼此连接。
[0318]
具体地,包括在本发明的液体制剂中的长效缀合物可以是由上述化学式1表示的缀合物。
[0319]
在上述化学式1中,q和z可以通过l以共价键彼此连接。
[0320]
更具体地,q和l,以及l和z可以通过共价键彼此连接,并且具体而言,缀合物可以是其中q、l和z通过共价键按化学式1的顺序彼此连接的缀合物。
[0321]
此外,q可以与z直接连接(即,在上述化学式1中a是0)或者可以通过接头(l)连接。
[0322]
在一个实施方式中,la(其为化学式1的长效缀合物的一种组分)可以是包含乙二醇重复单元的接头,例如(聚乙二醇),并且此外,那些在本领域已知的衍生物和可以在本领域技术人员的技术水平下容易制备的衍生物包括在本发明的范围内。
[0323]
l(其为包含乙二醇重复单元的接头)可以在末端包括官能团,其用于制备缀合物,然后将其形成为缀合物。根据本发明的长效缀合物可以是其中q和z通过官能团连接的形式,但不限于此。在本发明中,含有乙二醇重复单元的接头可以包括两个或三个或更多个官能团,并且每个官能团可以是彼此相同或不同的,但不限于此。
[0324]
具体地,接头可以是由下述化学式3表示的聚乙二醇(peg),但不限于此:
[0325]
[化学式3]
[0326][0327]
其中n是10至2,400,n是10至480,或n是50至250,但是n的范围不限于此。
[0328]
在上述长效缀合物中,peg部分不仅可以包括
–
(ch2ch2o)n–
结构,而且还可以包括插入连接元素和
–
(ch2ch2o)n–
结构之间的氧原子,但是peg部分不限于此。
[0329]
聚乙二醇是包括所有形式的乙二醇均聚物、peg共聚物和单甲基取代的peg聚合物(mpeg)(但不特别限于此)的通用术语。
[0330]
在一个实施方式中,乙二醇重复单元可以由例如[och2ch2]n表示,并且n值为自然数,并且肽缀合物中[och2ch2]n区的平均分子量,例如数均分子量,可以确定为大于0kda至约100kda,但不限于此。在另一个实例中,n值为自然数,并且肽缀合物中[och2ch2]n区的平均分子量,例如数均分子量,可以为约1kda至约100kda、约1kda至约80kda、约1kda至约50kda、约1kda至约30kda、约1kda至约25kda、约1kda至约20kda、约1kda至约15kda、约1kda至约13kda、约1kda至约11kda、约1kda至约10kda、约1kda至约8kda、约1kda至约5kda、约1kda至约3.4kda、约3kda至约30kda、约3kda至约27kda、约3kda至约25kda、约3kda至约22kda、约3kda至约20kda、约3kda至约18kda、约3kda至约16kda、约3kda至约15kda、约3kda至约13kda、约3kda至约11kda、约3kda至约10kda、约3kda至约8kda、约3kda至约5kda、约3kda至约3.4kda、约8kda至约30kda、约8kda至约27kda、约8kda至约25kda、约8kda至约22kda、约8kda至约20kda、约8kda至约18kda、约8kda至约16kda、约8kda至约15kda、约8kda至约13kda、约8kda至约11kda、约8kda至约10kda、约9kda至约15kda、约9kda至约14kda、约9kda至约13kda、约9kda至约12kda、约9kda至约11kda、约9.5kda至约10.5kda或约10kda,但不限于此。
[0331]
在一个实施方式中,接头的两端可以与免疫球蛋白fc区的硫醇基、氨基或羟基结合,并且可以与通式1的肽的硫醇基、氨基、叠氮基或羟基结合。
[0332]
具体地,接头可以包括能够在两端与免疫球蛋白fc和通式1的肽中的每一个结合的反应性基团。具体地,接头可以包括可以与半胱氨酸的硫醇基;位于赖氨酸、精氨酸、谷氨酰胺和/或组氨酸的n-末端的氨基;和/或位于免疫球蛋白fc片段中的c-末端并且可以与半胱氨酸的硫醇基结合的羟基;赖氨酸、精氨酸、谷氨酰胺和/或组氨酸的氨基;叠氮基-赖氨酸的叠氮基;和/或通式1的肽中的羟基结合的反应性基团,但是反应性基团不限于此。
[0333]
更具体地,接头的反应性基团可以是选自醛基、马来酰亚胺基和琥珀酰亚胺衍生物的一种或多种,但不限于此。
[0334]
在上述中,作为醛基的实例,可以使用丙醛基或丁醛基,但是醛基不限于此。
[0335]
在上述中,作为琥珀酰亚胺衍生物,可以使用羧甲基琥珀酰亚胺、琥珀酰亚胺戊酸酯、琥珀酰亚胺基丁酸甲酯、琥珀酰亚胺基丙酸甲酯、琥珀酰亚胺丁酸酯、琥珀酰亚胺丙酸酯、n-羟基琥珀酰亚胺、羟基琥珀酰亚胺或琥珀酰亚胺碳酸酯,但是琥珀酰亚胺衍生物不限于此。
[0336]
接头可以通过反应性基团与z(免疫球蛋白fc)和q(通式1的肽)连接,以转化为接头部分。
[0337]
此外,通过醛键还原胺化产生的最终产物比通过酰胺键连接的最终产物要稳定得多。醛反应性基团在低ph下在n-末端选择性反应,而在高ph(例如,ph 9.0)下可以与赖氨酸残基形成共价键,但不限于此。
[0338]
本发明的接头的末端反应性基团可以是彼此相同或不同的。接头可在两端具有醛反应性基团。可选地,接头可在每一端具有醛基和马来酰亚胺基,或可在每一端具有醛基和
琥珀酰亚胺反应性基团,但不限于此。
[0339]
例如,接头可以在一端具有马来酰亚胺基,并且在另一端具有醛基、丙醛基或丁醛基。作为另一个实例,接头可以在一端具有琥珀酰亚胺基,并且在另一端具有丙醛基或丁醛基。
[0340]
当将在丙醛端具有羟基反应性基团的聚乙二醇用作接头时,可以通过已知的化学反应将羟基活化为各种反应性基团或通过使用具有改性反应性基团的商业上可获得的聚乙二醇来制备本发明的缀合物。
[0341]
在具体实施方式中,接头的反应性基团可以与通式1的肽的半胱氨酸残基,更具体地与半胱氨酸的
–
sh基团连接,但是接头不限于此。
[0342]
当使用马来酰亚胺
–
peg
–
醛时,马来酰亚胺基团可以通过硫醚键与通式1的肽的的
–
sh基团连接,并且醛基可以通过还原烷基化与免疫球蛋白fc的
–
nh2基团连接,但不限于此,并且这仅仅是一个实施方式。
[0343]
通过还原烷基化,可以通过具有
–
ch2ch2ch2–
结构的接头反应性基团将在免疫球蛋白fc片段的n-末端的氨基与位于peg的一端的氧原子连接形成诸如
–
peg
–o–
ch2ch2ch2nh
–
免疫球蛋白fc的结构;并且可以形成其中通过硫醚键将peg的一端与位于通式1的肽的半胱氨酸的硫原子连接的结构。上述硫醚键可以包括下述结构:
[0344][0345]
然而,接头并不特别限于上述实施方式,并且这仅仅是一个实施方式。
[0346]
此外,在上述缀合物中,接头的反应性基团可以与位于免疫球蛋白fc片段的n-末端的
–
nh2连接,但是这仅仅是一个实施方式。
[0347]
此外,在缀合物中,通式1的肽可以通过c-末端与具有反应性基团的接头连接,但是这仅仅是一个实施方式。
[0348]
如在本文中使用的,术语“c-末端”是指肽的羧基末端,并且是指出于本发明的目的能够与接头结合的位置。例如,c-末端可以包括在c-末端的最末端处的所有氨基酸残基和在c-末端附近的氨基酸残基,并且具体地,可以包括从最末端开始的第1至20个氨基酸残基,尽管c-末端不限于此。
[0349]
在一个实施方式中,化学式1的缀合物可以具有下述化学式2的结构:
[0350]
[化学式2]
[0351][0352]
在化学式2中,q是上述化学式1的肽;
[0353]
z是免疫球蛋白fc片段;和
[0354]
n可以是自然数。具体而言,对n的描述与上文所述相同。
[0355]
在一个实施方式中,化学式2的长效缀合物具有其中seq id no:47的化学式1的肽q和免疫球蛋白fc片段z通过乙二醇重复单元共价连接的结构,其中每个q可以与化学式2的琥珀酰亚胺环连接,并且z可以与化学式2的氧丙烯基连接。
[0356]
在上述化学式2中,n值可以确定为使得肽缀合物中[och2ch2]n区的平均分子量,例如数均分子量为1kda至100kda、或1kda至20kda、或10kda,但不限于此。
[0357]
肽缀合物的q可以是对胰高血糖素受体、glp-1受体和gip受体具有活性的肽。
[0358]
在一个实施方式中,q与化学式2的琥珀酰亚胺环连接的部分可以是q的c-末端半胱氨酸的硫原子。
[0359]
化学式1或2的z是免疫球蛋白fc片段,并且本说明书中的免疫球蛋白fc区不仅包括由免疫球蛋白的木瓜蛋白酶消化获得的天然序列,而且还包括其衍生物、取代基,例如,变体,其中天然序列中的一个或多个氨基酸残基通过删除、插入、非保守或保守取代、或其组合被转化,并且因此序列变得与天然序列不同,等等。上述衍生物、取代基和变体需要保留fcrn结合能力。
[0360]
与z中氧丙烯基连接的部分没有具体限制。在本发明的一个实施方式中,z的与氧丙烯基连接的部分可以是n-末端氮或z的内部残基的氮原子(例如,赖氨酸的ε氮)。在本发明的一个具体实施方式中,其中z与化学式1的氧丙烯基连接的部分可以是z的n-末端脯氨酸,但不限于此。
[0361]
z可以具有其中两条多肽链通过分子间二硫键连接的结构或其中两条多肽链通过两条链中的仅一条中的氮原子连接的结构,但不限于此。通过氮原子的连接可以经由还原胺化与赖氨酸的ε氨基原子或n-末端氨基连接。
[0362]
还原胺化反应是指这样的反应,其中一种反应物的胺基或氨基与另一种反应物的醛(即,能够还原胺化的官能团)反应以产生胺,并且此后通过还原反应形成胺键。还原胺化反应是本领域广泛知晓的有机合成反应。
[0363]
在一个实施方式中,z可以通过其n-末端脯氨酸的氮原子连接,但不限于此。
[0364]
如在本文中使用的,术语“免疫球蛋白fc片段”是指不包括免疫球蛋白的重链和轻链可变区域的重链恒定区。具体地,免疫球蛋白fc片段可以包括重链恒定区2(ch2)和/或重链恒定区3(ch3)部分,并且更具体地可以进一步包括铰链区(铰链区的全部或部分)。
[0365]
免疫球蛋白fc片段可以是构成本发明的化学式1的肽缀合物的部分的结构。具体地,它可以对应于上述化学式1中的z。
[0366]
这种免疫球蛋白fc片段可以包括重链恒定区中的铰链区,但不限于此。
[0367]
在本发明中,免疫球蛋白fc片段可以在n-末端包括特定铰链序列。
[0368]
如在本文中使用的,术语“铰链序列”是指位于重链中并通过分子间二硫键形成免疫球蛋白fc片段的二聚体的区域。
[0369]
在本发明中,铰链序列可以被修饰,使得具有下述氨基酸序列的铰链序列的一部分被删除,并且因此在该序列中只有一个半胱氨酸残基,但不限于此:
[0370]
glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro
–
ser
–
cys
–
pro(seq id no:55)。
[0371]
铰链序列可以这样的序列,其中seq id no:55的铰链序列的第8个或第11个半胱氨酸残基被删除并且因此在该序列中仅包括一个半胱氨酸残基。本发明的铰链序列可以由3至12个氨基酸(仅包括一个半胱氨酸残基)组成,但是铰链序列不限于此。更具体地,本发明的铰链序列可以具有下述序列:glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
pro
–
ser
–
cys
–
pro(seq id no:56)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro
–
ser
–
pro(seq id no:57)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro
–
ser(seq id no:58)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro
–
pro(seq id no:59)、lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro
–
ser(seq id no:60)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys(seq id no:61)、glu
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys(seq id no:62)、glu
–
ser
–
pro
–
ser
–
cys
–
pro(seq id no:63)、glu
–
pro
–
ser
–
cys
–
pro(seq id no:64)、pro
–
ser
–
cys
–
pro(seq id no:65)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
ser
–
cys
–
pro(seq id no:66)、lys
–
tyr
–
gly
–
pro
–
pro
–
pro
–
ser
–
cys
–
pro(seq id no:67)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
ser
–
cys
–
pro(seq id no:68)、glu
–
ser
–
lys
–
tyr
–
gly
–
pro
–
pro
–
cys(seq id no:69)、lys
–
tyr
–
gly
–
pro
–
pro
–
cys
–
pro(seq id no:70)、glu
–
ser
–
lys
–
pro
–
ser
–
cys
–
pro(seq id no:71)、glu
–
ser
–
pro
–
ser
–
cys
–
pro(seq id no:72)、glu
–
pro
–
ser
–
cys(seq id no:73),和ser
–
cys
–
pro(seq id no:74)。更具体地,铰链序列可以包括seq id no:74(ser
–
cys
–
pro)或seq id no:65(pro
–
ser
–
cys
–
pro)的氨基酸序列,但不限于此。
[0372]
本发明的免疫球蛋白fc片段可以是其中由于其中存在铰链序列而使免疫球蛋白fc链的两个分子形成二聚体的形式,并且另外,本发明的化学式1的长效缀合物可以是其中接头的一端与二聚体免疫球蛋白fc片段的一条链连接的形式,但是免疫球蛋白fc片段和缀合物不限于此。
[0373]
如在本文中使用的,术语“n-末端”是指蛋白质或多肽的氨基末端,并且它可以包括从最末端开始的1、2、3、4、5、6、7、8、9或10或更多个氨基酸或氨基末端的最末端。本发明的免疫球蛋白fc片段可以包括n-末端的铰链序列,但不限于此。
[0374]
此外,本发明的免疫球蛋白fc片段可以是扩展的fc片段,其包括重链恒定区1(ch1)和/或轻链恒定区1(cl1)的全部或部分,不包括免疫球蛋白的重链和轻链可变区,只要它与其天然类型相比具有基本上相当或改善的效果。此外,本发明的免疫球蛋白fc片段可以是其中对应于ch2和/或ch3的一些相当长的氨基酸序列被移除的区域。
[0375]
例如,本发明的免疫球蛋白fc片段可以是:1)ch1结构域、ch2结构域、ch3结构域和ch4结构域;2)ch1结构域和ch2结构域;3)ch1结构域和ch3结构域;4)ch2结构域和ch3结构域;5)(i)ch1结构域、ch2结构域、ch3结构域和ch4结构域中的一个或两个或更多个结构域和(ii)免疫球蛋白铰链区(或铰链区的一部分)的组合;或6)重链恒定区和轻链恒定区的每个结构域的二聚体,但是免疫球蛋白fc区不限于此。
[0376]
此外,在一个实施方式中,免疫球蛋白fc片段可以具有二聚体形式,并且通式1的肽的一个分子可以与二聚体形式的一个fc区共价连接,具体而言,免疫球蛋白fc和通式1的肽可以通过含有乙二醇重复单元的接头彼此共价连接。同时,还有可能将通式1的肽的两个分子与二聚体形式的一个fc区对称连接。具体而言,免疫球蛋白fc和通式1的肽可以通过含有乙二醇重复单元的接头彼此连接,但不限于上述实施方式。
[0377]
此外,本发明的免疫球蛋白fc片段包括天然氨基酸序列以及其序列衍生物。氨基酸序列衍生物是指由于在天然氨基酸序列中一个或多个氨基酸残基的删除、插入、非保守或保守取代、或其组合而使该序列与天然氨基酸序列不同。
[0378]
例如,已知对连接很重要的igg fc中第214至238、297至299、318至322或327至331位的氨基酸残基可用作适合修饰的位点。
[0379]
此外,可以获得各种类型的衍生物,例如,其中去除能够形成分子间二硫键的位点的衍生物;其中从天然fc去除几个n-末端氨基酸的衍生物;其中将甲硫氨酸残基添加到天然fc的n-末端的衍生物,等等。此外,可以去除补体结合位点(例如,c1q结合位点)或抗体依赖性细胞介导的细胞毒性(adcc)位点以消除效应器功能。在国际公开号wo 97/34631、wo 96/32478等中公开了用于制备这些免疫球蛋白fc片段的序列衍生物的技术。
[0380]
蛋白质或肽中不改变分子的整体活性的氨基酸取代在本领域是众所周知的(h.neurath,r.l.hill,the proteins,academic press,new york,1979)。最常见的取代发生在以下的氨基酸残基之间:ala/ser、val/ile、asp/glu、thr/ser、ala/gly、ala/thr、ser/asn、ala/val、ser/gly、thy/phe、ala/pro、lys/arg、asp/asn、leu/ile、leu/val、ala/glu和asp/gly。在一些情况下,氨基酸可以通过磷酸化、硫酸盐化、丙烯酰化、糖基化、甲基化、法尼酰化、乙酰化、酰胺化等被修饰。
[0381]
上述fc衍生物可以是展现出与本发明的fc片段相同的生物活性并具有增加的fc片段对热、ph等的结构稳定性的那些。
[0382]
此外,这种fc片段可以获得自从人或动物(例如,母牛、山羊、猪、小鼠、兔子、仓鼠、大鼠、豚鼠等)分离的天然类型或可以是从转化的动物细胞或微生物获得的重组体或其衍生物。具体而言,fc区可以通过从活人或动物分离出整个免疫球蛋白并用蛋白酶处理分离出的免疫球蛋白而从天然免疫球蛋白获得。当用木瓜蛋白酶处理整个免疫球蛋白时,它被裂解为fab和fc片段,而当用胃蛋白酶处理时,它被裂解为pf
′
c和f(ab)2片段。fc或pf
′
c可以使用尺寸排阻色谱法等分离。在更具体实施方式中,fc片段可以是重组免疫球蛋白fc片段,其中人衍生的fc片段从微生物中获得。
[0383]
此外,免疫球蛋白fc片段可以是天然聚糖的形式、与天然类型相比增加或减少的聚糖、或去糖基化形式。免疫球蛋白fc聚糖的增加、减少或去除可以通过常规方法比如化学方法、酶法以及使用微生物的基因工程方法来实现。具体而言,其中从fc中除去聚糖的免疫球蛋白fc片段显示出对补体(c1q)的结合亲和力显著下降以及抗体依赖性细胞毒性或补体依赖性细胞毒性的降低或去除,并且因此它在体内不会诱发不必要的免疫反应。在这方面,去糖基化或无糖基化形式的免疫球蛋白fc片段可能更适合满足本发明作为药物载体的初始目的。
[0384]
如在本文中使用的,术语“去糖基化”是指其中用酶除去聚糖的fc片段,和术语“无糖基化”是指在原核生物中产生的非糖基化的fc片段,并且更具体地是大肠埃希杆菌。
[0385]
同时,免疫球蛋白fc片段可以源自人或动物(例如,母牛、山羊、猪、小鼠、兔子、仓鼠、大鼠、豚鼠等),并且在更具体的实施方式中,它可以源自人。
[0386]
此外,免疫球蛋白fc片段可以源自igg、iga、igd、ige、igm或其组合或杂合体。在更具体实施方式中,免疫球蛋白fc片段可以源自igg或igm,它们是人类血液中最丰富的蛋白质之一,并且在甚至更具体的实施方式中,它可以源自igg,已知它能够提高配体结合蛋白的半衰期。在甚至更具体的实施方式中,免疫球蛋白fc片段可以是igg4 fc片段,并且在最具体的实施方式中,它可以是源自人igg4的无糖基化的fc片段,但不限于此。
[0387]
此外,在具体实施方式中,免疫球蛋白fc片段(为人igg4 fc片段)可以是同源二聚体的形式,其中两个单体通过半胱氨酸(其为每个单体的第3个氨基酸)之间的分子间二硫键(链间形式)连接。具体而言,同源二聚体的每个单体独立地具有/或可以具有在第35和95位的半胱氨酸之间的分子内二硫键;和在第141和199位的半胱氨酸之间的分子内二硫键(即,两个内部二硫键(链内形式))。关于氨基酸的数量,每个单体可以由221个氨基酸组成,并且形成同源二聚体的氨基酸可以由总共442个氨基酸组成,但是氨基酸的数量不限于此。具体地,免疫球蛋白fc片段可以是这样的片段,其中具有seq id no:79的氨基酸序列的两个单体(由221个氨基酸组成)通过半胱氨酸(其为每个单体的第3个氨基酸)之间的分子间二硫键形成同源二聚体,并且其中同源二聚体的单体独立地形成在第35和95位的半胱氨酸之间的内部二硫键和在第141和199位的半胱氨酸之间的内部二硫键,但是免疫球蛋白fc片段不限于此。
[0388]
化学式1中的z可以包括seq id no:76的氨基酸序列的单体,并且z可以是seq id no:76的氨基酸序列的单体的同源二聚体,但不限于此。
[0389]
在一个实施例中,免疫球蛋白fc片段可以是包括seq id no:75的氨基酸序列的同源二聚体(由442个氨基酸组成),但不限于此。
[0390]
同时,如在本文中使用的,术语“组合”是指编码同一来源的单链免疫球蛋白fc片段的多肽与不同来源的单链多肽连接以形成二聚体或多聚体。即,可以由选自igg fc、iga fc、igm fc、igd fc和ige fc的fc片段的两个或更多个片段制备二聚体或多聚体。
[0391]
如在本文中使用的,术语“杂合”是指在免疫球蛋白恒定区的一条链中存在对应于两个或多个不同来源的免疫球蛋白fc片段的序列。在本发明中,各种杂合形式都是可能的。例如,杂合结构域可以由选自igg fc、igm fc、igafc、ige fc和igd fc的ch1、ch2、ch3和ch4的1至4个结构域组成,并且可以进一步包括铰链区。
[0392]
同时,igg也可以划分为igg1、igg2、igg3和igg4亚类,并且本发明可以包括其组合或杂合。优选的是igg2和igg4亚类,并且最优选的是igg4的fc片段,它很少具有效应功能,比如补体依赖性细胞毒性(cdc)。
[0393]
同时,液体制剂可用于预防或治疗代谢综合症。
[0394]
如在本文中使用的,术语“预防”是指通过施用上述缀合物或包括该缀合物的制剂抑制或延迟代谢综合症的发生的所有活动,并且术语“治疗”是指通过施用上述缀合物或包括该缀合物的制剂来改善或有利地改变代谢综合症的症状的所有活动。
[0395]
如在本文中使用的,术语“施用”是指通过任何适当的方法将特定材料引入患者体内,并且组合物的施用途径没有特别限制,但是可以是能够将组合物输送到体内目标的任何常规途径(例如,腹膜内施用、静脉内施用、肌内施用、皮下施用、皮内施用、口服施用、局
部施用、鼻内施用、肺内施用、直肠内施用等)。
[0396]
实施本发明的另一个方面提供了用于制备液体制剂的方法。
[0397]
具体地,制备方法可以包括:混合(a)对胰高血糖素受体、glp-1受体和gip受体具有活性的肽的长效缀合物,其中对胰高血糖素受体、glp-1受体和gip受体具有活性的肽和免疫球蛋白fc片段彼此连接,与(b)包括i)缓冲剂和ii)糖醇、糖或组合的稳定剂。
[0398]
同时,稳定剂可以进一步包括选自等渗剂、非离子表面活性剂和氨基酸的一种或多种组分,但不特别限于此。
[0399]
长效粘合剂、缓冲剂、糖醇、糖或其组合、等渗剂、非离子表面活性剂、氨基酸和稳定剂与上述相同。
[0400]
实施本发明的又另一个方面提供了用于预防或治疗代谢综合症的方法,其包括:将液体制剂施用至有需要的受试者。
[0401]
液体制剂、代谢综合症、预防和治疗与上述相同。
[0402]
受试者是指需要施用本发明的液体制剂的受试者,并且包括但不限于任何可以用本发明的液体制剂治疗的受试者,并且具体包括人类或哺乳动物,包括大鼠、家畜等。
[0403]
本发明的治疗方法可以包括以药学有效量施用该液体制剂。液体制剂的适当的每日总剂量可在执业医师正确的医疗判断范围内确定,并且液体制剂可一次或多次分次施用。然而,出于本发明的目的,优选的是任何特定患者的液体制剂的具体治疗有效剂量根据要达到的反应的种类和程度、具体组合物(包括是否偶尔与其他药剂一起使用)、患者的年龄、体重、一般健康状况、性别和饮食、施用时间、施用途径、组合物的排泄率、治疗持续时间、包括药物与具体组合物联合或同时使用的各种因素以及在医学领域众所周知的类似因素而不同地应用。
[0404]
实施本发明的又另一个实施方式提供了液体制剂在制备用于预防或治疗代谢综合症的药物中的用途。
[0405]
液体制剂、代谢综合症、预防和治疗与上述相同。
[0406]
实施本发明的又另一个实施方式提供了液体制剂用于预防或治疗代谢综合症的用途。
[0407]
液体制剂、代谢综合症、预防和治疗与上述相同。
[0408]
下文将参照以下实施例对本发明进行更详细的描述。然而,这些实施例仅用于说明目的,并且本发明的范围不受这些实施例的限制。
[0409]
制备例:胰高血糖素、glp-1和gip三重激动剂的长效缀合物的制备
[0410]
通过下述方法制备胰高血糖素、glp-1和gip三重激动剂的长效缀合物。
[0411]
1-1:胰高血糖素、glp-1和gip三重激动剂的制备
[0412]
制备了显示对glp-1受体、gip受体和胰高血糖素受体中所有具有活性的三重激动剂,并且其氨基酸序列如下表1所示。
[0413]
[表1]
[0414]
[0415]
[0416][0417]
在表1所述的序列中,x代表的氨基酸是氨基丁酸(aib),它是一种非天然的氨基酸,并且加下划线的氨基酸表示在加下划线的氨基酸之间形成环。此外,在表1中,ca代表4-咪唑乙酰基,并且y代表酪氨酸。
[0418]
1-2:三重激动剂的体外活性的测量
[0419]
为了测量实施例1-1中制备的三重激动剂的活性,使用用细胞系测量体外细胞活性的方法,其中glp-1受体、胰高血糖素(gcg)受体和gip受体各自转化。
[0420]
上述各细胞系是这样的细胞系,其中将人glp-1受体、人gcg受体和人gip受体的基因分别转化到中国仓鼠卵巢(cho)中,在其中表达,并且因此适合于测量glp-1、gcg和gip的活性。因此,使用各自转化的细胞系来测量各部分的活性。
[0421]
为了测量实施例1-1中制备的三重激动剂的glp-1活性,将人glp-1进行从50nm到0.000048nm的4倍连续稀释,并将实施例1-1中制备的三重激动剂进行从400nm到0.00038nm的4倍连续稀释。从培养的cho细胞中除去培养液,在其中表达人glp-1受体,并将每种连续稀释的物质分别以5μl的量加入cho细胞中,并将含有camp抗体的缓冲液以5μl的量加入其中,并在室温下培养15分钟。然后,将含有细胞裂解缓冲液的检测混合物以10μl的量加入其中,用于裂解细胞,并在室温下反应90分钟。将完成反应后的细胞裂解液应用于lance camp试剂盒(perkinelmer,美国),以通过累积的camp计算ec
50
值,并将这些值相互比较。相对于人glp-1的相对滴度显示在下面的表2中。
[0422]
为了测量实施例1-1中制备的三重激动剂的gcg活性,将人gcg进行从50nm到0.000048nm的4倍连续稀释,并将实施例1-1中制备的三重激动剂进行从400nm到0.00038nm的4倍连续稀释。从培养的cho细胞中除去培养液,在其中表达人gcg受体,并将每一种连续稀释的物质分别以5μl的量加入cho细胞中,并将含有camp抗体的缓冲溶液以5μl的量加入
其中,在室温下培养15分钟。然后,将含有细胞裂解缓冲液的检测混合物以10μl的量加入其中,用于裂解细胞,并在室温下反应90分钟。将反应完成后的细胞裂解液应用于lance camp试剂盒(perkinelmer,美国)以通过累积的camp计算ec
50
值,并将这些值相互比较。相对于人gcg的相对滴度显示在下面的表2中。
[0423]
为了测量实施例1-1中制备的三重激动剂的gip活性,将人gip进行从50nm到0.000048nm的4倍连续稀释,并将实施例1-1中制备的三重激动剂进行从400nm到0.00038nm的4倍连续稀释。从培养的cho细胞中除去培养液,在其中表达人gip受体,并将每种连续稀释的物质分别以5μl的量加入cho细胞中,并将含有camp抗体的缓冲液以5μl的量加入其中,并在室温下培养15分钟。然后,将含有细胞裂解缓冲液的检测混合物以10μl的量加入其中,用于裂解细胞,并在室温下反应90分钟。将完成反应后的细胞裂解液应用于lance camp试剂盒(perkinelmer,美国),以通过累积的camp计算ec50值,并将这些值相互比较。相对于人gip的相对滴度显示在下面的表2中。
[0424]
[表2]
[0425]
三重激动剂的相对滴度比
[0426]
[0427][0428]
经证实,上述制备的三重激动剂对glp-1、gip和胰高血糖素受体中所有都有很好的作用。
[0429]
1-3:三重激动剂的长效缀合物的制备
[0430]
长效缀合物使用seq id no:9的肽作为代表性三重激动剂来制备。为了制备三重激动剂和聚乙二醇接头之间的接头,使马来酰亚胺-peg-醛(japan nof inc.)(其为一种分子量为10kda的线性改性聚乙二醇,其中两端的氢分别被3-(3-马来酰亚胺丙酰胺)丙基和3-氧代丙基(丙醛基)取代)与三重激动剂的半胱氨酸残基反应,使在马来酰亚胺-peg-醛的马来酰亚胺端的三重激动剂peg化。具体来说,三重激动剂和马来酰亚胺-peg-醛以1:1至3的摩尔比以1mg/ml至5mg/ml的蛋白质浓度在低温下反应0.5至3小时。具体而言,反应是在向50mm tris缓冲液(ph 7.5)中加入20%至60%的异丙醇的环境下进行的。在反应完成后,将反应溶液应用于sp sepharose hp(ge healthcare,美国)以纯化半胱氨酸被单peg化的三重激动剂。
[0431]
通过在国际专利公开号wo2007/021129中描述的方法,使用在n-末端具有pro-ser-cys-pro序列的铰链区的免疫球蛋白fc片段(49.8kda,seq id no:76的两条链通过分子内二硫键连接的同源二聚体)来制备免疫球蛋白fc片段。
[0432]
然后,将纯化的单peg化的三重激动剂和免疫球蛋白fc以1:1至5的摩尔比以10mg/ml至50mg/ml的蛋白浓度在4℃至8℃下反应12至18小时。反应是在其中在100mm磷酸钾黄油(ph 6.0)中加入10mm至50mm氰硼氢化钠(还原剂)和10%至30%异丙醇的环境中进行的。在反应完成后,将反应溶液应用于butyl sepharose ff纯化柱(ge healthcare,美国)和source iso纯化柱(ge healthcare,美国),以纯化三重激动剂的长效缀合物,其中单peg化的三重激动剂的醛侧的聚乙二醇端与免疫球蛋白fc同源二聚体的两条链中的一条的n-末端脯氨酸处的氮连接。
[0433]
在制备完成后,通过反相色谱法、尺寸排除色谱法和离子交换色谱法分析的纯度显示为95%或更高。
[0434]
具体而言,将其中胰高血糖素、glp-1和gip三重激动剂和免疫球蛋白fc片段通过peg连接的缀合物被命名为“胰高血糖素、glp-1和gip三重激动剂的长效缀合物”。
[0435]
实施例1:评估根据ph的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0436]
基于由缓冲剂、作为糖醇的甘露糖醇、作为表面活性剂的聚山梨醇酯20和甲硫氨酸组成的液体制剂,在不同的ph下比较胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。作为比较例,使用了ph为4.5的制剂。
[0437]
使用表3中显示的组分将上述制备例中获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,然后通过离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0438]
在表4中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以在保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0439]
[表3]
[0440][0441][0442]
[表4]
[0443][0444]
*n/d:由于蛋白质沉淀,无法进行分析
[0445]
从上述结果可以看出,具有柠檬酸钠和ph 5.0的组成的制剂(#1)和具有柠檬酸钠和ph5.5的组成的制剂(#2)在25℃下在6周内显示出高稳定性。具有ph 6.0的组成的制剂(#3)和具有ph 6.5的组成的制剂(#4)也在6周内展现出稳定性。在ph 4.5的组成(其为比较例)的情况下,证实在第6周时发生了沉淀。
[0446]
实施例2:评估根据糖或糖醇的类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0447]
为了提高胰高血糖素、glp-1和gip三重激动剂长效缀合物的储存稳定性,可以另外包括的糖或糖醇的实例可以包括单糖,比如甘露糖、葡萄糖、岩藻糖和木糖,以及多糖,比如乳糖、麦芽糖、蔗糖、山梨糖醇、棉子糖和葡糖。其中,根据实施例1中证实的甘露糖醇、蔗糖和山梨糖醇,比较了胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。具体而言,甘露糖醇、蔗糖和山梨糖醇的浓度是在考虑到商业上可获得的制剂的最大允许范围和许可机构推荐的浓度的情况下选择的。
[0448]
使用表5中显示的组成将上述获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,并且然后通过离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0449]
在表6中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0450]
[表5]
[0451][0452][0453]
[表6]
[0454][0455]
从上述结果可以看出,当甘露糖醇、山梨糖醇和蔗糖(其是为了增加胰高血糖素、glp-1和gip三重激动剂的长效缀合物的储存稳定性而可能包括的糖或糖醇)分别以5%、5%和8%的浓度加入时观察到类似的稳定性。
[0456]
实施例3:评估根据糖或糖醇的浓度的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0457]
基于实施例1或2中证实的液体制剂的组成(柠檬酸钠(ph 5.5)、甘露糖醇、聚山梨醇酯20和甲硫氨酸),比较根据糖或糖醇的浓度的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。具体而言,考虑到商业上可获得的制剂的允许范围和正常血浆渗透压,选择了一起加入的等渗剂的浓度。
[0458]
使用表7中显示的组分将上述获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,并且然后用离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0459]
在表8中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以在保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0460]
[表7]
[0461][0462]
[表8]
[0463][0464][0465]
从上述结果可以看出,当胰高血糖素、glp-1和gip三重激动剂的长效缀合物的制剂中含有浓度为1%至5%的糖醇时,观察到类似的稳定性。
[0466]
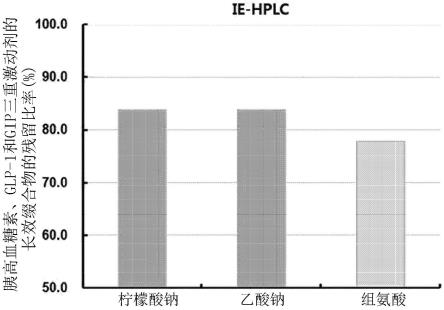
实施例4:评估根据缓冲剂的类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0467]
基于液体制剂的组成(柠檬酸钠(ph 5.5)、甘露糖醇、聚山梨醇酯20和甲硫氨酸)
比较根据缓冲剂的类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。
[0468]
使用表9中显示的组成将上述获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,并且然后通过离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0469]
在表10中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0470]
[表9]
[0471][0472]
[表10]
[0473][0474]
*n/d:由于蛋白质沉淀,无法进行分析
[0475]
从上述结果可以看出,当使用柠檬酸钠(#1)和乙酸钠(#2)作为缓冲剂时,在25℃下6周内表现出高稳定性。此外,证实即使在使用组氨酸(#3)作为缓冲剂时,也表现出良好的稳定性(图1a和b)。
[0476]
实施例5:评估根据非离子表面活性剂的类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0477]
在具有乙酸钠、蔗糖和甲硫氨酸的组成的液体制剂中比较了根据非离子表面活性剂的类型的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。
[0478]
具体而言,考虑到商业上可获得的制剂,选择一定浓度的聚山梨醇酯20、聚山梨醇酯80和泊洛沙姆188作为非离子表面活性剂。
[0479]
使用表11中显示的组分将上述获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,并且然后通过离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0480]
在表12中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0481]
[表11]
[0482][0483]
[表12]
[0484][0485]
分别含有聚山梨醇酯20(#1)、聚山梨醇酯80(#2)和泊洛沙姆188(#3)作为非离子表面活性剂的制剂显示出类似的稳定性。
[0486]
实施例6:评估根据非离子表面活性剂和氨基酸的存在或不存在的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0487]
当液体制剂含有或不含有非离子表面活性剂或氨基酸稳定剂时,比较了胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性。
[0488]
使用表13显示的组合物将上述获得的三重激动剂的长效缀合物制备成液体制剂(长效缀合物的浓度为183.79nmol/ml)并在25℃下储存6周,并且然后通过离子交换高效液相色谱法(ie-hplc)和反相高效液相色谱法(rp-hplc)分析其稳定性。
[0489]
在表14中,ie-hplc(%)和rp-hplc(%)表示测量时的面积%除以保存试验期间的初始面积%的比率(面积%/初始面积%),表示从三重激动剂的长效缀合物的初始浓度(183.79nmol/ml)开始的残留比率。
[0490]
[表13]
[0491][0492]
[表14]
[0493][0494]
从上述结果可以看出,含有非离子表面活性剂和氨基酸的制剂和不含其的制剂显示出类似的稳定性。
[0495]
实施例7:评估根据浓度的胰高血糖素、glp-1和gip三重激动剂的长效缀合物的稳定性
[0496]
在表15所示的浓度下,证实了实施例6中由乙酸钠、蔗糖、聚山梨醇酯20和甲硫氨酸组成的液体制剂在ph 5.1下高浓度应用的长期储存稳定性和加速稳定性。
[0497]
为此,在5℃
±
3℃和25℃
±
2℃储存后,用离子交换高效液相色谱法、反相高效液相色谱法和大小排阻色谱法进行分析。在表16和17中,ie-hplc(%)、rp-hplc(%)和se-hplc(%)表示测量时的面积%除以保存试验时的初始面积%的比率(面积%/初始面积%),表示三重激动剂的长效缀合物的残留比率。
[0498]
[表15]
[0499][0500]
[表16]
[0501][0502][0503]
[表17]
[0504][0505]
如上述结果所示,作为长期储存稳定性测试的结果,证实在本发明的液体制剂中,
蛋白质浓度为183.79nmol/ml至551.37nmol/ml的胰高血糖素、glp-1和gip三重激动剂的长效缀合物同样稳定。即,这些结果表明,各种浓度的胰高血糖素、glp-1和gip三重激动剂的长效缀合物在本发明的液体制剂的组合物中都具有稳定性。
[0506]
从上述内容来看,本发明所涉及领域的技术人员能够理解,本发明可以在不修改本发明的技术概念或基本特征的情况下以其他具体形式体现出来。在这方面,本文公开的示例性实施方式仅用于说明目的,并且不应解释为限制本发明的范围。相反,本发明旨在不仅包括示例性实施方式,而且还包括可能包括在本发明的精神和范围内的各种替代方案、修改方案、等同方案和其他实施方式,如所附的权利要求书所限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1