一种高稳定性自载体储氧材料的制备方法与流程
本发明涉及化学链循环氧储氢领域,特别涉及一种用于化学链循环氧储氢的高稳定性自载体储氧材料及其制备方法。
背景技术:
氢能是一种燃烧热值大,无污染的可再生能源,被视为21世纪最具发展潜力的清洁能源。有效利用氢能的关键是开发高效、可大规模应用的储氢技术。
目前最常见的储氢技术分为物理储氢和化学储氢。物理储氢中的高压储氢和液压储氢,已经能够实现大规模商业化的氢能存储,但是高压带来的安全隐患依旧制约着这两种储氢技术的应用,除此之外,高压储氢和液压储氢还存在能耗高、占地面积大等缺点;化学储氢主要实施方式有储氢合金、金属氢化物和有机物储氢等。化学储氢材料具有储氢密度高、反应条件温和、安全性好等优点。但由于制备成本过高,化学储氢材料现在还处于实验室研究阶段,未见商业化报道。易污染环境等缺点也给化学储氢技术的推广带来困难。
化学链循环氧储氢是一种新型的间接储氢技术,采用在储氧材料中创造氧空位,再由氧空位逆变产氢的方式间接储氢,理论上一个氧空位可逆变得到两个氢,因此储氢密度将是传统储氢方式的两倍。以钴铁储氧材料为例说明其储氢原理:储氢过程:
释氢过程:
储氧材料中活性成分为铁氧化物。储氢过程中,铁氧化物中的氧与氢结合变成水,铁氧化物被还原为低价铁氧化物。每1个氧原子结合2个氢原子,对应产生一个氧空位。释氢过程中,1个氧空位裂解1分子水,水中的氧填补氧空位,氢则以氢气的形式释放出来,同时低价铁氧化物被氧化,储氧材料可以再次用于储氢,从而实现氢气的可逆储放。
目前用于化学链循环氧储氢的储氧材料,存在储氧密度低、循环稳定性差等缺点。因此,寻找用于化学链循环氧储氢的高稳定性储氧材料具有重要意义。
技术实现要素:
技术问题:为了解决现有储氧材料存在的储氧密度低、循环稳定性差等问题,本发明提供了一种用于化学链循环氧储氢的高稳定性自载体储氧材料及其制备方法。该材料可用于化学链循环氧储氢,理论储氢密度是传统氢空位储氢的两倍。该材料具有尖晶石结构,抗烧结能力强,材料循环稳定性大大提高。
技术方案:本发明的高稳定性自载体储氧材料具有尖晶石结构,热膨胀系数大,能够借助晶格膨胀形成稳定的固溶体,抗烧结能力强,材料微粒在不易因高温而烧结、团聚,材料循环稳定性大大提高。
该储氧材料分子式为cofealo4,o2-立方紧密堆积,co2+填充在四面体空隙中,fe3+、al3+填充在八面体空隙中,总相对分子质量为205.76。
本发明的高稳定性自载体储氧材料的制备方法,采用燃烧合成法制备,具体制法是将装有硝酸盐溶液的烧杯放入恒温油浴锅中加热,直到溶液变为干凝胶;取出烧杯放入干燥箱中干燥,得到的固体粉末放入马弗炉中,在200℃~300℃的空气条件下点燃,燃烧结束后,将马弗炉升温到900~1100℃对上述材料进行煅烧,最后得到用于化学链循环氧储氢的高稳定性自载体储氧材料。
所述的硝酸盐溶液由co(no3)2·6h2o、fe(no3)3·9h2o、al(no3)3·9h2o按阳离子摩尔比co2+:fe3+:al3+=1:1:1称取后用去离子水溶解,再加入柠檬酸和聚乙二醇配成溶液。
加热过程中控制溶液温度为90~95℃,并用磁力转子不断搅拌。
所述的马弗炉煅烧时间为2~2.5小时。
有益效果:与现有技术相比,本发明至少具有以下明显有点:
1.本发明制备的自载体储氧材料cofealo4可以用于化学链循环氧储氢。通过在材料中制造氧空位,再由氧空位逆变产氢的方式间接储氢,理论上一个氧空位可逆变得到两个氢,因此储氢密度将是传统储氢方式的两倍。理论上,材料储氢质量分数可达4.5%以上,体积储氢密度可达120kgh2/m3以上。
2.本发明制备的这种自载体储氧材料具有尖晶石结构,热膨胀系数大,能够借助晶格膨胀形成稳定的固溶体,抗烧结能力强,因此材料不易在高温下失活,在高温下进行多次充放氢循环后储氢性能依然保持稳定。20次充放氢循环后,材料储氢密度下降仅6.4%,120次循环后,储氢密度下降不到20%。
附图说明
图1为实施实例1所制备的高稳定性自载体储氧材料cofealo4的sem表征结果。其中图(a)为新鲜样品sem表征结果;图(b)~(d)分别为700℃、800℃、900℃下进行20个充放氢循环后样品的sem表征结果。
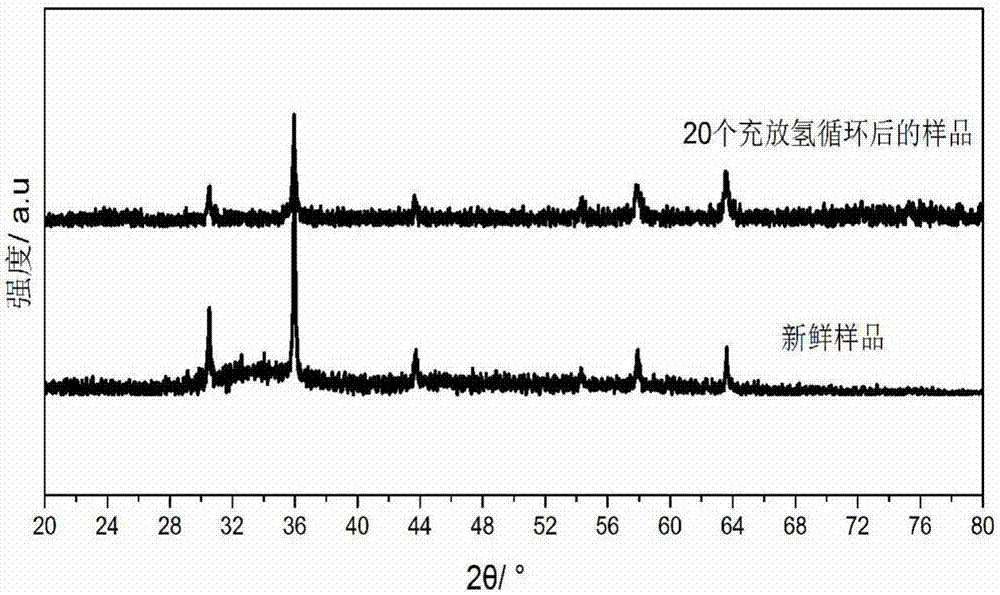
图2为实施实例1所制备的高稳定性自载体储氧材料cofealo4新鲜样品以及800℃下进行20个充放氢循环后的样品的xrd图。
图3为实施实例1所制备的高稳定性自载体储氧材料cofealo4在二十个充放氢循环中储氢密度的变化情况,反应温度为800℃。
具体实施方式
下面通过实施实例进一步说明本发明。
实施例1:燃烧合成法合成具有尖晶石结构的cofealo4
将co(no3)2·6h2o、fe(no3)3·9h2o、al(no3)3·9h2o阳离子摩尔比例co2+:fe3+:al3+=1:1:1称取后用去离子水溶解,再加入适量的柠檬酸和聚乙二醇配成溶液。
将装有上述溶液的烧杯放入恒温油浴锅中加热,保持溶液温度为90~95℃并用磁力转子不断搅拌,直到溶液变为干凝胶。取出烧杯放入干燥箱中干燥,得到的固体粉末放入马弗炉中,在200℃的空气气氛中点燃,燃烧结束后,升温到900℃煅烧2小时,即得到目标产物。
具体工况如下表:
实施例2:燃烧合成法合成具有尖晶石结构的cofealo4
制备方法与实施实例1相同,具体工况如下表:
由实施实例1的sem表征结果(图1)可以看出新鲜样品的材料微粒排列致密,这样的结构使材料不易在高温下烧结和团聚。700℃下进行20个循环后,材料结构变得较疏松,出现了烧结和颗粒团聚的现象。在800℃条件下进行20个充放氢循环之后,材料颗粒之间依然保持致密的排列,材料颗粒出现了轻微的烧结、颗粒之间出现了一些孔道。900℃条件下进行20个循环后,材料颗粒形貌基本没有发生变化,基本没有出现烧结和团聚的现象。综上所述,初步推测,在700℃~900℃的温度区间内,反应温度越高,材料微粒烧结、团聚的现象就越弱。
由实施实例1所制备的材料的新鲜样品和800℃下进行20个充放氢循环后的样品的xrd表征结果(图2)的对比可得,新鲜样品和20个循环后样品的xrd图特征峰的位置和强度基本没有变化,说明样品的尖晶石结构非常稳定,20次充放氢循环后基本没有发生变化。
由材料在20个充放氢循环中储氢密度的变化情况(图3)可得,材料的平均储氢密度为9012uoml·g-1,折合为体积储氢密度约为102kgh2/m3。材料的储氢密度在20个充放氢循环后衰减仅为6.4%。
以上对本发明的具体实施例进行了详细的说明描述,且对不同的实施例的产物现象进行了描述,但其只是作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行的等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明的精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
- 还没有人留言评论。精彩留言会获得点赞!