一种氨基酸神经四肽的合成方法与流程
本发明属于肽合成技术领域,尤其涉及一种氨基酸神经四肽的合成方法。
背景技术:
酶催化肽合成的研究现状:生物活性肽是一类重要的物质,在生命活动中具有各种各样的生物功能,但它们在体内含量极少,提取困难,因此用人工方法合成它们,具有重要的理论意义和实际意义。例如高血压、胃肠病、糖尿病等的起因与治疗均与活性肽相关。目前,在国外,尤其美、日、德等发达国家,医用肽的研究非常活跃。生物技术在肽研制方法的应用已经产生了一批以新方式治疗疾病并确之有效的新药。我国在这一领域的研究有了飞速的发展。合成功能短肽,已有不少报导,有些功能短肽合成已达到工业化的规模。酶法合成的肽类现在主要集中在有实际意义的多肽激素与具有营养的肽类,并且在这些方面,国内外有文献报导,其中较为成功的有利用嗜热菌蛋白酶或木瓜蛋白酶进行天冬糖精的生产,它是一种低热量的新型食品添加剂,对糖尿病人尤其有益。用木瓜蛋白酶和胰凝乳蛋白酶合成Leu和Met-脑菲肽,用羧肽酶-Y和胰凝乳蛋白酶合成Met-脑菲肽,用嗜热菌蛋白酶、木瓜蛋白酶、枯草杆菌蛋白酶、胃蛋白酶等合成雨蛙肽等。陈水田等人用Alcalse在乙醇中合成了含有D型氨基酸的二肽,在理论和实际应用上都有重要的意义。在国外生物活性肽的研究非常活跃,并在肽研制的应用方面产生了一批新药,带来巨大经济效益。日本Grnrtch公司研制的松弛肽用来治疗创伤和侏儒症,以及美国Telios制药公司生产的一种治疗创伤的小肽。创伤愈合肽类在美国年销售额达十亿美元。应用肽类药物攻克艾滋病HIV-1已成为新的尝试,生物活性肽的合成也是一个很活跃的领域,继化学法合成了胰岛素之后,有用酶促半合成法制备了胰岛素类似物。此外,在脑菲肽、心房肽及其类似物的合成,以及人参多肽的研制方面取得了较好的结果。
目前肽合成主要有3种方法:化学法、重组DNA技术、酶法。总体上来说,化学法在工业上仍然使用得最多;重组DNA技术由于需要一个长期、昂贵的研究和发展阶段,而且在发酵阶段存在表达效率低和产品提取回收困难等问题,其应用受到很大限制;酶法虽然起步较晚,但近20年来,不少科学家已作了相当多的工作,而且因其与化学法相比,具有副反应少、反应条件温和、区域选择性高和侧链需要较少保护或不需要保护等优势,发展相当迅速。每种方法都有其优点和缺点,单采用一种方法总有难以克服的缺点。在合成的时候具体采用哪种方法合成主要看目标产物所要求的长度和纯度。完全的酶促肽合成主要用于小的肽段(<10)的合成或肽片段的缩合,DNA重组技术更适合用于含有数百个氨基酸的大肽的合成,而对于技术上已经成熟的化学法合成,虽然固相法可以用来合成含有近100个氨基酸的肽,但是其最有实用意义的应用还是用来合成中等长度(10-100)的肽段。现在实验室规模上合成肽主要用的就是化学法,尽管它有固相液相两种不同的方法,但是这两种方法在化学过程上是非常相似的。
促肾上腺皮质激素(andrenocorticotropic hormone)即ACTH或Corticotropin是一个含三十九个氨基酸的直连多肽,分子量约为4700,羊、猪、牛的ACTH已经提纯,它们除第25-33个氨基酸外,其余部分都相同,ACTH的一级结构如下:HN-丝-酪-丝-蛋-谷-组-苯丙-精-色-甘-赖-脯-缬-甘-赖-赖-精-精-脯-缬-赖-缬-酪-脯-天冬-甘-谷-丙-谷-天冬-丝-丙-谷胺-丙-苯丙-脯-亮-谷-苯丙-COOH,期中序列1-24氨基酸残基具有生物活性,4-10是生物活性中心,既是信息部位,又对受体的结合提供要素,第八位Arg第9位Trp为启动受体的活性中心之一,当Trp的吲哚环修饰后(甲基化或NPS化)或被Phe取代,仍能与肾上腺皮质细胞的脂膜结合,但不能激发c-AMP酶或皮质激素的释放。第9位Trp、第6位His、第5位Glu对皮质酮的生成起关键作用。25-33具有种属特异性及免疫特异性。促肾上腺皮质激素由垂体前叶分泌并受下丘脑促肾上腺皮质激素释放因子(CRF)的控制。反过来,ACTH的靶器官所分泌的皮质甾体激素对垂体和下丘脑也有反馈作用。ACTH首先在垂体中发现,之后在下丘脑,脑区都有ACHT免疫反应性的活性肽存在,甚至在胃肠中也有ACTH的存在。脑、下丘脑、垂体分泌的ACTH执行不同的功能,大脑中的ACTH可能参与意识行为的调控机理,脑神经元分泌的ACTH类活性肽,可以看作为神经递质的效应物,影响对效应细胞的作用,他们传递信号的距离上短得多,所放电流弱得多。垂体分泌的ACTH主要作用于肾上腺皮质,它能促进肾上腺皮质分泌激素,并促进体内贮存的胆固醇在肾上腺皮质中转化成肾上腺皮质酮。在应激过程中,如灼烧或损伤时,ACTH的分泌量均显著增加,这表明是全身总动员,调动神经与内分泌两个方面的积极活动,ACTH在脑与垂体中的分泌量均与应激程度呈平行关系,这也说明,ACTH族活性肽对神经活动与内分泌作用均有联系。
目前临床上使用的促肾上腺皮质激素(ACTH),是从猪的垂体前叶提取的39肽的,或者是化学合成的类似物18肽、24肽、28肽等。在医学实践上应用ACTH来诊断肾上腺皮质的生理状况,由于化学合成ACTH的成功,在临床上作为柯兴氏综合症的诊断及治疗风湿性关节炎、皮肤炎、眼炎及抗过敏症,也用它来治疗痛风、气喘及皮肤痛等疾患。有研究报导其活性部位七肽(Met-Glu-His-Phe-Arg-Trp-Gly)与人的行为有关,可以使精神健全者的观察力改善,可使人的注意力集中,可以改善人的情绪,使智障的理解力提高,还能使老年人的记忆力增强,它还能减轻焦虑的情绪。
在非水介质中酶法合成氨基酸神经四肽Phe-Arg-Trp-Gly(FRWG),从方法学来看,寡肽的酶法合成,较化学法具有明显的优越性,而且是向非水酶催化合成肽键技术难点冲击,即亲水性氨基酸的利用。手性药物的合成是当前药物合成研究的难点和热点,也是酶促合成优于化学合成具体体现。实际上,目标产物是具有重要应用价值的手性药物,并使在有机介质中合成肽键的方法更普遍化和有效化。在非水介质中酶法合成氨基酸神经四肽Phe-Arg-Trp-Gly(FRWG)是促肾上腺皮质激素(ACTH)活性部位四肽,对神经系统具有明显的调节作用,因而对开发新的肽类药物,具有非常好的应用前景。
技术实现要素:
本发明的目的在于提供一种反应条件温和、立体专一性强、不用侧链保护基、几无副反应、比通常的化学合成法环保、不产生手性分子、不用进一步拆分、收率高、并在非水介质中酶法合成氨基酸神经四肽Phe-Arg-Trp-Gly的方法。
本发明是这样实现的,一种氨基酸神经四肽的合成方法,该氨基酸神经四肽的合成方法包括以下步骤:
叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)的合成:叔丁氧羰基苯丙氨酸(BOC-Phe)加入质量为0.53g(2mmol),精氨酸甲脂(Arg-OMe)加入质量为1.04g(4mmol),有机溶剂二甲基甲酰胺(DMF)20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入胰凝乳蛋白酶(Chymotyrpsin)2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的合成:BOC-Trp加入质量为0.16g(2ml),Gly-OEt加入质量为0.62g(4mmol),有机溶剂二甲基甲酰胺(DMF)20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入胰凝乳蛋白酶(Chymotyrpsin)2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
碱性蛋白酶(Alcalase)的预处理:取2ml碱性蛋白酶(Alcalase)和15ml无水乙醇置于离心管中,旋涡振荡5分钟使其充分混合,混合物3000rpm离心10分钟,碱性蛋白酶(Alcalase)与溶剂无水乙醇完全分开,倾去上层的乙醇,此步操作重复三次;
叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的处理:将含有叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的有机溶剂二甲基甲酰胺(DMF),分别减压蒸馏除去有机溶剂二甲基甲酰胺(DMF),再用乙酸乙酯溶解,乙酸乙酯分别用冷柠檬酸洗三次,冷的碳酸氢钠洗两次,再用冷水洗两次,减压蒸馏,除乙酸乙酯,得微黄色无定型物;
叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)脱保护:叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)产物用TFA(CF3COOH):苯甲醚(9:1)刚好溶解,0℃振荡2-4小时后加入乙醚:石油醚(1:3),得沉淀,离心,再加入由乙醚与石油醚按照1:3比例混合构成的混合液洗沉淀,得色氨酸甘氨酸乙脂(Trp-Gly-OEt);
叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成:取2mmol的叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和4mmol的色氨酸甘氨酸乙脂(Trp-Gly-OEt)加入锥形瓶,加入有机溶剂叔丁醇20ml,碱性蛋白酶(Alcalase)2ml,1ml三乙胺,一定量的Na2CO3-NaHCO3缓冲液,37℃水浴振荡24小时,每隔4h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)脱保护:叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)产物用TFA(CF3COOH):苯甲醚(9:1)刚好溶解,0℃振荡2-4小时后加入乙醚:石油醚(1:3),得沉淀,离心,再加入由乙醚与石油醚按照1:3比例混合构成的混合液洗沉淀,得苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt);
苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)脱保护:取4.4g苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt),加入24ml甲醇,12.5mlNaOH(2mol/L),反应一小时,用HCl(1mol/L)调节pH至7,抽去甲醇,加水稀释,过滤,冰浴冷却,水洗到中性,得氨基酸神经四肽(Phe-Arg-Trp-Gly),用质谱检测产物;
肽产物分离纯化:柱料采用Sephadex G-10,层析柱为16mm×1000mm,洗脱液采用蒸馏水,检测波长为220nm,流速为1.0ml/min,取100g Sephadex G-10干柱料,加500ml蒸馏水浸泡过夜,减压除气泡后装柱,洗脱液平衡过夜,待分离液体0.5ml上样层析,收集产品峰,冻干得产物。
进一步,该氨基酸神经四肽的合成方法采用高效液相法(HPLC)检测肽合成纯度,定量分析肽产物的方法用于合成肽的分析检测,采用高效液相色谱仪,型号为C18,250×4.6mm的Diamosil色谱柱,220nm DAD紫外检测器,柱温25℃,溶剂A采用0.1%三氟乙酸的乙腈,溶剂B采用含0.1%三氟乙酸的水,流速为1.0ml/min,具体梯度为:
进一步,该氨基酸神经四肽的合成方法采用质谱确定分子量的方法鉴定肽产物,质谱(MS)条件如下:离子化模式:API–ES;极性:阳性;电压:4000V;喷雾器压力:35psig;烘干气流:10L/min;温度:350℃;扫描范围:100-800a.m.u.(atomic mass units)。
进一步,该氨基酸神经四肽的合成方法合成的肽产物用Sephedex G-10分子筛凝胶柱层析分离,收集产物洗脱液峰,旋转蒸发浓缩后二次重复上样,得到的洗脱液浓缩后,冻干,利用容器与产物的总质量减去容器本身质量的差量法,计算出所得肽产物的重量,再利用高效液相法检测,根据肽产物纯度乘以重量,得到纯产物的重量,此重量与理论产量的比例就是最终产率。
进一步,胰凝乳蛋白酶在有机溶剂二甲基甲酰胺(DMF)中催化合成二肽叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)时,胰凝乳蛋白酶与有机溶剂二甲基甲酰胺(DMF)构成的合成体系水含量在1.5%、反应温度在40℃、pH为7.5时,叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)产率最高;
胰凝乳蛋白酶在有机溶剂二甲基甲酰胺(DMF)中催化合成二肽叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)时,胰凝乳蛋白酶与有机溶剂二甲基甲酰胺(DMF)构成的合成体系水含量在1.5%、反应温度在40℃、pH为8.0时,叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)产率最高;
碱性蛋白酶(Alcalase)在有机溶剂叔丁醇中催化合成四肽叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)时,碱性蛋白酶(Alcalase)与有机溶剂叔丁醇构成的合成体系水含量在9%、反应温度在37℃、pH为9.0时,四肽叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成产率最高。
进一步,该氨基酸神经四肽的合成方法合成的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后,分子量为435.4,离子峰为436.4(M+1);
合成的二肽产物色氨酸甘氨酸乙脂(Trp-Gly-OEt)经过G-10柱层析纯化后,分子量为289.3,离子峰为290.3(M+1);
四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后,分子量为564.45,离子峰为565.45(M+1)。
本发明提供的氨基酸神经四肽的合成方法,包括:叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)的合成、叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的合成、碱性蛋白酶(Alcalase)的预处理、叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)脱保护、叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成、叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)脱保护、苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)脱保护、肽产物分离纯化,本发明在非水介质中酶法合成了氨基酸神经四肽Phe-Arg-Trp-Gly,是促肾上腺皮质激素(ACTH)活性中心部位的四肽,二肽合成时选择有机溶剂二甲基甲酰胺(DMF),四肽合成时选择有机溶剂叔丁醇,并采用在非水有机溶剂中加入三乙胺助溶剂和适当增加水含量,来增加亲水氨基酸的溶解度,解决了亲水氨基酸的利用问题。提高了亲水氨基酸的利用度,酶法合成反应条件温和,立体专一性强,不用侧链保护基、几无副反应,比通常所用的化学合成法环保,不产生手性分子,不用进一步拆分,提高了收率,并优化了反应条件。
附图说明
图1是本发明实施例提供的氨基酸神经四肽的合成方法的实现流程图;
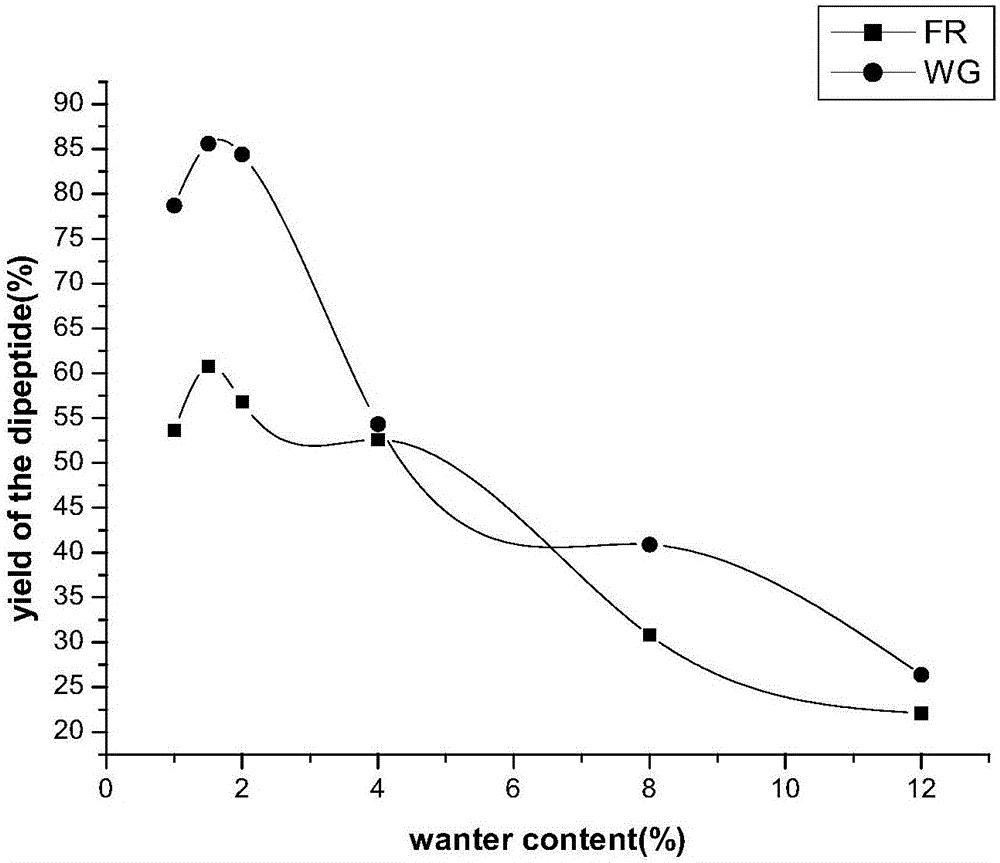
图2是本发明实施例提供的水含量对二肽合成产率的影响示意图;
图3是本发明实施例提供的为水含量对四肽合成产率的影响示意图;
图4是本发明实施例提供的温度对二肽合成产率的影响示意图;
图5是本发明实施例提供的温度对四肽合成产率的影响示意图;
图6是本发明实施例提供的pH对二肽合成产率的影响示意图;
图7是本发明实施例提供的pH对四肽合成产率的影响示意图;
图8是本发明实施例提供的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后的HPLC图;
图9是本发明实施例提供的合成的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后的质谱图;
图10是本发明实施例提供的合成的二肽产物色氨酸甘氨酸乙脂(Trp-Gly-OEt)经过G-10柱层析纯化后的HPLC图;
图11是本发明实施例提供的为合成的二肽产物Trp-Gly-OEt经过G-10柱层析纯化后的质谱图;
图12是本发明实施例提供的为合成的四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后的HPLC图;
图13是本发明实施例提供的合成的四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后的质谱图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
如图1所示,本发明是这样实现的,一种氨基酸神经四肽的合成方法,该氨基酸神经四肽的合成方法包括以下步骤:
步骤S101,叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)的合成:叔丁氧羰基苯丙氨酸(BOC-Phe)加入质量为0.53g(2mmol),精氨酸甲脂(Arg-OMe)加入质量为1.04g(4mmol),有机溶剂二甲基甲酰胺(DMF)20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入胰凝乳蛋白酶(Chymotyrpsin)2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
步骤S102,叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的合成:BOC-Trp加入质量为0.16g(2ml),Gly-OEt加入质量为0.62g(4mmol),有机溶剂二甲基甲酰胺(DMF)20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入胰凝乳蛋白酶(Chymotyrpsin)2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
步骤S103,碱性蛋白酶(Alcalase)的预处理:取2ml碱性蛋白酶(Alcalase)和15ml无水乙醇置于离心管中,旋涡振荡5分钟使其充分混合,混合物3000rpm离心10分钟,碱性蛋白酶(Alcalase)与溶剂无水乙醇完全分开,倾去上层的乙醇,此步操作重复三次;
步骤S104,叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的处理:将含有叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的有机溶剂二甲基甲酰胺(DMF),分别减压蒸馏除去有机溶剂二甲基甲酰胺(DMF),再用乙酸乙酯溶解,乙酸乙酯分别用冷柠檬酸洗三次,冷的碳酸氢钠洗两次,再用冷水洗两次,减压蒸馏,除乙酸乙酯,得微黄色无定型物;
步骤S105,叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)脱保护:叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)产物用TFA(CF3COOH):苯甲醚(9:1)刚好溶解,0℃振荡2-4小时后加入乙醚:石油醚(1:3),得沉淀,离心,再加入由乙醚与石油醚按照1:3比例混合构成的混合液洗沉淀,得色氨酸甘氨酸乙脂(Trp-Gly-OEt);
步骤S106,叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成:取2mmol的叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和4mmol的色氨酸甘氨酸乙脂(Trp-Gly-OEt)加入锥形瓶,加入有机溶剂叔丁醇20ml,碱性蛋白酶(Alcalase)2ml,1ml三乙胺,一定量的Na2CO3-NaHCO3缓冲液,37℃水浴振荡24小时,每隔4h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成;
步骤S107,叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)脱保护:叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)产物用TFA(CF3COOH):苯甲醚(9:1)刚好溶解,0℃振荡2-4小时后加入乙醚:石油醚(1:3),得沉淀,离心,再加入由乙醚与石油醚按照1:3比例混合构成的混合液洗沉淀,得苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt);
步骤S108,苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)脱保护:取4.4g苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt),加入24ml甲醇,12.5mlNaOH(2mol/L),反应一小时,用HCl(1mol/L)调节pH至7,抽去甲醇,加水稀释,过滤,冰浴冷却,水洗到中性,得氨基酸神经四肽(Phe-Arg-Trp-Gly),用质谱检测产物;
步骤S109,肽产物分离纯化:柱料采用Sephadex G-10,层析柱为16mm×1000mm,洗脱液采用蒸馏水,检测波长为220nm,流速为1.0ml/min,取100g Sephadex G-10干柱料,加500ml蒸馏水浸泡过夜,减压除气泡后装柱,洗脱液平衡过夜,待分离液体0.5ml上样层析,收集产品峰,冻干得产物。
在本发明实施例中,该氨基酸神经四肽的合成方法采用高效液相法(HPLC)检测肽合成纯度,定量分析肽产物的方法用于合成肽的分析检测,采用高效液相色谱仪,型号为C18,250×4.6mm的Diamosil色谱柱,220nm DAD紫外检测器,柱温25℃,溶剂A采用0.1%三氟乙酸的乙腈,溶剂B采用含0.1%三氟乙酸的水,流速为1.0ml/min,具体梯度为:
在本发明实施例中,该氨基酸神经四肽的合成方法采用质谱确定分子量的方法鉴定肽产物,质谱(MS)条件如下:离子化模式:API–ES;极性:阳性;电压:4000V;喷雾器压力:35psig;烘干气流:10L/min;温度:350℃;扫描范围:100-800a.m.u.(atomic mass units)。
在本发明实施例中,该氨基酸神经四肽的合成方法合成的肽产物用Sephedex G-10分子筛凝胶柱层析分离,收集产物洗脱液峰,旋转蒸发浓缩后二次重复上样,得到的洗脱液浓缩后,冻干,利用容器与产物的总质量减去容器本身质量的差量法,计算出所得肽产物的重量,再利用高效液相法检测,根据肽产物纯度乘以重量,得到纯产物的重量,此重量与理论产量的比例就是最终产率。
在本发明实施例中,胰凝乳蛋白酶在有机溶剂二甲基甲酰胺(DMF)中催化合成二肽叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)时,胰凝乳蛋白酶与有机溶剂二甲基甲酰胺(DMF)构成的合成体系水含量在1.5%、反应温度在40℃、pH为7.5时,叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)产率最高;
胰凝乳蛋白酶在有机溶剂二甲基甲酰胺(DMF)中催化合成二肽叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)时,胰凝乳蛋白酶与有机溶剂二甲基甲酰胺(DMF)构成的合成体系水含量在1.5%、反应温度在40℃、pH为8.0时,叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)产率最高;
碱性蛋白酶(Alcalase)在有机溶剂叔丁醇中催化合成四肽叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)时,碱性蛋白酶(Alcalase)与有机溶剂叔丁醇构成的合成体系水含量在9%、反应温度在37℃、pH为9.0时,四肽叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成产率最高。
在本发明实施例中,该氨基酸神经四肽的合成方法合成的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后,分子量为435.4,离子峰为436.4(M+1);
合成的二肽产物色氨酸甘氨酸乙脂(Trp-Gly-OEt)经过G-10柱层析纯化后,分子量为289.3,离子峰为290.3(M+1);
四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后,分子量为564.45,离子峰为565.45(M+1)。
下面结合附图及具体实施例对本发明的应用原理作进一步描述。
3实验部分
3.1实验材料
3.1.1氨基酸及其衍生物
BOC-Phe;Arg-OMe.2HCl;BOC-Trp;Gly-OEt.HCl.(均购自吉尔生化)
3.1.2酶
木瓜蛋白酶(Papain,Merch Germany,
胰凝乳蛋白酶(Chymotrypsin),Serva USA,
胰蛋白酶(trypsin),购自北京鼎国生物技术有限责任公司(Geview分装)
碱性蛋白酶Alcalase,购自Novo-Nordisk(丹麦)
3.1.3试剂
四氢呋喃,无水乙醇,无水甲醇,冰乙酸,浓盐酸,三氟乙酸(自上海吉尔生化有限责任公司),乙腈(色谱级)(DIKMA,USA),氢氧化钠,磷酸氢二钠,磷酸二氢钠,二甲基甲酰胺(DMF),稀盐酸,NaCl,碳酸钠,碳酸氢钠,三羟甲基氨基甲烷(Tris),乙酸乙酯,异丙醇,柠檬酸,苯甲醚,乙醚,石油醚,甲醇,异丁醇,叔丁醇等均为分析纯。
3.1.4分离纯化填料
层析填料SephadexG-10,Pharmacia
3.2仪器
Power DryLL3000冷冻干燥机(Heto公司),
J2-21M高速冷冻离心机(Beckman,美国),
JJ-1型定时电动搅拌器(江苏中大仪器厂),
pH S-2C型精密酸度计(上海雷磁仪器厂),
ESJ180-4电子天平(沈阳龙腾电子称量仪器有限公司),
ZFQ85A型旋转蒸发仪(上海医疗器械厂),
SHA-C型水浴恒温振荡器(江苏常州国华仪器厂),
干燥箱(上海实验仪器总厂),
色谱柱(反相柱Diamosil C18,250×4.6mm),
HD-2000型紫外检测器(上海嘉鹏科技有限公司),
分析型高压液相色谱仪(Waters美国),
LM17型记录仪(永青示波器厂),
P-1型横流泵(Pharmacia瑞典),
HL-2型横流泵(上海精科实业有限公司),
电喷雾质谱仪(美国应用生物系统公司)
3.3实验方法
3.3.1肽的酶促合成
3.3.1.1二肽的酶促合成
(1)叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)的合成
叔丁氧羰基苯丙氨酸(BOC-Phe)加入质量为0.53g(2mmol),精氨酸甲脂(Arg-OMe)加入质量为1.04g(4mmol),有机溶剂20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入酶2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成。
(2)叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的合成
BOC-Trp加入质量为0.16g(2ml),Gly-OEt加入质量为0.62g(4mmol),有机溶剂20ml,1ml三乙胺,一定量的三羟甲基氨基甲烷-盐酸缓冲液(Tris-HCl buffer),加入酶2g,40℃水浴振荡3天,每隔8h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成。
3.3.1.2 Phe-Arg-Trp-Gly四肽的酶促合成
(1)酶的预处理:取2ml Alcalase和15ml无水乙醇置于离心管中,旋涡振荡5分钟使其充分混合,混合物3000rpm离心10分钟,酶与溶剂完全分开,倾去上层的乙醇,此步操作重复三次。
(2)二肽产品处理:将含有叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的有机溶剂,分别减压蒸馏除去有机溶剂,产品再用乙酸乙酯溶解。乙酸乙酯分别用冷柠檬酸洗三次,冷的碳酸氢钠洗两次,再用冷水洗两次,减压蒸馏,除乙酸乙酯。得微黄色无定型物。
(3)叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)脱保护:叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)产物用TFA(CF3COOH):苯甲醚(9:1)刚好溶解,0℃振荡2-4小时后加入乙醚:石油醚(1:3),得沉淀,离心。再加入由乙醚与石油醚按照1:3比例混合构成的混合液洗沉淀,得色氨酸甘氨酸乙脂(Trp-Gly-OEt)。
(4)四肽合成:取2mmol的叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)和4mmol的色氨酸甘氨酸乙脂(Trp-Gly-OEt)加入锥形瓶,加入有机溶剂20ml,酶2ml,1ml三乙胺,一定量的Na2CO3-NaHCO3缓冲液,37℃水浴振荡24小时,每隔4h取50μl加入500μl冰乙酸终止反应,用质谱检测产物的生成。
(5)叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)四肽脱保护方法同3.3.1.2(3)叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)二肽脱保护的方法,得苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)。
(6)苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)脱保护,取4.4g上步骤(5)苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt),加入24ml甲醇,12.5mlNaOH(2mol/L),反应一小时,用HCl(1mol/L)调pH7,抽去甲醇,加水稀释,过滤,冰浴冷却,水洗到中性,得Phe-Arg-Trp-Gly用质谱检测产物。
3.3.2肽产物分离纯化
柱料:Sephadex G-10,层析柱:16mm×1000mm,洗脱液:蒸馏水,检测波长:220nm,流速:1.0ml/min;
取100g Sephadex G-10干柱料,加500ml蒸馏水浸泡过夜,减压除气泡后装柱。洗脱液平衡过夜。待分离液体0.5ml上样层析。主要用于合成二肽、四肽及其衍生物的分离纯化。收集产品峰,冻干得产物。
3.3.3肽产物的分析
高效液相法(HPLC)检测肽合成纯度:
定量分析肽产物的方法,用于合成肽的分析检测,
高效液相色谱仪:Waters
色谱柱:C18,250×4.6mm,Diamosil
检测器:DAD紫外检测器,220nm
柱温:25℃
洗脱条件:
溶剂A:0.1%三氟乙酸的乙腈
溶剂B:0.1%三氟乙酸的水
流速:1.0ml/min。
3.3.4肽产物的鉴定
产物的鉴定主要使用质谱确定分子量的方法。酶促肽合成因其条件温和,催化专一性强,故基本没有氨基酸内部共价键的断裂,而且由于使用N端保护氨基酸为底物,基本避免了与目标产物氨基酸顺序相反的副产物的产生,因此通过确定分子量的方法就可以鉴定产物。质谱(MS)条件如下:离子化模式:API–ES;极性:阳性;电压:4000V;喷雾器压力:35psig;烘干气流:10L/min;温度:350℃;扫描范围:100-800a.m.u.(atomic mass units)。
3.3.5产率计算
合成的肽产物用Sephedex G-10分子筛凝胶柱层析分离,收集产物洗脱液峰,旋转蒸发浓缩后二次重复上样,得到的洗脱液浓缩后,冻干,利用差量法(容器与产物的总质量减去容器本身的质量)计算出所得产物的重量,再利用高效液相法检测,根据其纯度乘以重量,得到纯产物的重量,此重量与理论产量的比例就是最终产率。
4结果和讨论
4.1酶和有机溶剂的选择
(1)酶促二肽的合成
在不同的有机溶剂中使用不同的酶,操作步骤见方法3.3.1.1,溶液pH值均用Tris-HCl缓冲液调整,水含量及使用的有机溶剂见表1,结果见表1。
表1酶催化二肽合成
注:F(BOC-Phe),R(Arg-OMe),F-R(BOC-Phe-ArgOMe)
W(BOC-Trp),G(Gly-OEt),W-G(叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt))
木瓜蛋白酶(papain),胰蛋白酶(Trypsin)
胰凝乳蛋白酶(Chymotyrpsin),DMF(二甲基甲酰胺)
采用四种酶催化二肽的合成,从表1中可看出,一般情况下,酶促肽合成产率在20-40%左右,但是胰凝乳蛋白酶在DMF中催化合成产率较高,达到60%以上,说明此体系适合二肽的合成。这是因为Phe和Trp等芳香族氨基酸是胰凝乳蛋白酶的水解底物,与胰凝乳蛋白酶活性中心相吻合,胰凝乳蛋白酶的活性中心利于芳香族氨基酸进入,因此合成产率会最高。而其它的酶由于底物与酶的活性中心结构不很吻合,所以产率较低。
(2)叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)四肽的酶促合成
酶催化四肽的合成,见方法3.3.1.2(4),叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)四肽的酶促合成结果见表2。
表2酶催化四肽合成
从表2中看出Alcalase在叔丁醇中合成四肽产率最高。Alcalase是从枯草杆菌中提取的一种蛋白酶,主要成分枯草杆菌(Subtilisin)丝氨酸蛋白酶,是细菌蛋白酶之一,它在醇溶液中能保持很好的活力。在四肽合成时,利用Alcalase在叔丁醇中催化四肽合成,由于叔丁醇溶剂亲水,所以二肽底物溶解性比其它有机溶剂溶解性要高,三乙胺也能促进底物的溶解,另外Alcalase对于含亲水性氨基酸的合成产率较高。由于溶剂亲水性增强,木瓜蛋白酶、胰蛋白酶和胰凝乳蛋白酶在叔丁醇中活力丧失很多,而在其它溶剂中又必须加入大量水使底物很好溶解,否则产率很低。同时,二肽底物并不符合胰凝乳蛋白酶的活性中心结构,所以产率不是很高。通过实验,找到了对肽合成起决定作用的酶Alcalase。
酶促肽合成中有机溶剂的选择也是很重要的,这是因为用有机溶剂代替水相,平衡向肽合成方向进行,肽生成后,扩散到有机溶剂中,反应才能顺利进行。酶也只有在某些有机溶剂中才有活力,在其它溶剂中活力很小或没有。针对不同溶剂的亲水性和极性情况,合成二肽和四肽分别选用了不同的有机溶剂,从实验结果来看,这些有机溶剂对酶促肽合成产率有一定的影响,其中胰凝乳蛋白酶在二甲基甲酰胺中产率较高,Alcalase在叔丁醇中产率较高。选择有机溶剂首先要考虑其亲水性,亲水性的有机溶剂能溶解亲水性的氨基酸,增加底物浓度就可以提高产率,DMF和叔丁醇均与水互溶。另一个考虑因素是有机溶剂的沸点,在产物处理时需要减压蒸馏或旋转蒸发,若沸点过高,产物分离很困难。DMF和叔丁醇沸点在100℃左右。另外还要考虑的是有机溶剂毒性,尽量选择毒性较小的有机溶剂,DMF和叔丁醇的毒性很小。
4.2体系水含量对肽合成的影响
图2为水含量对二肽合成产率的影响示意图,图3为水含量对四肽合成产率的影响示意图。从图2看出,水含量在1.5%时,二肽产率达到最高。从图3看出水含量在9%时,四肽产率达到最高。有机溶剂中水含量对酶活性的影响是非常重要的,通常体系中的水以三种方式存在:与酶结合的水,与水不溶物的结合水,游离在溶剂中的水。酶在有机溶剂中催化有一个最适含水量,当含水量高于最适水含量时,水会竞争亲核试剂的结合位点,造成酯底物水解,降低了目标产物的收率,当含水量低于最适水含量时酶构象过于刚性,同时溶剂的强极性夺取了酶的必须水,造成酶的催化活力降低甚至失活,只有在最适合水含量下,酶分子既有一定的刚性,又有一定的柔性,肽产率才能最高。系统的含水量与溶剂的疏水性有关,溶剂越亲水,系统含水量就越多,因为溶剂亲水,争夺酶的必需水的能力就越强,只有多加些水,才能保证酶的活性。这也是Alcalase-叔丁醇体系中的含水量高于胰凝乳蛋白酶-DMF体系含水量的原因之一,叔丁醇的亲水性要大于DMF的亲水性。另外,反应体系中的水含量不仅影响酶的催化活性,还影响酶的立体选择性,这是因为水改变了酶分子的柔性,对映体的选择性和含水量有依赖关系。
4.3反应温度的影响
图4为温度对二肽合成产率的影响示意图,图5为温度对四肽合成产率的影响示意图。从图4看出,当反应温度在40℃时,二肽产率达到最高;从图5看出,当反应温度在37℃时,四肽产率达到最高。通常提高反应温度可以提高酶催化的反应速度。温度过低,反应速度很慢;但温度过高会引起酶变性,造成酶催化活力明显下降。本研究考察了反应温度对目标肽合成收率的影响。分析认为在酶分子处于最适合温度,活力达到最高。在实验中发现,酶在有机溶剂中的最适温度要高于水相的最适温度,这是因为在有机溶剂中酶分子静电相互作用要大于在水相中的静电作用,分子刚性增强,柔性降低,其热稳定性提高,这也是酶在有机溶剂中催化肽合成的一个优点。
4.4体系pH的影响
图6为pH对二肽合成产率的影响示意图,图7为pH对四肽合成产率的影响示意图。从图6中看出,当pH为7.5时,叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)产率达到最高,当pH为8.0时,叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)合成产率达到最高;从图7中看出,当pH为9.0时,四肽叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成产率达到最高。在有机溶剂中酶也有最适pH范围,与水相相比差别不大。pH既能影响底物分子的解离状态,也会影响酶分子的解离状态,最适pH与二者的解离都有关系,在最适pH下,底物分子和酶的活性中心分子处于最易结合状态,在此条件下酶活力最高,能很好的结合形成复合中间体,有利于肽合成。另外,在有机溶剂中pH影响酶分子一些基团的解离,是酶的构象发生改变,使其最适pH发生变化,也影响肽合成的产率。
4.5肽产物的分析和鉴定
图8显示的是合成的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后的HPLC图。
图9为合成的二肽产物叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)经过G-10柱层析纯化后的质谱图,分子量为435.4,在质谱图上离子峰为436.4(M+1)。
图10为合成的二肽产物色氨酸甘氨酸乙脂(Trp-Gly-OEt)经过G-10柱层析纯化后的HPLC图。
图11为合成的二肽产物色氨酸甘氨酸乙脂(Trp-Gly-OEt)经过G-10柱层析纯化后的质谱图,分子量为289.3,在质谱图上离子峰为290.3(M+1)。
图12为合成的四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后的HPLC图。
图13.显示的是合成的四肽产物Phe-Arg-Trp-Gly经过G-10柱层析纯化后的质谱图,分子量为564.45,在质谱图上离子峰为565.45(M+1)。
5结论
在以氨基酸神经四肽Phe-Arg-Trp-Gly为目标的肽合成研究中,考察了对肽合成有影响的许多因素,首先找到了最佳的酶来催化肽的合成,其次发现有机溶剂对肽合成的产率也有影响,找到了适合的有机溶剂DMF和叔丁醇。在实验中改变体系水含量、pH和反应温度来寻找最佳反应条件,构建了最佳反应模型,使二肽的产率分别到达61.25%,85.6%,四肽产率也达到68.32%。
本实验要解决的一个问题是亲水性底物的利用问题,那么首先要考虑亲水性底物在有机溶剂中溶解度,这就必须选择适当的有机溶剂,二肽合成时选择DMF,四肽合成时选择叔丁醇,这两种溶剂都对底物有良好的溶解性,其次加入三乙胺,其目的是增加底物的溶解性,有助于反应的进行。
本发明实施例提供的氨基酸神经四肽的合成方法,包括:叔丁氧羰基苯丙氨酸精氨酸甲脂(BOC-Phe-Arg-OMe)的合成、叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)的合成、碱性蛋白酶(Alcalase)的预处理、叔丁氧羰基色氨酸甘氨酸乙脂(BOC-Trp-Gly-OEt)脱保护、叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)合成、叔丁氧羰基苯丙氨酸精氨酸色氨酸甘氨酸乙脂(BOC-Phe-Arg-Trp-Gly-OEt)脱保护、苯丙氨酸精氨酸色氨酸甘氨酸乙脂(Phe-Arg-Trp-Gly-OEt)脱保护、肽产物分离纯化,本发明在非水介质中酶法合成了氨基酸神经四肽Phe-Arg-Trp-Gly,是促肾上腺皮质激素(ACTH)活性中心部位的四肽,二肽合成时选择有机溶剂二甲基甲酰胺(DMF),四肽合成时选择有机溶剂叔丁醇,并采用在非水有机溶剂中加入三乙胺助溶剂和适当增加水含量,来增加亲水氨基酸的溶解度,解决了亲水氨基酸的利用问题。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 合成含有氨基酸和/或肽的接枝共聚物的制作方法
- 一种新的多肽——人兴奋型氨基酸转动器16和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人兴奋性氨基酸转运蛋白10和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人兴奋性氨基酸转动蛋白9和编码这种多肽的多核苷酸的制作方法
- 含有非天然氨基酸和多肽的组合物、涉及非天然氨基酸和多肽的方法以及非天然氨基酸 ...的制作方法
- 用于修饰非天然氨基酸和非天然氨基酸多肽的促进剂的制作方法
- 一种新的多肽——核糖体蛋白l299.13和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人s4核糖体蛋白79.2和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人核糖体蛋白s613.31和编码这种多肽的多核苷酸的制作方法
- 一种新的多肽——人s4核糖体蛋白10和编码这种多肽的多核苷酸的制作方法