Carboxy-DiI类化合物及其制备方法和应用与流程
本发明涉及检测领域,尤其涉及一种carboxy-dii类化合物及其制备方法和应用。
背景技术:
荧光染料作为标记探针在化学、生物等领域得到广泛的应用,尤其是在生命科学、临床分子诊断、免疫功能分析等方面备受关注。其中,cy系列荧光染料是应用最广的染料,具有摩尔消光系数大、稳定性好、荧光量子产率高等优点。例如,在红外(nir)可见光区的吸收及发射范围内,羰化青染料作为有助于生物成像的探针试剂,具有折光率小、组织渗透深、背景自发荧光干扰小等优点,近些年来备受瞩目。然而,对于慢性心脏病患者而言,尤其是慢性心梗患者,心脏的供血及供氧离不开冠脉微循环系统,常规羰化青染料却不适用于对其进行检测评估。
技术实现要素:
基于此,有必要提供一种carboxy-dii类化合物及其制备方法和应用,能够适用于微小动脉血管的检测、评估。
本发明提供一种carboxy-dii类化合物,具有如式(i)所示的结构:
其中,r1、r4分别独立选自氢、磺酸基、磺酸盐、羧基、羧酸盐、苯甲酸基、苯甲酸盐、苯磺酸基或者苯磺酸盐,r2和r3分别独立选自氢、c1-c4烷基或者卤素,r5和r6分别独立选自c12-c20烷基,y-为一价负离子。
其中一些实施例中,r2和r3优选均为氢。r5和r6相同,优选c14-c18烷基。y-优选自高氯酸根、氯离子、溴离子或者碘离子。
其中一些实施例中,所述carboxy-dii类化合物优选自结构如式(ii)所示化合物或者结构如式(iii)所示化合物:
本发明还提供一种carboxy-dii类化合物的制备方法,包括如下步骤:
式(iv)所示化合物与式(v)所示化合物反应,制备获得如式(vi)所示的中间产物m1。
中间产物m1和式(vii)所示化合物反应,制备获得如式(viii)所示的中间产物m2。
中间产物m2与r1-b(oh)2反应,制备获得目标产物,即得。
其中,r1选自氢、磺酸基、磺酸盐、羧基、羧酸盐、苯甲酸基、苯甲酸盐、苯磺酸基或者苯磺酸盐,r5选自c14-c18烷基,r7选自氢或者卤素,y-为一价负离子,优选碘离子。
优选地,式(iii)所示化合物的合成路如下:
本发明还提供上述任一项所述的carboxy-dii类化合物作为水溶性荧光染料在制备发光材料、制备生物荧光探针或者生物荧光成像中的应用。
本发明还提供一种标记检测动脉血管分布的方法,包括如下步骤:采用上述所述的carboxy-dii类化合物作为水溶性荧光染料进行心脏灌注,利用多聚甲醛固定和琼脂糖包埋,进行心脏组织切片;利用激光共聚焦显微镜扫描所述心脏组织切片,获得血管3d网络分布图像。
与现有技术相比,本发明carboxy-dii类化合物为水溶性荧光染料,可在磷酸缓冲液溶解均一,能够适用于心脏活体动脉灌注,透过细胞膜脂质双分子层标记血管内皮细胞,均匀标记微小动脉血管内皮细胞,选择性好,特异性高,荧光标记效率也高。
附图说明
图1为实施例1中的化合物2制备过程中的lcms检测图;
图2为实施例1中的化合物3制备过程中的lcms检测图;
图3为实施例1中的化合物4制备过程中的lcms检测图;
图4为实施例1中的目标化合物a制备过程中的lcms检测图;
图5为实施例1中的目标化合物a的质谱图;
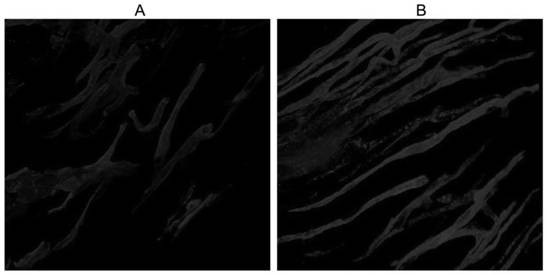
图6为实施例4测试获得的血管动脉分布图。
具体实施方式
以下对本发明的原理和特征进行描述,所举实例只用于解释本发明,并非用于限定本发明的范围。除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。
实施例1
本实施例提供一种carboxy-dii类化合物a的合成方法,包括如下步骤:
s1,参照如下反应式,在25℃条件下,将化合物1(10.0g,1.00eq,hcl)溶解于80ml醋酸溶液(含化合物1a,7.71g,9.57ml,2.00eq)中,加热至130℃,反应16h,得含化合物2的反应混合物。采用200ml水洗反应混合物后,采用乙酸乙酯分三次提取反应混合物,每次用量100ml,得有机层混合物,再用饱和nahco3水溶液调ph至8,用无水硫酸钠吸水,真空干燥,得棕色油状化合物2,产率88.6%,纯度94.4%。化合物2反应进程采用lcms监测,结果如附图1所示。
s2,参照如下反应式,将步骤s2制备的化合物2(4.00g,1.00eq)和化合物2a(7.01g,1.00eq)混合,于140℃条件下,搅拌反应4h,得反应混合物。将反应混合物冷却至25℃,用100ml乙醇溶解,在搅拌条件下加入100mlki,反应1h,过滤,滤饼真空干燥,得红色固体化合物3粗品4.40g。反应化合物3反应进程采用lcms监测,结果如附图2所示。
s3,参照如下反应式,在20℃条件下,将化合物3a(500g,1.00eq)溶解于20.0ml二甲氧基乙烷中,再加入步骤s2制备的化合物3粗品(500g,1.00eq),加热至120℃,反应2h,真空浓缩,得浓缩反应混合物。再采用硅胶柱层析(石油醚/乙酸乙酯=1/1,二氯甲烷/甲醇=10/1,rf=0.4)纯化反应混合物,得紫色固体化合物4粗品2.00g。反应化合物4反应进程采用lcms监测,结果如附图3所示。
s4,将步骤s3制备的化合物4(237.25mg,1eq)、羧基苯硼酸(106.36mg,3eq)、k2co3(118.11mg,4eq)和pd(dppf)cl2(15.63mg,0.1eq)混合,加入5ml四氢呋喃和2ml双蒸水,加热100℃,搅拌反应16h,浓缩混合物后,再用100ml二氯甲烷稀释,再分别用1nhcl(aq.,50ml)和1mnaoh(aq.,50ml)洗涤,浓缩二氯甲烷层得到粗提物。将粗提物用色谱柱层析法纯化(sio2,二氯甲烷:甲醇=10:1to1:1,产物rf=0.2by二氯甲烷:甲醇=4:1),得到黑棕色目标产物a(189mg,产率83.55%,纯度96.2%)。目标产物a反应进程采用lcms监测,结果如附图4所示,hnmr图如图5所示。
实施例2
本实施例提供一种利用carboxy-dii类化合物标记检测动脉血管分布的方法,包括如下步骤:
(1)心脏灌注,制备组织标本:
将实验大鼠结扎左前降支45min后进行心脏灌注。心脏灌注开始前,连接好2个三通活栓和3个10ml注射器,其内分别装有pbs缓冲液、含carboxy-dii类化合物工作液(取5mg实施例1制备获得的carboxy-dii类化合物a粉末溶解于1ml无水乙醇,再转溶解于50ml由按体积比1:4混pbs缓冲液和5%葡萄糖溶液混合而成的缓冲液中)以及4%多聚甲醛,并排空注射器内气泡。用25号蝶形针从左心室扎入并固定,开右心房剪一开口引流灌注液,自左心室分别依次缓慢注入37℃pbs缓冲液、carboxy-dii工作液和4%多聚甲醛各10ml(1-2ml/min)。carboxy-dii工作液顺应血流从动脉泵出染色动脉血管,心脏灌注结束后,留取心肌标本,在4%的多聚甲醛液内避光固定24h后,将各组标本在包埋盒内用60℃5%琼脂糖(111860,gene公司)包埋,组织标本块可在4℃冰箱内避光保存1个月。
(2)采用激光共聚焦评估动脉血管开放状态,实现血管3d网络化重建:
取琼脂糖包埋的心脏组织标本,震荡切片(厚度100μm),80%甘油覆盖封片后,用confoacl显微镜检查分析c-dii灌注后的心脏血管密度。利用荧光显微镜(leicadmi8german)检测:物镜10×,目镜10×,聚焦后通过调整细准焦螺旋来观看微血管脉络的走向。所有照片均未经过任何亮度、对比度调节等处理。激光共聚焦显微镜(leicasp8stedgerman)观察,z轴步距0.4μm,激发波长570nm,发射波长590nm。采用扫描程序对整张切片进行无损伤连续断层扫描,首先手动确定图像的顶部,然后逐层往图像底部扫描,手动确定图像底部后按z轴步距连续扫描。将数字化图像存储,采用自带软件对所取图像进行图像提取和分析。
通过使用激光扫描共聚焦显微镜(leicasted/sp8st3d,leicamicrosystems)将整个心脏组织扫描至100μm的深度来观察血管网络。通过用fijiimagej软件的血管分析模块评估,归一化至整个扫描的心脏组织的carboxy-dii标记的血管的总量来量化心脏血管密度。从z系列堆栈生成共焦图像堆栈的正交投影。使用体3d图像分析执行共焦图像堆栈的三维(3d)渲染,结果如图6中的a图和b图所示。
由图6可以看出,采用本发明carboxy-dii类化合物可作为水溶性荧光染料,均匀标记微小动脉血管内皮细胞,特异性高,荧光标记效率高。
以上实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述仅为本发明的较佳实施例,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!