一种研磨法制备N,N-二甲基二硫代乙酸苯酯类化合物的方法与流程
本发明属于医药中间体制备技术领域,具体涉及一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法。
背景技术:
有机含硫化合物是非常重要的原料,广泛用于存在于医药农药、食品香料和功能材料结构中。碳-硫键偶联反应是制备有机含硫化合物的主要途径,也是有机反应中的一类重要的化学反应之一,吸引着越来越多的有机合成工作者的兴趣。传统构建碳-硫键方法是通过具有亲核性质的硫和具有亲电性的碳反应。但是,硫醇(酚)等参与的硫化过程中可能会遇到以下困难:①硫原子上孤对电子对金属催化剂具的毒化作用;②极易氧化生成副产物过硫化合物;③亲核性单一,不能满足反应多样性的要求。除此之外,大多数有机硫化物的使用,常常面临着刺激恶臭、有毒有害等生产缺点。本方法无需过渡金属催化剂,以无难闻气味和便宜易得的原料,经过三组分反应一步实现n,n-二甲基二硫代乙酸苯酯类化合物的高效制备,具有成本低廉、原料简单易得,适用范围广泛、产率优秀,产物处理方便、符合环保的要求。本方法能够实现一锅二硫代脂类化合物的合成,在相关的医药合成领域具有重要的应用前景。
技术实现要素:
针对现有技术中存在的问题,本发明目的在于在提供n,n-二甲基二硫代乙酸苯酯类化合物的方法。
本发明通过以下技术方案加以实现:
所述的一种研磨法制备式(ⅳ)所示的n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于制备方法为:式(ⅰ)所示的苯硫酚类化合物、式(ⅱ)所示的二氯亚砜和式(ⅲ)所示的n,n-二甲基苯甲酰基烯丙胺,常温、常压下在有机溶剂介质中,在有机碱的促进下,通过研磨充分反应,制得产物,所述产物通过后处理制得n,n-二甲基二硫代乙酸苯酯类化合物;所述的有机碱为三乙胺(tea),所述有机溶剂为二氯甲烷(dce),
式(ⅰ)r1选自下列之一:氢、甲基、甲氧基、烯丙基、醛基、苯基。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于所述苯硫酚类化合物、二氯亚砜和溶剂二氯甲烷的比例为5mmol/6mmol/15ml。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于所述苯硫酚类化合物、二氯亚砜和与三乙胺的比例为5mmol/6mmol/15mmol。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于所述苯硫酚类化合物、二氯亚砜与n,n-二甲基苯甲酰基烯丙胺的当量比为1:(1-1.2):1。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于所述反应温度为常温25℃,反应时间为10小时。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于所述后处理的具体方法由以下步骤组成:
1)萃取:反应结束后,往反应物中加入10ml饱和氯化钠水溶液,然后用乙酸乙酯萃取3次,每次10ml,萃取液合并;
2)浓缩:将萃取液用无水硫酸钠干燥,旋转蒸发仪旋干,得浓缩物;
3)将浓缩物用柱层析硅胶吸附,加入到200-300目的层析硅胶柱中,以正己烷:乙酸乙酯按一定的比例快速柱层析,洗脱液合并,旋转蒸发仪旋干,油泵抽得产物n,n-二甲基二硫代乙酸苯酯类化合物。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于步骤2)中干燥时间为2小时。
所述的一种研磨法制备n,n-二甲基二硫代乙酸苯酯类化合物的方法,其特征在于步骤3)中正己烷和乙酸乙酯的比例为3:1-1:1。
本发明原料无难闻气味、简便易得;制备条件温和,反应在常压、常温下进行,节约成本,对设备的要求较低,易于推广;无需过渡金属催化剂催化,产物后处理方便;方法完全符合环保要求,所得产物在医药合成领域有非常重要的应用价值,适用于二硫代酯类化合物大规模工业化生产,具有极大的工业应用前景。
附图说明
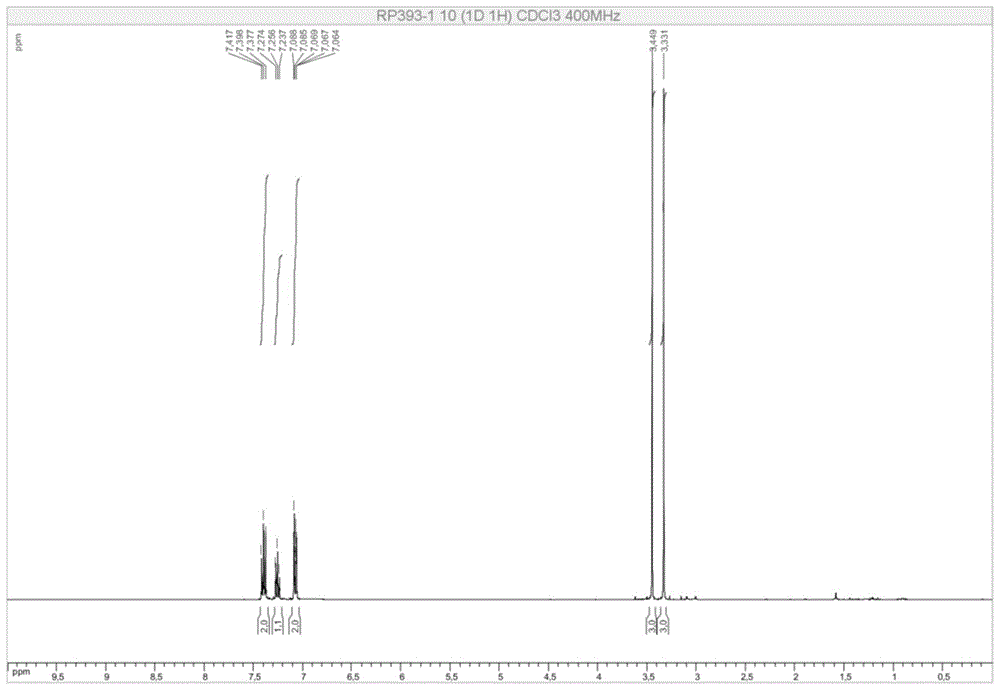
图1为本发明中产物4a的1h-nmr谱;
图2为本发明中产物4b的1h-nmr谱;
图3为本发明中产物4c的1h-nmr谱;
图4为本发明中产物4d的1h-nmr谱;
图5为本发明中产物4e的1h-nmr谱;
图6为本发明中产物4f的1h-nmr谱;
图7为本发明中产物4g的1h-nmr谱;
图8为本发明中产物4h的1h-nmr谱;
图9为本发明中产物4i的1h-nmr谱;
图10为本发明中产物4j的1h-nmr谱;
图11为本发明中产物4k的1h-nmr谱;
图12为本发明中产物4l的1h-nmr谱;
图13为本发明中产物4g的1h-nmr谱;
图14为本发明中产物4g的13c-nmr谱;
图15为本发明中产物4h的1h-nmr谱;
图16为本发明中产物4h的13c-nmr谱;
具体实施方式
以下结合具体实施例对本发明予以进一步详述。
本发明合成步骤,在25ml的圆底烧瓶中分别加入5mmol苯硫酚类化合物1、6mmol二氯亚砜2和5mmol的n,n-二甲基苯甲酰基烯丙胺3,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4纯品,产率83-95%。具体实施例和表征数据如下,所有产物结构经过核磁共振和质谱结果对比得以确定。
实施例1:产物4a的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4a纯品(839mg,产率89%,淡黄色固体)。4a1hnmr图谱见图1,4a13cnmr图谱见图2。
1hnmr(400mhz,cdcl3)δ:7.43-7.37(m,2h),7.29-7.23(m,1h),7.10-7.05(m,2h),3.45(s,3h),3.33(s,3h);
13cnmr(100mhz,cdcl3)δ:187.9,154.2,129.3,126.0,122.9,43.3,38.8;
hrms(apci):[m+h]+calcd.m/zforc10h14ns2212.0562,foundm/z212.0560.
实施例2:产物4b的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol对甲基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4b纯品(956mg,产率85%,淡黄色固体)。4b1hnmr图谱见图3,4b13cnmr图谱见图4。
1hnmr(600mhz,cdcl3)δ:7.19(d,j=8.0hz,2h),6.95(d,j=8.0hz,2h),3.46(s,3h),3.34(s,3h),2.36(s,3h);
13cnmr(150mhz,cdcl3)δ:188.3,152.0,135.7,129.9,122.5,43.4,38.8,21.1;
hrms(esi):[m+h]+calcd.forc11h16ns2m/z226.0719,foundm/z226.0717.
实施例3:产物4c的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol对烯丙基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4c纯品(1042mg,产率83%,淡黄色固体)。4c1hnmr图谱见图5,4c13cnmr图谱见图6。
1hnmr(400mhz,cdcl3)δ:6.98(d,j=8.2hz,1h),6.82(bs,1h),6.82(d,j=8.2hz,1h),6.01(ddt,j=17hz,10.1hz,6.8hz),5.18-5.08(m,2h),3.84(s,3h),3.48(s,3h),3.42(d,j=6.8hz,2h),3.37(s,3h);
13cnmr(100mhz,cdcl3)δ:188.1,151.3,141.3,138.9,137.1,123.7,116.2,120.5,113.0,56.0,43.4,40.2,38.7;
hrms(esi):[m+h]+calcd.forc13h18ns2m/z252.0875,foundm/z252.0873.
实施例4:产物4d的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol2,4,5-三甲基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4d纯品(1088mg,产率86%,淡黄色固体)。4d1hnmr图谱见图7,4d13cnmr图谱见图8。
1hnmr(400mhz,cdcl3)δ:6.91(s,2h),3.51(s,3h),3.40(s,3h),2.31(s,3h),2.16(s,6h);
13cnmr(100mhz,cdcl3)δ:186.6,149.0,135.3,130.4,129.2,43.3,38.4,20.9,16.5;
hrms(apci):[m+h]+calcd.forc13h20ns2m/z254.1032,foundm/z254.1030.
实施例5:产物4e的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol3-甲氧基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4e纯品(1085mg,产率90%,淡黄色固体)。4e1hnmr图谱见图9,4e13cnmr图谱见图10。
1hnmr(400mhz,cdcl3)δ:7.28(t,j=8.0hz,1h),6.80(ddd,j=8.4hz,j=2.3,0.7hz,1h),6.67(ddd,j=8.4hz,j=2.3,0.7hz,1h),6.63(t,j=2.3hz,1h),3.80(s,3h),3.46(s,3h),3.34(s,3h);
13cnmr(100mhz,cdcl3)δ:187.7,160.4,155.0,129.5,115.1,111.8,108.9,55.5,43.3,38.8;
hrms(esi):[m+h]+calcd.forc11h16nos2m/z242.0668,foundm/z242.0666.
实施例6:产物4f的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol4-甲氧基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4f纯品(1109mg,产率92%,淡黄色固体)。4f1hnmr图谱见图11,4f13cnmr图谱见图12。
1hnmr(400mhz,cdcl3)δ:6.97(d,j=9.0hz,2h),6.89(d,j=9.0hz,2h),3.80(s,3h),3.45(s,3h),3.33(s,3h);
13cnmr(100mhz,cdcl3)δ:188.5,157.4,147.8,123.5,114.2,55.6,43.37,38.72;
hrms(esi):[m+h]+calcd.forc11h16nos2m/z242.0668,foundm/z242.0666.
实施例7:产物4g的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol4-甲氧基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4g纯品(1224mg,产率91%,无色固体)。4g1hnmr图谱见图13,4g13cnmr图谱见图14。
1hnmr(400mhz,cdcl3)δ:10.04(s,1h),7.39(d,j=3.1hz,1h),7.18(dd,j=8.9hz,j=3.1hz,1h),7.06(d,j=8.9hz,1h),3.88(s,3h),3.49(s,3h),3.43(s,3h);
13cnmr(100mhz,cdcl3)δ:188.1,187.8,157.6,149.6,129.6,125.4,121.9,111.4,55.8,43.6,38.9;
hrms(apci):[m+h]+calcd.forc12h16no2s2m/z270.0617,foundm/z270.0615.
实施例8:产物4h的制备
室温下,在25ml的圆底烧瓶中分别加入5mmol4-甲氧基苯硫酚、6mmol二氯亚砜和5mmol的n,n-二甲基苯甲酰基烯丙胺,然后依次加入15ml二氯甲烷、15mmol的三乙胺,反应在常温下研磨10小时。反应完全后向体系中加入10ml饱和氯化钠水溶液,用乙酸乙酯萃取3次,每次10ml,合并有机相,用无水硫酸钠干燥后,蒸除溶剂,200-300目的硅胶柱层析得n,n-二甲基二硫代乙酸苯酯类化合物4h纯品(1240mg,产率95%,淡黄色固体)。4h1hnmr图谱见图15,4h13cnmr图谱见图16。
1hnmr(400mhz,cdcl3)δ:7.94-7.89(m,1h),7.88-7.83(m,1h),7.80(d,j=8.2hz,1h),7.57-7.49(m,3h),7.25(d,j=7.5hz,1h),3.56(s,3h),3.53(s,3h)
13cnmr(100mhz,cdcl3)δ:188.0,150.0,134.6,128.2,127.5,126.5,126.4,126.1,125.3,121.6,119.6,43.5,38.9;
hrms(esi):[m+h]+calcd.forc14h16ns2m/z262.0719,foundm/z262.0717。
- 还没有人留言评论。精彩留言会获得点赞!