增强鲁米诺体系的电化学发光生物传感器的制备方法与流程
本发明涉及一种基于增强鲁米诺体系电化学发光信号,构建用于检测miRNA生物传感器的新方法,属于生物传感器制备领域。该方法可应用于miRNA临床诊断以及对miRNA的定量分析。
背景技术:
MicroRNAs(miRNAs)是一类含有19—23个碱基的非编码单链小分子RNA,广泛存在于人体和几乎所有模式生物的细胞中,这些小分子RNA通过碱基配对与信使RNA(mRNA)序列的3′UTR区或编码区结合从而调控靶基因的表达,在动植物的发育、细胞生长分化和凋亡、代谢等生命活动过程中发挥重要的调控作用。最近有研究结果表明,miRNA的异常表达与多数癌症相关,如胰腺癌、肺癌、肝癌、胃癌、乳腺癌、结肠癌和卵巢癌等。这些miRNA所起的作用类似于抑癌基因和癌基因的功能。因此,对细胞或组织样本中miRNA的定量检测将有利于人们进一步了解miRNA的表达与癌症发生之间的关系。miRNA也有望被用作有价值的标志物,用于早期的癌症诊断和预后,这对与探索生物进化及防治人类疾病具有重要意义。
由于miRNA序列短、在细胞内的表达水平比较低,而且许多同源miRNA(如let-7家族)序列相似度高,仅差1—2个碱基,使设计的分析探针与miRNA杂交的效率低。所以,miRNA的研究给分析化学在检测的灵敏度和选择性方面都提出了新的挑战。当前,miRNA的检测方法主要有Northern印迹、微阵列芯片、聚合酶链式反应(PCR)扩增和原位杂交,但是因为操作繁琐、耗时长、灵敏度低等缺点这些传统方法在应用上受到限制。近年来,为了提高miRNA检测的灵敏度,多种DNA扩增技术如恒温滚环扩增技术等相继被应用于miRNA分析;为了提高miRNA的检测通量,相继开发了多种探针标记技术以及检测新方法。
本实验中采用的检测信号是电化学发光(ECL)信号。ECL是在电极上施加一定的电压使电极反应产物之间或电极反应产物与溶液中某组分进行电化学反应而产生的一种光辐射。它包括了电化学分析和化学发光分析两个进程,因此既保留了化学发光方法灵敏度高、线性范围宽、观察方便和仪器简单等优点;同时增加了许多化学发光方法无法比拟的优点,如重现性好、试剂稳定、控制容易,从而引起人们的注意并得到了广泛的应用。
技术实现要素:
本发明所要解决的技术问题在于提供一种基于增强鲁米诺体系ECL信号,用于miRNA检测的生物传感器制备方法。此方法从电化学发光的反应机理出发,利用血红素作为辣根过氧化物类似物,可有效催化过氧化氢的分解的特性,在本质上实现了鲁米诺体系电化学发光信号的增强,从而更灵敏地检测目标miRNA。该方法灵敏度高、特异性强、检测成本低。
本发明采取如下技术方案:
1.增强鲁米诺体系的电化学发光生物传感器的制备方法,其特征
在于,包括以下步骤:
1)确定待检测的目标miRNA,设计与其碱基互补的DNA探针序列;
2)玻碳电极的预处理:打磨玻碳电极,超声清洗,氮气吹干后将电极浸入5mM氯金酸溶液中,通过循环伏安法,初始电压和低电位设置为0V,高电位为1V,在此区间内循环扫描电沉积金纳米颗粒;
3)将DNA探针溶液滴加在电极表面,室温下于湿盒中自组装16-20h,带有巯基修饰的探针通过Au-S键固定到金纳米颗粒表面;
4)滴加葡萄糖氧化酶封闭电极表面非特异性活性位点,于4℃下培育3h;
5)将目标miRNA滴加到电极表面,室温下杂交30min,形成miRNA-DNA双链结构;
6)将血红素溶液滴加到杂交后的电极表面,室温下培育1h。
2.进一步,设计的DNA探针自身不会杂交。
3.进一步,所用玻碳电极的直径是3mm,打磨粉为0.05μm Al2O3粉末。
4.进一步,电沉积过程中的扫速为50mV/s,扫描圈数为5圈。
5.进一步,滴加的DNA探针溶液由PBS缓冲液配置,浓度为25μM,体积为10μL;PBS缓冲液浓度为5mM,PBS的pH=7.4,
6.进一步,滴加的葡萄糖氧化酶浓度为0.5mg/mL,体积为10μL。
7.进一步,滴加的血红素溶液浓度为10μM,体积为10μL。
优选的是,设计的DNA探针自身不会杂交缠绕,不会形成发卡或者其他结构,相关检测干扰达到最低。
优选的是,DNA的储备液是由PBS缓冲液配置,浓度为5mM,pH=7.4。
优选的是,目标miRNA与电极表面的DNA探针杂交时间为30min。
优选的是,滴加在电极表面的血红素溶液浓度为10μM。
优选的是,血红素嵌入miRNA-DNA双链复合物反应时间为1h。
优选的是,测试电化学发光信号时,电解液中葡萄糖浓度为1×10-2M。
优选的是,电沉积金纳米颗粒过程所设置的初始电位以及低电位为0V,高电位为1V,扫描圈数为5圈,扫速为50mV/s。
本发明与现有技术相比,具有以下优点和良好效果:
1)利用血红素可催化H2O2分解生成超氧阴离子的特性,结合鲁米诺电化学发光机理,从本质上实现了鲁米诺的ECL信号的增强,并用于miRNA的检测。
2)高特异性:因血红素与miRNA-DNA之间结合形式为嵌入作用,对于其他miRNA,其杂交效率要远远小于目标miRNA,因此结合的血红素数量大大降低,导致最终测得ECL增强效果明显不同。
3)高灵敏度:鲁米诺自身发光效果较低,结合血红素的增强作用后,对于不同浓度目标miRNA可灵敏响应。
4)无污染:整个检测过程不需要用到有毒试剂。
附图说明
图1为本发明基于增强鲁米诺体系电化学发光信号的生物传感器制备的示意图。
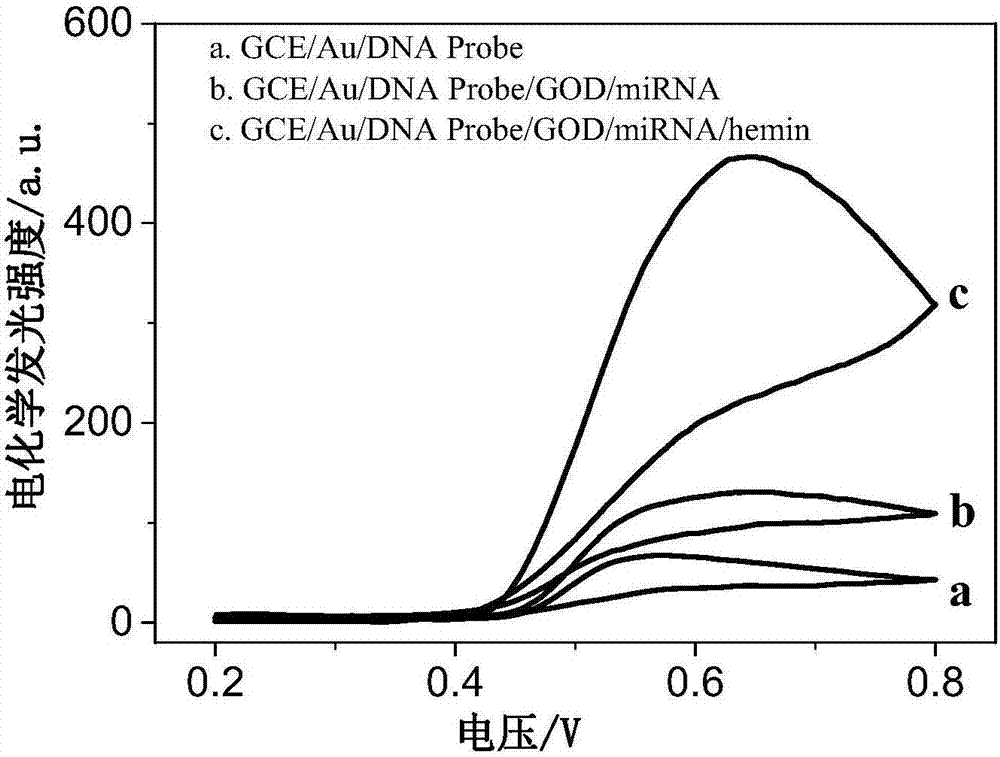
图2为三种不同修饰状态电极所测得的ECL信号比较图。
图3为本发明设计的生物传感器对于目标miRNA实现高特异性检测图。
具体实施方式
为了使本发明的内容、目的、技术方案及优点更加清楚明白,以下结合说明书附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。本领域内的技术人员所熟知的一般替换也涵盖在本发明的保护范围内。
基于增强鲁米诺体系电化学发光信号的生物传感器制备,包括以下步骤:
1)确定待检测的目标miRNA,遵循碱基互补原则,设计与其互补的DNA探针序列。
2)玻碳电极的预处理:打磨玻碳电极,超声清洗,氮气吹干。将电极浸入5mM氯金酸溶液中,通过循环伏安法,初始电压以及低电位设置为0V,高电位为1V,在此区间内电沉积金纳米颗粒。
3)将10μL DNA探针滴加在电极表面,室温下于湿盒中自组装16-20h,5’端修饰巯基的探针从而通过Au-S键被固定到金纳米颗粒表面。
4)滴加10μL葡萄糖氧化酶用于封闭电极表面的非特异性活性位点,于4℃下培育3h。
5)将目标miRNA滴加到电极表面,室温下杂交,形成miRNA-DNA双链结构。
6)将10μL血红素溶液滴加到杂交后的电极表面,以嵌入双链结构中。
7)电极洗净后,在5mL含葡萄糖和鲁米诺的PBS溶液中测量电化学发光。
实施例一
1.DNA探针的设计
选择的目标miRNA为let-7d,其碱基序列:
5’-AGAGGUAGUAGGUUGCAUAGUU-3’
DNA探针序列为:
5’-HS-CCACCACGAACTATGCAACCTACTACCTCT-3’
其中,需要说明的是,设计的DNA探针序列中下划线部分为与目标miRNA互补序列。DNA探针自身不会缠绕在一起,不会形成发卡或者其他结构,结构最小自由能为零,具有相当稳定的单链结构且与人体中已发现的基因组保持最小相似度,相关检测干扰达到最低。
2.实验部分
1)将订购的DNA探针干粉离心5min,转速设置为6000转/分钟,加入5mM PBS缓冲液(pH=7.4),配成25μM的浓度,震荡5min至溶液充分均匀。
2)将订购的目标miRNA干粉离心5min,转速设置为10000转/分钟,加入DEPC处理水,震荡5min至充分溶解。
3)用0.05μm Al2O3粉末打磨玻碳电极,依次用二次水、乙醇、二次水进行超声清洗,氮气吹干。浸入5mM氯金酸溶液中,通过循环伏安法电沉积纳米金,初始电压以及低电压设置为0V,高电压设置为1V,扫描速率为50mV/s,沉积圈数为5圈。
4)滴加10μL25μM的DNA探针溶液,室温下于湿盒中自组装16-20h,带有巯基修饰的探针DNA会通过Au-S键固定在金纳米颗粒表面。用5mM PBS充分清洗,氮气吹干后,滴加10μL 0.5mg/mL的葡萄糖氧化酶封闭电极表面剩余活性位点,在4℃下培育3h。
5)将目标miRNA滴加到封闭后的电极表面,于室温下杂交30min。清洗电极,氮气吹干后,滴加10μL10μM的血红素,室温下培育1h。
6)将电极冲洗干净,进行电化学发光检测,底液为0.1M PBS(pH=7.4;含1×10-4M鲁米诺和2×10-2M葡萄糖),电位扫描范围为0.2V~0.8V,扫速为100mV/s,光电倍增管电压设置为800V。
7)为了验证增强策略的可行性,测试了三种不同修饰状态下的电极ECL信号(附图2);为了考察生物传感器的特异性,选择与目标miRNA为同源家族的其他三种核苷酸序列作为对照(附图3)。
尽管本发明已以较佳实施例公开如上,但其并不仅仅限于说明书和实施方式中所列运用,所述实施例仅为了便于说明而已,对于熟悉本领域的人员而言,在不脱离本发明精神和范围的前提下可作若干的更动与润饰,本发明所主张的保护范围应以权利要求书所述为准。
- 还没有人留言评论。精彩留言会获得点赞!