一种基于贵金属纳米粒子快速现场检测溴氰菊酯的方法与流程
本发明属于分析化学领域,具体涉及一种基于金纳米粒子光学探针检测样品中溴氰菊酯的现场快速检测方法。
背景技术:
中国是一个农业大国,每年需施用大量农药以保证粮食产量。据不完全统计,我国每年使用农药约21万吨,种类近400种,居世界首位。农药是把双刃剑,虽然能确保农业生产正常进行,但也会带来严重的农药残留问题。据美国康奈尔大学的研究,每年施用的农药大约只有1%能起到实际作用,99%的农药会分散到农产品、土壤、大气、水环境中,大多数农药在自然环境中的半衰期期极长,会随着自然界中物质循环进行迁移,造成大范围、跨区域、持久性的污染。农药的乱用,滥用更是加剧了农药污染问题。
溴氰菊酯是杀虫活性最大的拟除虫菊酯类杀虫剂。其杀虫活性马拉硫磷的440倍,双对氯苯基三氯乙烷(ddt)的100倍,西维因的80倍,对硫磷的40倍。其杀虫谱广,触杀作用迅速,广泛应用于瓜果蔬菜的害虫防治。溴氰菊酯属中等毒素,接触皮肤后会出现刺激症状,出现红色丘疹。急性中毒轻者头痛、头晕、恶心、呕吐食欲不振、乏力;重者会出现肌束震颤和抽搐甚至死亡。并且极易在生物体内累积。
目前检测溴氰菊酯比较成熟的技术主要有薄层色谱法、气相色谱法,高效液相色谱法,反相高效液相色谱法以及色谱-质谱联用等方法。然而这些方法往往操作繁琐,检测时间长,检测结果晦涩难懂等缺陷,并且这些方法还需要大型仪器,难以运用到实时现场快速检测。
因此,开发出一种操作简单、反应迅速、灵敏可靠能实时现场检测出样品中溴氰菊酯的方法并能应用于实际中有着重要的应用价值。
技术实现要素:
本发明的目的是提供一种简单、快速、灵敏、可靠能实时现场检测样品中溴氰菊酯的方法。
为实现上述目的,本发明提供如下技术方案:
一种基于贵金属纳米粒子快速现场检测溴氰菊酯的方法,具体步骤如下:
(1)制备2-巯基-6-硝基-苯并噻唑修饰的响应型金纳米光学探针,作为检测液;
(2)溴氰菊酯的定性检测:
向所述检测液加入待测样本,形成第一混合液;
向所述检测液加入与待测样本体积相等的无水乙醇,形成第二混合液;
比较第一混合液与第二混合液的颜色,若发生颜色变化,则说明待测样本中含有溴氰菊酯;若未发生颜色变化,则待测样本中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。
或者测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度,若紫外可见吸收峰值、强度发生变化,则待测样本中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
(3)溴氰菊酯的定量检测:
向所述检测液加入待测样本,形成第一混合液;
建立溴氰菊酯浓度与检测液颜色变化关系的标准比色卡,将第一混合液的颜色变化图片与标准比色图片对比,通过裸眼判断出第一混合液中溴氰菊酯浓度;
或者建立溴氰菊酯浓度与检测液紫外可见吸收谱线相关参数变化关系的标准曲线和相关公式,通过将第一混合液液紫外可见吸收谱线相关参数与标准曲线对比,计算出第一混合液中溴氰菊酯浓度。
优选地,所述的2-巯基-6-硝基-苯并噻唑修饰的响应型金纳米粒子光学探针的制备方法如下:
(a)金纳米粒子胶体的制备
将aucl3·hcl·4h2o溶液加入到超纯水中并混合均匀,在5分钟之内滴加nabh4水溶液,在滴加过程中边滴加边搅拌,滴加完毕后再搅拌25~35min,溶液颜色由桃红变为酒红色,即得金纳米粒子胶体,放入3-5℃冰箱中静置待用;
(b)从冰箱中取出金纳米粒子胶体,恢复到室温,加入2-巯基-6-硝基-苯并噻唑乙醇溶液,边加入边搅拌,滴加完毕后再搅拌90-125min,即得到mnbt修饰的响应型金纳米粒子光学探针,并作为检测液。
优选地,步骤(a)中aucl3·hcl·4h2o溶液的浓度为5~10mmol·l-1,nabh4水溶液的浓度为0.05~0.2mol·l-1,aucl3·hcl·4h2o溶液、超纯水与nabh4水溶液的体积比为:5~20:200:3~10。
优选地,步骤(b)中2-巯基-6-硝基-苯并噻唑乙醇溶液的浓度为1~5mmol·l-1,金纳米粒子胶体与2-巯基-6-硝基-苯并噻唑乙醇溶液的体积比为:2000~6000:1~5。
优选地,所述的检测液ph范围为4~11。
优选地,步骤(3)中溴氰菊酯浓度与检测液颜色变化关系的标准比色卡通过如下方法建立:配置一系列不同浓度的溴氰菊酯的乙醇溶液,将溴氰菊酯乙醇溶液加入到检测液中制得第一混合液,反应3~10min,观察不同浓度溴氰菊酯引起检测液的颜色变化,以此建立标准比色卡。
优选地,步骤(3)中溴氰菊酯浓度与检测液紫外可见吸收谱线相关参数变化关系的标准曲线和相关公式的建立方法如下:
配置一系列不同浓度的溴氰菊酯的乙醇溶液,将溴氰菊酯乙醇溶液加入到检测液中,反应3~10min,使用紫外可见分光光度计测定其紫外吸收谱线,绘制标准曲线及设置相关参数求相关公式。
本发明的有益效果在于:
本发明提供的溴氰菊酯检测方法操作简单、检测快速、成本低、选择性好、抗干扰力强、灵敏度高,并且可以在实时实地操作,适用于瓜果蔬菜上溴氰菊酯的检测。
附图说明
图1为实施例1中2-巯基-6-硝基-苯并噻唑修饰的响应型金纳米光学探针的透射电子显微镜图片;
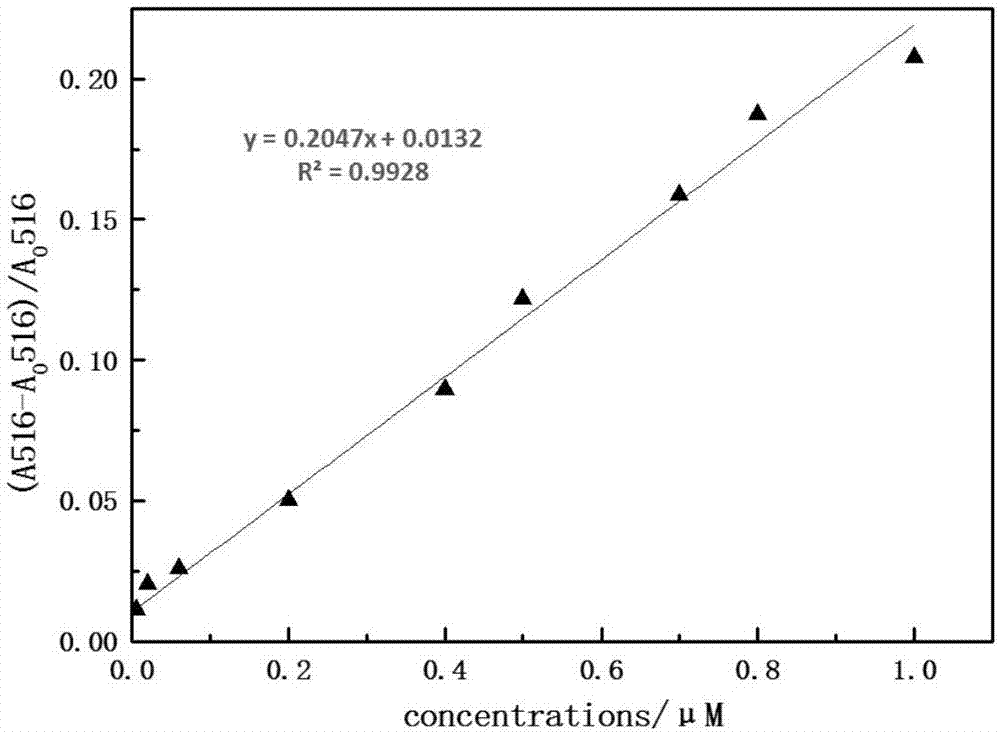
图2为实施例1中2-巯基-6-硝基-苯并噻唑修饰的响应型金纳米光学探针检测溴氰菊酯绘制得到的溴氰菊酯与吸光度的标准曲线图。
具体实施方式
下面通过具体的实施例进一步描述本发明,需要说明的是,以下所述具体实施例意在便于对本发明的理解,不限制本发明的内容。
实施例1
一种基于贵金属纳米粒子快速现场检测溴氰菊酯的方法,具体步骤如下:
(1)2-巯基-6-硝基-苯并噻唑(mnbt)修饰的响应型金纳米粒子光学探针的制备:
(a)金纳米粒子胶体的制备,20ml5mmol/laucl3·hcl·4h2o加入到200ml的超纯水中并混合均匀,在5分钟之内滴加5ml0.1mol/l新配置的nabh4水溶液,在滴加过程中边滴加边搅拌,滴加完毕后再搅拌30min,溶液颜色由桃红变为酒红色,,即得金纳米粒子胶体,放入4℃冰箱中静置待用;
(b)取40ml步骤(a)中制备的金纳米粒子胶体,恢复到室温,加入mnbt乙醇溶液,边加入边搅拌,继续搅拌2h,即可得到mnbt修饰的响应型金纳米粒子光学探针,并作为检测液。
(2)溴氰菊酯的定性检测:
向所述检测液加入待测样本,形成第一混合液;
向所述检测液加入与待测样本体积相等的无水乙醇,形成第二混合液;
比较第一混合液与第二混合液的颜色,若发生颜色变化,则说明待测样本中含有溴氰菊酯;若未发生颜色变化,则待测样本中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。
或者测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度,若紫外可见吸收峰值、强度发生变化,则待测样本中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
(3)溴氰菊酯的定量检测:
向所述检测液加入待测样本,形成第一混合液;
建立溴氰菊酯浓度与检测液颜色变化关系的标准比色卡,将第一混合液的颜色变化图片与标准比色图片对比,通过裸眼判断出第一混合液中溴氰菊酯浓度;
其中,溴氰菊酯浓度与检测液颜色变化关系的标准比色卡通过如下方法建立:配置一系列不同浓度的溴氰菊酯的乙醇溶液,将溴氰菊酯乙醇溶液加入到检测液中制得第一混合液,反应5min,观察不同浓度溴氰菊酯引起检测液的颜色变化,以此建立标准比色卡。
或者建立溴氰菊酯浓度与检测液紫外可见吸收谱线相关参数变化关系的标准曲线和相关公式,通过将第一混合液液紫外可见吸收谱线相关参数与标准曲线对比,计算出第一混合液中溴氰菊酯浓度。
其中,溴氰菊酯浓度与检测液紫外可见吸收谱线相关参数变化关系的标准曲线和相关公式的建立方法如下:
配置一系列不同浓度的溴氰菊酯的乙醇溶液,将溴氰菊酯乙醇溶液加入到检测液中,反应5min,使用紫外可见分光光度计测定其紫外吸收谱线,绘制标准曲线及设置相关参数求相关公式。
实施例2
(1)20μl1mmol/l2-巯基-6-硝基-苯并噻唑(mnbt)修饰的响应型金纳米粒子光学探针的制备:
(a)金纳米粒子胶体的制备,20ml5mmaucl3·hcl·4h2o加入到200ml的超纯水中并混合均匀,在5分钟之内滴加5ml0.1mol/l新配置的nabh4水溶液,在滴加过程中边滴加边搅拌,滴加完毕后再搅拌30min,溶液颜色由桃红变为酒红色,放入4℃冰箱中静置待用;
(b)取40ml步骤(a)中制备的金纳米粒子胶体,恢复到室温,加入20μl1mmol/l的mnbt乙醇溶液,边加入边搅拌,继续搅拌2h,即可得到mnbt修饰的响应型金纳米粒子光学探针,并作为检测液。
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例3
(1)40μl1mmol/l的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1步骤(1)中(a)所制备的金纳米粒子40ml,加入40μl1mmol/l的mnbt乙醇溶液,边加入边搅拌,继续搅拌2h,即可得到mnbt修饰的响应型金纳米粒子光学探针,并作为检测液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例4
(1)50μl1mmol/l的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1步骤(1)中(a)所制备的金纳米粒子40ml,加入50μl1mmol/l的mnbt乙醇溶液,边加入边搅拌,继续搅拌2h,即可得到mnbt修饰的响应型金纳米粒子光学探针,并作为检测液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例5
(1)ph为4的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针40ml,用适量盐酸调节ph到4,并作为检测溶液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例6
(1)ph为7的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针40ml,用适量盐酸调节ph到7,并作为检测溶液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例7
(1)ph为9的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针40ml,用适量氢氧化钠溶液调节ph到9,并作为检测溶液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例8
(1)ph为11的mnbt修饰的金纳米粒子光学探针的制备:
取实施例1中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针40ml,用适量氢氧化钠溶液调节ph到11,并作为检测溶液;
(2)溴氰菊酯的检测:
(a)取两份等体积步骤(1)中所制备的mnbt修饰的金纳米粒子光学探针胶体:配置不含溴氰菊酯的乙醇溶液作为对比液,将待检测溶液和与之等体积的对比液分别加入所述的两份mnbt修饰的响应型金纳米粒子光学探针胶体中,形成第一混合液和第二混合液;
(b)反应5分钟后,比较第一混合液与第二混合液的颜色,如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例9
(1)mnbt修饰的金纳米粒子光学探针的制备:
取实施例8中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针作为检测溶液;
(2)mnbt修饰的金纳米粒子光学探针的特异性:
(a)取15份等体积的步骤(1)所制得的mnbt修饰的金纳米粒子光学探针,分别加入已知浓度的溴氰菊酯以及相同浓度等体积的13种其他农药(异丙威,二氧威,速灭威,毒死蜱,草甘膦,二甲四氯钠,仲丁威,地亚农,茚虫威,扑海因,灭多威,丙草胺,敌百虫)和等体积的无水乙醇;
(b)反应5分钟后,比较各组颜色变化,如果只有加入溴氰菊酯组颜色发生改变,则mnbt修饰的金纳米粒子光学探针对溴氰菊酯有良好的特异性,反之则mnbt修饰的金纳米粒子光学探针对溴氰菊酯的特异性差。
实验结果如下:比较各组颜色变化发现:只有加入溴氰菊酯组颜色发生改变,说明mnbt修饰的金纳米粒子光学探针对溴氰菊酯有良好的特异性。
实施例10
(1)mnbt修饰的金纳米粒子光学探针的制备:
取实施例8中步骤(1)所制备的mnbt修饰的金纳米粒子光学探针作为检测溶液;
(2)mnbt修饰的金纳米粒子光学探针的抗干扰性:
(a)已知浓度的溴氰菊酯与13种农药(异丙威,二氧威,速灭威,毒死蜱,草甘膦,二甲四氯钠,仲丁威,地亚农,茚虫威,扑海因,灭多威,丙草胺,敌百虫)等体积混合制得干扰农药混合液,溴氰菊酯与其他农药的摩尔比为1∶5。再取已知浓度一半的溴氰菊酯做对比;
(b)取15份等体积的步骤(1)所制得的mnbt修饰的金纳米粒子光学探针,分别加入步骤(2)中(a)所制的干扰农药混合液、溴氰菊酯和无水乙醇。
(c)反应5分钟后,比较各组颜色变化。如果干扰农药混合液组与溴氰菊酯组颜色变化相同,则mnbt修饰的金纳米粒子光学探针有良好的抗干扰性;反之则mnbt修饰的金纳米粒子光学探针抗干扰性差。
实验结果如下:干扰农药混合液组与溴氰菊酯组颜色变化相同,说明mnbt修饰的金纳米粒子光学探针有良好的抗干扰性。
实施例11
小番茄上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为4;
(2)待测样品的采集:用无水乙醇淋洗一定量的小番茄,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例12
小番茄上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为7;
(2)待测样品的采集:用无水乙醇淋洗一定量的小番茄,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例13
小番茄上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量氢氧化钠溶液调节纳米金检测液ph为11;
(2)待测样品的采集:用无水乙醇淋洗一定量的小番茄,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例14
樱桃上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为4;
(2)待测样品的采集:用无水乙醇淋洗一定量的樱桃,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的金检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例15
樱桃上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为7;
(2)待测样品的采集:用无水乙醇淋洗一定量的樱桃,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的金检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例16
樱桃上溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量氢氧化钠溶液调节纳米金检测液ph为11;
(2)待测样品的采集:用无水乙醇淋洗一定量的樱桃,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的金检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例17
茶叶中溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为4;
(2)待测样品的采集:用无水乙醇浸泡一定量的茶叶,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的金检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例18
茶叶中溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量盐酸调节纳米金检测液ph为7;
(2)待测样品的采集:用无水乙醇浸泡一定量的茶叶,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
实施例19
茶叶中溴氰菊酯的检测:
(1)取实施例3中(1)中所制得的金纳米粒子光学探针作为检测液,用适量氢氧化钠溶液调节纳米金检测液ph为11;
(2)待测样品的采集:用无水乙醇浸泡一定量的茶叶,反复三次,过滤掉杂质,获得待测样品;
(3)待测样品的检测:
(a)取50μl待测样品,加入到950μl步骤(1)所制的检测液中,混合均匀获得检测混合液。并用同体积无水乙醇做空白对照;
(b)对比检测混合液与空白对照颜色变化,判断待检样品中是否含有溴氰菊酯:如果发生颜色变化,则说明待检测溶液中含有溴氰菊酯;如未发生颜色变化,则待检测溶液中不含有溴氰菊酯或其含量低于2.5×10-7mol/l。亦可测定第一混合液和第二混合液的紫外可见光吸收光谱,对比二者的紫外可见吸收峰值、强度等,如果紫外可见吸收峰值、强度等发生变化,则待检溶液中含有溴氰菊酯,并且可以通过线性工作曲线计算出溴氰菊酯浓度,反之则不含溴氰菊酯或溴氰菊酯含量低于5×10-9mol/l。
- 还没有人留言评论。精彩留言会获得点赞!
- 具吡啶二硫功能基的磁性纳米粒子Fe3O4@SiO2@S-S-Py的制备及生物医药中的应用的制造方法与工艺
- 聚乙二醇化包裹聚多巴胺载药磁性纳米颗粒的制备方法与流程
- 一种PQQ‑DA印迹磁性纳米粒子的制备方法及其应用与制造工艺
- 一种可降解聚合物磁性纳米粒子及其制备方法与制造工艺
- 一种山梨酸-茶多酚复合纳米粒子及其应用的制造方法与工艺
- 一种实现纳米线生物传感器表面修饰的方法与制造工艺
- 磁性纳米粒子和产生自由基的酶的介孔催化剂及其使用方法与制造工艺
- 一种靶向性超顺磁性纳米探针的制备方法和应用方法与制造工艺
- 油酸包裹的超顺磁性纳米Fe3O4及其制备方法与制造工艺
- 一种贵金属纳米粒子间距可控的SERS衬底制备方法与制造工艺